实验活动 8 粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 实验活动 8 粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年人教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 54.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览



文档简介
实验活动 8 粗盐中难溶性杂质的去除 同步练习
一、单选题
1.对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法。下列对实验现象的分析合理的是( )
A.某无色气体混入空气后点燃爆炸,可证明该气体一定是H2
B.KNO3溶于水会使溶液温度降低,可证明KNO3溶于水吸热
C.物质在空气中燃烧生成二氧化碳和水,可证明该物质一定含碳、氢、氧三种元素
D.某溶液能使酚酞试液变红,可证明该溶液一定是碱溶液
2.下列说法中,合理的是( )
A.用托盘天平称量氯化钠固体时,能称准到0.1g
B.过滤操作时,液面高于滤纸边缘
C.向正在燃着的酒精灯里添加酒精
D.用量筒量取液体时,仰视凹液面最低处读数
3.水是生命之源。下列有关水的说法错误的是( )
A.可用肥皂水区分硬水和软水
B.河水经沉淀、过滤后得到的水仍是混合物
C.水由氢原子和氧原子构成
D.水在通电条件下分解成氢气和氧气
4.下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A. 鉴别某固体是否为铵态氮肥 加稀盐酸,闻气味
B. 鉴别稀盐酸、氢氧化钠、氯化钠三种溶液 分别滴加酚酞溶液,再相互混合
C. 除去碳酸钙中混有的少量氯化钙 加水溶解、过滤、蒸发
D. 除去硫酸钠溶液中混有的少量氢氧化钠 加入过量的硫酸铜溶液,过滤
A.A B.B C.C D.D
5.下列实验操作能达到实验目的的是(括号内为杂质)( )
选项 物质 目的 主要实验操作
A CH4、CO、N2 检验 将燃着的木条分别伸入集气瓶中
B 稀H2SO4、Ca(OH)2溶液、NaNO3溶液 鉴别 取样,滴加碳酸钠溶液
C KNO3、NaCl 分离 取样,加水溶解,蒸发结晶
D Fe(Fe2O3) 除杂 取样,加入稀盐酸,过滤
A.A B.B C.C D.D
6.下列有关实验基本操作中先后顺序的叙述错误的是( )
A.用托盘天平称量药品时,先调节天平平衡,后称量
B.制备气体时,先检查装置的气密性,后装入药品
C.双氧水制氧气的实验中,先加入双氧水,后加入二氧化锰
D.给试管中的药品加热时,先对试管均匀加热,后对准装药品的部位集中加热
7.初中化学教科书中的下列实验,其操作顺序正确的是( )
A.在实验室中制取二氧化碳气体时,要先检验、再收集,最后检验是否收集满
B.在实验室中加热高锰酸钾,用排水法收集氧气完毕时,要先停止加热,再把导管移出水面
C.做一氧化碳还原氧化铁实验时,要先加热,再通入一氧化碳气体
D.做证明稀盐酸和氢氧化钠溶液恰好完全反应实验时,要先向烧杯中加入稀盐酸,然后滴入几滴酚酞溶液,最后缓慢滴入氢氧化钠溶液
8.小明用托盘天平称取药品,砝码的质量是10g,游码的质量是0.2g,发现将砝码和药品放反了,则称量的实际质量是多少( )
A.9.8g B.10g C.10.2g D.10.4g
9.下列对实验现象的描述正确的是( )
A.碳在氧气中燃烧发出白光,生成二氧化碳
B.硫在氧气中燃烧,发出淡蓝色火焰,产生有刺激性气味的气体
C.细铁丝在氧气中燃烧,火星四射,生成黑色固体
D.磷在空气中燃烧,发出黄光,产生白色的烟雾
10.用托盘天平称量一包未知质量的药品时,天平的指针向左偏转,要使天平平衡,应进行的操作是( )
A.增加药品 B.增加砝码 C.减少药品 D.减少砝码
11.日常生活中的下列做法错误的是( )
A.向食品包装袋充入氧气防腐
B.将易拉罐放入可回收垃圾桶
C.食用含铁酱油预防贫血
D.利用金刚石的硬度制作玻璃刻刀
12.两同学用托盘天平称量9.4g(1g以下用游码)药品,他们在放好9g砝码,并把游码调到0.4g后。另一同学称量时误将砝码和药品在托盘上的位置颠倒了,请问该同学称得药品的质量为( )
A.9.40g B.8.6g C.9.4g D.8.60g
二、填空题
13.人类只有一个地球,我们只有一个家园,保护环境人人有责.
①燃放烟花爆竹时,除了会带来噪音污染外,还会带来 等环境污染.
②为了我们的青山绿水,请你用学过的知识回答和解决问题.
我县锰矿资源丰富,某电解金属锰厂排放的废水中含有硫酸等物质,从经济和可行方面考虑,你认为最好选择什么物质处理该废水中的硫酸?
14.晶晶过滤含有泥沙的水后,滤液仍然浑浊,可能的原因是( )
A 倾倒液体时液面高于滤纸边缘
B 漏斗的下端未靠在烧杯壁上
C 未用玻璃棒引流
D
15.实验室除去粗实验中难溶性杂质的主要实验步骤有:溶解、 、蒸发;除去粗实验水中的杂质CaCl2、MgCl2、Na2SO4,可依次加入过量的NaOH、 、Na2CO3溶液,分离出沉淀后,再加入适量盐酸,其作用是 。
16.地球是太阳系八大行星之中唯一被液态水所覆盖的星球。
(1)自然界的水需要经过沉降、 、吸附、消毒等多步净化处理才能成为城市生活用水(即自来水)。
(2)自来水中仍含有一些可溶性杂质,需要经过进一步净化才能符合某些实验的要求。
①若自来水中含有较多的可溶性钙和镁的化合物则为硬水。可用来区分软水和硬水的试剂是 。
②实验室所用的净化程度较高的水,可以通过 (填分离方法)自来水制取。
③写出水在实验室中的一种用途 。
(3)爱护水资源一方面需要节约用水,另一方面要防治水体污染。下列措施中,有助于防治水体污染的是_____(填字母序号)。
A.禁止使用农药化肥
B.直接将工业废水排入大海
C.集中处理生活污水后再排放
D.园林浇灌改大水漫灌为喷灌、滴灌
17.下表各组中,实验操作和目的对应关系错误的是
A 加热试管时,先均匀加热后集中加热 防止试管炸裂
B 量取液体时,视线与凹液面最低处保持水平 防止读数误差
C 铁丝在氧气中燃烧时,集气瓶底部放少量水 使实验现象更加明显
D 用双氧水制氧气时,加入少量二氧化锰
18.一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 3.4 2.2 13.6 0.9
反应后质量/g 待测 8.8 0 4.5
则反应后A的质量为 :该反应所属的基本反应类型是 ;该反应中B和D两种物质变化的质量比为 。
三、综合题
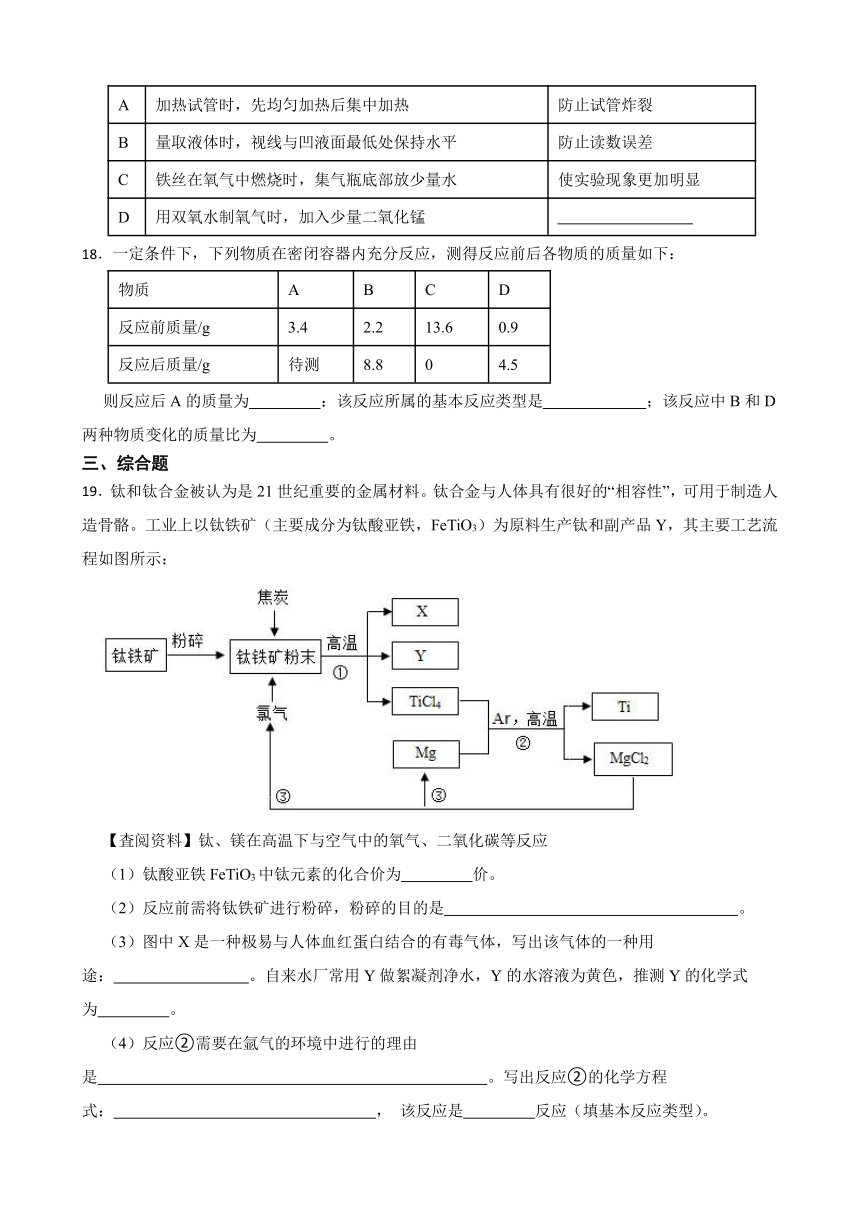
19.钛和钛合金被认为是21世纪重要的金属材料。钛合金与人体具有很好的“相容性”,可用于制造人造骨骼。工业上以钛铁矿(主要成分为钛酸亚铁,FeTiO3)为原料生产钛和副产品Y,其主要工艺流程如图所示:
【査阅资料】钛、镁在高温下与空气中的氧气、二氧化碳等反应
(1)钛酸亚铁FeTiO3中钛元素的化合价为 价。
(2)反应前需将钛铁矿进行粉碎,粉碎的目的是 。
(3)图中X是一种极易与人体血红蛋白结合的有毒气体,写出该气体的一种用途: 。自来水厂常用Y做絮凝剂净水,Y的水溶液为黄色,推测Y的化学式为 。
(4)反应②需要在氩气的环境中进行的理由是 。写出反应②的化学方程式: , 该反应是 反应(填基本反应类型)。
(5)反应②所得金属钛中可能含有少量的金属单质Mg,若要除去该杂质,可选用的试剂是 。
(6)该流程中能循环利用的物质有 。
20.某化学小组对当地河水水样进行如下甲、乙两种净化处理,回答下列问题:
(1)用图甲装置对所取水样进行过滤,玻璃棒的作用是 ,操作有一处不正确是 ,向滤液中加入活性炭,利用其 性除去异味,再次过滤。
(2)图乙装置中冷凝管的进水口是 (填“a”或“b”)。
(3)为了比较以上两种方法得到的水的硬度,可以分别向得到的水样中加入 ,振荡,根据产生泡沫的多少判断。
(4)下列做法有利于保护水资源的是______(填字母)。
A.化肥和农药的过度使用
B.工业废水处理达标后排放
C.推行生活污水集中处理
21.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)发电厂是利用垃圾焚烧产生的 转变为电能.
(2)吸收步骤中,石灰浆的作用是 .
(3)溶解步骤中,产生的H2的化学方程式为 .除此反应外,溶解步骤还能发生两个反应:
①Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
②Fe+Fe2(SO4)3═3FeSO4,
其中属于化合反应的是 (填序号).反应前后铁元素的化合价不变的是 (填序号).
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、 (填操作名称),得到硫酸亚铁晶体,其中氮气的作用是 .
(5)请你就成都市生活垃圾处理提一条建议 .
22.保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:
(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应类型为 .
(2)反应Ⅱ为复分解反应,该反应的化学方程式为 .
(3)操作a的名称为 .
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是 ,加入NaCl的原因是
(5)198gZn(OH)2理论上能得到Zn的质量为 g.
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】C
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】C
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】空气污染,粉尘污染;酸和碱能够反应中和反应,废水中的硫酸可用较为廉价的生石灰除去
14.【答案】A;滤纸破损或接收装置不干净等
15.【答案】过滤;BaCl2;除去溶液中过量的NaOH和Na2CO3
16.【答案】(1)过滤
(2)肥皂水;蒸馏;作溶剂
(3)C
17.【答案】C;加快反应速率
18.【答案】6.8g;分解反应;11:6
19.【答案】(1)+4
(2)增大反应物接触面积,加快反应速率
(3)用于金属冶炼;FeCl3
(4)钛、镁在高温下与空气中的氧气、二氧化碳等反应;;置换
(5)稀盐酸
(6)氯气、镁
20.【答案】(1)引流;漏斗下端管口没有紧靠烧杯内壁;吸附
(2)b
(3)肥皂水
(4)B;C
21.【答案】(1)热能
(2)除去烟气中含有的SO2、HCl
(3)Fe+H2SO4═FeSO4+H2↑;②;①
(4)过滤;保护气,避免+2价的铁元素被空气中的氧气氧化
(5)生活垃圾分类回收等
22.【答案】(1)化合反应
(2)ZnS2O4+2NaOH═Zn(OH)2↓+Na2S2O4
(3)过滤
(4)可调节溶液为碱性,使 Na2S2O4结晶稳定存在;氯化钠的存在使Na2S2O4的溶解度降低,更易结晶析出,提高产率
(5)130g
一、单选题
1.对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法。下列对实验现象的分析合理的是( )
A.某无色气体混入空气后点燃爆炸,可证明该气体一定是H2
B.KNO3溶于水会使溶液温度降低,可证明KNO3溶于水吸热
C.物质在空气中燃烧生成二氧化碳和水,可证明该物质一定含碳、氢、氧三种元素
D.某溶液能使酚酞试液变红,可证明该溶液一定是碱溶液
2.下列说法中,合理的是( )
A.用托盘天平称量氯化钠固体时,能称准到0.1g
B.过滤操作时,液面高于滤纸边缘
C.向正在燃着的酒精灯里添加酒精
D.用量筒量取液体时,仰视凹液面最低处读数
3.水是生命之源。下列有关水的说法错误的是( )
A.可用肥皂水区分硬水和软水
B.河水经沉淀、过滤后得到的水仍是混合物
C.水由氢原子和氧原子构成
D.水在通电条件下分解成氢气和氧气
4.下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A. 鉴别某固体是否为铵态氮肥 加稀盐酸,闻气味
B. 鉴别稀盐酸、氢氧化钠、氯化钠三种溶液 分别滴加酚酞溶液,再相互混合
C. 除去碳酸钙中混有的少量氯化钙 加水溶解、过滤、蒸发
D. 除去硫酸钠溶液中混有的少量氢氧化钠 加入过量的硫酸铜溶液,过滤
A.A B.B C.C D.D
5.下列实验操作能达到实验目的的是(括号内为杂质)( )
选项 物质 目的 主要实验操作
A CH4、CO、N2 检验 将燃着的木条分别伸入集气瓶中
B 稀H2SO4、Ca(OH)2溶液、NaNO3溶液 鉴别 取样,滴加碳酸钠溶液
C KNO3、NaCl 分离 取样,加水溶解,蒸发结晶
D Fe(Fe2O3) 除杂 取样,加入稀盐酸,过滤
A.A B.B C.C D.D
6.下列有关实验基本操作中先后顺序的叙述错误的是( )
A.用托盘天平称量药品时,先调节天平平衡,后称量
B.制备气体时,先检查装置的气密性,后装入药品
C.双氧水制氧气的实验中,先加入双氧水,后加入二氧化锰
D.给试管中的药品加热时,先对试管均匀加热,后对准装药品的部位集中加热
7.初中化学教科书中的下列实验,其操作顺序正确的是( )
A.在实验室中制取二氧化碳气体时,要先检验、再收集,最后检验是否收集满
B.在实验室中加热高锰酸钾,用排水法收集氧气完毕时,要先停止加热,再把导管移出水面
C.做一氧化碳还原氧化铁实验时,要先加热,再通入一氧化碳气体
D.做证明稀盐酸和氢氧化钠溶液恰好完全反应实验时,要先向烧杯中加入稀盐酸,然后滴入几滴酚酞溶液,最后缓慢滴入氢氧化钠溶液
8.小明用托盘天平称取药品,砝码的质量是10g,游码的质量是0.2g,发现将砝码和药品放反了,则称量的实际质量是多少( )
A.9.8g B.10g C.10.2g D.10.4g
9.下列对实验现象的描述正确的是( )
A.碳在氧气中燃烧发出白光,生成二氧化碳
B.硫在氧气中燃烧,发出淡蓝色火焰,产生有刺激性气味的气体
C.细铁丝在氧气中燃烧,火星四射,生成黑色固体
D.磷在空气中燃烧,发出黄光,产生白色的烟雾
10.用托盘天平称量一包未知质量的药品时,天平的指针向左偏转,要使天平平衡,应进行的操作是( )
A.增加药品 B.增加砝码 C.减少药品 D.减少砝码
11.日常生活中的下列做法错误的是( )
A.向食品包装袋充入氧气防腐
B.将易拉罐放入可回收垃圾桶
C.食用含铁酱油预防贫血
D.利用金刚石的硬度制作玻璃刻刀
12.两同学用托盘天平称量9.4g(1g以下用游码)药品,他们在放好9g砝码,并把游码调到0.4g后。另一同学称量时误将砝码和药品在托盘上的位置颠倒了,请问该同学称得药品的质量为( )
A.9.40g B.8.6g C.9.4g D.8.60g
二、填空题
13.人类只有一个地球,我们只有一个家园,保护环境人人有责.
①燃放烟花爆竹时,除了会带来噪音污染外,还会带来 等环境污染.
②为了我们的青山绿水,请你用学过的知识回答和解决问题.
我县锰矿资源丰富,某电解金属锰厂排放的废水中含有硫酸等物质,从经济和可行方面考虑,你认为最好选择什么物质处理该废水中的硫酸?
14.晶晶过滤含有泥沙的水后,滤液仍然浑浊,可能的原因是( )
A 倾倒液体时液面高于滤纸边缘
B 漏斗的下端未靠在烧杯壁上
C 未用玻璃棒引流
D
15.实验室除去粗实验中难溶性杂质的主要实验步骤有:溶解、 、蒸发;除去粗实验水中的杂质CaCl2、MgCl2、Na2SO4,可依次加入过量的NaOH、 、Na2CO3溶液,分离出沉淀后,再加入适量盐酸,其作用是 。
16.地球是太阳系八大行星之中唯一被液态水所覆盖的星球。
(1)自然界的水需要经过沉降、 、吸附、消毒等多步净化处理才能成为城市生活用水(即自来水)。
(2)自来水中仍含有一些可溶性杂质,需要经过进一步净化才能符合某些实验的要求。
①若自来水中含有较多的可溶性钙和镁的化合物则为硬水。可用来区分软水和硬水的试剂是 。
②实验室所用的净化程度较高的水,可以通过 (填分离方法)自来水制取。
③写出水在实验室中的一种用途 。
(3)爱护水资源一方面需要节约用水,另一方面要防治水体污染。下列措施中,有助于防治水体污染的是_____(填字母序号)。
A.禁止使用农药化肥
B.直接将工业废水排入大海
C.集中处理生活污水后再排放
D.园林浇灌改大水漫灌为喷灌、滴灌
17.下表各组中,实验操作和目的对应关系错误的是
A 加热试管时,先均匀加热后集中加热 防止试管炸裂
B 量取液体时,视线与凹液面最低处保持水平 防止读数误差
C 铁丝在氧气中燃烧时,集气瓶底部放少量水 使实验现象更加明显
D 用双氧水制氧气时,加入少量二氧化锰
18.一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 3.4 2.2 13.6 0.9
反应后质量/g 待测 8.8 0 4.5
则反应后A的质量为 :该反应所属的基本反应类型是 ;该反应中B和D两种物质变化的质量比为 。
三、综合题
19.钛和钛合金被认为是21世纪重要的金属材料。钛合金与人体具有很好的“相容性”,可用于制造人造骨骼。工业上以钛铁矿(主要成分为钛酸亚铁,FeTiO3)为原料生产钛和副产品Y,其主要工艺流程如图所示:
【査阅资料】钛、镁在高温下与空气中的氧气、二氧化碳等反应
(1)钛酸亚铁FeTiO3中钛元素的化合价为 价。
(2)反应前需将钛铁矿进行粉碎,粉碎的目的是 。
(3)图中X是一种极易与人体血红蛋白结合的有毒气体,写出该气体的一种用途: 。自来水厂常用Y做絮凝剂净水,Y的水溶液为黄色,推测Y的化学式为 。
(4)反应②需要在氩气的环境中进行的理由是 。写出反应②的化学方程式: , 该反应是 反应(填基本反应类型)。
(5)反应②所得金属钛中可能含有少量的金属单质Mg,若要除去该杂质,可选用的试剂是 。
(6)该流程中能循环利用的物质有 。
20.某化学小组对当地河水水样进行如下甲、乙两种净化处理,回答下列问题:
(1)用图甲装置对所取水样进行过滤,玻璃棒的作用是 ,操作有一处不正确是 ,向滤液中加入活性炭,利用其 性除去异味,再次过滤。
(2)图乙装置中冷凝管的进水口是 (填“a”或“b”)。
(3)为了比较以上两种方法得到的水的硬度,可以分别向得到的水样中加入 ,振荡,根据产生泡沫的多少判断。
(4)下列做法有利于保护水资源的是______(填字母)。
A.化肥和农药的过度使用
B.工业废水处理达标后排放
C.推行生活污水集中处理
21.城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合利用的部分流程如下:
资料1:垃圾焚烧产生的烟气中含有SO2、HCl等有害气体.
资料2:+2价的铁元素容易被空气中的氧气氧化.
回答下列问题:
(1)发电厂是利用垃圾焚烧产生的 转变为电能.
(2)吸收步骤中,石灰浆的作用是 .
(3)溶解步骤中,产生的H2的化学方程式为 .除此反应外,溶解步骤还能发生两个反应:
①Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
②Fe+Fe2(SO4)3═3FeSO4,
其中属于化合反应的是 (填序号).反应前后铁元素的化合价不变的是 (填序号).
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、 (填操作名称),得到硫酸亚铁晶体,其中氮气的作用是 .
(5)请你就成都市生活垃圾处理提一条建议 .
22.保险粉(化学式为Na2S2O4)在工农业生产中有广泛的用途,Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定,在NaCl存在下,Na2S2O4在水中溶解度显著下降.制备流程如图:
(1)反应Ⅰ的原理为:Zn+2SO2═ZnS2O4,该反应类型为 .
(2)反应Ⅱ为复分解反应,该反应的化学方程式为 .
(3)操作a的名称为 .
(4)滤液中含有Na2S2O4,为使Na2S2O4结晶析出还需要加入少量NaOH的原因是 ,加入NaCl的原因是
(5)198gZn(OH)2理论上能得到Zn的质量为 g.
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】C
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】C
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】空气污染,粉尘污染;酸和碱能够反应中和反应,废水中的硫酸可用较为廉价的生石灰除去
14.【答案】A;滤纸破损或接收装置不干净等
15.【答案】过滤;BaCl2;除去溶液中过量的NaOH和Na2CO3
16.【答案】(1)过滤
(2)肥皂水;蒸馏;作溶剂
(3)C
17.【答案】C;加快反应速率
18.【答案】6.8g;分解反应;11:6
19.【答案】(1)+4
(2)增大反应物接触面积,加快反应速率
(3)用于金属冶炼;FeCl3
(4)钛、镁在高温下与空气中的氧气、二氧化碳等反应;;置换
(5)稀盐酸
(6)氯气、镁
20.【答案】(1)引流;漏斗下端管口没有紧靠烧杯内壁;吸附
(2)b
(3)肥皂水
(4)B;C
21.【答案】(1)热能
(2)除去烟气中含有的SO2、HCl
(3)Fe+H2SO4═FeSO4+H2↑;②;①
(4)过滤;保护气,避免+2价的铁元素被空气中的氧气氧化
(5)生活垃圾分类回收等
22.【答案】(1)化合反应
(2)ZnS2O4+2NaOH═Zn(OH)2↓+Na2S2O4
(3)过滤
(4)可调节溶液为碱性,使 Na2S2O4结晶稳定存在;氯化钠的存在使Na2S2O4的溶解度降低,更易结晶析出,提高产率
(5)130g
同课章节目录
