2022-2023学年高一化学人教版(2019)必修第二册课件:第五章实验活动5 不同价态含硫物质的转化(共32张PPT)
文档属性
| 名称 | 2022-2023学年高一化学人教版(2019)必修第二册课件:第五章实验活动5 不同价态含硫物质的转化(共32张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览








文档简介
(共32张PPT)
自
主
探
新
知
预
习
【实验目的】
试管、托盘天平、量筒、酒精灯、铁架台、试管架、橡胶塞、乳胶管、胶头滴管、玻璃导管、石棉网、玻璃棒、药匙、棉花、镊子、火柴。
浓硫酸、铜片、硫粉、铁粉、硫化钠溶液、酸性高锰酸钾溶液、氢氧化钠溶液、亚硫酸溶液、品红溶液。
【实验用品】
1.通过实验加深对硫及其化合物性质的认识。
2.应用氧化还原反应的原理实现不同价态含硫物质的转化。
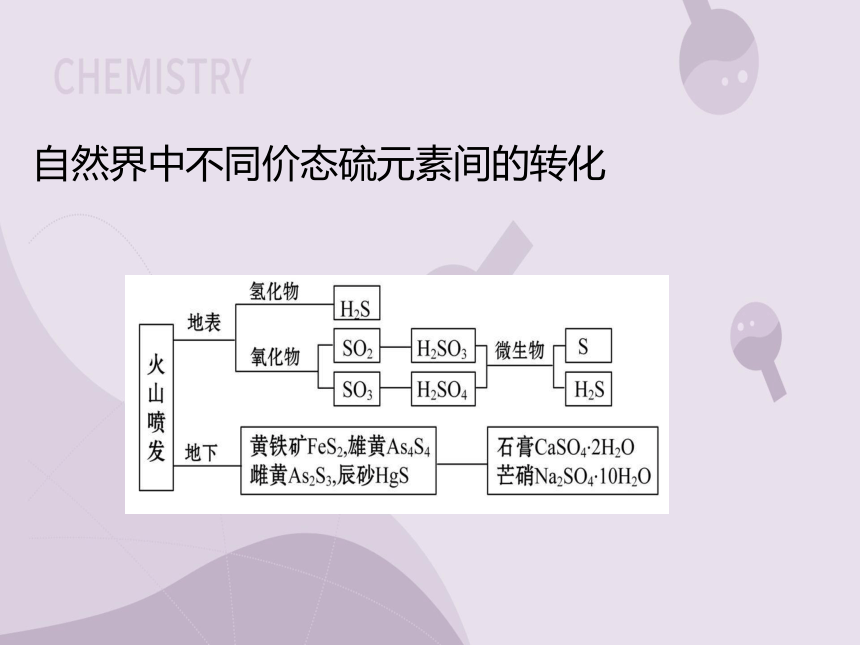
自然界中不同价态硫元素间的转化
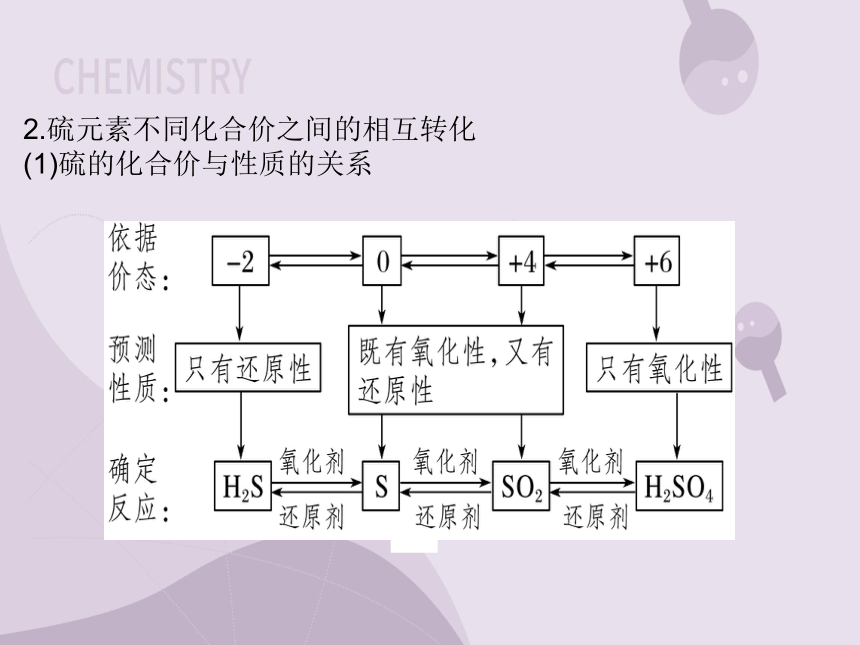
2.硫元素不同化合价之间的相互转化
(1)硫的化合价与性质的关系
(2)设计实验实现不同价态含硫物质的转化
序号 转化
目标 转化前的
含硫物质 选择试剂 转化后的
含硫物质
① -2→0 H2S ________ S
___
② 0→-2 S __ H2S
_______ _________
O2(不足)
SO2
H2
Fe或Cu
FeS或Cu2S
序号 转化
目标 转化前的
含硫物质 选择试剂 转化后的
含硫物质
③ -2→+4 H2S ________ SO2
④ 0→+4 S __ SO2
⑤ +4→0 SO2 ___ S
⑥ +4→+6 SO2 __ SO3
___ H2SO4
⑦ +6→+4 H2SO4 ___ SO2
O2(足量)
O2
H2S
O2
Cl2
Cu
核
心
攻
重
难
突
破
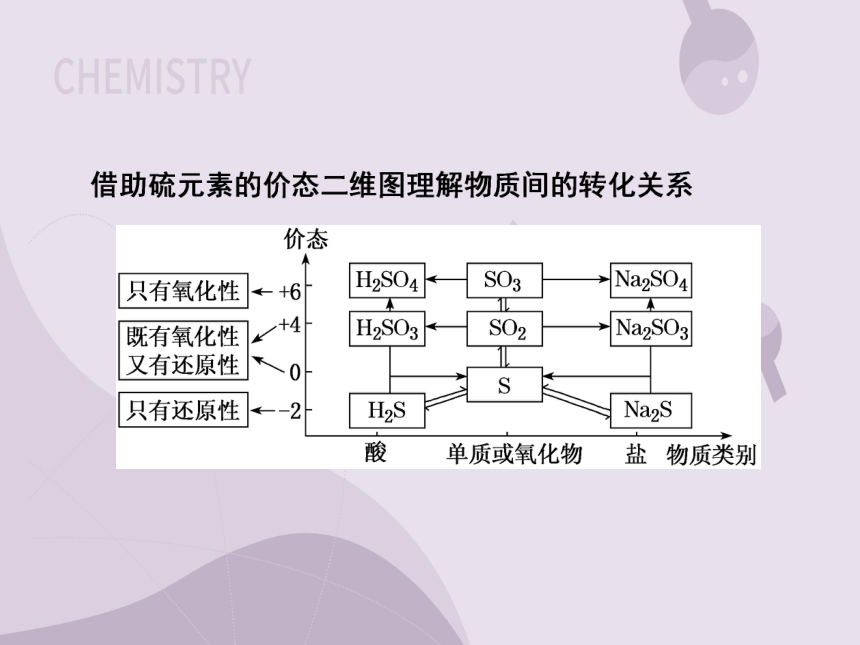
知识点 不同价态含硫物质的转化
1.常见含硫的物质的转化
【重点释疑】
当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,如:
相邻价态的粒子不发生氧化还原反应:如S和H2S、S和SO2、SO2和浓硫酸之间不发生氧化还原反应。
(2)归中规律
当硫元素的高价态粒子与低价态粒子反应时,一般生成中间价态,如:
2H2S+SO2===3S+2H2O,
2Na2S+Na2SO3+3H2SO4===3Na2SO4+3S↓+3H2O。
(3)含硫物质的连续氧化
当
堂
提
素
养
达
标
自
主
探
新
知
预
习
【实验目的】
试管、托盘天平、量筒、酒精灯、铁架台、试管架、橡胶塞、乳胶管、胶头滴管、玻璃导管、石棉网、玻璃棒、药匙、棉花、镊子、火柴。
浓硫酸、铜片、硫粉、铁粉、硫化钠溶液、酸性高锰酸钾溶液、氢氧化钠溶液、亚硫酸溶液、品红溶液。
【实验用品】
1.通过实验加深对硫及其化合物性质的认识。
2.应用氧化还原反应的原理实现不同价态含硫物质的转化。
自然界中不同价态硫元素间的转化
2.硫元素不同化合价之间的相互转化
(1)硫的化合价与性质的关系
(2)设计实验实现不同价态含硫物质的转化
序号 转化
目标 转化前的
含硫物质 选择试剂 转化后的
含硫物质
① -2→0 H2S ________ S
___
② 0→-2 S __ H2S
_______ _________
O2(不足)
SO2
H2
Fe或Cu
FeS或Cu2S
序号 转化
目标 转化前的
含硫物质 选择试剂 转化后的
含硫物质
③ -2→+4 H2S ________ SO2
④ 0→+4 S __ SO2
⑤ +4→0 SO2 ___ S
⑥ +4→+6 SO2 __ SO3
___ H2SO4
⑦ +6→+4 H2SO4 ___ SO2
O2(足量)
O2
H2S
O2
Cl2
Cu
核
心
攻
重
难
突
破
知识点 不同价态含硫物质的转化
1.常见含硫的物质的转化
【重点释疑】
当硫元素的化合价升高或降低时,一般升高或降低到其相邻的价态,即台阶式升降,如:
相邻价态的粒子不发生氧化还原反应:如S和H2S、S和SO2、SO2和浓硫酸之间不发生氧化还原反应。
(2)归中规律
当硫元素的高价态粒子与低价态粒子反应时,一般生成中间价态,如:
2H2S+SO2===3S+2H2O,
2Na2S+Na2SO3+3H2SO4===3Na2SO4+3S↓+3H2O。
(3)含硫物质的连续氧化
当
堂
提
素
养
达
标
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
