5.3 无机非金属材料(教学课件)(共22张PPT)—— 2022-2023学年高一化学人教版(2019)必修第二册
文档属性
| 名称 | 5.3 无机非金属材料(教学课件)(共22张PPT)—— 2022-2023学年高一化学人教版(2019)必修第二册 |

|
|
| 格式 | ppt | ||
| 文件大小 | 5.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
无机非金属材料的主角—硅
(第一课时)
黄山
黄土高原
东方明珠
玛瑙
硅元素在地壳中的含量及分布
1、硅在地壳中的含量为26.3%,仅次于氧。
2、硅是构成岩石与许多矿物的基本元素。
3、硅在地壳中的主要存在形式是氧化物及硅酸盐。
一、硅单质
1、种类
晶体和无定形
2、晶体硅的结构
与金刚石类似,晶体硅中每个Si原子结合周围4个Si原子形成正四面体结构,伸展成空间网状结构。
一、硅单质
3、物理性质
晶体硅是带有金属光泽的灰黑色固体,熔点高,硬度大,有脆性,导电性介于导体和绝缘体之间,是良好的半导体材料。
硅芯片是各种计算机、微电子产品的核心
硅太阳能电池
(光电池)
观察碳原子和硅原子的结构示意图,分析硅化学
性质活不活泼,为什么?硅的主要化合价是多少?
C
Si
硅的结构与位置
Si原子最外层有4个电子,既不易失电子,也不易得电子,所以硅的化学性质不活泼。主要形成正四价的化合物。
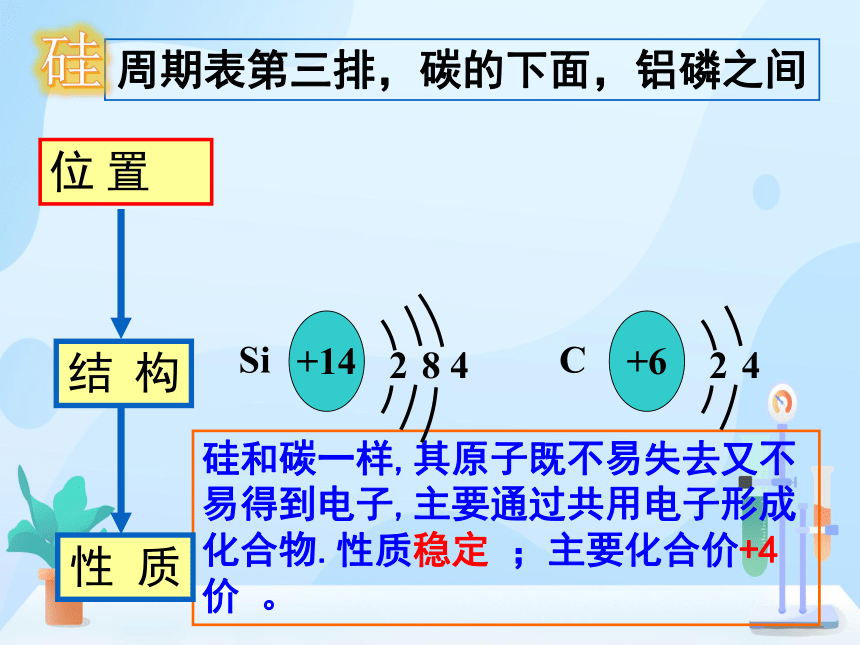
硅和碳一样,其原子既不易失去又不易得到电子,主要通过共用电子形成化合物.性质稳定 ;主要化合价+4价 。
位 置
结 构
性 质
周期表第三排,碳的下面,铝磷之间
+6
C
4
+14
Si
8 4
一、硅单质
4、化学性质
⑴常温下,硅的化学性质不活泼,除HF、F2、强碱
溶液外不跟其他物质起反应;
⑵加热情况下,硅也能跟一些O2、Cl2、C反应。
Si+2NaOH+H2O==Na2SiO3+2H2↑
Si+O2 SiO2
△
思考:常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?(课本P74)
1、与氟气反应:
2、仅与氢氟酸反应,不与其它酸反应
3、与强碱溶液反应:
4、与氯气反应:
5、与氧气反应
Si+2F2==SiF4
Si+4HF==SiF4↑+2H2 ↑
Si+2NaOH+H2O==Na2SiO3+2H2 ↑
Si+2Cl2==SiCl4
Si+O2==SiO2
△
高温
思考:常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?
硅与碳一样是一种亲氧元素,但是硅的亲氧能力更强.在自然界中它总是以稳定的氧化物和硅酸盐的形式存在
二、二氧化硅(SiO2 )
1、存在
天然二氧化硅有结晶形和无定形两类,统称硅石。沙子、石英、水晶、玛瑙的主要成分都是SiO2 。
根据SiO2的存在,分析SiO2具有什么物理性质?
玛瑙
石英砂
沙子
水晶
具有彩色环状或层状的石英称为玛瑙
石英中无色透明的晶体
就是通常所说的水晶
2、物理性质
晶体熔点高,硬度大, 难溶于水。
质疑:为什么SiO2和CO2物理性质差别很大?
阅读《科学视野》P74-75
SiO2晶体是由Si原子和O原子按1∶2的比例所组成的立体网状结构的晶体。基本单元是[SiO4]四面体结构。
结论:结构决定性质。
二、二氧化硅(SiO2 )
回顾二氧化碳的性质
二氧化碳
二氧化硅
CO2+H2O=H2CO3
CO2+2NaOH=Na2CO3+H2O
CO2+CaO=CaCO3
不反应
化学性质
与水反应
与NaOH反应
与CaO反应
与酸反应
?
思考与讨论
玻璃的主要成分是SiO2,化学性质不活泼,不与水反应,不与除氢氟酸(HF)外的酸反应,所以在生活中常用HF来雕刻玻璃。
SiO2 + 4HF = SiF4↑+ 2H2O
思考:实验室HF存放在 瓶中。
塑料
1、玻璃上的花纹是怎样雕刻上去的?
2、为什么实验室盛装NaOH溶液的试剂瓶用橡皮塞
而不用玻璃塞(玻璃中含有SiO2) ?
SiO2 + 2NaOH = Na2SiO3 +H2O
思考与交流
玻璃中含有SiO2, SiO2与NaOH溶液反应生成黏性的Na2SiO3,会使瓶塞和瓶口粘在一起,不易打开。
结论: SiO2是一种酸性氧化物。
SiO2+CaO 高温 CaSiO3
与碱性氧化物反应盐
不与水反应
①沙子是基本的建筑材料。
②石英可用于制作耐高温的石英坩埚等。
③水晶、玛瑙用于制作装饰品。
④纯净的SiO2是现代光学和光纤制品的基本原料,可制作光导纤维。
4、用途
二、二氧化硅(SiO2 )
构成
存在
物理性质
化学性质 与H2O
与CaO
与NaOH
与酸
反应
二氧化碳
二氧化硅
空气
石英、水晶、玛瑙、沙子
熔、沸点低, 能溶于水
熔点高,硬度大
不溶于水
CO2+H2O=H2CO3
不反应
CO2+2NaOH=Na2CO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
CO2+CaO=CaCO3
不反应
SiO2+4HF=SiF4↑+2H2O
小结:二氧化碳和二氧化硅的比较
CO2分子
Si原子、 O原子
SiO2+CaO 高温 CaSiO3
问题与讨论
1、SiO2既可与碱反应,也能与氢氟酸反应,所以SiO2
为两性氧化物。该结论是否正确
不正确。因为SiO2只跟氢氟酸反应,不跟其它酸反应,且跟氢氟酸反应生成的SiF4不是盐。所以SiO2属于酸性氧化物。
2、硅在自然界中主要以二氧化硅和硅酸盐的形式存在,如何从硅的氧化物中制取单质呢?
课本P81 第9题
粗硅的制取
SiO2+2 C Si+2CO↑
高温
粗硅转变为纯硅
Si+ 2Cl2 SiCl4
△
SiCl4+2 H2 Si+4HCl
高温
(含有C、SiO2等杂质)
纯硅的制备
还原剂
化合反应或氧化还原反应
置换反应或氧化还原反应
Si
价值5元的沙子
SiO2
点沙成金
价值5000元的芯片
4、怎么理解从沙滩到用户?
无机非金属材料的主角—硅
(第一课时)
黄山
黄土高原
东方明珠
玛瑙
硅元素在地壳中的含量及分布
1、硅在地壳中的含量为26.3%,仅次于氧。
2、硅是构成岩石与许多矿物的基本元素。
3、硅在地壳中的主要存在形式是氧化物及硅酸盐。
一、硅单质
1、种类
晶体和无定形
2、晶体硅的结构
与金刚石类似,晶体硅中每个Si原子结合周围4个Si原子形成正四面体结构,伸展成空间网状结构。
一、硅单质
3、物理性质
晶体硅是带有金属光泽的灰黑色固体,熔点高,硬度大,有脆性,导电性介于导体和绝缘体之间,是良好的半导体材料。
硅芯片是各种计算机、微电子产品的核心
硅太阳能电池
(光电池)
观察碳原子和硅原子的结构示意图,分析硅化学
性质活不活泼,为什么?硅的主要化合价是多少?
C
Si
硅的结构与位置
Si原子最外层有4个电子,既不易失电子,也不易得电子,所以硅的化学性质不活泼。主要形成正四价的化合物。
硅和碳一样,其原子既不易失去又不易得到电子,主要通过共用电子形成化合物.性质稳定 ;主要化合价+4价 。
位 置
结 构
性 质
周期表第三排,碳的下面,铝磷之间
+6
C
4
+14
Si
8 4
一、硅单质
4、化学性质
⑴常温下,硅的化学性质不活泼,除HF、F2、强碱
溶液外不跟其他物质起反应;
⑵加热情况下,硅也能跟一些O2、Cl2、C反应。
Si+2NaOH+H2O==Na2SiO3+2H2↑
Si+O2 SiO2
△
思考:常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?(课本P74)
1、与氟气反应:
2、仅与氢氟酸反应,不与其它酸反应
3、与强碱溶液反应:
4、与氯气反应:
5、与氧气反应
Si+2F2==SiF4
Si+4HF==SiF4↑+2H2 ↑
Si+2NaOH+H2O==Na2SiO3+2H2 ↑
Si+2Cl2==SiCl4
Si+O2==SiO2
△
高温
思考:常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有?
硅与碳一样是一种亲氧元素,但是硅的亲氧能力更强.在自然界中它总是以稳定的氧化物和硅酸盐的形式存在
二、二氧化硅(SiO2 )
1、存在
天然二氧化硅有结晶形和无定形两类,统称硅石。沙子、石英、水晶、玛瑙的主要成分都是SiO2 。
根据SiO2的存在,分析SiO2具有什么物理性质?
玛瑙
石英砂
沙子
水晶
具有彩色环状或层状的石英称为玛瑙
石英中无色透明的晶体
就是通常所说的水晶
2、物理性质
晶体熔点高,硬度大, 难溶于水。
质疑:为什么SiO2和CO2物理性质差别很大?
阅读《科学视野》P74-75
SiO2晶体是由Si原子和O原子按1∶2的比例所组成的立体网状结构的晶体。基本单元是[SiO4]四面体结构。
结论:结构决定性质。
二、二氧化硅(SiO2 )
回顾二氧化碳的性质
二氧化碳
二氧化硅
CO2+H2O=H2CO3
CO2+2NaOH=Na2CO3+H2O
CO2+CaO=CaCO3
不反应
化学性质
与水反应
与NaOH反应
与CaO反应
与酸反应
?
思考与讨论
玻璃的主要成分是SiO2,化学性质不活泼,不与水反应,不与除氢氟酸(HF)外的酸反应,所以在生活中常用HF来雕刻玻璃。
SiO2 + 4HF = SiF4↑+ 2H2O
思考:实验室HF存放在 瓶中。
塑料
1、玻璃上的花纹是怎样雕刻上去的?
2、为什么实验室盛装NaOH溶液的试剂瓶用橡皮塞
而不用玻璃塞(玻璃中含有SiO2) ?
SiO2 + 2NaOH = Na2SiO3 +H2O
思考与交流
玻璃中含有SiO2, SiO2与NaOH溶液反应生成黏性的Na2SiO3,会使瓶塞和瓶口粘在一起,不易打开。
结论: SiO2是一种酸性氧化物。
SiO2+CaO 高温 CaSiO3
与碱性氧化物反应盐
不与水反应
①沙子是基本的建筑材料。
②石英可用于制作耐高温的石英坩埚等。
③水晶、玛瑙用于制作装饰品。
④纯净的SiO2是现代光学和光纤制品的基本原料,可制作光导纤维。
4、用途
二、二氧化硅(SiO2 )
构成
存在
物理性质
化学性质 与H2O
与CaO
与NaOH
与酸
反应
二氧化碳
二氧化硅
空气
石英、水晶、玛瑙、沙子
熔、沸点低, 能溶于水
熔点高,硬度大
不溶于水
CO2+H2O=H2CO3
不反应
CO2+2NaOH=Na2CO3+H2O
SiO2+2NaOH=Na2SiO3+H2O
CO2+CaO=CaCO3
不反应
SiO2+4HF=SiF4↑+2H2O
小结:二氧化碳和二氧化硅的比较
CO2分子
Si原子、 O原子
SiO2+CaO 高温 CaSiO3
问题与讨论
1、SiO2既可与碱反应,也能与氢氟酸反应,所以SiO2
为两性氧化物。该结论是否正确
不正确。因为SiO2只跟氢氟酸反应,不跟其它酸反应,且跟氢氟酸反应生成的SiF4不是盐。所以SiO2属于酸性氧化物。
2、硅在自然界中主要以二氧化硅和硅酸盐的形式存在,如何从硅的氧化物中制取单质呢?
课本P81 第9题
粗硅的制取
SiO2+2 C Si+2CO↑
高温
粗硅转变为纯硅
Si+ 2Cl2 SiCl4
△
SiCl4+2 H2 Si+4HCl
高温
(含有C、SiO2等杂质)
纯硅的制备
还原剂
化合反应或氧化还原反应
置换反应或氧化还原反应
Si
价值5元的沙子
SiO2
点沙成金
价值5000元的芯片
4、怎么理解从沙滩到用户?
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
