8.2 海水“晒盐 ”同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 8.2 海水“晒盐 ”同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 86.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-02 00:00:00 | ||
图片预览



文档简介
8.2 海水“晒盐 ”同步练习
一、单选题
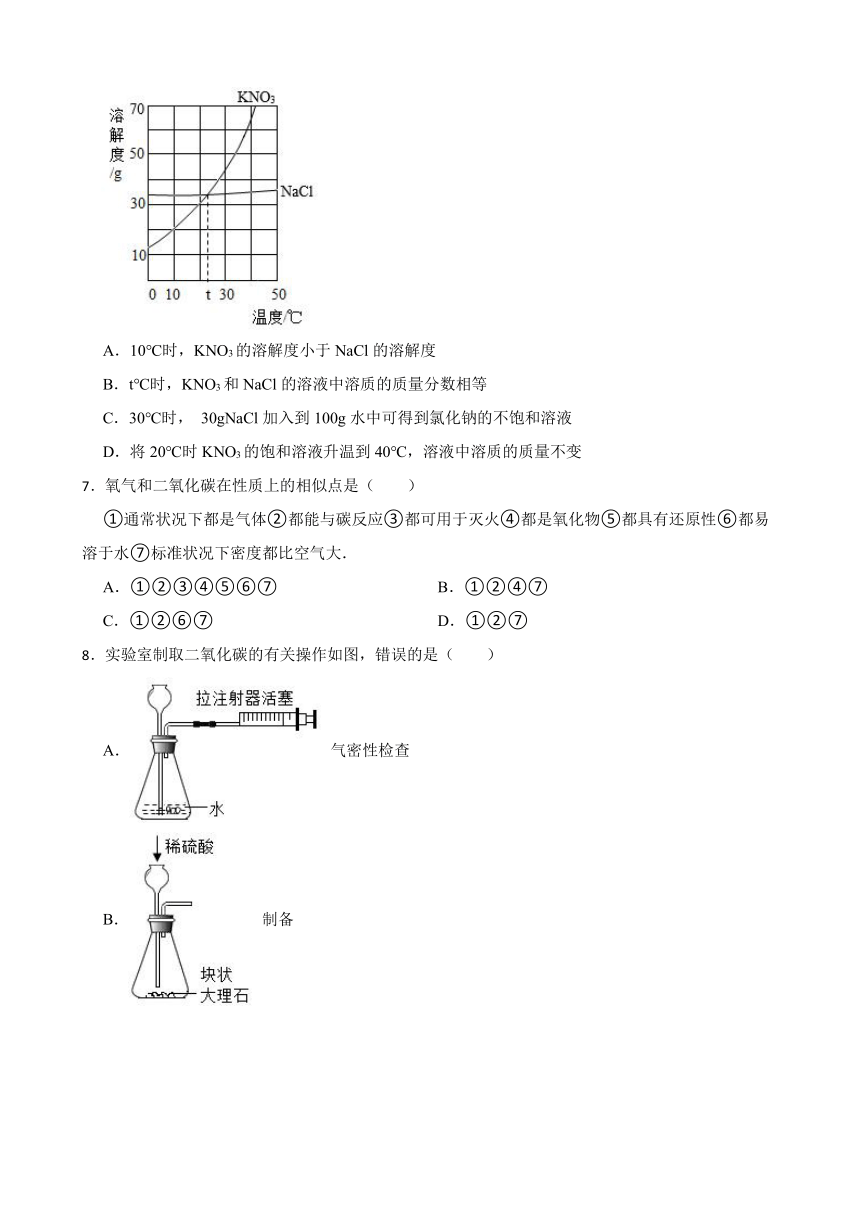
1.甲、乙两种固体物质的溶解度曲线如下图所示,下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.20℃时,乙的饱和溶液的溶质质量分数为36%
C.40℃时,使甲的饱和溶液析出晶体可采用升温、降温和蒸发溶剂三种方法
D.将等质量的甲、乙的饱和溶液分别从40℃降温至10℃,乙溶液中没有晶体析出
2.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.将镁片和锌片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向硫酸和硫酸铜的混合溶液中加入过量的氢氧化钠溶液
3.物质的结构决定性质,下列有关说法错误的是( )
A.过氧化氢与水化学性质不同的原因是由于分子构成不同
B.盐酸与硫酸化学性质相似的原因是在水溶液中都含有H+
C.氢氧化钠与氢氧化钙化学性质相似的原因是在水溶液中都含有OH﹣
D.金刚石与石墨物理性质差异较大的原因是由于碳原子的结构不同
4.下列不属于影响固体物质溶解度的因素的是( )
A.溶质的种类 B.溶剂的种类 C.压强 D.温度
5.甲、乙两种不含结晶水的固体物质在不同温度下的溶解度如下:
物质温度 0℃ 20℃ 30℃ 50℃ 80℃
甲 13.3g 31.6 g 36.2g 85.8g 169 g
乙 35.7g 36.O g 36.2g 36.5 g 37.1 g
根据上表中的数据进行判断,下列有关说法正确的是 ( )
A.甲的溶解度大于乙的溶解度
B.30℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等
C.使乙物质从它的一定温度下的饱和溶液中析出,一般采用冷却的方法
D.升高温度可使甲的不饱和溶液转变为饱和溶液
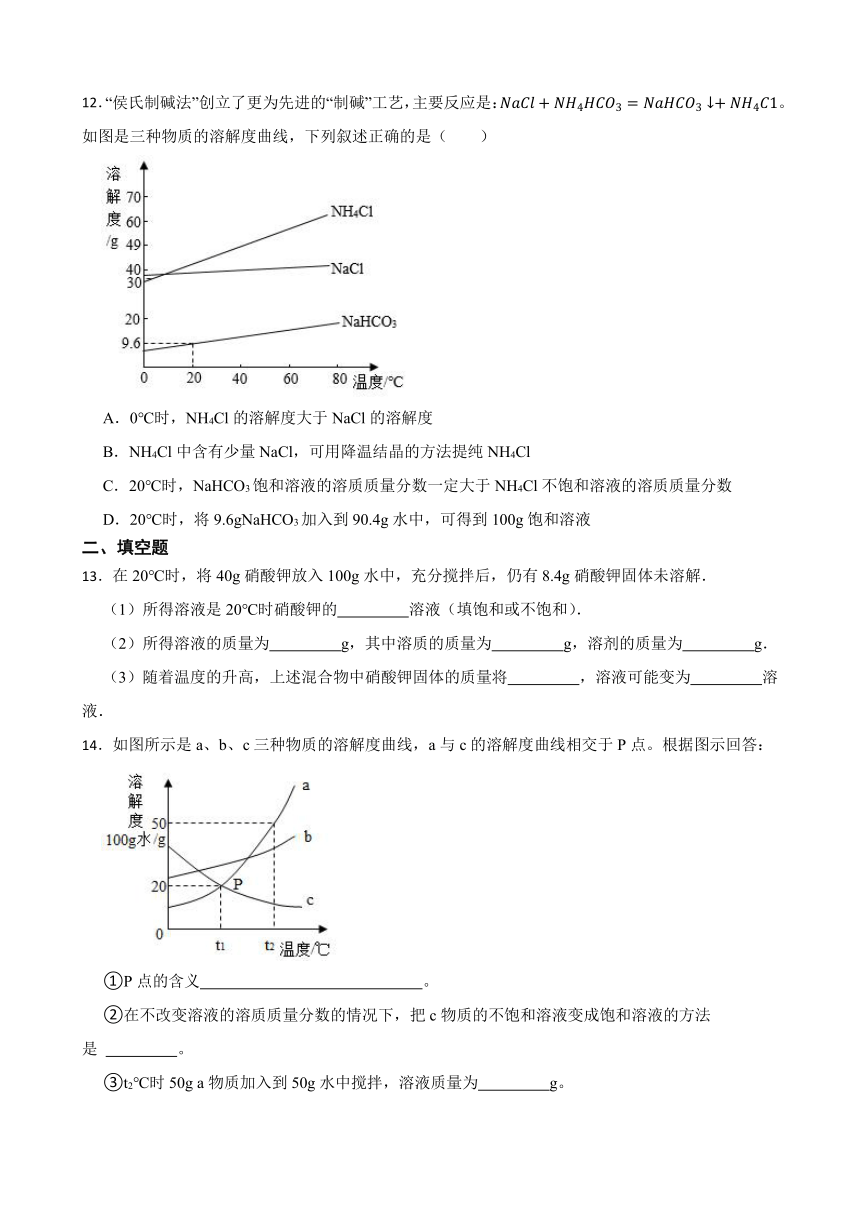
6.如图是KNO3和NaCl的溶解度曲线,下列说法错误的是( )
A.10℃时,KNO3的溶解度小于NaCl的溶解度
B.t℃时,KNO3和NaCl的溶液中溶质的质量分数相等
C.30℃时, 30gNaCl加入到100g水中可得到氯化钠的不饱和溶液
D.将20℃时KNO3的饱和溶液升温到40℃,溶液中溶质的质量不变
7.氧气和二氧化碳在性质上的相似点是( )
①通常状况下都是气体②都能与碳反应③都可用于灭火④都是氧化物⑤都具有还原性⑥都易溶于水⑦标准状况下密度都比空气大.
A.①②③④⑤⑥⑦ B.①②④⑦
C.①②⑥⑦ D.①②⑦
8.实验室制取二氧化碳的有关操作如图,错误的是( )
A. 气密性检查
B. 制备
C. 收集
D. 验满
9.图表资料能为我们提供很多信息,下列说法中,错误的是()
A.根据原子结构示意图,能推断原子的中子数
B.根据元素周期表,能查找元素的原子序数、元素符号、相对原子质量
C.根据金属活动顺序表,能判断金属是否容易被稀盐酸腐蚀
D.根据溶解度曲线图,能判断从溶质中获取晶体的方法
10.除去下列物质中的少量杂质(括号内为杂质)所用除去杂质的方法及操作均正确的是( )
选项 待提纯的物质 除去杂质的方法
A FeCl2 (CuCl2) 加水溶解、加过量铁粉、过滤、洗涤
B Fe粉(CuSO4) 加水溶解、过滤、洗涤、干燥
C CO2(CO) 点燃
D MnO2固体 (KCl) 加水溶解、过滤、洗涤、干燥
A.A B.B C.C D.D
11.a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.15℃时,a、b 的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变
D.20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液
12.“侯氏制碱法”创立了更为先进的“制碱”工艺,主要反应是:。如图是三种物质的溶解度曲线,下列叙述正确的是( )
A.0℃时,NH4Cl的溶解度大于NaCl的溶解度
B.NH4Cl中含有少量NaCl,可用降温结晶的方法提纯NH4Cl
C.20℃时,NaHCO3饱和溶液的溶质质量分数一定大于NH4Cl不饱和溶液的溶质质量分数
D.20℃时,将9.6gNaHCO3加入到90.4g水中,可得到100g饱和溶液
二、填空题
13.在20℃时,将40g硝酸钾放入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解.
(1)所得溶液是20℃时硝酸钾的 溶液(填饱和或不饱和).
(2)所得溶液的质量为 g,其中溶质的质量为 g,溶剂的质量为 g.
(3)随着温度的升高,上述混合物中硝酸钾固体的质量将 ,溶液可能变为 溶液.
14.如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。根据图示回答:
①P点的含义 。
②在不改变溶液的溶质质量分数的情况下,把c物质的不饱和溶液变成饱和溶液的方法是 。
③t2℃时50g a物质加入到50g水中搅拌,溶液质量为 g。
15.人类社会发展离不开能源,而开发氢能源是实现社会可持续发展的需要.
(1)目前人类生活、生产中重要的三大化石燃料:煤、石油、天然气:其中天然气主要成分的化学式为 ;化石燃料燃烧会加剧温室效应.下列符合“低碳生活”理念的做法是 (填序号).
A.提倡用燃煤火力发电
B.推广利用太阳能、风能、缓解温室效应
C.出行多乘坐公交车,少开私家车
(2)氢气是理想的清洁、高能燃料.工业上可用煅烧黄铁矿(主要成分FeS2)产生的二氧化硫,通过下列工艺过程制取氢气:
①写出膜反应器中HI气体发生分解反应的化学方程式 ;
②生产流程中可被循环利用的物质是 .
16.海水淡化可采用膜分离技术.如图一所示,对淡化膜右侧的海水加压,在其左侧得到淡水,其原因是海水中的水分子可以透过滤液淡化膜,到其他各种离子不能透过.请回答:
(1)采用膜分离技术淡化海水的原理,与化学实验中常见的 操作相似.
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会 (填”增大“、”减小“或”不变“)
(3)海水中含有大量的氧化钠,图二示氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是 结晶(填”降温“或”蒸发“).
17.如图是氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:
(1)30℃时,氯化钠的溶解度 碳酸钠的溶解度.(填“>”、“<”或“=”)
(2)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,两种溶液中溶质的质量分数大的是 溶液;
(3)将30℃时相同质量的饱和溶液,分别降温到10℃,晶体析出较多的是 .
(4)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是 (填字母序号).
A.氢氧化钠 B.生石灰 C.硝酸铵 D.浓硫酸.
18.如图为A,B, C三种固体物质的溶解度曲线。
(1)在 ℃时,A,C两种物质的溶解度相等。
(2)在t3℃时,A,B,C三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是 。
三、综合题
19.今年国庆假期,小美从邕江带回一瓶浑浊的河水,她在化学实验室模拟自来水厂的净水过程,最终制成蒸馏水,流程如图所示:
(1)操作①的名称是 ,实验室进行该操作时需要用到的仪器为铁架台、烧杯、玻璃棒和 。
(2)操作②主要是利用活性炭的 性除去一些异味和色素。
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 (填“硬水”或“软水”),生活中通过 可以降低水的硬度。
(4)请你列举一条有利于保护水资源的做法 。
20.甲、乙两种物质的溶解度曲线如图所示。请回答以下问题:
(1)t1℃时,甲物质的溶解度为 。
(2)降温能使 (填“甲”或“乙”)的不饱和溶液变成饱和溶液。若甲中混有少量的乙,提纯甲可采取 的方法;
(3)以下说法中正确的是 。
A t1℃时,等质量的甲、乙不饱和溶液升温至t2℃,两种溶液一定都不会析出晶体
B t1℃时,等质量的甲、乙饱和溶液恒温蒸发等质量的水,析出晶体的质量相等
C t2℃时,等质量甲、乙分别配成饱和溶液,完全溶解所需水的质量甲>乙
D 将t2℃时甲、乙的饱和溶液降温至t1℃,所得甲、乙溶液的溶质质量分数相等
21.2016年10月17日早晨7时30分,搭载两名宇航员的“神舟十一号”飞船在中国酒泉卫星发射中心成功发射!并与天宫二号自动交会对接成功。
(1)搭载着神舟十一号载人飞船的长征二号F遥十一运载火箭的部分燃料是液态氢气和液态氧气。请写出氢气和氧气点燃时反应的表达式 ,该反应的基本类型是 (选填“化合”或“分解”)反应。
(2)“天宫二号”舱内需提供给人呼吸的气体是 。该气体是由 (选填“分子”、“原子”或“离子”)构成的。
22.化学与生活息息相关.完成下列问题:
(1)通过一年的化学学习,我们熟悉了许多物质.请从①石墨;②活性炭;③尿素;
④氢气;⑤食盐;⑥氧气中,选取相应物质的序号填空.
①腌制蔬菜、鱼、肉等常用的调味品是 ;②最清洁的燃料是 ;③用于急救病人的气体是 ;④可作干电池电极的是 .
(2)能源与环境成为人们日益关注的问题.2014年世界环境日,中国的主题是“向污染宣战”,倡导全社会共同行动,打一场治理污染的攻坚战.请回答下列有关问题:
①化石燃料燃烧使化学能转化为 能,是当今人类生产、生活中重要的能源.但是化石燃料的燃烧会产色和温室气体 (填一种),导致温室效应.因此,对于化石燃料的使用,你的看法是: (写一点).
②我国积极发展绿色能源,以减少污染性气体的排放.对于①水力发电;②风力发电;③天然气发电;④太阳能发电;⑤垃圾焚烧发电等5种发电方式,你认为有利于减少温室气体排放的是 (填序号).
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】D
4.【答案】C
5.【答案】B
6.【答案】B
7.【答案】D
8.【答案】B
9.【答案】A
10.【答案】D
11.【答案】D
12.【答案】B
13.【答案】(1)饱和
(2)131.6;31.6;100
(3)减小;不饱和
14.【答案】t1℃时a和c 的溶解度相等;升温;75克
15.【答案】CH4;B C;2HI H2+I2;I2(或碘单质)
16.【答案】过滤;增大;蒸发
17.【答案】=;氯化钠;碳酸钠溶液;C
18.【答案】(1)t1
(2)C>B>A
19.【答案】(1)过滤;漏斗
(2)吸附
(3)硬水;煮沸
(4)废水处理达标后排放
20.【答案】(1)50
(2)甲;降温结晶或冷却热的饱和溶液
(3)B
21.【答案】(1)氢气+氧气 水;化合
(2)氧气;分子
22.【答案】(1)⑤;④;⑥;①
(2)热;二氧化碳;改造或淘汰高能耗、高污染产业;①、②、④
一、单选题
1.甲、乙两种固体物质的溶解度曲线如下图所示,下列叙述正确的是( )
A.甲的溶解度随温度的升高而增大
B.20℃时,乙的饱和溶液的溶质质量分数为36%
C.40℃时,使甲的饱和溶液析出晶体可采用升温、降温和蒸发溶剂三种方法
D.将等质量的甲、乙的饱和溶液分别从40℃降温至10℃,乙溶液中没有晶体析出
2.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.将镁片和锌片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向硫酸和硫酸铜的混合溶液中加入过量的氢氧化钠溶液
3.物质的结构决定性质,下列有关说法错误的是( )
A.过氧化氢与水化学性质不同的原因是由于分子构成不同
B.盐酸与硫酸化学性质相似的原因是在水溶液中都含有H+
C.氢氧化钠与氢氧化钙化学性质相似的原因是在水溶液中都含有OH﹣
D.金刚石与石墨物理性质差异较大的原因是由于碳原子的结构不同
4.下列不属于影响固体物质溶解度的因素的是( )
A.溶质的种类 B.溶剂的种类 C.压强 D.温度
5.甲、乙两种不含结晶水的固体物质在不同温度下的溶解度如下:
物质温度 0℃ 20℃ 30℃ 50℃ 80℃
甲 13.3g 31.6 g 36.2g 85.8g 169 g
乙 35.7g 36.O g 36.2g 36.5 g 37.1 g
根据上表中的数据进行判断,下列有关说法正确的是 ( )
A.甲的溶解度大于乙的溶解度
B.30℃时,甲、乙两种物质的饱和溶液中溶质的质量分数相等
C.使乙物质从它的一定温度下的饱和溶液中析出,一般采用冷却的方法
D.升高温度可使甲的不饱和溶液转变为饱和溶液
6.如图是KNO3和NaCl的溶解度曲线,下列说法错误的是( )
A.10℃时,KNO3的溶解度小于NaCl的溶解度
B.t℃时,KNO3和NaCl的溶液中溶质的质量分数相等
C.30℃时, 30gNaCl加入到100g水中可得到氯化钠的不饱和溶液
D.将20℃时KNO3的饱和溶液升温到40℃,溶液中溶质的质量不变
7.氧气和二氧化碳在性质上的相似点是( )
①通常状况下都是气体②都能与碳反应③都可用于灭火④都是氧化物⑤都具有还原性⑥都易溶于水⑦标准状况下密度都比空气大.
A.①②③④⑤⑥⑦ B.①②④⑦
C.①②⑥⑦ D.①②⑦
8.实验室制取二氧化碳的有关操作如图,错误的是( )
A. 气密性检查
B. 制备
C. 收集
D. 验满
9.图表资料能为我们提供很多信息,下列说法中,错误的是()
A.根据原子结构示意图,能推断原子的中子数
B.根据元素周期表,能查找元素的原子序数、元素符号、相对原子质量
C.根据金属活动顺序表,能判断金属是否容易被稀盐酸腐蚀
D.根据溶解度曲线图,能判断从溶质中获取晶体的方法
10.除去下列物质中的少量杂质(括号内为杂质)所用除去杂质的方法及操作均正确的是( )
选项 待提纯的物质 除去杂质的方法
A FeCl2 (CuCl2) 加水溶解、加过量铁粉、过滤、洗涤
B Fe粉(CuSO4) 加水溶解、过滤、洗涤、干燥
C CO2(CO) 点燃
D MnO2固体 (KCl) 加水溶解、过滤、洗涤、干燥
A.A B.B C.C D.D
11.a、b 两种物质的溶解度曲线如图所示.下列说法不正确的是( )
A.15℃时,a、b 的溶解度均为20g
B.加水或升温均可使b的饱和溶液变为不饱和溶液
C.将 30℃时a的饱和溶液降温至15℃,溶质的质量分数不变
D.20℃时分别向100g 水中加入20ga和 b,升温至30℃,所得溶液均为饱和溶液
12.“侯氏制碱法”创立了更为先进的“制碱”工艺,主要反应是:。如图是三种物质的溶解度曲线,下列叙述正确的是( )
A.0℃时,NH4Cl的溶解度大于NaCl的溶解度
B.NH4Cl中含有少量NaCl,可用降温结晶的方法提纯NH4Cl
C.20℃时,NaHCO3饱和溶液的溶质质量分数一定大于NH4Cl不饱和溶液的溶质质量分数
D.20℃时,将9.6gNaHCO3加入到90.4g水中,可得到100g饱和溶液
二、填空题
13.在20℃时,将40g硝酸钾放入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解.
(1)所得溶液是20℃时硝酸钾的 溶液(填饱和或不饱和).
(2)所得溶液的质量为 g,其中溶质的质量为 g,溶剂的质量为 g.
(3)随着温度的升高,上述混合物中硝酸钾固体的质量将 ,溶液可能变为 溶液.
14.如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。根据图示回答:
①P点的含义 。
②在不改变溶液的溶质质量分数的情况下,把c物质的不饱和溶液变成饱和溶液的方法是 。
③t2℃时50g a物质加入到50g水中搅拌,溶液质量为 g。
15.人类社会发展离不开能源,而开发氢能源是实现社会可持续发展的需要.
(1)目前人类生活、生产中重要的三大化石燃料:煤、石油、天然气:其中天然气主要成分的化学式为 ;化石燃料燃烧会加剧温室效应.下列符合“低碳生活”理念的做法是 (填序号).
A.提倡用燃煤火力发电
B.推广利用太阳能、风能、缓解温室效应
C.出行多乘坐公交车,少开私家车
(2)氢气是理想的清洁、高能燃料.工业上可用煅烧黄铁矿(主要成分FeS2)产生的二氧化硫,通过下列工艺过程制取氢气:
①写出膜反应器中HI气体发生分解反应的化学方程式 ;
②生产流程中可被循环利用的物质是 .
16.海水淡化可采用膜分离技术.如图一所示,对淡化膜右侧的海水加压,在其左侧得到淡水,其原因是海水中的水分子可以透过滤液淡化膜,到其他各种离子不能透过.请回答:
(1)采用膜分离技术淡化海水的原理,与化学实验中常见的 操作相似.
(2)对淡化膜右侧的海水加压后,海水中溶质的质量分数会 (填”增大“、”减小“或”不变“)
(3)海水中含有大量的氧化钠,图二示氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是 结晶(填”降温“或”蒸发“).
17.如图是氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题:
(1)30℃时,氯化钠的溶解度 碳酸钠的溶解度.(填“>”、“<”或“=”)
(2)10℃时,向两只盛有100g水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,两种溶液中溶质的质量分数大的是 溶液;
(3)将30℃时相同质量的饱和溶液,分别降温到10℃,晶体析出较多的是 .
(4)如图2所示,20℃时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是 (填字母序号).
A.氢氧化钠 B.生石灰 C.硝酸铵 D.浓硫酸.
18.如图为A,B, C三种固体物质的溶解度曲线。
(1)在 ℃时,A,C两种物质的溶解度相等。
(2)在t3℃时,A,B,C三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是 。
三、综合题
19.今年国庆假期,小美从邕江带回一瓶浑浊的河水,她在化学实验室模拟自来水厂的净水过程,最终制成蒸馏水,流程如图所示:
(1)操作①的名称是 ,实验室进行该操作时需要用到的仪器为铁架台、烧杯、玻璃棒和 。
(2)操作②主要是利用活性炭的 性除去一些异味和色素。
(3)取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是 (填“硬水”或“软水”),生活中通过 可以降低水的硬度。
(4)请你列举一条有利于保护水资源的做法 。
20.甲、乙两种物质的溶解度曲线如图所示。请回答以下问题:
(1)t1℃时,甲物质的溶解度为 。
(2)降温能使 (填“甲”或“乙”)的不饱和溶液变成饱和溶液。若甲中混有少量的乙,提纯甲可采取 的方法;
(3)以下说法中正确的是 。
A t1℃时,等质量的甲、乙不饱和溶液升温至t2℃,两种溶液一定都不会析出晶体
B t1℃时,等质量的甲、乙饱和溶液恒温蒸发等质量的水,析出晶体的质量相等
C t2℃时,等质量甲、乙分别配成饱和溶液,完全溶解所需水的质量甲>乙
D 将t2℃时甲、乙的饱和溶液降温至t1℃,所得甲、乙溶液的溶质质量分数相等
21.2016年10月17日早晨7时30分,搭载两名宇航员的“神舟十一号”飞船在中国酒泉卫星发射中心成功发射!并与天宫二号自动交会对接成功。
(1)搭载着神舟十一号载人飞船的长征二号F遥十一运载火箭的部分燃料是液态氢气和液态氧气。请写出氢气和氧气点燃时反应的表达式 ,该反应的基本类型是 (选填“化合”或“分解”)反应。
(2)“天宫二号”舱内需提供给人呼吸的气体是 。该气体是由 (选填“分子”、“原子”或“离子”)构成的。
22.化学与生活息息相关.完成下列问题:
(1)通过一年的化学学习,我们熟悉了许多物质.请从①石墨;②活性炭;③尿素;
④氢气;⑤食盐;⑥氧气中,选取相应物质的序号填空.
①腌制蔬菜、鱼、肉等常用的调味品是 ;②最清洁的燃料是 ;③用于急救病人的气体是 ;④可作干电池电极的是 .
(2)能源与环境成为人们日益关注的问题.2014年世界环境日,中国的主题是“向污染宣战”,倡导全社会共同行动,打一场治理污染的攻坚战.请回答下列有关问题:
①化石燃料燃烧使化学能转化为 能,是当今人类生产、生活中重要的能源.但是化石燃料的燃烧会产色和温室气体 (填一种),导致温室效应.因此,对于化石燃料的使用,你的看法是: (写一点).
②我国积极发展绿色能源,以减少污染性气体的排放.对于①水力发电;②风力发电;③天然气发电;④太阳能发电;⑤垃圾焚烧发电等5种发电方式,你认为有利于减少温室气体排放的是 (填序号).
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】D
4.【答案】C
5.【答案】B
6.【答案】B
7.【答案】D
8.【答案】B
9.【答案】A
10.【答案】D
11.【答案】D
12.【答案】B
13.【答案】(1)饱和
(2)131.6;31.6;100
(3)减小;不饱和
14.【答案】t1℃时a和c 的溶解度相等;升温;75克
15.【答案】CH4;B C;2HI H2+I2;I2(或碘单质)
16.【答案】过滤;增大;蒸发
17.【答案】=;氯化钠;碳酸钠溶液;C
18.【答案】(1)t1
(2)C>B>A
19.【答案】(1)过滤;漏斗
(2)吸附
(3)硬水;煮沸
(4)废水处理达标后排放
20.【答案】(1)50
(2)甲;降温结晶或冷却热的饱和溶液
(3)B
21.【答案】(1)氢气+氧气 水;化合
(2)氧气;分子
22.【答案】(1)⑤;④;⑥;①
(2)热;二氧化碳;改造或淘汰高能耗、高污染产业;①、②、④
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
