到实验室去 探究金属的性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 到实验室去 探究金属的性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 120.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览




文档简介
到实验室去 探究金属的性质 同步练习
一、单选题
1.将质量相等的A,B,C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是.(已知:A,B,C在生成物中均为+2价)( )
A.放出H2的质量是B>C>A B.金属活动性顺序是A>B>C
C.反应速率最大的是A D.相对原子质量是C>B>A
2.物质的性质在很大程度上决定了物质的用途,下列物质的性质与用途对应关系错误的是( )
A.金刚石的硬度很大﹣﹣切割玻璃
B.氧气具有助燃性﹣﹣富氧炼钢
C.氢气具有可燃性﹣﹣作燃料
D.铜具有导热性﹣﹣作电线
3.下列有关金属及合金的说法错误的是( )
A.金属在常温下大多数都是固体
B.钨制灯丝是利用钨的熔点高
C.不锈钢可用于制造医疗器械
D.铁是地壳中含量最多的金属元素
4.化学的学习使我们学会了从微观的角度想,下列对宏观现象解释不正确的是( )。
A.水变为水蒸气体积变大﹣分子间间隔增大
B.干冰升华﹣分子的体积变大
C.氧化汞受热分解﹣分子在化学变化中可以再分
D.闻到远处花香﹣分子在不断地运动
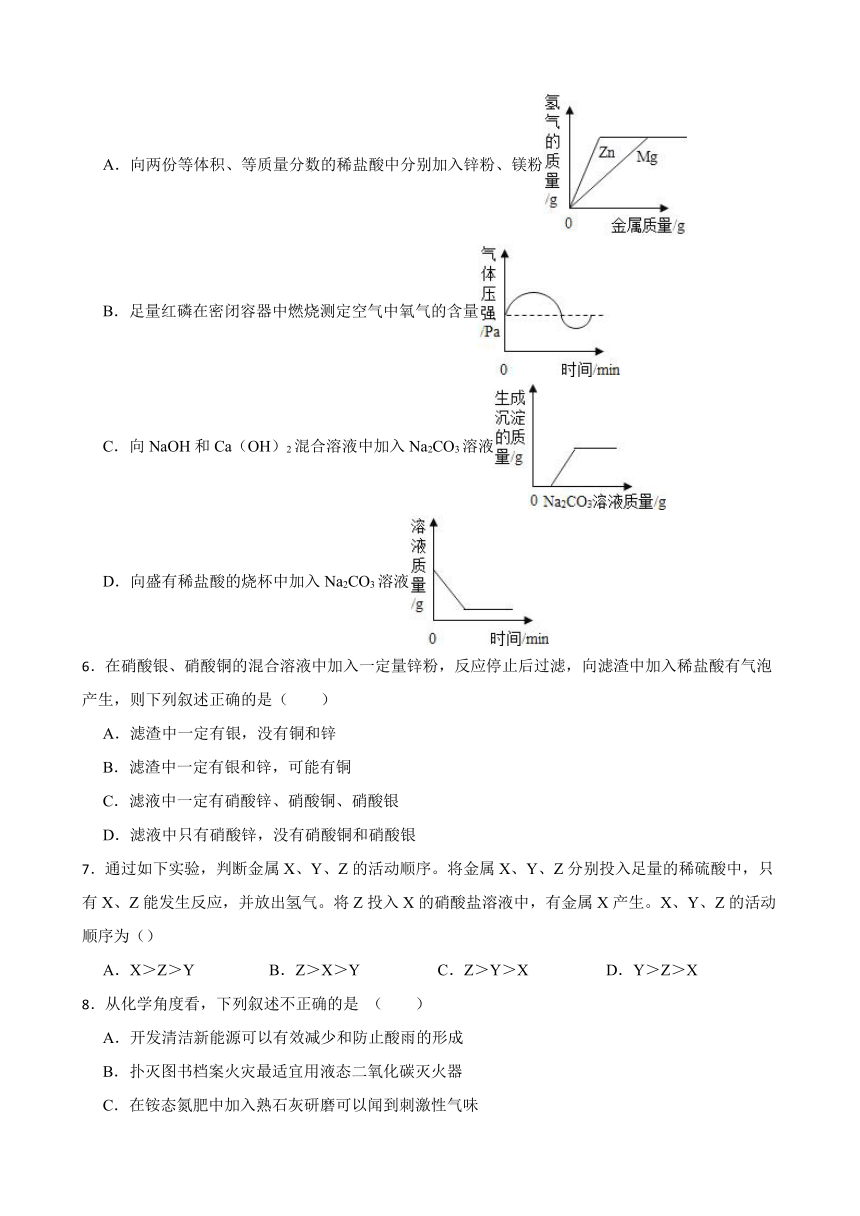
5.下列4个图象能正确反映对应变化关系的是( )
A.向两份等体积、等质量分数的稀盐酸中分别加入锌粉、镁粉
B.足量红磷在密闭容器中燃烧测定空气中氧气的含量
C.向NaOH和Ca(OH)2混合溶液中加入Na2CO3溶液
D.向盛有稀盐酸的烧杯中加入Na2CO3溶液
6.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )
A.滤渣中一定有银,没有铜和锌
B.滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中只有硝酸锌,没有硝酸铜和硝酸银
7.通过如下实验,判断金属X、Y、Z的活动顺序。将金属X、Y、Z分别投入足量的稀硫酸中,只有X、Z能发生反应,并放出氢气。将Z投入X的硝酸盐溶液中,有金属X产生。X、Y、Z的活动顺序为()
A.X>Z>Y B.Z>X>Y C.Z>Y>X D.Y>Z>X
8.从化学角度看,下列叙述不正确的是 ( )
A.开发清洁新能源可以有效减少和防止酸雨的形成
B.扑灭图书档案火灾最适宜用液态二氧化碳灭火器
C.在铵态氮肥中加入熟石灰研磨可以闻到刺激性气味
D.常用钢丝球擦洗铝壶可以使其光亮洁净和更耐用
9.现有两份等质量的铜和氧化铜的混合粉末,向其中一份通入足量的CO,反应后得到ag固体,将另一份在足量O2中充分反应,得到固体bg,则a,b的比值为( )
A.2:1 B.4:5 C.5:4 D.无法确定
10.下列有关实验现象描述正确的是( )
A.NH4NO3固体溶于水,溶液的温度升高
B.打开盛有浓盐酸试剂瓶的瓶塞,瓶口出现大量白烟
C.加热碱式碳酸铜,固体从绿色变为黑色
D.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
11.天平两边的托盘中分别装有等质量、等溶质质量分数的稀盐酸的烧杯,再将等质量的铝和铁分别加入两烧杯中,充分反应,下列说法正确的是( )
A.若天平不平衡,则指针一定偏向铝的一侧
B.若天平不平衡,则两个烧杯中的酸一定有剩余
C.若反应后两烧杯中的金属均有剩余,则天平平衡
D.若反应后两烧杯中的酸均有剩余,则天平一定平衡
12.下列事实与解释不相符的是()
A.浓氨水挥发﹣﹣分子不断运动
B.干冰升华﹣﹣分子间的间隔变大
C.稀盐酸、稀硫酸均显酸性﹣﹣溶液中都含有氢元素
D.金刚石和石墨的物理性质不同﹣﹣碳原子的排列方式不同
二、填空题
13.下列对生活中的化学现象解释正确的是 。(填序号)
①活性炭能吸附一些有颜色或气味的杂质,是因为活性炭疏松多孔表面积大
②铁制品比铝制品抗腐蚀性能差,是因为铁比铝活泼
③食品袋中充入氮气可延长食品的保质期,是因为液氮是很好的制冷剂
④火灾发生后应用湿毛巾捂住口鼻迅速逃离,是为了避免烟雾呛鼻和毒气的吸入
⑤不锈钢可以用作餐具,是因为不锈钢具有金属光泽
14.“东方之星”号客轮于2015年6月1日发生翻沉事故.6月3日为了方便用生命探测仪进行搜救,在舱底用氧炔焰对空气舱位置进行切割.
(1)氧炔焰是乙炔(C2H2)气体和氧气反应产生的高温火焰.乙炔气体属于 (填“有机物”或“无机物”).
(2)切割的舱底属于 (填“金属”或“合成”)材料.
(3)由于沉船燃料没有抽掉,切割可能导致起火,现场准备了灭火设施,可燃物燃烧的条件是 、 .
(4)二氧化碳能灭火是因为 .
A.不能燃烧,也不支持燃烧 B.能与水反应 C.密度比空气大 D.不能供给呼吸.
15.推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。请对下列错误观点举出相应的否定例证(填化学式或化学方程式)。
错误观点 否定例证
① 有单质和化合物生成的反应一定是置换反应 举例:CuO+CO Cu+CO2
②
含氧元素的化合物一定是氧化物
③
与酸反应放出气体的物质,一定是活泼金属
④
生成盐和水的反应一定是中和反应
16.人类的生产和生活都离不开金属
(1)生铁和钢中最主要的元素是 ;用铝壶烧水主要利用铝具有良好的 性.
(2)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的 .
(3)验证Zn、Cu、Ag的金属活动性顺序,可选择的试剂是 (填字母序号).
A.Zn、Ag、CuCl2溶液 B.Cu、Ag、ZnSO4溶液
C.Zn、Cu、AgNO3溶液 D.Zn、Cu、Ag、稀硫酸.
17. 某校同学以“比较锰、铁、铜3种金属的活动性”为课题进行探究。
提供的药品:铁片、铜片、锰片、稀盐酸、硫酸亚铁溶液、硫酸铜溶液、硫酸锰溶液。
【做出猜想】他们考虑到铁的活动性比铜强,对3种金属的活动性顺序作出如下猜想。
猜想一:锰>铁>铜;猜想二:铁>铜>锰;
猜想三: 。
【设计实验】为了验证猜想成立,同学们分成三组,分别针对一种猜想设计实验方案。
(1)第一组验证猜想一。实验方案是将锰片、铁片分别放入稀盐酸中,观察现象。
(2)第二组验证猜想二。实验方案是将锰片放入 中,观察现象。
(3)第三组验证猜想三。实验方案是(只用两个实验): 。
【实验及结论】各组通过实验和交流,确认猜想一是正确的。第一组同学的实验现象是: 。
【拓展探究】随后同学们对探究金属活动性的方案设计作了进一步研究。
为了验证甲、乙、丙、丁4种金属的活动性依次减弱,某同学设计了如下方案:①把甲放入乙的化合物溶液中;②把乙放入丙的化合物溶液中;③把乙放入丁的化合溶液中;④把丁放入丙的化合物溶液中。你认为哪个实验没有必要做?请说明理由。 。
18.化学与生活、生产息息相关,请运用化学知识回答以下问题.
(1)铝制品在空气中表面失去金属光泽 (用化学方程式表示).
(2)用熟石灰处理废硫酸 (用化学方程式表示).
(3)医疗上用碳酸氢钠治疗胃酸过多 (用化学方程式表示)
(4)青少年合理的饮食相当重要.例如:①猪肉中富含蛋白质、 等营养物质(营养素),但饮食过量往往会导致某些疾病的发生;②骨头汤中含有 元素,若人体缺少该元素可能导致骨骼疏松、畸形,易得佝偻病.
三、综合题
19.2015年5月12日,海西高速公路网的重要组成部分:福建省最长跨海大桥﹣﹣泉州湾大桥正式通车.大桥的建设及通行涉及到许多的化学知识.
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,钢属于 (选填“金属”或“无机非金属”)材料.
(2)工人给大桥钢铁器件喷上油漆,目的是为了防止铁与 发生反应而生锈.
(3)大桥的建成,把隔海相望的泉州环湾城市群连成一片,驱车跨跃泉州湾只需8分钟,有利于减少化石燃料的使用,从而有利于减缓 (填序号).
A.雾霾天气 B.温室效应 C.酸雨的形成.
(4)将等质量的镁、锌两种金属分别放入两份溶质质量分数相同的稀盐酸中,生成H2的质量与反应时间的关系如图所示.金属X是 (填化学式,下同),反应后一定有剩余的金属是 .
20.2019年诺贝尔化学奖授予三位科学家,因他们研制出锂电池。
(1)“无‘锂’不走天下”,锂电池改变了我们的生活。下列说法正确的是______(填序号)。
A.锂离子的相对原子质量是
B.锂原子核外电子数为3
C.锂离子电池放电时,电能转化成化学能
(2)锂被誉“21世纪的能源金属”,是世界上最轻的金属。在化学反应中容易 (填“得到”或“失去”)电子,锂离子化学符号为 。
(3)锂是一种比铁活泼的金属。锂与稀硫酸反应的化学方程式为 ,化学基本反应类型为 反应。
(4)高性能锂空气电池的反应原理: ,二氧化锰是反应中的 (填“反应物”、“生成物”或“催化剂”)。
(5)扬州纯电动公交车使用磷酸亚铁锂(LiFePO4)电池,磷酸亚铁锂中非金属元素的原子个数比为 ,锂、铁元素的质量比为 ,铁元素的质量分数为 (精确到0.1%)。
(6)储氢材料也会用到锂,氢化锂(LiH)可用于储存氢气,氢化锂与水反应生成氢氧化锂(LiOH)和一种可燃性气体,该反应的化学反应方程式为 。
21.厉害了,我的国!“中国智慧”“中国制造”誉满全球,图一为2022年冬奥会闭幕式上,演员穿着熊猫木偶服饰进行轮滑表演,图二为“复兴号”铝合金车体。
(1)如图一,制作熊猫木偶服饰中的材料中,属于合成材料的是 。
(2)铜丝线用于连接LED灯,主要是利用其 性;铁生锈的条件是铁与 同时接触。金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是 (填序号)。
A.齿轮表面涂油 B.钢刀浸泡在盐水中 C.车圈镀铬
(3)在空气中,铝表面生成一层致密的氧化膜,写出反应的化学方程式 。
(4)为比较X、Y、Z三种金属活动性大小,进行如下实验。则X、Y、Z三种金属的活动性由强到弱的顺序是____(填序号)。
A.Z>Y>X B.X>Y>Z C.Y>X>Z D.Y>Z>X
(5)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青(硫酸铜溶液)得铁则化为铜”,请你写出与之相关的一个反应的化学方程式 ,其基本反应类型是 。
22.用下图装置研究酸、碱的性质。
(1)向1中滴加Na2CO3溶液,观察到的现象是 。
(2)向2、3中滴加无色酚酞溶液,溶液变红的是 (填序号);再向3中滴加NaOH溶液,NaOH与盐酸反应的化学方程式为 。
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】D
4.【答案】B
5.【答案】D
6.【答案】D
7.【答案】B
8.【答案】D
9.【答案】B
10.【答案】C
11.【答案】C
12.【答案】C
13.【答案】①④
14.【答案】有机物;金属;与氧气或空气接触;温度必须达到燃烧所需的最低温度即着火点;AC
15.【答案】C2H5OH或Na2CO3;Na2CO3或NaHCO3;Fe2O3+6HCl=2FeCl3+3H2O 或2NaOH+CO2=Na2CO3+H2O
16.【答案】铁元素;导热;氧化铝保护膜;A
17.【答案】铁>锰>铜;硫酸铜溶液;将铁片、铜片分别插入硫酸锰溶液中或将锰片分别插入硫酸亚铁溶液、硫酸铜溶液中;铁片和锰片表面都有气泡产生,且锰片表面的气泡比铁片多;③通过①②④三个实验就可以判断出甲、乙、丙、丁4种金属的活动性
18.【答案】4Al+3O2=2Al2O3;Ca(OH)2+H2SO4═CaSO4↓+2H2O;NaHCO3+HCl═NaCl+H2O+CO2↑;油脂;钙
19.【答案】(1)金属
(2)水和氧气
(3)B
(4)Mg;镁
20.【答案】(1)B
(2)失去;
(3);置换
(4)催化剂
(5)1:4;1:8;
(6)
21.【答案】(1)塑料
(2)导电;水和氧气;B
(3)
(4)B
(5);置换反应
22.【答案】(1)澄清石灰水变浑浊
(2)2;NaOH+HCl=NaCl+H2O
一、单选题
1.将质量相等的A,B,C三种金属,同时分别放入三份溶质质量分数相同且足量的稀盐酸中,反应生成H2的质量与反应时间的关系如图所示.根据图中所提供的信息,得出的结论正确的是.(已知:A,B,C在生成物中均为+2价)( )
A.放出H2的质量是B>C>A B.金属活动性顺序是A>B>C
C.反应速率最大的是A D.相对原子质量是C>B>A
2.物质的性质在很大程度上决定了物质的用途,下列物质的性质与用途对应关系错误的是( )
A.金刚石的硬度很大﹣﹣切割玻璃
B.氧气具有助燃性﹣﹣富氧炼钢
C.氢气具有可燃性﹣﹣作燃料
D.铜具有导热性﹣﹣作电线
3.下列有关金属及合金的说法错误的是( )
A.金属在常温下大多数都是固体
B.钨制灯丝是利用钨的熔点高
C.不锈钢可用于制造医疗器械
D.铁是地壳中含量最多的金属元素
4.化学的学习使我们学会了从微观的角度想,下列对宏观现象解释不正确的是( )。
A.水变为水蒸气体积变大﹣分子间间隔增大
B.干冰升华﹣分子的体积变大
C.氧化汞受热分解﹣分子在化学变化中可以再分
D.闻到远处花香﹣分子在不断地运动
5.下列4个图象能正确反映对应变化关系的是( )
A.向两份等体积、等质量分数的稀盐酸中分别加入锌粉、镁粉
B.足量红磷在密闭容器中燃烧测定空气中氧气的含量
C.向NaOH和Ca(OH)2混合溶液中加入Na2CO3溶液
D.向盛有稀盐酸的烧杯中加入Na2CO3溶液
6.在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,向滤渣中加入稀盐酸有气泡产生,则下列叙述正确的是( )
A.滤渣中一定有银,没有铜和锌
B.滤渣中一定有银和锌,可能有铜
C.滤液中一定有硝酸锌、硝酸铜、硝酸银
D.滤液中只有硝酸锌,没有硝酸铜和硝酸银
7.通过如下实验,判断金属X、Y、Z的活动顺序。将金属X、Y、Z分别投入足量的稀硫酸中,只有X、Z能发生反应,并放出氢气。将Z投入X的硝酸盐溶液中,有金属X产生。X、Y、Z的活动顺序为()
A.X>Z>Y B.Z>X>Y C.Z>Y>X D.Y>Z>X
8.从化学角度看,下列叙述不正确的是 ( )
A.开发清洁新能源可以有效减少和防止酸雨的形成
B.扑灭图书档案火灾最适宜用液态二氧化碳灭火器
C.在铵态氮肥中加入熟石灰研磨可以闻到刺激性气味
D.常用钢丝球擦洗铝壶可以使其光亮洁净和更耐用
9.现有两份等质量的铜和氧化铜的混合粉末,向其中一份通入足量的CO,反应后得到ag固体,将另一份在足量O2中充分反应,得到固体bg,则a,b的比值为( )
A.2:1 B.4:5 C.5:4 D.无法确定
10.下列有关实验现象描述正确的是( )
A.NH4NO3固体溶于水,溶液的温度升高
B.打开盛有浓盐酸试剂瓶的瓶塞,瓶口出现大量白烟
C.加热碱式碳酸铜,固体从绿色变为黑色
D.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
11.天平两边的托盘中分别装有等质量、等溶质质量分数的稀盐酸的烧杯,再将等质量的铝和铁分别加入两烧杯中,充分反应,下列说法正确的是( )
A.若天平不平衡,则指针一定偏向铝的一侧
B.若天平不平衡,则两个烧杯中的酸一定有剩余
C.若反应后两烧杯中的金属均有剩余,则天平平衡
D.若反应后两烧杯中的酸均有剩余,则天平一定平衡
12.下列事实与解释不相符的是()
A.浓氨水挥发﹣﹣分子不断运动
B.干冰升华﹣﹣分子间的间隔变大
C.稀盐酸、稀硫酸均显酸性﹣﹣溶液中都含有氢元素
D.金刚石和石墨的物理性质不同﹣﹣碳原子的排列方式不同
二、填空题
13.下列对生活中的化学现象解释正确的是 。(填序号)
①活性炭能吸附一些有颜色或气味的杂质,是因为活性炭疏松多孔表面积大
②铁制品比铝制品抗腐蚀性能差,是因为铁比铝活泼
③食品袋中充入氮气可延长食品的保质期,是因为液氮是很好的制冷剂
④火灾发生后应用湿毛巾捂住口鼻迅速逃离,是为了避免烟雾呛鼻和毒气的吸入
⑤不锈钢可以用作餐具,是因为不锈钢具有金属光泽
14.“东方之星”号客轮于2015年6月1日发生翻沉事故.6月3日为了方便用生命探测仪进行搜救,在舱底用氧炔焰对空气舱位置进行切割.
(1)氧炔焰是乙炔(C2H2)气体和氧气反应产生的高温火焰.乙炔气体属于 (填“有机物”或“无机物”).
(2)切割的舱底属于 (填“金属”或“合成”)材料.
(3)由于沉船燃料没有抽掉,切割可能导致起火,现场准备了灭火设施,可燃物燃烧的条件是 、 .
(4)二氧化碳能灭火是因为 .
A.不能燃烧,也不支持燃烧 B.能与水反应 C.密度比空气大 D.不能供给呼吸.
15.推理是学习化学的一种重要方法,但不合理的推理会得出错误的结论。请对下列错误观点举出相应的否定例证(填化学式或化学方程式)。
错误观点 否定例证
① 有单质和化合物生成的反应一定是置换反应 举例:CuO+CO Cu+CO2
②
含氧元素的化合物一定是氧化物
③
与酸反应放出气体的物质,一定是活泼金属
④
生成盐和水的反应一定是中和反应
16.人类的生产和生活都离不开金属
(1)生铁和钢中最主要的元素是 ;用铝壶烧水主要利用铝具有良好的 性.
(2)铝制品有良好的抗腐蚀性,其原因是在空气中铝的表面易形成致密的 .
(3)验证Zn、Cu、Ag的金属活动性顺序,可选择的试剂是 (填字母序号).
A.Zn、Ag、CuCl2溶液 B.Cu、Ag、ZnSO4溶液
C.Zn、Cu、AgNO3溶液 D.Zn、Cu、Ag、稀硫酸.
17. 某校同学以“比较锰、铁、铜3种金属的活动性”为课题进行探究。
提供的药品:铁片、铜片、锰片、稀盐酸、硫酸亚铁溶液、硫酸铜溶液、硫酸锰溶液。
【做出猜想】他们考虑到铁的活动性比铜强,对3种金属的活动性顺序作出如下猜想。
猜想一:锰>铁>铜;猜想二:铁>铜>锰;
猜想三: 。
【设计实验】为了验证猜想成立,同学们分成三组,分别针对一种猜想设计实验方案。
(1)第一组验证猜想一。实验方案是将锰片、铁片分别放入稀盐酸中,观察现象。
(2)第二组验证猜想二。实验方案是将锰片放入 中,观察现象。
(3)第三组验证猜想三。实验方案是(只用两个实验): 。
【实验及结论】各组通过实验和交流,确认猜想一是正确的。第一组同学的实验现象是: 。
【拓展探究】随后同学们对探究金属活动性的方案设计作了进一步研究。
为了验证甲、乙、丙、丁4种金属的活动性依次减弱,某同学设计了如下方案:①把甲放入乙的化合物溶液中;②把乙放入丙的化合物溶液中;③把乙放入丁的化合溶液中;④把丁放入丙的化合物溶液中。你认为哪个实验没有必要做?请说明理由。 。
18.化学与生活、生产息息相关,请运用化学知识回答以下问题.
(1)铝制品在空气中表面失去金属光泽 (用化学方程式表示).
(2)用熟石灰处理废硫酸 (用化学方程式表示).
(3)医疗上用碳酸氢钠治疗胃酸过多 (用化学方程式表示)
(4)青少年合理的饮食相当重要.例如:①猪肉中富含蛋白质、 等营养物质(营养素),但饮食过量往往会导致某些疾病的发生;②骨头汤中含有 元素,若人体缺少该元素可能导致骨骼疏松、畸形,易得佝偻病.
三、综合题
19.2015年5月12日,海西高速公路网的重要组成部分:福建省最长跨海大桥﹣﹣泉州湾大桥正式通车.大桥的建设及通行涉及到许多的化学知识.
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,钢属于 (选填“金属”或“无机非金属”)材料.
(2)工人给大桥钢铁器件喷上油漆,目的是为了防止铁与 发生反应而生锈.
(3)大桥的建成,把隔海相望的泉州环湾城市群连成一片,驱车跨跃泉州湾只需8分钟,有利于减少化石燃料的使用,从而有利于减缓 (填序号).
A.雾霾天气 B.温室效应 C.酸雨的形成.
(4)将等质量的镁、锌两种金属分别放入两份溶质质量分数相同的稀盐酸中,生成H2的质量与反应时间的关系如图所示.金属X是 (填化学式,下同),反应后一定有剩余的金属是 .
20.2019年诺贝尔化学奖授予三位科学家,因他们研制出锂电池。
(1)“无‘锂’不走天下”,锂电池改变了我们的生活。下列说法正确的是______(填序号)。
A.锂离子的相对原子质量是
B.锂原子核外电子数为3
C.锂离子电池放电时,电能转化成化学能
(2)锂被誉“21世纪的能源金属”,是世界上最轻的金属。在化学反应中容易 (填“得到”或“失去”)电子,锂离子化学符号为 。
(3)锂是一种比铁活泼的金属。锂与稀硫酸反应的化学方程式为 ,化学基本反应类型为 反应。
(4)高性能锂空气电池的反应原理: ,二氧化锰是反应中的 (填“反应物”、“生成物”或“催化剂”)。
(5)扬州纯电动公交车使用磷酸亚铁锂(LiFePO4)电池,磷酸亚铁锂中非金属元素的原子个数比为 ,锂、铁元素的质量比为 ,铁元素的质量分数为 (精确到0.1%)。
(6)储氢材料也会用到锂,氢化锂(LiH)可用于储存氢气,氢化锂与水反应生成氢氧化锂(LiOH)和一种可燃性气体,该反应的化学反应方程式为 。
21.厉害了,我的国!“中国智慧”“中国制造”誉满全球,图一为2022年冬奥会闭幕式上,演员穿着熊猫木偶服饰进行轮滑表演,图二为“复兴号”铝合金车体。
(1)如图一,制作熊猫木偶服饰中的材料中,属于合成材料的是 。
(2)铜丝线用于连接LED灯,主要是利用其 性;铁生锈的条件是铁与 同时接触。金属腐蚀造成的损失巨大,对金属腐蚀的控制尤为重要。下列对金属的防护措施不合理的是 (填序号)。
A.齿轮表面涂油 B.钢刀浸泡在盐水中 C.车圈镀铬
(3)在空气中,铝表面生成一层致密的氧化膜,写出反应的化学方程式 。
(4)为比较X、Y、Z三种金属活动性大小,进行如下实验。则X、Y、Z三种金属的活动性由强到弱的顺序是____(填序号)。
A.Z>Y>X B.X>Y>Z C.Y>X>Z D.Y>Z>X
(5)我国早在西汉时期就有“湿法炼铜”的记载,在《淮南万毕术》一书中就写道“曾青(硫酸铜溶液)得铁则化为铜”,请你写出与之相关的一个反应的化学方程式 ,其基本反应类型是 。
22.用下图装置研究酸、碱的性质。
(1)向1中滴加Na2CO3溶液,观察到的现象是 。
(2)向2、3中滴加无色酚酞溶液,溶液变红的是 (填序号);再向3中滴加NaOH溶液,NaOH与盐酸反应的化学方程式为 。
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】D
4.【答案】B
5.【答案】D
6.【答案】D
7.【答案】B
8.【答案】D
9.【答案】B
10.【答案】C
11.【答案】C
12.【答案】C
13.【答案】①④
14.【答案】有机物;金属;与氧气或空气接触;温度必须达到燃烧所需的最低温度即着火点;AC
15.【答案】C2H5OH或Na2CO3;Na2CO3或NaHCO3;Fe2O3+6HCl=2FeCl3+3H2O 或2NaOH+CO2=Na2CO3+H2O
16.【答案】铁元素;导热;氧化铝保护膜;A
17.【答案】铁>锰>铜;硫酸铜溶液;将铁片、铜片分别插入硫酸锰溶液中或将锰片分别插入硫酸亚铁溶液、硫酸铜溶液中;铁片和锰片表面都有气泡产生,且锰片表面的气泡比铁片多;③通过①②④三个实验就可以判断出甲、乙、丙、丁4种金属的活动性
18.【答案】4Al+3O2=2Al2O3;Ca(OH)2+H2SO4═CaSO4↓+2H2O;NaHCO3+HCl═NaCl+H2O+CO2↑;油脂;钙
19.【答案】(1)金属
(2)水和氧气
(3)B
(4)Mg;镁
20.【答案】(1)B
(2)失去;
(3);置换
(4)催化剂
(5)1:4;1:8;
(6)
21.【答案】(1)塑料
(2)导电;水和氧气;B
(3)
(4)B
(5);置换反应
22.【答案】(1)澄清石灰水变浑浊
(2)2;NaOH+HCl=NaCl+H2O
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
