8.3 酸和碱的反应 同步练习(含答案) 2022-2023学年科粤版九年级下册化学
文档属性
| 名称 | 8.3 酸和碱的反应 同步练习(含答案) 2022-2023学年科粤版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 115.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览



文档简介
8.3 酸和碱的反应 同步练习
一、单选题
1.下列有关汽水的说法正确的是( )
A.胃酸过多的人要多喝汽水
B.汽水的pH为3~4,它显碱性
C.CO2易溶于水,所以用来制汽水
D.打开汽水瓶盖时,有大量气泡冒出,说明气体的溶解度随压强减小而减小
2.下列实验现象描述不正确的是( )
A.镁与稀盐酸反应产生气体,放出热量
B.加热碱式碳酸铜,固体慢慢从绿色变成黑色
C.氢氧化钠溶液和硫酸铜溶液混合后产生蓝色沉淀
D.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
3.物质都是由微粒构成的,下列物质由分子构成的是( )
A.氯化钠 B.干冰 C.金刚石 D.铜
4.水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到l 6 5K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
A.同温度同质量液态水和玻璃态水,体积不同
B.玻璃态水不属于氧化物
C.玻璃态水和普通水的化学性质相同
D.玻璃态水分子不运动
5.关于化学反应X+Y=Z+R,下列说法正确的是( )
A.若生成物Z和R分别是盐和水,则反应物一定是酸和碱
B.若该反应是置换反应,Y和R是化合物,X是金属单质,则Z一定是金属单质
C.若X是可溶性碱,Y是可溶性盐,则Z和R可能是两种沉淀
D.若X、Y各取10g混合,使其充分反应,则Z、R质量之和一定为20g
6.为完全中和某一盐酸溶液,需用10克质量分数为10%的NaOH溶液,如果改用10克质量分数为10%的KOH溶液,反应后的pH值( )
A.大于7 B.小于7 C.等于7 D.无法判断
7.下列实验方案不能达到实验目的是( )
A. 探究影响溶解性的因素
B. 证明可燃物燃烧需要氧气
C. 证明二氧化碳能溶于水
D. 比较Fe、Ag、Zn的金属活动性
8.被蚊虫叮咬后,蚊虫分泌出蚁酸使皮肤痛痒,涂抹碱性物质能减轻痛痒。被蚊虫叮咬后,为减轻痛痒,宜涂抹的物质是( )
选项 A B C D
常见物质 葡萄汁 牛奶 苹果汁 牙膏
pH 3.5 —4.5 6.3—6.6 3.0 9.0
A.A B.B C.C D.D
9.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法错误的是( )
物质 a b c d
反应前质量(g) 10 10 10 2
反应后质量(g) 待测 2 21 2
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量“待测”为3g
10.在含石蕊试液的氢氧化钠溶液中逐滴滴加稀硫酸至过量,溶液颜色的变化顺序是( )
A..蓝色﹣紫色﹣红色 B..蓝色﹣红色﹣紫色
C..紫色﹣红色﹣无色 D..紫色﹣蓝色﹣红色
11.除去下列物质所含少量杂质,所用试剂或方法不正确的是( )
选项 物质 所含杂质 试剂或方法
A N2 O2 通过足量灼热的铜网
B CO2 CO 通入O2,点燃
C 铜粉 铁粉 加足量盐酸,过滤、洗涤、干燥
D MnO2 KCl 加水过滤、洗涤、干燥
A.A B.B C.C D.D
12.归纳整理是学习化学的重要方法,下面知识归纳正确的是( )
A.纯碱、烧碱都属于碱类
B.有氧气参加的反应一定是氧化反应
C.分解反应的生成物一定是两种
D.生成盐和水的反应一定是中和反应
二、填空题
13.在氢气还原氧化铜的反应中,氢元素的化合价由零价升高至+1价,氢气是还原剂;铜元素的化合价从+2价降低至零价,氧化铜是氧化剂.则在2Na+CL2 2NaCL反应中, 元素化合价升高, 元素化合价降低; 是氧化剂, 是还原剂.
14.盐酸、硫酸、氢氧化钠和氢氧化钙时初中化学中常见的物质,它们由着较广泛的用途.
(1)酸与碱之间能发生 反应.
(2)氢氧化钙可以用来调节土壤的 性,它的水溶液常用来检验 气体的存在.
(3)一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该溶液的pH(填“>”、“<”或“=”) 7.要准确测定该溶液的pH,需要用到的仪器是 .
15.目前衡阳市区很多的出租车和公交车都用压缩天然气代替汽油,大大降低了汽车尾气的排放量,减缓了对环境污染的压力,则天然气属于 (填“可再生”或“不可再生”)能源.其主要成分是 (填化学式),写出天然气在空气中完全燃烧时的化学方程式 .
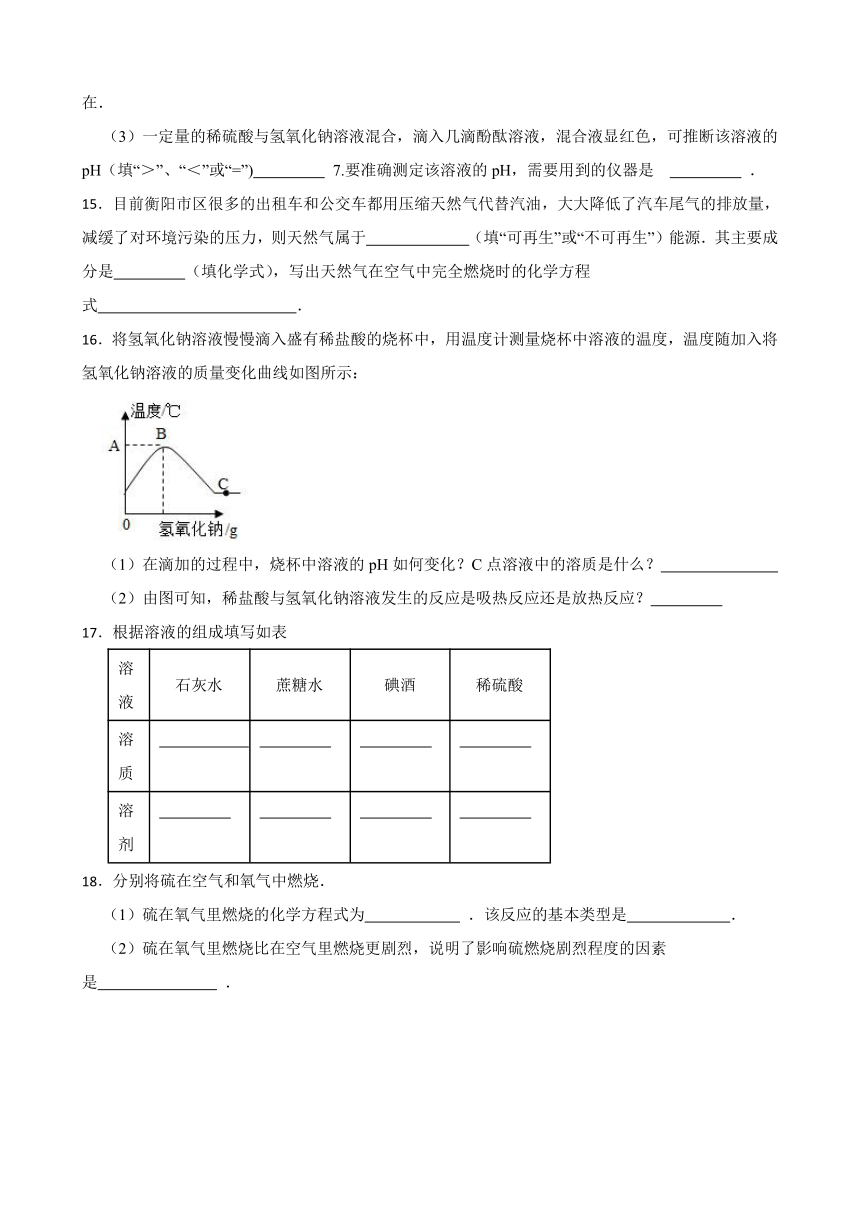
16.将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入将氢氧化钠溶液的质量变化曲线如图所示:
(1)在滴加的过程中,烧杯中溶液的pH如何变化?C点溶液中的溶质是什么?
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是吸热反应还是放热反应?
17.根据溶液的组成填写如表
溶液 石灰水 蔗糖水 碘酒 稀硫酸
溶质
溶剂
18.分别将硫在空气和氧气中燃烧.
(1)硫在氧气里燃烧的化学方程式为 .该反应的基本类型是 .
(2)硫在氧气里燃烧比在空气里燃烧更剧烈,说明了影响硫燃烧剧烈程度的因素是 .
三、综合题
19.动手学化学是一种很好的学习方法.请根据实验回答下列问题.
(1)测得碳酸饮料的pH (填“<”、“=”或“>”)7.
(2)下列使用pH试纸的方法中,正确的是 (填字母).
A.将pH试纸直接插入待测液中
B.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
C.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.读数时,将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图所示的四种常见错误操作.请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法序号为 .
(4)下列溶液pH>7的是 .
A. Na2CO3 B.HCl C. NaCl D. KNO3
20.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),完成下列问题:
(1)该反应产生的CO2气体质量为 g.
(2)计算反应后所得溶液中溶质质量分数(写出计算过程).
21.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
(1)三种物质中 (填“甲”、“乙”或“丙”)的溶解度随温度变化的趋势与气体溶解度随温度变化的趋势相似。
(2)将t2℃时甲、乙两物质的饱和溶液分别蒸发等质量的水,析出固体的质量:甲 (填“>”、“<”或“=”)乙。
(3)若甲的饱和溶液中混有少量乙,可采用的 方法提纯甲。
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为 。
22.归纳总结是学习知识的重要方法。小军同学用图1总结了NaOH的四条化学性质。
(1)验证反应①:将紫色石蕊溶液滴入NaOH溶液中,溶液会变成 色。
(2)图2利用微观示意图来说明反应③的发生,请写出该反应的化学方程式: ;从该图还可以看出,反应后的溶液pH 7(填“>”、“=”或“<”)。
(3)如果反应④能够发生,你选择的物质是________(填序号)。
A.HCl
B.Na2CO3
C.CuSO4
(4)另外,NaOH溶液还能与某些金属(如Al)发生反应。请配平该反应的化学方程式: NaOH+ H2O+ Al= NaAlO2+ H2↑。
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】B
4.【答案】C
5.【答案】C
6.【答案】B
7.【答案】A
8.【答案】D
9.【答案】D
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】钠;氯;Cl2;Na
14.【答案】中和;酸;二氧化碳;>;pH计
15.【答案】不可再生;CH4;CH4 + 2O2 CO2 + 2H2O
16.【答案】(1)从小于7逐渐变化到大于7,氢氧化钠和氯化钠
(2)放热
17.【答案】氢氧化钙;蔗糖;碘;硫酸;水;水;酒精;水
18.【答案】S+O2SO2;化合反应;氧气的浓度
19.【答案】(1)<
(2)BD
(3)图③滴瓶上的滴管不用清洗直接放回原瓶
(4)A
20.【答案】(1)4.4
(2)解:设碳酸钠的质量为x,生成氯化钠的质量为y,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
== ,
x=10.6g,y=11.7g,
反应后所得溶液中溶质氯化钠的质量分数为: ×100%=11.7%,
答:反应后所得溶液中溶质氯化钠的质量分数为11.7%.
21.【答案】(1)丙
(2)>
(3)冷却热的饱和溶液或降温结晶
(4)丙>乙>甲
22.【答案】(1)蓝
(2);=
(3)C
(4)2;2;2;2;3
一、单选题
1.下列有关汽水的说法正确的是( )
A.胃酸过多的人要多喝汽水
B.汽水的pH为3~4,它显碱性
C.CO2易溶于水,所以用来制汽水
D.打开汽水瓶盖时,有大量气泡冒出,说明气体的溶解度随压强减小而减小
2.下列实验现象描述不正确的是( )
A.镁与稀盐酸反应产生气体,放出热量
B.加热碱式碳酸铜,固体慢慢从绿色变成黑色
C.氢氧化钠溶液和硫酸铜溶液混合后产生蓝色沉淀
D.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
3.物质都是由微粒构成的,下列物质由分子构成的是( )
A.氯化钠 B.干冰 C.金刚石 D.铜
4.水的状态除了气、液和固态外,还有玻璃态.它是由液态水急速冷却到l 6 5K时形成的,玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
A.同温度同质量液态水和玻璃态水,体积不同
B.玻璃态水不属于氧化物
C.玻璃态水和普通水的化学性质相同
D.玻璃态水分子不运动
5.关于化学反应X+Y=Z+R,下列说法正确的是( )
A.若生成物Z和R分别是盐和水,则反应物一定是酸和碱
B.若该反应是置换反应,Y和R是化合物,X是金属单质,则Z一定是金属单质
C.若X是可溶性碱,Y是可溶性盐,则Z和R可能是两种沉淀
D.若X、Y各取10g混合,使其充分反应,则Z、R质量之和一定为20g
6.为完全中和某一盐酸溶液,需用10克质量分数为10%的NaOH溶液,如果改用10克质量分数为10%的KOH溶液,反应后的pH值( )
A.大于7 B.小于7 C.等于7 D.无法判断
7.下列实验方案不能达到实验目的是( )
A. 探究影响溶解性的因素
B. 证明可燃物燃烧需要氧气
C. 证明二氧化碳能溶于水
D. 比较Fe、Ag、Zn的金属活动性
8.被蚊虫叮咬后,蚊虫分泌出蚁酸使皮肤痛痒,涂抹碱性物质能减轻痛痒。被蚊虫叮咬后,为减轻痛痒,宜涂抹的物质是( )
选项 A B C D
常见物质 葡萄汁 牛奶 苹果汁 牙膏
pH 3.5 —4.5 6.3—6.6 3.0 9.0
A.A B.B C.C D.D
9.在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如表所示,下列说法错误的是( )
物质 a b c d
反应前质量(g) 10 10 10 2
反应后质量(g) 待测 2 21 2
A.该反应是化合反应,d可能是催化剂
B.a、b两种物质中元素种类一定与c物质中元素种类相同
C.b物质可能是单质
D.反应后a物质的质量“待测”为3g
10.在含石蕊试液的氢氧化钠溶液中逐滴滴加稀硫酸至过量,溶液颜色的变化顺序是( )
A..蓝色﹣紫色﹣红色 B..蓝色﹣红色﹣紫色
C..紫色﹣红色﹣无色 D..紫色﹣蓝色﹣红色
11.除去下列物质所含少量杂质,所用试剂或方法不正确的是( )
选项 物质 所含杂质 试剂或方法
A N2 O2 通过足量灼热的铜网
B CO2 CO 通入O2,点燃
C 铜粉 铁粉 加足量盐酸,过滤、洗涤、干燥
D MnO2 KCl 加水过滤、洗涤、干燥
A.A B.B C.C D.D
12.归纳整理是学习化学的重要方法,下面知识归纳正确的是( )
A.纯碱、烧碱都属于碱类
B.有氧气参加的反应一定是氧化反应
C.分解反应的生成物一定是两种
D.生成盐和水的反应一定是中和反应
二、填空题
13.在氢气还原氧化铜的反应中,氢元素的化合价由零价升高至+1价,氢气是还原剂;铜元素的化合价从+2价降低至零价,氧化铜是氧化剂.则在2Na+CL2 2NaCL反应中, 元素化合价升高, 元素化合价降低; 是氧化剂, 是还原剂.
14.盐酸、硫酸、氢氧化钠和氢氧化钙时初中化学中常见的物质,它们由着较广泛的用途.
(1)酸与碱之间能发生 反应.
(2)氢氧化钙可以用来调节土壤的 性,它的水溶液常用来检验 气体的存在.
(3)一定量的稀硫酸与氢氧化钠溶液混合,滴入几滴酚酞溶液,混合液显红色,可推断该溶液的pH(填“>”、“<”或“=”) 7.要准确测定该溶液的pH,需要用到的仪器是 .
15.目前衡阳市区很多的出租车和公交车都用压缩天然气代替汽油,大大降低了汽车尾气的排放量,减缓了对环境污染的压力,则天然气属于 (填“可再生”或“不可再生”)能源.其主要成分是 (填化学式),写出天然气在空气中完全燃烧时的化学方程式 .
16.将氢氧化钠溶液慢慢滴入盛有稀盐酸的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入将氢氧化钠溶液的质量变化曲线如图所示:
(1)在滴加的过程中,烧杯中溶液的pH如何变化?C点溶液中的溶质是什么?
(2)由图可知,稀盐酸与氢氧化钠溶液发生的反应是吸热反应还是放热反应?
17.根据溶液的组成填写如表
溶液 石灰水 蔗糖水 碘酒 稀硫酸
溶质
溶剂
18.分别将硫在空气和氧气中燃烧.
(1)硫在氧气里燃烧的化学方程式为 .该反应的基本类型是 .
(2)硫在氧气里燃烧比在空气里燃烧更剧烈,说明了影响硫燃烧剧烈程度的因素是 .
三、综合题
19.动手学化学是一种很好的学习方法.请根据实验回答下列问题.
(1)测得碳酸饮料的pH (填“<”、“=”或“>”)7.
(2)下列使用pH试纸的方法中,正确的是 (填字母).
A.将pH试纸直接插入待测液中
B.将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
C.将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上
D.读数时,将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图所示的四种常见错误操作.请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法序号为 .
(4)下列溶液pH>7的是 .
A. Na2CO3 B.HCl C. NaCl D. KNO3
20.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),完成下列问题:
(1)该反应产生的CO2气体质量为 g.
(2)计算反应后所得溶液中溶质质量分数(写出计算过程).
21.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
(1)三种物质中 (填“甲”、“乙”或“丙”)的溶解度随温度变化的趋势与气体溶解度随温度变化的趋势相似。
(2)将t2℃时甲、乙两物质的饱和溶液分别蒸发等质量的水,析出固体的质量:甲 (填“>”、“<”或“=”)乙。
(3)若甲的饱和溶液中混有少量乙,可采用的 方法提纯甲。
(4)将t3℃时等质量的甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶剂质量由大到小的顺序为 。
22.归纳总结是学习知识的重要方法。小军同学用图1总结了NaOH的四条化学性质。
(1)验证反应①:将紫色石蕊溶液滴入NaOH溶液中,溶液会变成 色。
(2)图2利用微观示意图来说明反应③的发生,请写出该反应的化学方程式: ;从该图还可以看出,反应后的溶液pH 7(填“>”、“=”或“<”)。
(3)如果反应④能够发生,你选择的物质是________(填序号)。
A.HCl
B.Na2CO3
C.CuSO4
(4)另外,NaOH溶液还能与某些金属(如Al)发生反应。请配平该反应的化学方程式: NaOH+ H2O+ Al= NaAlO2+ H2↑。
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】B
4.【答案】C
5.【答案】C
6.【答案】B
7.【答案】A
8.【答案】D
9.【答案】D
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】钠;氯;Cl2;Na
14.【答案】中和;酸;二氧化碳;>;pH计
15.【答案】不可再生;CH4;CH4 + 2O2 CO2 + 2H2O
16.【答案】(1)从小于7逐渐变化到大于7,氢氧化钠和氯化钠
(2)放热
17.【答案】氢氧化钙;蔗糖;碘;硫酸;水;水;酒精;水
18.【答案】S+O2SO2;化合反应;氧气的浓度
19.【答案】(1)<
(2)BD
(3)图③滴瓶上的滴管不用清洗直接放回原瓶
(4)A
20.【答案】(1)4.4
(2)解:设碳酸钠的质量为x,生成氯化钠的质量为y,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
== ,
x=10.6g,y=11.7g,
反应后所得溶液中溶质氯化钠的质量分数为: ×100%=11.7%,
答:反应后所得溶液中溶质氯化钠的质量分数为11.7%.
21.【答案】(1)丙
(2)>
(3)冷却热的饱和溶液或降温结晶
(4)丙>乙>甲
22.【答案】(1)蓝
(2);=
(3)C
(4)2;2;2;2;3
