10.2 酸和碱的中和反应 同步练习(含答案) 2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 10.2 酸和碱的中和反应 同步练习(含答案) 2022-2023学年人教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 73.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览



文档简介
10.2 酸和碱的中和反应 同步练习
一、单选题
1.下列有关实验的叙述正确的是( )
A.用pH试纸测得未知溶液的酸碱度时,应将pH试纸预先用水湿润
B.实验室用高锰酸钾制取O2,在实验结束时应先停止加热,再将导管移出水面
C.稀释浓硫酸时,要把浓硫酸缓慢注入盛有水的烧杯中,并用玻璃棒不断搅拌
D.在粗盐提纯实验中,蒸发溶剂时,待水全部蒸干后,再停止加热
2.下列化学反应属于中和反应的是( )
A.CaO+2HCl=CaCl2+H2O B.Ca(OH )2+2HCl=CaCl2+2H2O
C.CaCO3+2HCl=CaCl2+H2O+CO2↑ D.2NaOH+CO2=Na2CO3+H2O
3.下列推理正确的是( )
A.向某无色溶液中滴加酚酞无现象,则溶液一定呈中性
B.原子核由质子和中子构成,但并不是所有的原子核中都含有质子和中子
C.在同一化合物中,金属元素显正价,则非金属元素一定显负价
D.酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应
4.下列类比或推理正确的是( )
A.浓盐酸有挥发性,所以浓硫酸也有挥发性
B.酸雨是酸性的,所以pH<7的雨水称为酸雨
C.洗涤剂去油污是利用了乳化作用,所以汽油去油污也是利用了乳化作用
D.同种元素的原子具有相同质子数,所以具有相同质子数的原子为同种元素
5.推理是学习化学的一种重要方法.根据下列实验事实推理出结论正确的是( )
编号 实验事实 实验结论
A 某溶液使石蕊溶液变红 该溶液一定是稀盐酸
B 经测定某物质中含有氧元素 该物质一定是氧化物
C 常温下,测定某溶液的pH=12 该溶液一定呈碱性
D 某粒子带有电荷 该粒子一定是离子
A.A B.B C.C D.D
6.某化学课外活动小组开展下列实验活动:取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔5分钟测一次pH,其数据如下表所示。下列对测定结果的分析中正确的是( )
测定时刻 17∶05 17∶10 17∶15 17∶20 17∶25 17∶30 17∶35
pH 4.95 4.94 4.92 4.88 4.86 4.85 4.85
A.在测定期间,该雨水的酸性逐渐减弱
B.该雨水对农作物的生长没有影响
C.若在17:40测定,pH一定小于4.85
D.pH=4.95与某些工厂排放的酸性气体有关
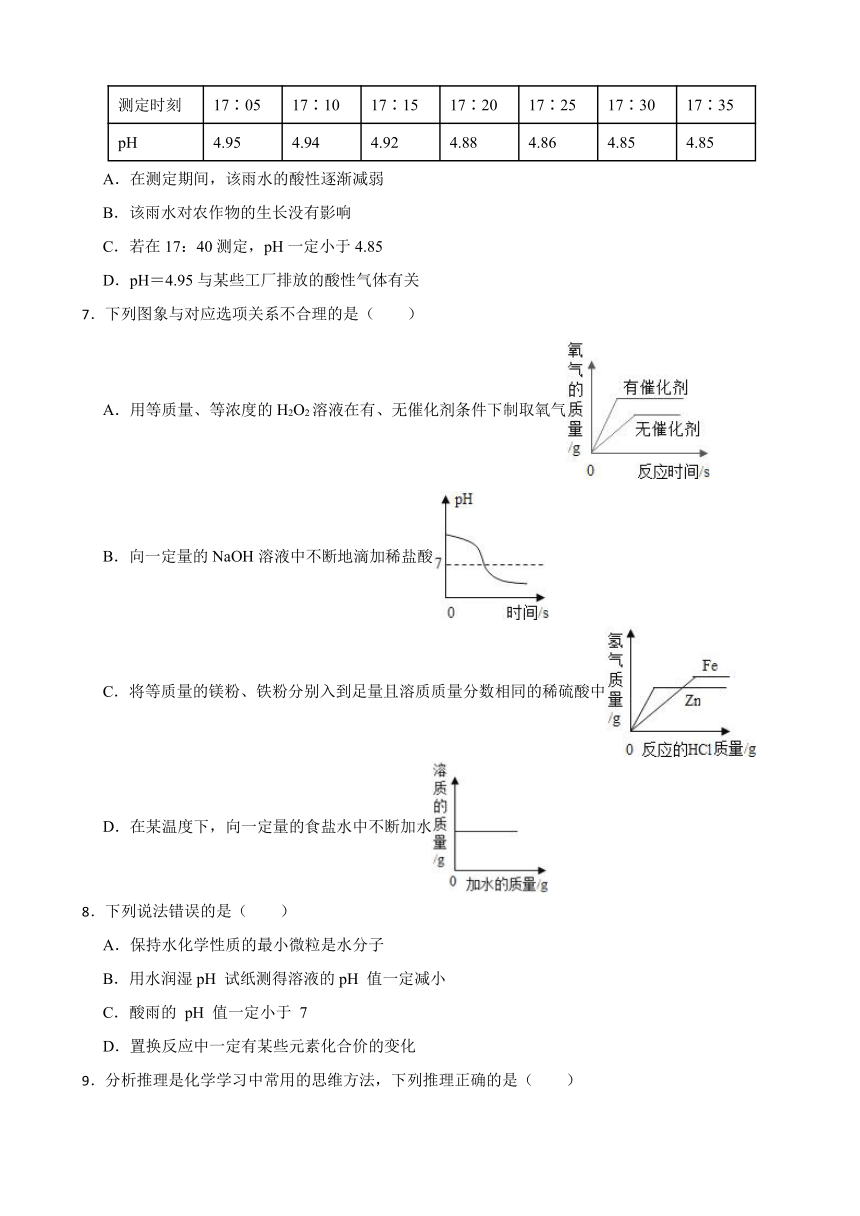
7.下列图象与对应选项关系不合理的是( )
A.用等质量、等浓度的H2O2溶液在有、无催化剂条件下制取氧气
B.向一定量的NaOH溶液中不断地滴加稀盐酸
C.将等质量的镁粉、铁粉分别入到足量且溶质质量分数相同的稀硫酸中
D.在某温度下,向一定量的食盐水中不断加水
8.下列说法错误的是( )
A.保持水化学性质的最小微粒是水分子
B.用水润湿pH 试纸测得溶液的pH 值一定减小
C.酸雨的 pH 值一定小于 7
D.置换反应中一定有某些元素化合价的变化
9.分析推理是化学学习中常用的思维方法,下列推理正确的是( )
A.分子、原子都是不显电性的粒子,所以不显电性的粒子一定是分子或原子
B.金属都能导电,所以能导电的物质一定为金属
C.在化学反应中。CO和H2都能夺取氧化铜中的氧,所以CO和H2都具有还原性
D.中和反应生成盐和水,生成盐和水的一定是中和反应
10.图示为某些物品对应的pH范围,其中显弱碱性的是( )
A.小苏打 B.杨梅 C.栗子 D.菠萝
11.某地区酸雨频发,其主要原因可能是( )
A.矿物燃料燃烧产生CO2过多
B.汽车流量过多,产生大量CO气体
C.燃料煤质量差,产生SO2量大
D.市建规模大,排放粉尘剧增
12.化学概念在逻辑上存在如图所示关系,对下列概念间的关系说法正确的是( )
A.纯净物与混合物属于包含关系
B.化合物与氧化物属于包含关系
C.单质与化合物属于交叉关系
D.中和反应与复分解反应属于并列关系
二、填空题
13.向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有 ;氧化铜与稀硫酸反应的化学反应方程式为 .实验室用浓硫酸配制一定量的稀硫酸,正确操作是将 ,并不断搅拌.
14.化学与我们生活息息相关,请从①氮气、②金刚石、③甲烷、④二氧化硫、⑤氢气、⑥酒精中选择适当物质序号填空:
(1)形成酸雨的气体是 ;
(2)“可燃冰”的主要成分是 ;
(3)自然界最硬的是 ;
(4)用作保护气体是 ;
(5)实验室常用的燃料是 ;
(6)最清洁能源是 。
15.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为 ;当加入熟石灰mg时,溶液中的溶质为 (填写化学式)
16.如图为某化学反应的微观模拟图,根据模拟图回答:
(1)请写出此化学反应的方程式 ;
(2)请从微观角度判断该变化是化学变化的依据为 ;
(3)从图中得出此化学变化的实质是 .
17.氮在周期表中的信息和原子结构示意图如图.根据信息,氮元素的相对原子质量为 ,原子最外层电子数为 ;氮元素与氢元素形成的化合物中氮的化合价为 价,该物质的水溶液pH 7(填“>”、“<”或“=”).
18.利用能源、节约能源、保护环境是我们大家共同关注的社会问题。
(1)最清洁的燃料是
(2)我国发射“嫦娥一号”的火箭使用C2H8N2(偏二甲肼)和N2O4为推进剂,请完成该化学方程式:C2H8N2+2N2O4=2CO2+3 +4H2O
(3)SO2的大量排放能形成酸雨,pH小于 的降雨称为酸雨,某火电厂在燃煤中加入石灰石以降低废气中SO2的含量,假设燃烧后得到50t废渣,若该废液中含硫元素的质量分数为24%,相当于少排放 t二氧化硫
(4)天然气燃烧不充分时,可调大气灶 (填“空气”或“燃气”)进入量
(5)金属镁着火不能使用二氧化碳扑灭,因为镁能在二氧化碳中继续燃烧,生成一种黑色单质和氧化镁两种固体粉末,写出该反应的化学方程式
三、综合题
19.某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如表所示
试剂 稀盐酸 稀醋酸 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
请分析上表,并回答下列问题:
(1)该花汁 (填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒,要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的 。
(3)胃酸的主要成分是盐酸,Al(OH)3和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式 。
(4)取少量澄清石灰水于试管中,然后滴入2滴该黄色花汁,接着逐滴滴入白醋,可以观察到试管中溶液颜色的变化是_____
A.黄色变成绿色最后变成红色 B.绿色变成红色最后变成黄色
C.绿色变成黄色最后变成红色 D.红色变成黄色最后变成绿色
(5)某溶液pH是13.5,如果要使溶液的pH降低,可以选择上述的 试剂。(写一种即可)
20.在2019年九年级化学实验操作技能考试中,小聪同学抽到的试题是“探究酸和碱之间的中和反应“。他向盛有氢氧化钠溶液的烧杯中缓慢滴加稀盐酸,一会儿后,想起忘记加指示剂了,便补加几滴无色酚酞溶液,搅拌,观察到溶液不变色,于是他得出“酸碱恰好完全中和”的结论。
(1)该中和反应的化学方程式是 ;
(2)老师给予小聪的评定是结论不准确。请你帮小聪分析老师的理由是: ;
(3)请你另外设计一个实验,探究小聪实验后烧杯中的溶液是否“恰好完全中和”。
填写下表:
实验步骤 实验现象 实验结论
取少量溶液于试管中, 稀盐酸过量
(4)反思:中和反应过程中,往往无明显的实验现象,无法确定反应是否发生及反应进行的程度,因此,需要借助一定的方法来判断。除上述方法以外,还可以用 进行检验。
21.金属具有广泛的应用.
(1)下列金属制品中,利用金属导热性的是 (填字母)
A.金属硬币 B.铝制导线 C.铜制火锅
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是 (用化学方程式表示)
(3)防止金属锈蚀是保护金属资源的有效途径之一.洁净的铁钉在下列情况下容易生锈的是 (填字母).
A.在干燥的空气中 B.在潮湿的空气中 C.浸没在植物油中
(4)铝具有良好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.氧化铝难溶于水,却能溶于酸.写出氧化铝与稀硫酸反应生成硫酸铝和水的化学方程式 .
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得滤渣和滤液.向滤液中加一洁净铁片,未看到铁片有任何变化.则滤液
中含有的溶质是 (填化学式),滤渣中一定含有的物质是 (填化学式)
22.
(1)对于硫酸而言,溶质的质量分数越大,溶液的酸性越强。常温下,10%的稀硫酸的pH (填“大于”“小于”或“等于”)2%的稀硫酸的pH。
(2)如果要使稀硫酸的pH升高。你采取的方法有:
不发生化学反应的方法: ;
(3)有化学反应的方法(要求各种方法中所选的物质类别不同) ; ; 。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】B
4.【答案】D
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】C
12.【答案】B
13.【答案】铜;CuO+H2SO4=CuSO4+H2O;要把浓硫酸沿容器壁慢慢注入水中
14.【答案】(1)④
(2)③
(3)②
(4)①
(5)⑥
(6)⑤
15.【答案】Ca(OH)2+2HCl=CaCl2+2H2O;CaCl2和HCl
16.【答案】NaOH+HCl═NaCl+H2O;有新分子生成;盐酸中的(每一个)氢离子和氢氧化钠溶液中的(每一个)氢氧根离子结合生成(一个)水分子
17.【答案】14.01;5;﹣3;>
18.【答案】(1)氢气
(2)N2
(3)5.6;24
(4)空气
(5)2Mg+CO2 2MgO+C
19.【答案】(1)可以
(2)肥皂水
(3)NaHCO3+HCl═NaCl+H2O+CO2↑
(4)A
(5)稀盐酸(或稀醋酸)
20.【答案】(1)NaOH+HCl=NaCl+H2O
(2)酸过量滴加酚酞也不变色,不变色可能是酸过量
(3)加入铁丝;产生气泡;没有气泡;氢氧化钠和稀盐酸恰好完全中和
(4)测pH值
21.【答案】(1)C
(2)Fe+CuSO4=FeSO4+Cu
(3)B
(4)Al2O3+3H2SO4=Al2(SO4)3+3H2O
(5)FeSO4;Cu
22.【答案】(1)小于
(2)加入一定量的水
(3)适量的锌;氧化钙;氢氧化钠溶液
一、单选题
1.下列有关实验的叙述正确的是( )
A.用pH试纸测得未知溶液的酸碱度时,应将pH试纸预先用水湿润
B.实验室用高锰酸钾制取O2,在实验结束时应先停止加热,再将导管移出水面
C.稀释浓硫酸时,要把浓硫酸缓慢注入盛有水的烧杯中,并用玻璃棒不断搅拌
D.在粗盐提纯实验中,蒸发溶剂时,待水全部蒸干后,再停止加热
2.下列化学反应属于中和反应的是( )
A.CaO+2HCl=CaCl2+H2O B.Ca(OH )2+2HCl=CaCl2+2H2O
C.CaCO3+2HCl=CaCl2+H2O+CO2↑ D.2NaOH+CO2=Na2CO3+H2O
3.下列推理正确的是( )
A.向某无色溶液中滴加酚酞无现象,则溶液一定呈中性
B.原子核由质子和中子构成,但并不是所有的原子核中都含有质子和中子
C.在同一化合物中,金属元素显正价,则非金属元素一定显负价
D.酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应
4.下列类比或推理正确的是( )
A.浓盐酸有挥发性,所以浓硫酸也有挥发性
B.酸雨是酸性的,所以pH<7的雨水称为酸雨
C.洗涤剂去油污是利用了乳化作用,所以汽油去油污也是利用了乳化作用
D.同种元素的原子具有相同质子数,所以具有相同质子数的原子为同种元素
5.推理是学习化学的一种重要方法.根据下列实验事实推理出结论正确的是( )
编号 实验事实 实验结论
A 某溶液使石蕊溶液变红 该溶液一定是稀盐酸
B 经测定某物质中含有氧元素 该物质一定是氧化物
C 常温下,测定某溶液的pH=12 该溶液一定呈碱性
D 某粒子带有电荷 该粒子一定是离子
A.A B.B C.C D.D
6.某化学课外活动小组开展下列实验活动:取刚降到地面的雨水水样,用pH计(测pH的仪器)每隔5分钟测一次pH,其数据如下表所示。下列对测定结果的分析中正确的是( )
测定时刻 17∶05 17∶10 17∶15 17∶20 17∶25 17∶30 17∶35
pH 4.95 4.94 4.92 4.88 4.86 4.85 4.85
A.在测定期间,该雨水的酸性逐渐减弱
B.该雨水对农作物的生长没有影响
C.若在17:40测定,pH一定小于4.85
D.pH=4.95与某些工厂排放的酸性气体有关
7.下列图象与对应选项关系不合理的是( )
A.用等质量、等浓度的H2O2溶液在有、无催化剂条件下制取氧气
B.向一定量的NaOH溶液中不断地滴加稀盐酸
C.将等质量的镁粉、铁粉分别入到足量且溶质质量分数相同的稀硫酸中
D.在某温度下,向一定量的食盐水中不断加水
8.下列说法错误的是( )
A.保持水化学性质的最小微粒是水分子
B.用水润湿pH 试纸测得溶液的pH 值一定减小
C.酸雨的 pH 值一定小于 7
D.置换反应中一定有某些元素化合价的变化
9.分析推理是化学学习中常用的思维方法,下列推理正确的是( )
A.分子、原子都是不显电性的粒子,所以不显电性的粒子一定是分子或原子
B.金属都能导电,所以能导电的物质一定为金属
C.在化学反应中。CO和H2都能夺取氧化铜中的氧,所以CO和H2都具有还原性
D.中和反应生成盐和水,生成盐和水的一定是中和反应
10.图示为某些物品对应的pH范围,其中显弱碱性的是( )
A.小苏打 B.杨梅 C.栗子 D.菠萝
11.某地区酸雨频发,其主要原因可能是( )
A.矿物燃料燃烧产生CO2过多
B.汽车流量过多,产生大量CO气体
C.燃料煤质量差,产生SO2量大
D.市建规模大,排放粉尘剧增
12.化学概念在逻辑上存在如图所示关系,对下列概念间的关系说法正确的是( )
A.纯净物与混合物属于包含关系
B.化合物与氧化物属于包含关系
C.单质与化合物属于交叉关系
D.中和反应与复分解反应属于并列关系
二、填空题
13.向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有 ;氧化铜与稀硫酸反应的化学反应方程式为 .实验室用浓硫酸配制一定量的稀硫酸,正确操作是将 ,并不断搅拌.
14.化学与我们生活息息相关,请从①氮气、②金刚石、③甲烷、④二氧化硫、⑤氢气、⑥酒精中选择适当物质序号填空:
(1)形成酸雨的气体是 ;
(2)“可燃冰”的主要成分是 ;
(3)自然界最硬的是 ;
(4)用作保护气体是 ;
(5)实验室常用的燃料是 ;
(6)最清洁能源是 。
15.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为 ;当加入熟石灰mg时,溶液中的溶质为 (填写化学式)
16.如图为某化学反应的微观模拟图,根据模拟图回答:
(1)请写出此化学反应的方程式 ;
(2)请从微观角度判断该变化是化学变化的依据为 ;
(3)从图中得出此化学变化的实质是 .
17.氮在周期表中的信息和原子结构示意图如图.根据信息,氮元素的相对原子质量为 ,原子最外层电子数为 ;氮元素与氢元素形成的化合物中氮的化合价为 价,该物质的水溶液pH 7(填“>”、“<”或“=”).
18.利用能源、节约能源、保护环境是我们大家共同关注的社会问题。
(1)最清洁的燃料是
(2)我国发射“嫦娥一号”的火箭使用C2H8N2(偏二甲肼)和N2O4为推进剂,请完成该化学方程式:C2H8N2+2N2O4=2CO2+3 +4H2O
(3)SO2的大量排放能形成酸雨,pH小于 的降雨称为酸雨,某火电厂在燃煤中加入石灰石以降低废气中SO2的含量,假设燃烧后得到50t废渣,若该废液中含硫元素的质量分数为24%,相当于少排放 t二氧化硫
(4)天然气燃烧不充分时,可调大气灶 (填“空气”或“燃气”)进入量
(5)金属镁着火不能使用二氧化碳扑灭,因为镁能在二氧化碳中继续燃烧,生成一种黑色单质和氧化镁两种固体粉末,写出该反应的化学方程式
三、综合题
19.某同学把自制的一种黄色花汁,分别滴加到下列不同的试剂中,并记录观察到的现象如表所示
试剂 稀盐酸 稀醋酸 蔗糖水 蒸馏水 肥皂水 烧碱溶液 石灰水
颜色 红 红 黄 黄 绿 绿 绿
请分析上表,并回答下列问题:
(1)该花汁 (填“可以”或“不可以”)作酸碱指示剂。
(2)蚊子叮咬人时射入蚁酸(具有酸的性质),使皮肤红肿、痛痒,要缓解这种症状,简易可行的办法是在叮咬处涂抹上述试剂中的 。
(3)胃酸的主要成分是盐酸,Al(OH)3和小苏打常用于治疗胃酸过多症,写出小苏打治疗胃酸过多症时的化学反应方程式 。
(4)取少量澄清石灰水于试管中,然后滴入2滴该黄色花汁,接着逐滴滴入白醋,可以观察到试管中溶液颜色的变化是_____
A.黄色变成绿色最后变成红色 B.绿色变成红色最后变成黄色
C.绿色变成黄色最后变成红色 D.红色变成黄色最后变成绿色
(5)某溶液pH是13.5,如果要使溶液的pH降低,可以选择上述的 试剂。(写一种即可)
20.在2019年九年级化学实验操作技能考试中,小聪同学抽到的试题是“探究酸和碱之间的中和反应“。他向盛有氢氧化钠溶液的烧杯中缓慢滴加稀盐酸,一会儿后,想起忘记加指示剂了,便补加几滴无色酚酞溶液,搅拌,观察到溶液不变色,于是他得出“酸碱恰好完全中和”的结论。
(1)该中和反应的化学方程式是 ;
(2)老师给予小聪的评定是结论不准确。请你帮小聪分析老师的理由是: ;
(3)请你另外设计一个实验,探究小聪实验后烧杯中的溶液是否“恰好完全中和”。
填写下表:
实验步骤 实验现象 实验结论
取少量溶液于试管中, 稀盐酸过量
(4)反思:中和反应过程中,往往无明显的实验现象,无法确定反应是否发生及反应进行的程度,因此,需要借助一定的方法来判断。除上述方法以外,还可以用 进行检验。
21.金属具有广泛的应用.
(1)下列金属制品中,利用金属导热性的是 (填字母)
A.金属硬币 B.铝制导线 C.铜制火锅
(2)波尔多液是一种农业上常用的杀菌剂,它由硫酸铜、生石灰加水配制而成,不能用铁质容器配制波尔多液的原因是 (用化学方程式表示)
(3)防止金属锈蚀是保护金属资源的有效途径之一.洁净的铁钉在下列情况下容易生锈的是 (填字母).
A.在干燥的空气中 B.在潮湿的空气中 C.浸没在植物油中
(4)铝具有良好的抗腐蚀性能,原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.氧化铝难溶于水,却能溶于酸.写出氧化铝与稀硫酸反应生成硫酸铝和水的化学方程式 .
(5)向铁粉和氧化铜粉末的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,得滤渣和滤液.向滤液中加一洁净铁片,未看到铁片有任何变化.则滤液
中含有的溶质是 (填化学式),滤渣中一定含有的物质是 (填化学式)
22.
(1)对于硫酸而言,溶质的质量分数越大,溶液的酸性越强。常温下,10%的稀硫酸的pH (填“大于”“小于”或“等于”)2%的稀硫酸的pH。
(2)如果要使稀硫酸的pH升高。你采取的方法有:
不发生化学反应的方法: ;
(3)有化学反应的方法(要求各种方法中所选的物质类别不同) ; ; 。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】B
4.【答案】D
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】C
12.【答案】B
13.【答案】铜;CuO+H2SO4=CuSO4+H2O;要把浓硫酸沿容器壁慢慢注入水中
14.【答案】(1)④
(2)③
(3)②
(4)①
(5)⑥
(6)⑤
15.【答案】Ca(OH)2+2HCl=CaCl2+2H2O;CaCl2和HCl
16.【答案】NaOH+HCl═NaCl+H2O;有新分子生成;盐酸中的(每一个)氢离子和氢氧化钠溶液中的(每一个)氢氧根离子结合生成(一个)水分子
17.【答案】14.01;5;﹣3;>
18.【答案】(1)氢气
(2)N2
(3)5.6;24
(4)空气
(5)2Mg+CO2 2MgO+C
19.【答案】(1)可以
(2)肥皂水
(3)NaHCO3+HCl═NaCl+H2O+CO2↑
(4)A
(5)稀盐酸(或稀醋酸)
20.【答案】(1)NaOH+HCl=NaCl+H2O
(2)酸过量滴加酚酞也不变色,不变色可能是酸过量
(3)加入铁丝;产生气泡;没有气泡;氢氧化钠和稀盐酸恰好完全中和
(4)测pH值
21.【答案】(1)C
(2)Fe+CuSO4=FeSO4+Cu
(3)B
(4)Al2O3+3H2SO4=Al2(SO4)3+3H2O
(5)FeSO4;Cu
22.【答案】(1)小于
(2)加入一定量的水
(3)适量的锌;氧化钙;氢氧化钠溶液
同课章节目录
