6.3 金属矿物与冶炼 同步练习(含答案) 2022-2023学年科粤版九年级下册化学
文档属性
| 名称 | 6.3 金属矿物与冶炼 同步练习(含答案) 2022-2023学年科粤版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 125.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览



文档简介
6.3 金属矿物与冶炼 同步练习
一、单选题
1.下列对有关事实的解释,错误的是( )
A.生铁和钢的性能不同﹣﹣含碳量不同
B.氢元素和氧元素种类不同﹣﹣质子数不同
C.酒精需要密封保存﹣﹣酒精分子间有间隔
D.冰水共存物属于纯净物﹣﹣冰和水都由水分子构成
2.下列关于金属制品的使用不合理的是( )
A.铜可以用来制作导线
B.不锈钢可用于制作外科手术刀
C.在铁桶中加入硫酸铜溶液和石灰水配制农药
D.不能经常用钢丝球擦洗铝锅
3.铁犁的使用体现了我国古代人民的劳动智慧。铁犁的犁头由生铁制成,生铁属于( )
A.盐 B.碱 C.合金 D.有机物
4.把铁矿石、焦炭和石灰石一起加入高炉中进行冶炼,得到的产物是( )
A.生铁 B.铜 C.纯铁 D.钢
5.生铁和钢的主要区别在于( )
A.生铁和钢的主要成分都是铁,其含碳量不同,性能也不同
B.生铁是铁,钢是铁的氧化物
C.生铁硬而有韧性,既可铸又可煅
D.钢是用铁矿石和焦炭作原料炼制而成
6.做完CO还原Fe2O3的实验后,清洗试管壁上留下的黑色物质时可选用的方法是( )
A.用大量水边洗边冲 B.用盐酸清洗后,再用水冲洗
C.用肥皂水清洗后,再用水冲洗 D.用试管刷上下、左右猛烈刷
7.中国诗词既蕴含人文思想,又焕发理性光辉.对下列划线部分的化学解释不合理的是( )
A.花气袭人知骤暖,喜鹊穿树喜新晴﹣温度高分子运动加快
B.何意百炼钢,化为绕指柔﹣生铁经不断煅烧捶打氧化,降低碳的含量,变成钢
C.千锤万凿出深山,烈火焚烧若等闲﹣煅烧石灰石,不发生化学变化
D.美人首饰侯王印,尽是沙中浪底来﹣金的性质稳定,在自然界中以单质形态存在
8.下列对有关事实的解释中,错误的是( )
A.氧和氟的元素种类不同﹣﹣质子数不同
B.生铁和钢的性能不同﹣﹣含碳量不同
C.水和过氧化氢的化学性质不同﹣﹣氧原子个数不同
D.硫在空气和氧气中燃烧的火焰颜色不同﹣﹣氧气浓度不同
9.中华传统文化蕴含丰富的化学知识。从化学视角对下列诗词的解释合理的是( )
A.“迟日江山丽,春风花草香”说明分子在不断地运动
B.“千锤万凿出深山,烈火焚烧若等闲”说明石灰石只发生了物理变化
C.“美人首饰侯王印,尽是沙中浪底来”说明金在自然界中以化合态存在
D.“釜底抽薪”和“钻木取火”都说明燃烧需要达到可燃物的着火点
10.含铁质量分数最小的是( )
A.生铁 B.钢 C.Fe2O3 D.Fe3O4
11.下列有关金属及合金的说法错误的是( )
A.黄铜的硬度大于纯铜
B.武德合金熔点高常用作保险丝
C.生铁和不锈钢都是金属材料
D.铝片表面容易形成致密的氧化铝膜
12.如图是CO还原氧化铁的实验装置。取2g氧化铁粉末进行实验,实验结束后称得装置中剩余固体质量为X。下列说法错误的是( )
(已知: )
A.X的取值范围为1.4g<X<2g
B.实验中所需CO的量可实现控制
C.实验中没涉及置换反应
D.实验时先挤压软塑料滴瓶,再点燃酒精喷灯
二、填空题
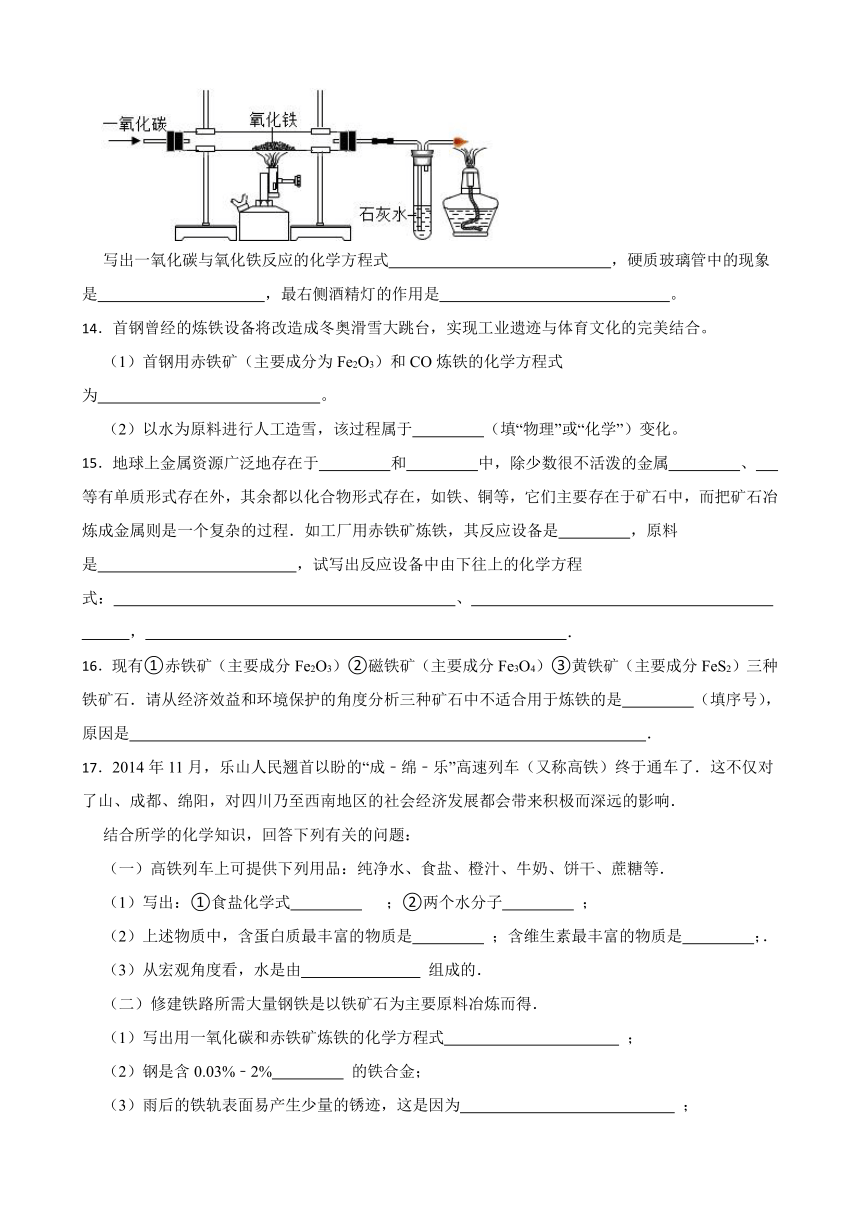
13.实验室模拟工业炼铁的装置图如图所示。
写出一氧化碳与氧化铁反应的化学方程式 ,硬质玻璃管中的现象是 ,最右侧酒精灯的作用是 。
14.首钢曾经的炼铁设备将改造成冬奥滑雪大跳台,实现工业遗迹与体育文化的完美结合。
(1)首钢用赤铁矿(主要成分为Fe2O3)和CO炼铁的化学方程式为 。
(2)以水为原料进行人工造雪,该过程属于 (填“物理”或“化学”)变化。
15.地球上金属资源广泛地存在于 和 中,除少数很不活泼的金属 、 等有单质形式存在外,其余都以化合物形式存在,如铁、铜等,它们主要存在于矿石中,而把矿石冶炼成金属则是一个复杂的过程.如工厂用赤铁矿炼铁,其反应设备是 ,原料是 ,试写出反应设备中由下往上的化学方程式: 、 , .
16.现有①赤铁矿(主要成分Fe2O3)②磁铁矿(主要成分Fe3O4)③黄铁矿(主要成分FeS2)三种铁矿石.请从经济效益和环境保护的角度分析三种矿石中不适合用于炼铁的是 (填序号),原因是 .
17.2014年11月,乐山人民翘首以盼的“成﹣绵﹣乐”高速列车(又称高铁)终于通车了.这不仅对了山、成都、绵阳,对四川乃至西南地区的社会经济发展都会带来积极而深远的影响.
结合所学的化学知识,回答下列有关的问题:
(一)高铁列车上可提供下列用品:纯净水、食盐、橙汁、牛奶、饼干、蔗糖等.
(1)写出:①食盐化学式 ;②两个水分子 ;
(2)上述物质中,含蛋白质最丰富的物质是 ;含维生素最丰富的物质是 ;.
(3)从宏观角度看,水是由 组成的.
(二)修建铁路所需大量钢铁是以铁矿石为主要原料冶炼而得.
(1)写出用一氧化碳和赤铁矿炼铁的化学方程式 ;
(2)钢是含0.03%﹣2% 的铁合金;
(3)雨后的铁轨表面易产生少量的锈迹,这是因为 ;
(4)实验室可用盐酸除铁锈,其化学方程式为 ;
(三)与高铁的电动列车形成鲜明对比的是以煤炭燃烧为动力的乐山嘉阳小火车,它是目前世界上仅存的少数几辆仍在运行的蒸汽机车之一,被称为“工业文明的活化石”.
(1)煤炭燃烧应具备的条件:①与空气(或氧气)接触,② ;
(2)从化学的角度分析蒸汽列车被电动列车淘汰的原因(任举一点) .
18.某研究性学习小组的同学在研究某种气体(纯净物)的性质时做了如下实验:
Ⅰ.将铜丝绕成螺旋状放在酒精灯火焰上加热,铜丝表面由光亮的红色变为黑色.
Ⅱ.趁热将Ⅰ表面变黑的铜丝放入盛有这种气体并且密闭的集气瓶中,观察发现铜丝表面的黑色又变为光亮的红色.试根据以上实验现象推断:
①上述实验中黑色物质是(写化学式) .
②这种气体可能是(只写一种) ,该实验能验证此气体具有的化学性质是 .
③请设计实验、验证你推断的气体是正确的(简要填写实验步骤、现象、结论).
实验步骤 实验现象 实验结论
三、综合题
19.回答:
(1)铝(Al)是自然界中含量最多的金属元素,铝是活泼金属,常温下在空气中铝的表面会形成致密的氧化膜,使铝不会进一步氧化并能耐腐蚀。因此,铝粉常用来做涂料,俗称银粉、银漆。以保护铁制品不被锈蚀,而且美观。
铝的密度很小,质地较软,可制成硬铝、超硬铝、防锈铝等各种铝合金。汽车、火车、船舶、宇宙火箭、航天飞机、人造卫是等,也是用大量的铝及其合金制造而成的。
①“银粉”、“银漆”保护铁制品不被锈蚀的原因是是隔绝了 。
②铝合金制造超音速飞机是利用了铝合金 的性质。
(2)高炉炼铁的主要原理运用了热还原法,写出以赤铁矿为原料炼铁的化学方程式: 。
(3)我国的青铜文化历史悠久,波尔多液不能用铁质容器来盛装的原因。请写出有关反应的化学方程式: 。
(4)通过置换反应可判断金属活动性顺序,某同学通过实验来比较铝、铁、铜的金属活动性顺序,现有铝、铁、铜的三种单质,如果另外只选用一种试剂达到实验目的,可以选用下列试剂中的____。
A.硫酸铜溶液 B.氯化亚铁溶液
C.硝酸铝溶液 D.稀硫酸
(5)向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,反应停止后过滤,则反应所得溶液中的溶质组成有 种情况。
20.下列是初中化学中的一些常见实验。请回答:
(1)甲实验进行一段时间后,在装置A中观察到的实验现象是 ,右端导气管口酒精灯的作用是点燃多余的CO,防止污染空气。
(2)乙实验中,将紫色石蕊浸泡过的小花一半烘干放入盛有CO2的集气瓶中,观察到的现象是 。
(3)下列关于丙实验的说法正确的是____(填字母序号)。
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷可以换成木炭
C.选用红磷是因为反应可以消耗氧气且生成固态的P2O5
21.人类文明的发展和社会的进步与材料密切相关。请根据相关信息回答下列问题:
(1)解码智慧冬奥:
①2022年北京冬奥会,碲化镉发电玻璃成为绿色和科技办奥交汇的创新点。如下图是碲的原子结构示意图,有关信息正确的是 。
A.碲是金属元素
B.碲的核电荷数为52
C.相对原子质量为127.6g
D.蹄元素位于第六周期
②氢能“黑科技”将亮相北京冬奥会。冬奥会“飞扬“火炬科技亮点之一是采用氢气作为燃料,其优点是什么 。
③冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。金属资源储量有限,钢铁生锈是世界面临的难题。你知道铁生锈的主要条件是什么 。
(2)近年来,我国高铁建设飞速发展,建造高铁需要大量的钢铁。上右图为模拟炼铁的装置,写出a中发生反应的化学方程式 ;b处发生反应的化学方程式 。
22.多数金属以矿物形式存在于自然界,金属矿物可用来冶炼金属.
冶炼方法 反应表示式(其他产物已略去) 代表性金属
热还原法 金属A的氧化物+还原剂 {#mathmL#}{#/mathmL#} 金属A 锌、铜
电解法 金属B的化合物 {#mathmL#}{#/mathmL#} 金属B 钾、铝
热分解法 金属C的氧化物 {#mathmL#}{#/mathmL#} 金属C 汞、银
(1)写出工业上常用的赤铁矿(主要成分是Fe2O3)炼铁的化学反应方程式 .
(2)写出用氧化铝冶炼金属铝的化学方程式 .
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】C
4.【答案】A
5.【答案】A
6.【答案】B
7.【答案】C
8.【答案】C
9.【答案】A
10.【答案】C
11.【答案】B
12.【答案】A
13.【答案】;红色粉末逐渐变黑;点燃尾气,防止CO污染空气
14.【答案】(1)
(2)物理
15.【答案】地壳;海洋;金;银;高炉;铁矿石、石灰石和焦炭;C+O2 CO2;CO2+C 2CO;Fe2O3+3CO 2Fe+3CO2
16.【答案】③;FeS2的含铁量少,而且在冶炼的过程中,会产生二氧化硫而污染空气
17.【答案】NaCl;2H2O;牛奶;橙汁;氢、氧元素;3CO+Fe2O32Fe+3CO2;碳;铁在潮湿的空气中易生锈;Fe2O3+6HCl=2FeCl3+3H2O;温度达到着火点;对环境有污染
18.【答案】CuO;H2;还原性;将气体在导管口点燃,并在上方罩一个干燥的烧杯;气体能燃烧,并在烧杯内壁有水珠出现;该气体是氢气
19.【答案】(1)氧气和水蒸气;密度小、硬度大或抗腐蚀性能好
(2)
(3)
(4)B;D
(5)3或三
20.【答案】(1)红棕色粉末逐渐变黑
(2)湿润的一半由紫色变为红色,另一半无明显变化
(3)C
21.【答案】(1)B;燃烧产物只有水,比较环保,燃烧值大;铁与氧气和水接触
(2);
22.【答案】(1)Fe2O3+3CO {#mathmL#}{#/mathmL#} 2Fe+3CO2
(2)2Al2O3 {#mathmL#}{#/mathmL#} 4Al+3O2↑
一、单选题
1.下列对有关事实的解释,错误的是( )
A.生铁和钢的性能不同﹣﹣含碳量不同
B.氢元素和氧元素种类不同﹣﹣质子数不同
C.酒精需要密封保存﹣﹣酒精分子间有间隔
D.冰水共存物属于纯净物﹣﹣冰和水都由水分子构成
2.下列关于金属制品的使用不合理的是( )
A.铜可以用来制作导线
B.不锈钢可用于制作外科手术刀
C.在铁桶中加入硫酸铜溶液和石灰水配制农药
D.不能经常用钢丝球擦洗铝锅
3.铁犁的使用体现了我国古代人民的劳动智慧。铁犁的犁头由生铁制成,生铁属于( )
A.盐 B.碱 C.合金 D.有机物
4.把铁矿石、焦炭和石灰石一起加入高炉中进行冶炼,得到的产物是( )
A.生铁 B.铜 C.纯铁 D.钢
5.生铁和钢的主要区别在于( )
A.生铁和钢的主要成分都是铁,其含碳量不同,性能也不同
B.生铁是铁,钢是铁的氧化物
C.生铁硬而有韧性,既可铸又可煅
D.钢是用铁矿石和焦炭作原料炼制而成
6.做完CO还原Fe2O3的实验后,清洗试管壁上留下的黑色物质时可选用的方法是( )
A.用大量水边洗边冲 B.用盐酸清洗后,再用水冲洗
C.用肥皂水清洗后,再用水冲洗 D.用试管刷上下、左右猛烈刷
7.中国诗词既蕴含人文思想,又焕发理性光辉.对下列划线部分的化学解释不合理的是( )
A.花气袭人知骤暖,喜鹊穿树喜新晴﹣温度高分子运动加快
B.何意百炼钢,化为绕指柔﹣生铁经不断煅烧捶打氧化,降低碳的含量,变成钢
C.千锤万凿出深山,烈火焚烧若等闲﹣煅烧石灰石,不发生化学变化
D.美人首饰侯王印,尽是沙中浪底来﹣金的性质稳定,在自然界中以单质形态存在
8.下列对有关事实的解释中,错误的是( )
A.氧和氟的元素种类不同﹣﹣质子数不同
B.生铁和钢的性能不同﹣﹣含碳量不同
C.水和过氧化氢的化学性质不同﹣﹣氧原子个数不同
D.硫在空气和氧气中燃烧的火焰颜色不同﹣﹣氧气浓度不同
9.中华传统文化蕴含丰富的化学知识。从化学视角对下列诗词的解释合理的是( )
A.“迟日江山丽,春风花草香”说明分子在不断地运动
B.“千锤万凿出深山,烈火焚烧若等闲”说明石灰石只发生了物理变化
C.“美人首饰侯王印,尽是沙中浪底来”说明金在自然界中以化合态存在
D.“釜底抽薪”和“钻木取火”都说明燃烧需要达到可燃物的着火点
10.含铁质量分数最小的是( )
A.生铁 B.钢 C.Fe2O3 D.Fe3O4
11.下列有关金属及合金的说法错误的是( )
A.黄铜的硬度大于纯铜
B.武德合金熔点高常用作保险丝
C.生铁和不锈钢都是金属材料
D.铝片表面容易形成致密的氧化铝膜
12.如图是CO还原氧化铁的实验装置。取2g氧化铁粉末进行实验,实验结束后称得装置中剩余固体质量为X。下列说法错误的是( )
(已知: )
A.X的取值范围为1.4g<X<2g
B.实验中所需CO的量可实现控制
C.实验中没涉及置换反应
D.实验时先挤压软塑料滴瓶,再点燃酒精喷灯
二、填空题
13.实验室模拟工业炼铁的装置图如图所示。
写出一氧化碳与氧化铁反应的化学方程式 ,硬质玻璃管中的现象是 ,最右侧酒精灯的作用是 。
14.首钢曾经的炼铁设备将改造成冬奥滑雪大跳台,实现工业遗迹与体育文化的完美结合。
(1)首钢用赤铁矿(主要成分为Fe2O3)和CO炼铁的化学方程式为 。
(2)以水为原料进行人工造雪,该过程属于 (填“物理”或“化学”)变化。
15.地球上金属资源广泛地存在于 和 中,除少数很不活泼的金属 、 等有单质形式存在外,其余都以化合物形式存在,如铁、铜等,它们主要存在于矿石中,而把矿石冶炼成金属则是一个复杂的过程.如工厂用赤铁矿炼铁,其反应设备是 ,原料是 ,试写出反应设备中由下往上的化学方程式: 、 , .
16.现有①赤铁矿(主要成分Fe2O3)②磁铁矿(主要成分Fe3O4)③黄铁矿(主要成分FeS2)三种铁矿石.请从经济效益和环境保护的角度分析三种矿石中不适合用于炼铁的是 (填序号),原因是 .
17.2014年11月,乐山人民翘首以盼的“成﹣绵﹣乐”高速列车(又称高铁)终于通车了.这不仅对了山、成都、绵阳,对四川乃至西南地区的社会经济发展都会带来积极而深远的影响.
结合所学的化学知识,回答下列有关的问题:
(一)高铁列车上可提供下列用品:纯净水、食盐、橙汁、牛奶、饼干、蔗糖等.
(1)写出:①食盐化学式 ;②两个水分子 ;
(2)上述物质中,含蛋白质最丰富的物质是 ;含维生素最丰富的物质是 ;.
(3)从宏观角度看,水是由 组成的.
(二)修建铁路所需大量钢铁是以铁矿石为主要原料冶炼而得.
(1)写出用一氧化碳和赤铁矿炼铁的化学方程式 ;
(2)钢是含0.03%﹣2% 的铁合金;
(3)雨后的铁轨表面易产生少量的锈迹,这是因为 ;
(4)实验室可用盐酸除铁锈,其化学方程式为 ;
(三)与高铁的电动列车形成鲜明对比的是以煤炭燃烧为动力的乐山嘉阳小火车,它是目前世界上仅存的少数几辆仍在运行的蒸汽机车之一,被称为“工业文明的活化石”.
(1)煤炭燃烧应具备的条件:①与空气(或氧气)接触,② ;
(2)从化学的角度分析蒸汽列车被电动列车淘汰的原因(任举一点) .
18.某研究性学习小组的同学在研究某种气体(纯净物)的性质时做了如下实验:
Ⅰ.将铜丝绕成螺旋状放在酒精灯火焰上加热,铜丝表面由光亮的红色变为黑色.
Ⅱ.趁热将Ⅰ表面变黑的铜丝放入盛有这种气体并且密闭的集气瓶中,观察发现铜丝表面的黑色又变为光亮的红色.试根据以上实验现象推断:
①上述实验中黑色物质是(写化学式) .
②这种气体可能是(只写一种) ,该实验能验证此气体具有的化学性质是 .
③请设计实验、验证你推断的气体是正确的(简要填写实验步骤、现象、结论).
实验步骤 实验现象 实验结论
三、综合题
19.回答:
(1)铝(Al)是自然界中含量最多的金属元素,铝是活泼金属,常温下在空气中铝的表面会形成致密的氧化膜,使铝不会进一步氧化并能耐腐蚀。因此,铝粉常用来做涂料,俗称银粉、银漆。以保护铁制品不被锈蚀,而且美观。
铝的密度很小,质地较软,可制成硬铝、超硬铝、防锈铝等各种铝合金。汽车、火车、船舶、宇宙火箭、航天飞机、人造卫是等,也是用大量的铝及其合金制造而成的。
①“银粉”、“银漆”保护铁制品不被锈蚀的原因是是隔绝了 。
②铝合金制造超音速飞机是利用了铝合金 的性质。
(2)高炉炼铁的主要原理运用了热还原法,写出以赤铁矿为原料炼铁的化学方程式: 。
(3)我国的青铜文化历史悠久,波尔多液不能用铁质容器来盛装的原因。请写出有关反应的化学方程式: 。
(4)通过置换反应可判断金属活动性顺序,某同学通过实验来比较铝、铁、铜的金属活动性顺序,现有铝、铁、铜的三种单质,如果另外只选用一种试剂达到实验目的,可以选用下列试剂中的____。
A.硫酸铜溶液 B.氯化亚铁溶液
C.硝酸铝溶液 D.稀硫酸
(5)向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,反应停止后过滤,则反应所得溶液中的溶质组成有 种情况。
20.下列是初中化学中的一些常见实验。请回答:
(1)甲实验进行一段时间后,在装置A中观察到的实验现象是 ,右端导气管口酒精灯的作用是点燃多余的CO,防止污染空气。
(2)乙实验中,将紫色石蕊浸泡过的小花一半烘干放入盛有CO2的集气瓶中,观察到的现象是 。
(3)下列关于丙实验的说法正确的是____(填字母序号)。
A.燃烧匙中的红磷越多,水位上升越高
B.燃烧匙中的红磷可以换成木炭
C.选用红磷是因为反应可以消耗氧气且生成固态的P2O5
21.人类文明的发展和社会的进步与材料密切相关。请根据相关信息回答下列问题:
(1)解码智慧冬奥:
①2022年北京冬奥会,碲化镉发电玻璃成为绿色和科技办奥交汇的创新点。如下图是碲的原子结构示意图,有关信息正确的是 。
A.碲是金属元素
B.碲的核电荷数为52
C.相对原子质量为127.6g
D.蹄元素位于第六周期
②氢能“黑科技”将亮相北京冬奥会。冬奥会“飞扬“火炬科技亮点之一是采用氢气作为燃料,其优点是什么 。
③冬奥会国家速滑馆“冰丝带”采用面向未来的单层双向正交马鞍形索网结构,减少屋顶所用钢材2800吨。金属资源储量有限,钢铁生锈是世界面临的难题。你知道铁生锈的主要条件是什么 。
(2)近年来,我国高铁建设飞速发展,建造高铁需要大量的钢铁。上右图为模拟炼铁的装置,写出a中发生反应的化学方程式 ;b处发生反应的化学方程式 。
22.多数金属以矿物形式存在于自然界,金属矿物可用来冶炼金属.
冶炼方法 反应表示式(其他产物已略去) 代表性金属
热还原法 金属A的氧化物+还原剂 {#mathmL#}{#/mathmL#} 金属A 锌、铜
电解法 金属B的化合物 {#mathmL#}{#/mathmL#} 金属B 钾、铝
热分解法 金属C的氧化物 {#mathmL#}{#/mathmL#} 金属C 汞、银
(1)写出工业上常用的赤铁矿(主要成分是Fe2O3)炼铁的化学反应方程式 .
(2)写出用氧化铝冶炼金属铝的化学方程式 .
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】C
4.【答案】A
5.【答案】A
6.【答案】B
7.【答案】C
8.【答案】C
9.【答案】A
10.【答案】C
11.【答案】B
12.【答案】A
13.【答案】;红色粉末逐渐变黑;点燃尾气,防止CO污染空气
14.【答案】(1)
(2)物理
15.【答案】地壳;海洋;金;银;高炉;铁矿石、石灰石和焦炭;C+O2 CO2;CO2+C 2CO;Fe2O3+3CO 2Fe+3CO2
16.【答案】③;FeS2的含铁量少,而且在冶炼的过程中,会产生二氧化硫而污染空气
17.【答案】NaCl;2H2O;牛奶;橙汁;氢、氧元素;3CO+Fe2O32Fe+3CO2;碳;铁在潮湿的空气中易生锈;Fe2O3+6HCl=2FeCl3+3H2O;温度达到着火点;对环境有污染
18.【答案】CuO;H2;还原性;将气体在导管口点燃,并在上方罩一个干燥的烧杯;气体能燃烧,并在烧杯内壁有水珠出现;该气体是氢气
19.【答案】(1)氧气和水蒸气;密度小、硬度大或抗腐蚀性能好
(2)
(3)
(4)B;D
(5)3或三
20.【答案】(1)红棕色粉末逐渐变黑
(2)湿润的一半由紫色变为红色,另一半无明显变化
(3)C
21.【答案】(1)B;燃烧产物只有水,比较环保,燃烧值大;铁与氧气和水接触
(2);
22.【答案】(1)Fe2O3+3CO {#mathmL#}{#/mathmL#} 2Fe+3CO2
(2)2Al2O3 {#mathmL#}{#/mathmL#} 4Al+3O2↑
