7.2 碱及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 7.2 碱及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 294.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-03 00:00:00 | ||
图片预览



文档简介
7.2 碱及其性质 同步练习
一、单选题
1.用下图所示装置进行下列实验。其中,氢氧化钠溶液用于吸收硫燃烧产生的有毒气体二氧化硫。
步骤1:从A处通入空气,点燃酒精灯,观察到硫粉熔化、燃烧,产生微弱的淡蓝色火焰;
步骤2:从A处改通入氧气,观察到硫燃烧产生明亮的蓝紫色火焰。
下列说法错误的是( )
A.检查该装置气密性的操作:堵住A口,将导气管伸入液面以下,双手紧握U型管
B.实验结束时,继续通入气体,停止加热,一段时间后把导气管移出液面
C.步骤1中,硫粉只发生了化学变化
D.上述实验说明,氧气含量的高低是影响硫燃烧现象的因素之一
2.下列有关硫酸的说法,正确的是( )
A.打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾
B.浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%﹣5%的氢氧化钠溶液
C.实验室用稀硫酸和块状石灰石制取二氧化碳
D.硫酸可用于生产化肥、农药、染料以及冶炼金属等
3.下列实验现象记录正确且完整的是( )
A.镁在空气中燃烧,发出耀眼的白光,产生白烟,放出大量的热,生成白色固体物质
B.铁在空气中燃烧,火星四射,放出大量热,生成黑色固体
C.氢氧化铜使无色的酚酞试液变红色
D.硫在空气中燃烧,产生蓝色的光,放出大量的热
4.下列物质的用途错误的是( )
A.氦气用于飞艇
B.干冰用于食品的冷藏运输
C.用煤制取煤油
D.氢氧化钠去油污
5.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①石灰石和稀盐酸 ②镁和稀硫酸③固体氢氧化钠和水 ④生石灰和水
A.①②③④ B.①②③ C.①②④ D.②③④
6.欲除去氢氧化钠溶液中的少量杂质氢氧化钙,可以选用的试剂( )
A.氢氧化钾溶液 B.碳酸钠溶液
C.氯化钡溶液 D.稀盐酸
7.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而增大的是( )
A.浓盐酸 B.澄清石灰水
C.浓硫酸 D.氢氧化钠溶液
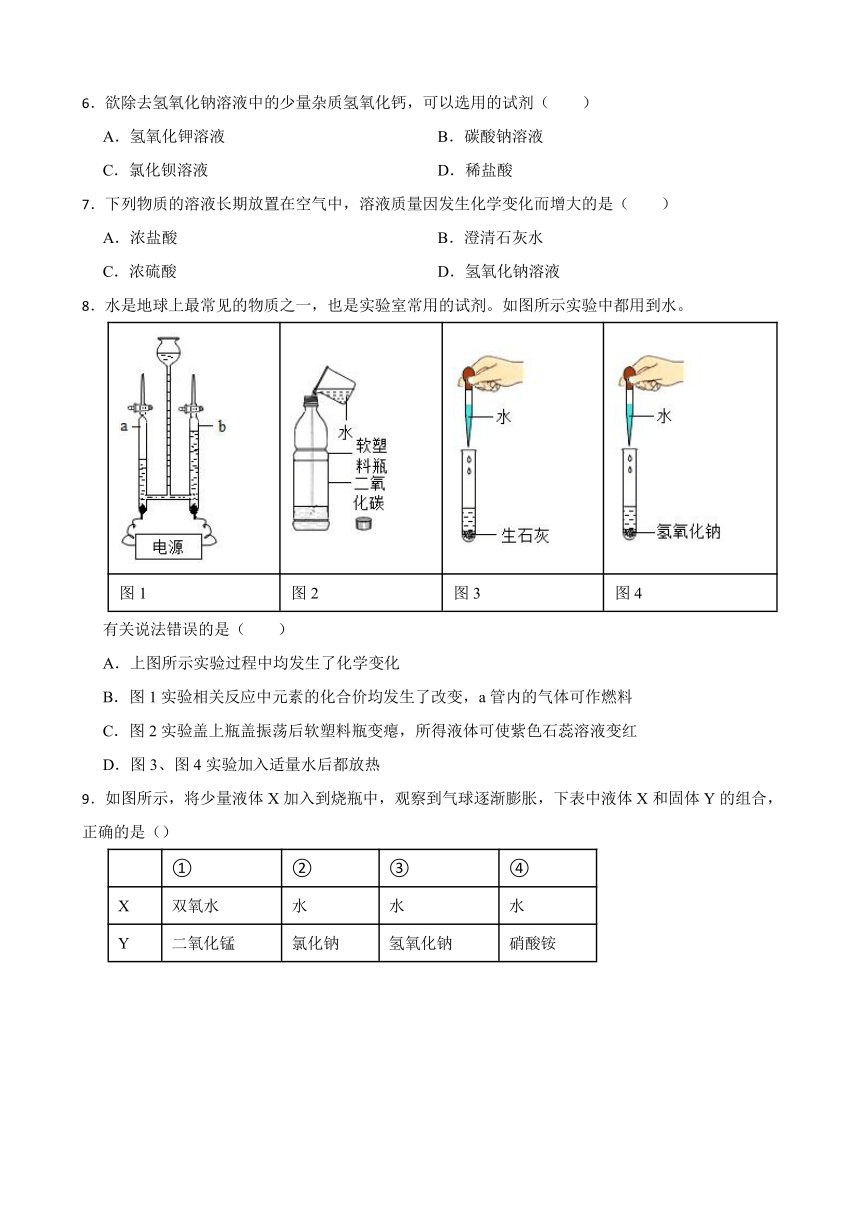
8.水是地球上最常见的物质之一,也是实验室常用的试剂。如图所示实验中都用到水。
图1 图2 图3 图4
有关说法错误的是( )
A.上图所示实验过程中均发生了化学变化
B.图1实验相关反应中元素的化合价均发生了改变,a管内的气体可作燃料
C.图2实验盖上瓶盖振荡后软塑料瓶变瘪,所得液体可使紫色石蕊溶液变红
D.图3、图4实验加入适量水后都放热
9.如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀,下表中液体X和固体Y的组合,正确的是()
① ② ③ ④
X 双氧水 水 水 水
Y 二氧化锰 氯化钠 氢氧化钠 硝酸铵
A.①② B.①③ C.①③④ D.②③④
10.日常生活中,我们经常会遇到一些化学问题。试根据所学化学知识判断,下列①~④的做法中正确的是( )
①用苛性钠稀溶液除去炉具上的油污 ②用硫酸制作汽车蓄电池
③用生石灰降低土壤碱性 ④用多喝食醋的方法缓解胃酸过多
A.①② B.③④ C.①③ D.②④
11.在含有H2SO4和CuSO4的混合溶液中,逐滴加入NaOH溶液至过量,下列图象能符合题意反映生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系是()
A. B.
C. D.
12.安全事故无小事。下图是一种危险化学品警示标记,在运输时应张贴该标记的是( )
A.食盐 B.纯碱 C.酒精 D.烧碱
二、填空题
13.去年,我国部分地区爆发了H7N9禽流感.为了防止禽流感蔓延,人们将家禽捕杀、掩埋,并在禽舍和掩埋坑中洒上大量热石灰.
(1)熟石灰属于 (填“酸”、“碱”或“盐”).用熟石灰处理硫酸厂废水中的硫酸,其化学方程式为 .
(2)熟石灰的溶解度曲线如图所示,30℃时,将1g 熟石灰加入100g水中充分搅拌、过滤,若不计溶液损失,得到溶液的质量是 g.将该溶液降温到20℃,是否有固体析出 ,(填“是”或“否”)溶液中溶质的质量分数将 (填序号)
A.不变B.增大C.减小.
14.现有①盐酸、②熟石灰、③烧碱 ④干冰、⑤硫酸、⑥生石灰六种物质,请选用相应物质填空(填序号):
常见的食品干燥剂 ;人体胃液中的酸是 ;用于人工降雨的 ;常用作改良酸性土壤的碱 .
15.同学们想制作“叶脉书签”送给老师.欲配制300克溶质质量分数为10%的氢氧化钠溶液,需要 克氢氧化钠,称量时应把氢氧化钠放在 ,若搅拌时不小心将氢氧化钠溶液迸溅到手上,要用较多的水冲洗,再涂上 溶液.
16.固体氢氧化钠曝露在空气中容易潮解,同时吸收空气中的 而变质,变质所涉及的化学方程为 ,因此,氢氧化钠固体必须 保存。
17.海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中或长途运输活鱼常常由于鱼多而缺氧,因此要设法增加水中的氧气含量。
材料一:已知过氧化钠(Na2O2)与水较快反应,反应方程式是 ,过氧化钙(CaO2)与Na2O2性质相似,与水缓慢反应放出氧气。
材料二:20℃时,NaOH的溶解度为109g,Ca(OH)2的溶解度为0.165g。
(1)试写出CaO2与H2O反应的化学方程式 ;
(2)长途运输活鱼,人们选择CaO2而不选择Na2O2作增氧剂的理由可能是 (写出一条即可)
18.实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 (用化学式表示),写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,常用 来清洗。
三、综合题
19.近年来我国在航天领域取得了重大成就,2021年10月16日0时23分,神舟十三号载人飞船成功发射。我国自主研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证,航天员舱外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),宇航服是保护宇航员在太空不受低温、射线等的侵害并提供人类生存所需的氧气的保护服。宇航服的氧气罐为太空人提供氧气,而排出的二氧化碳则由氢氧化锂所吸收。
(1)现宇航员呼吸出4.4g二氧化碳,航天员舱外服至少含有 g氢氧化锂(LiOH)才能完全吸收。
(2)你认为氢氧化锂不可能具有的化学性质是____(填标号)。
A.与二氧化碳反应 B.与盐酸反应
C.与氧化铁反应 D.与氯化铜溶液反应
(3)已知碳酸锂是微溶于水,其它锂的化合物都易溶于水,设计两种制备氢氧化锂的方案(要求含锂原料分别属于不同的物质类别)。完成下表:
方案 预期发生的化学方程式 依据的反应规律
① 金属氧化物和水反应生成碱
②
20.硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
21.化学试剂常常要密封保存,但原因各不相同。
(1)浓盐酸密封保存的原因是什么 ?
(2)氢氧化钠溶液若敞口放置会发生变质,请用化学方程式表示其变质原因 。
(3)如何检验NaOH溶液是否完全变质,请简述实验方法 。
22.实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键.造成下列实验后果的原因可能是:
(1)用试管加热固体,实验结束后,试管炸裂: ;
(2)用高锰酸钾制取氧气,水槽中的水变成了紫红色: ;
(3)用红磷测定空气中氧气含量的实验中,结果偏低 ;
(4)倾倒液体药品后,标签被腐蚀: ;
答案解析部分
1.【答案】C
2.【答案】D
3.【答案】A
4.【答案】C
5.【答案】A
6.【答案】B
7.【答案】D
8.【答案】A
9.【答案】B
10.【答案】A
11.【答案】B
12.【答案】D
13.【答案】碱;Ca(OH)2+H2SO4=CaSO4+2H2O;100.15;否;B
14.【答案】⑥;①;④;②
15.【答案】30;左盘的烧杯中;硼酸
16.【答案】二氧化碳或CO2;2NaOH+CO2=Na2CO3+H2O;密封
17.【答案】(1)2CaO2+2H2O═2Ca(OH)2+O2↑
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性(合理即可)
18.【答案】CaCO3;CO2+Ca(OH)2═CaCO3↓+H2O;不能;稀盐酸
19.【答案】(1)4.8
(2)C
(3);;盐和碱反应生成新碱和新盐,生成物有沉淀
20.【答案】(1)吸水性
(2)Fe+H2SO4=FeSO4+H2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;H2SO4+BaCl2=BaSO4↓+2HCl;①②
(3)②③
21.【答案】(1)浓盐酸具有挥发性
(2)2NaOH+CO2=Na2CO3+H2O
(3)取少量样品于试管中,加入足量氯化钙溶液,有白色沉淀产生;取少量充分反应后的溶液于试管中,滴入酚酞试液,若酚酞试液变红色,说明氢氧化钠溶液部分变质,若不变红色,说明氢氧化钠溶液全部变质
22.【答案】(1)试管未冷却就立即用冷水清洗
(2)试管口没有放一团棉花
(3)红磷量不足(装置漏气、未冷却至室温就打开弹簧夹)
(4)倾倒液体时,标签没有朝向手心
一、单选题
1.用下图所示装置进行下列实验。其中,氢氧化钠溶液用于吸收硫燃烧产生的有毒气体二氧化硫。
步骤1:从A处通入空气,点燃酒精灯,观察到硫粉熔化、燃烧,产生微弱的淡蓝色火焰;
步骤2:从A处改通入氧气,观察到硫燃烧产生明亮的蓝紫色火焰。
下列说法错误的是( )
A.检查该装置气密性的操作:堵住A口,将导气管伸入液面以下,双手紧握U型管
B.实验结束时,继续通入气体,停止加热,一段时间后把导气管移出液面
C.步骤1中,硫粉只发生了化学变化
D.上述实验说明,氧气含量的高低是影响硫燃烧现象的因素之一
2.下列有关硫酸的说法,正确的是( )
A.打开盛有浓硫酸的试剂瓶塞,瓶口出现白雾
B.浓硫酸不慎沾到皮肤上,立即用大量的水冲洗,然后再涂上3%﹣5%的氢氧化钠溶液
C.实验室用稀硫酸和块状石灰石制取二氧化碳
D.硫酸可用于生产化肥、农药、染料以及冶炼金属等
3.下列实验现象记录正确且完整的是( )
A.镁在空气中燃烧,发出耀眼的白光,产生白烟,放出大量的热,生成白色固体物质
B.铁在空气中燃烧,火星四射,放出大量热,生成黑色固体
C.氢氧化铜使无色的酚酞试液变红色
D.硫在空气中燃烧,产生蓝色的光,放出大量的热
4.下列物质的用途错误的是( )
A.氦气用于飞艇
B.干冰用于食品的冷藏运输
C.用煤制取煤油
D.氢氧化钠去油污
5.要使右图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①石灰石和稀盐酸 ②镁和稀硫酸③固体氢氧化钠和水 ④生石灰和水
A.①②③④ B.①②③ C.①②④ D.②③④
6.欲除去氢氧化钠溶液中的少量杂质氢氧化钙,可以选用的试剂( )
A.氢氧化钾溶液 B.碳酸钠溶液
C.氯化钡溶液 D.稀盐酸
7.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而增大的是( )
A.浓盐酸 B.澄清石灰水
C.浓硫酸 D.氢氧化钠溶液
8.水是地球上最常见的物质之一,也是实验室常用的试剂。如图所示实验中都用到水。
图1 图2 图3 图4
有关说法错误的是( )
A.上图所示实验过程中均发生了化学变化
B.图1实验相关反应中元素的化合价均发生了改变,a管内的气体可作燃料
C.图2实验盖上瓶盖振荡后软塑料瓶变瘪,所得液体可使紫色石蕊溶液变红
D.图3、图4实验加入适量水后都放热
9.如图所示,将少量液体X加入到烧瓶中,观察到气球逐渐膨胀,下表中液体X和固体Y的组合,正确的是()
① ② ③ ④
X 双氧水 水 水 水
Y 二氧化锰 氯化钠 氢氧化钠 硝酸铵
A.①② B.①③ C.①③④ D.②③④
10.日常生活中,我们经常会遇到一些化学问题。试根据所学化学知识判断,下列①~④的做法中正确的是( )
①用苛性钠稀溶液除去炉具上的油污 ②用硫酸制作汽车蓄电池
③用生石灰降低土壤碱性 ④用多喝食醋的方法缓解胃酸过多
A.①② B.③④ C.①③ D.②④
11.在含有H2SO4和CuSO4的混合溶液中,逐滴加入NaOH溶液至过量,下列图象能符合题意反映生成沉淀的质量(m1)与加入NaOH溶液的质量(m2)的关系是()
A. B.
C. D.
12.安全事故无小事。下图是一种危险化学品警示标记,在运输时应张贴该标记的是( )
A.食盐 B.纯碱 C.酒精 D.烧碱
二、填空题
13.去年,我国部分地区爆发了H7N9禽流感.为了防止禽流感蔓延,人们将家禽捕杀、掩埋,并在禽舍和掩埋坑中洒上大量热石灰.
(1)熟石灰属于 (填“酸”、“碱”或“盐”).用熟石灰处理硫酸厂废水中的硫酸,其化学方程式为 .
(2)熟石灰的溶解度曲线如图所示,30℃时,将1g 熟石灰加入100g水中充分搅拌、过滤,若不计溶液损失,得到溶液的质量是 g.将该溶液降温到20℃,是否有固体析出 ,(填“是”或“否”)溶液中溶质的质量分数将 (填序号)
A.不变B.增大C.减小.
14.现有①盐酸、②熟石灰、③烧碱 ④干冰、⑤硫酸、⑥生石灰六种物质,请选用相应物质填空(填序号):
常见的食品干燥剂 ;人体胃液中的酸是 ;用于人工降雨的 ;常用作改良酸性土壤的碱 .
15.同学们想制作“叶脉书签”送给老师.欲配制300克溶质质量分数为10%的氢氧化钠溶液,需要 克氢氧化钠,称量时应把氢氧化钠放在 ,若搅拌时不小心将氢氧化钠溶液迸溅到手上,要用较多的水冲洗,再涂上 溶液.
16.固体氢氧化钠曝露在空气中容易潮解,同时吸收空气中的 而变质,变质所涉及的化学方程为 ,因此,氢氧化钠固体必须 保存。
17.海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中或长途运输活鱼常常由于鱼多而缺氧,因此要设法增加水中的氧气含量。
材料一:已知过氧化钠(Na2O2)与水较快反应,反应方程式是 ,过氧化钙(CaO2)与Na2O2性质相似,与水缓慢反应放出氧气。
材料二:20℃时,NaOH的溶解度为109g,Ca(OH)2的溶解度为0.165g。
(1)试写出CaO2与H2O反应的化学方程式 ;
(2)长途运输活鱼,人们选择CaO2而不选择Na2O2作增氧剂的理由可能是 (写出一条即可)
18.实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 (用化学式表示),写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,常用 来清洗。
三、综合题
19.近年来我国在航天领域取得了重大成就,2021年10月16日0时23分,神舟十三号载人飞船成功发射。我国自主研制的航天员舱外服为航天员成功进行太空行走提供了可靠的保证,航天员舱外服内含有与氢氧化钠性质相似的氢氧化锂(LiOH),宇航服是保护宇航员在太空不受低温、射线等的侵害并提供人类生存所需的氧气的保护服。宇航服的氧气罐为太空人提供氧气,而排出的二氧化碳则由氢氧化锂所吸收。
(1)现宇航员呼吸出4.4g二氧化碳,航天员舱外服至少含有 g氢氧化锂(LiOH)才能完全吸收。
(2)你认为氢氧化锂不可能具有的化学性质是____(填标号)。
A.与二氧化碳反应 B.与盐酸反应
C.与氧化铁反应 D.与氯化铜溶液反应
(3)已知碳酸锂是微溶于水,其它锂的化合物都易溶于水,设计两种制备氢氧化锂的方案(要求含锂原料分别属于不同的物质类别)。完成下表:
方案 预期发生的化学方程式 依据的反应规律
① 金属氧化物和水反应生成碱
②
20.硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应:
②与碳酸钠溶液反应:
③与氯化钡溶液反应:
上述反应中,属于酸的共同性质的是 (填编号)
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
21.化学试剂常常要密封保存,但原因各不相同。
(1)浓盐酸密封保存的原因是什么 ?
(2)氢氧化钠溶液若敞口放置会发生变质,请用化学方程式表示其变质原因 。
(3)如何检验NaOH溶液是否完全变质,请简述实验方法 。
22.实验是学习化学的一条重要途径,正确的实验操作是实验成功的关键.造成下列实验后果的原因可能是:
(1)用试管加热固体,实验结束后,试管炸裂: ;
(2)用高锰酸钾制取氧气,水槽中的水变成了紫红色: ;
(3)用红磷测定空气中氧气含量的实验中,结果偏低 ;
(4)倾倒液体药品后,标签被腐蚀: ;
答案解析部分
1.【答案】C
2.【答案】D
3.【答案】A
4.【答案】C
5.【答案】A
6.【答案】B
7.【答案】D
8.【答案】A
9.【答案】B
10.【答案】A
11.【答案】B
12.【答案】D
13.【答案】碱;Ca(OH)2+H2SO4=CaSO4+2H2O;100.15;否;B
14.【答案】⑥;①;④;②
15.【答案】30;左盘的烧杯中;硼酸
16.【答案】二氧化碳或CO2;2NaOH+CO2=Na2CO3+H2O;密封
17.【答案】(1)2CaO2+2H2O═2Ca(OH)2+O2↑
(2)过氧化钠与水反应生成的氢氧化钠具有强烈的腐蚀性(合理即可)
18.【答案】CaCO3;CO2+Ca(OH)2═CaCO3↓+H2O;不能;稀盐酸
19.【答案】(1)4.8
(2)C
(3);;盐和碱反应生成新碱和新盐,生成物有沉淀
20.【答案】(1)吸水性
(2)Fe+H2SO4=FeSO4+H2↑;Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;H2SO4+BaCl2=BaSO4↓+2HCl;①②
(3)②③
21.【答案】(1)浓盐酸具有挥发性
(2)2NaOH+CO2=Na2CO3+H2O
(3)取少量样品于试管中,加入足量氯化钙溶液,有白色沉淀产生;取少量充分反应后的溶液于试管中,滴入酚酞试液,若酚酞试液变红色,说明氢氧化钠溶液部分变质,若不变红色,说明氢氧化钠溶液全部变质
22.【答案】(1)试管未冷却就立即用冷水清洗
(2)试管口没有放一团棉花
(3)红磷量不足(装置漏气、未冷却至室温就打开弹簧夹)
(4)倾倒液体时,标签没有朝向手心
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
