3.1.2物质的聚集状态与晶体的常识(第2课时 晶胞)(课件精讲)(共30张PPT)高二化学同步课件精讲(人教版2019选择性必修2)
文档属性
| 名称 | 3.1.2物质的聚集状态与晶体的常识(第2课时 晶胞)(课件精讲)(共30张PPT)高二化学同步课件精讲(人教版2019选择性必修2) |

|
|
| 格式 | pptx | ||
| 文件大小 | 16.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-04 00:00:00 | ||
图片预览








文档简介
(共30张PPT)
第一节 物质的聚集状态与晶体的常识
课时2
晶胞
第三章 晶体结构与性质
学习
目标
PART
01
PART
02
晶体化学式的确定
PART
03
均摊法
晶胞的概念
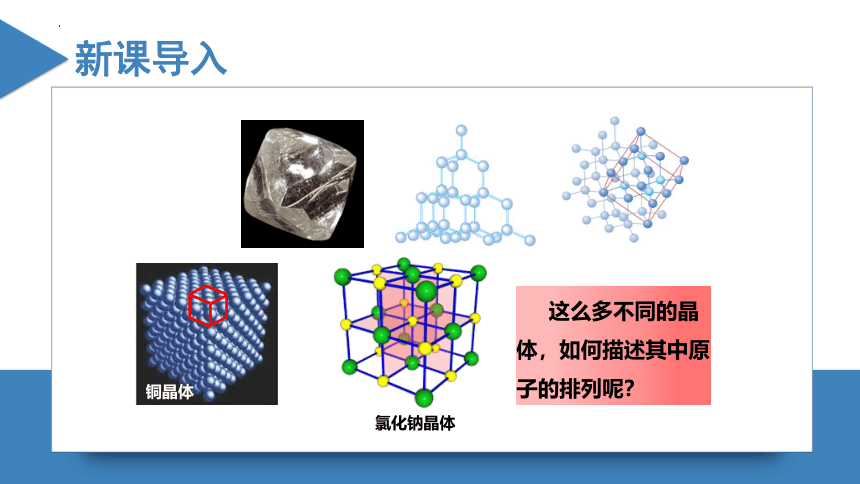
铜晶体
氯化钠晶体
这么多不同的晶体,如何描述其中原子的排列呢?
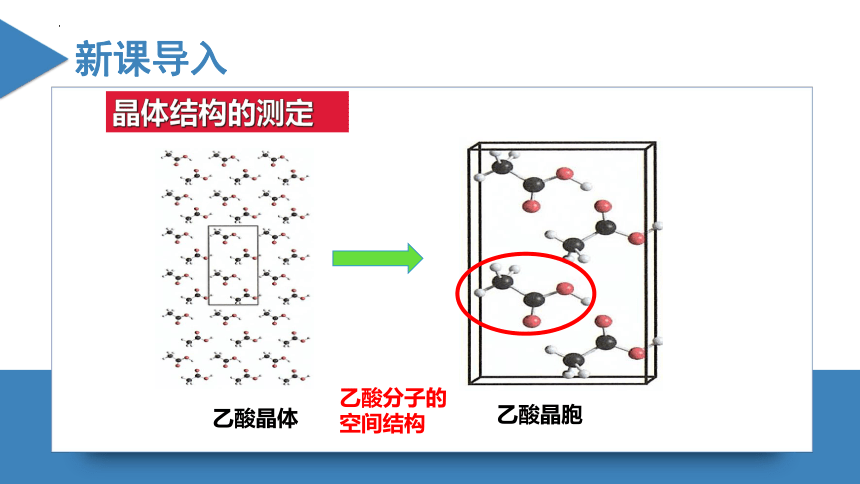
乙酸晶体
乙酸晶胞
乙酸分子的空间结构
晶体结构的测定
01
晶胞的概念
01、晶胞的概念
蜂巢与蜂室
铜晶体
铜晶胞
1.定义:描述晶体结构的基本单元。晶胞是晶体中最小的
结构重复单元。
01、晶胞的概念
晶体和晶胞的关系
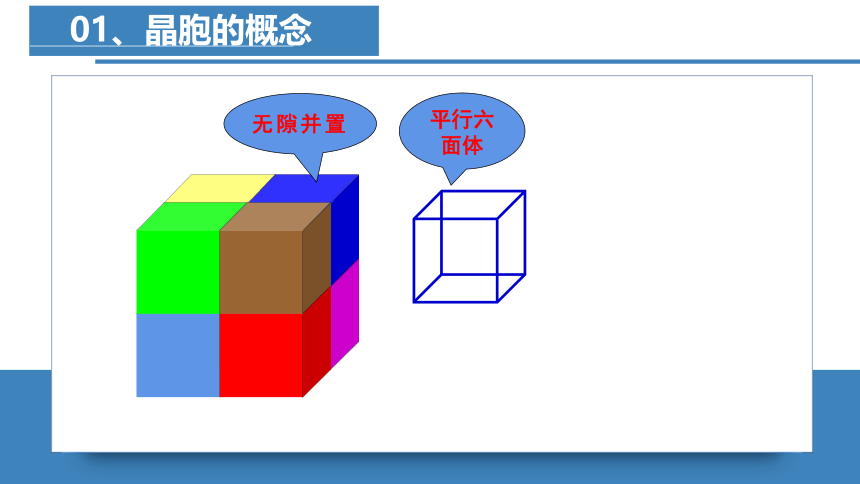
一般来说,常规的晶胞都是平行六面体,整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。
(1)“无隙”是相邻晶胞之间没有任何间隙。
(2)“并置”是所有晶胞都是平行排列的,取向相同。
(3)所有晶胞的形状及其内部的原子种类、个数及几何排列是完全相同的。
01、晶胞的概念
平行六面体
无隙并置
01、晶胞的概念
(1)晶胞是否全是平行六面体?(2)由晶胞构成的晶体,其化学式是否表示一个分子中原子的数目?
【提示】 (1)不一定,如有的晶胞呈六棱柱形。(2)不表示,只表示每个晶胞中各类原子的最简整数比。
【思考与讨论】
01、晶胞的概念
2.判断下列六面体是否是晶胞?
A图中的晶体结构满足
晶胞的特点,是晶胞。
B图中的晶体结构,不满足晶胞“8个顶角相同”的要求,无法进行“无隙并置”,不是晶胞。
C图中的晶体结构,不满足晶胞“三套各4根平行棱分别相同”的要求,无法进行“无隙并置”,不是晶胞。
D图中的晶体结构,不满足“三套各两个平行面分别相同”的要求,无法进行“无隙并置”,不是晶胞。
【思考与讨论】
02
均摊法
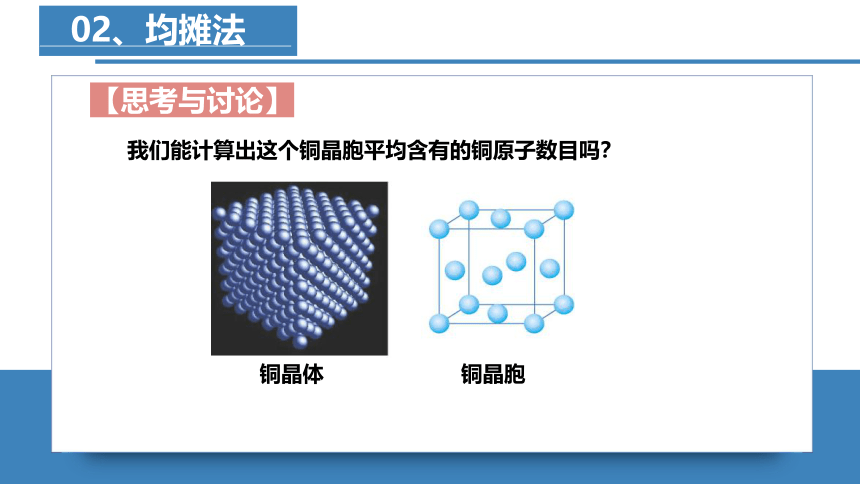
我们能计算出这个铜晶胞平均含有的铜原子数目吗?
铜晶体
铜晶胞
【思考与讨论】
02、均摊法
1
2
4
3
7
6
8
5
1
2
2
1
3
4
1
体心:1
面心:1/2
顶点:1/8
棱边:1/4
02、均摊法
立方晶胞
体心:
1
面心:
1/2
棱边:
1/4
顶点:
1/8
小结:晶胞对质点的占有率
02、均摊法
六方晶胞中粒子的计算方法
顶角:1/6
上、下棱:1/4
侧棱:1/3
面上:1/2
内部:1
02、均摊法
三棱柱
体心
1
面心
1/2
棱边
水平1/4 竖1/6
顶点
1/12
02、均摊法
(1)立方体
(2)三棱柱
(3)六棱柱
体心
1
面心
1/2
棱边
1/4
顶点
1/8
体心
1
面心
1/2
棱边
水平1/4 竖1/6
顶点
1/12
体心
1
面心
1/2
棱边
水平1/4 竖1/3
顶点
1/6
02、均摊法
金属铜的一个晶胞的原子数=8× +6× =4
2
1
8
1
金属钠(C) 金属锌(Zn) 碘(I2) 金刚石(C)
(1)晶胞有几套平行棱?有几套平行面?
(2)数一数,它们分别平均含有几个原子?
晶胞有3套平行棱,有3套平行面?
03
晶体化学式
的确定
03、晶体化学式的确定
A
B
1.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
化学式:
AB
03、晶体化学式的确定
2.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
A
B
化学式:
A2B
BA2
03、晶体化学式的确定
A
B
化学式:
3.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
AB
03、晶体化学式的确定
B
化学式:
A
4.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
C
ABC3
下图为高温超导领域的一种化合物——钙钛矿晶体结构,该结构是具有代表性的最小重复单元。
1)在该物质的晶体中,每个钛离子周围与它最接近且距离相等的钛离子共有 个
2)该晶体结构单元中,氧、钛、钙离子的个数比是 。
6
3∶1∶1
Ti
O
Ca
O:12×1/4=3
Ti: 8 ×1/8=1
Ca:1
1.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是
A.相邻晶胞之间没有任何间隙
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.“并置”是指所有晶胞都是平行排列的
B
2.钙、钛、氧可形成如图所示的晶胞,则所形成的物质的化学式可表示为( )
A.Ca8TiO12 B.Ca4TiO6 C.Ca4TiO3 D.CaTiO3
D
3.金属晶体中金属原子有三种常见的堆积方式,六方最密堆积、面心立方最密堆积和体心立方堆积,下图分别代表着三种晶体的晶体结构,其晶胞内金属原子个数比为
A.1∶2∶1 B.11∶8∶4 C.9∶8∶4 D.9∶14∶9
A
4.纳米材料的表面微粒数占微粒总数的比例极大,这是它有许多特殊性质的原因, 假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数占总微粒数的百分数为
A、33.3%B、50%
C、87.5%D、96.3%
D
5.某物质的晶体中,含A、B、C三种元素,其排列方式如右图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为
A.1:3:1 B.2:3:1C.2:2:1 D.1:3:3
A
第一节 物质的聚集状态与晶体的常识
课时2
晶胞
第三章 晶体结构与性质
学习
目标
PART
01
PART
02
晶体化学式的确定
PART
03
均摊法
晶胞的概念
铜晶体
氯化钠晶体
这么多不同的晶体,如何描述其中原子的排列呢?
乙酸晶体
乙酸晶胞
乙酸分子的空间结构
晶体结构的测定
01
晶胞的概念
01、晶胞的概念
蜂巢与蜂室
铜晶体
铜晶胞
1.定义:描述晶体结构的基本单元。晶胞是晶体中最小的
结构重复单元。
01、晶胞的概念
晶体和晶胞的关系
一般来说,常规的晶胞都是平行六面体,整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。
(1)“无隙”是相邻晶胞之间没有任何间隙。
(2)“并置”是所有晶胞都是平行排列的,取向相同。
(3)所有晶胞的形状及其内部的原子种类、个数及几何排列是完全相同的。
01、晶胞的概念
平行六面体
无隙并置
01、晶胞的概念
(1)晶胞是否全是平行六面体?(2)由晶胞构成的晶体,其化学式是否表示一个分子中原子的数目?
【提示】 (1)不一定,如有的晶胞呈六棱柱形。(2)不表示,只表示每个晶胞中各类原子的最简整数比。
【思考与讨论】
01、晶胞的概念
2.判断下列六面体是否是晶胞?
A图中的晶体结构满足
晶胞的特点,是晶胞。
B图中的晶体结构,不满足晶胞“8个顶角相同”的要求,无法进行“无隙并置”,不是晶胞。
C图中的晶体结构,不满足晶胞“三套各4根平行棱分别相同”的要求,无法进行“无隙并置”,不是晶胞。
D图中的晶体结构,不满足“三套各两个平行面分别相同”的要求,无法进行“无隙并置”,不是晶胞。
【思考与讨论】
02
均摊法
我们能计算出这个铜晶胞平均含有的铜原子数目吗?
铜晶体
铜晶胞
【思考与讨论】
02、均摊法
1
2
4
3
7
6
8
5
1
2
2
1
3
4
1
体心:1
面心:1/2
顶点:1/8
棱边:1/4
02、均摊法
立方晶胞
体心:
1
面心:
1/2
棱边:
1/4
顶点:
1/8
小结:晶胞对质点的占有率
02、均摊法
六方晶胞中粒子的计算方法
顶角:1/6
上、下棱:1/4
侧棱:1/3
面上:1/2
内部:1
02、均摊法
三棱柱
体心
1
面心
1/2
棱边
水平1/4 竖1/6
顶点
1/12
02、均摊法
(1)立方体
(2)三棱柱
(3)六棱柱
体心
1
面心
1/2
棱边
1/4
顶点
1/8
体心
1
面心
1/2
棱边
水平1/4 竖1/6
顶点
1/12
体心
1
面心
1/2
棱边
水平1/4 竖1/3
顶点
1/6
02、均摊法
金属铜的一个晶胞的原子数=8× +6× =4
2
1
8
1
金属钠(C) 金属锌(Zn) 碘(I2) 金刚石(C)
(1)晶胞有几套平行棱?有几套平行面?
(2)数一数,它们分别平均含有几个原子?
晶胞有3套平行棱,有3套平行面?
03
晶体化学式
的确定
03、晶体化学式的确定
A
B
1.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
化学式:
AB
03、晶体化学式的确定
2.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
A
B
化学式:
A2B
BA2
03、晶体化学式的确定
A
B
化学式:
3.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
AB
03、晶体化学式的确定
B
化学式:
A
4.根据离子晶体的晶胞结构,判断下列离子晶体的化学式:(A表示阳离子)
C
ABC3
下图为高温超导领域的一种化合物——钙钛矿晶体结构,该结构是具有代表性的最小重复单元。
1)在该物质的晶体中,每个钛离子周围与它最接近且距离相等的钛离子共有 个
2)该晶体结构单元中,氧、钛、钙离子的个数比是 。
6
3∶1∶1
Ti
O
Ca
O:12×1/4=3
Ti: 8 ×1/8=1
Ca:1
1.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是
A.相邻晶胞之间没有任何间隙
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.“并置”是指所有晶胞都是平行排列的
B
2.钙、钛、氧可形成如图所示的晶胞,则所形成的物质的化学式可表示为( )
A.Ca8TiO12 B.Ca4TiO6 C.Ca4TiO3 D.CaTiO3
D
3.金属晶体中金属原子有三种常见的堆积方式,六方最密堆积、面心立方最密堆积和体心立方堆积,下图分别代表着三种晶体的晶体结构,其晶胞内金属原子个数比为
A.1∶2∶1 B.11∶8∶4 C.9∶8∶4 D.9∶14∶9
A
4.纳米材料的表面微粒数占微粒总数的比例极大,这是它有许多特殊性质的原因, 假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数占总微粒数的百分数为
A、33.3%B、50%
C、87.5%D、96.3%
D
5.某物质的晶体中,含A、B、C三种元素,其排列方式如右图所示(其中前后两面心上的B原子不能画出),晶体中A、B、C的原子个数比依次为
A.1:3:1 B.2:3:1C.2:2:1 D.1:3:3
A
