化学人教版(2019)选择性必修3 2.3.1苯的结构与性质(共28张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 2.3.1苯的结构与性质(共28张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 10.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-06 10:12:09 | ||
图片预览




文档简介
(共28张PPT)
学习
目标
第1课时
苯的结构与性质
PART
01
PART
02
从化学键的特殊性了解苯的结构特点,进而理解苯性质的特殊性,培养宏观辨识与微观探析的能力。
通过回顾苯的发现史,了解研究有机物的一般过程。根据“结构决定性质”,预测苯的化学性质,并能设计实验进行验证
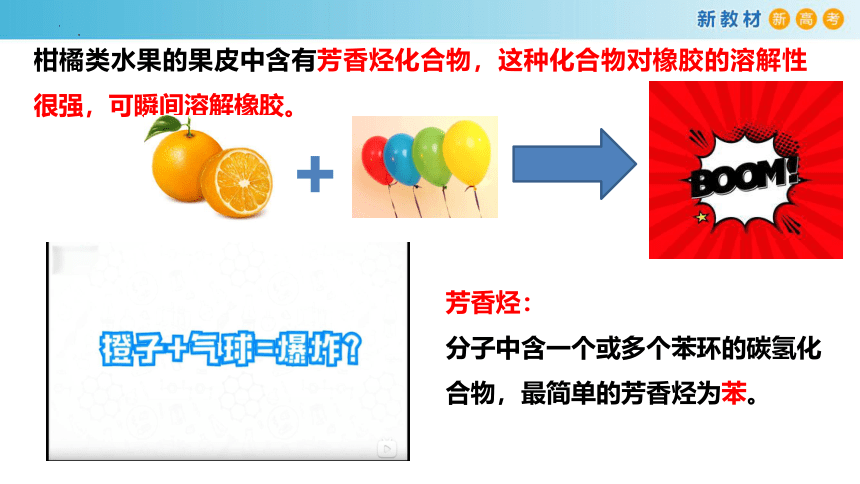
柑橘类水果的果皮中含有芳香烃化合物,这种化合物对橡胶的溶解性很强,可瞬间溶解橡胶。
芳香烃:
分子中含一个或多个苯环的碳氢化合物,最简单的芳香烃为苯。
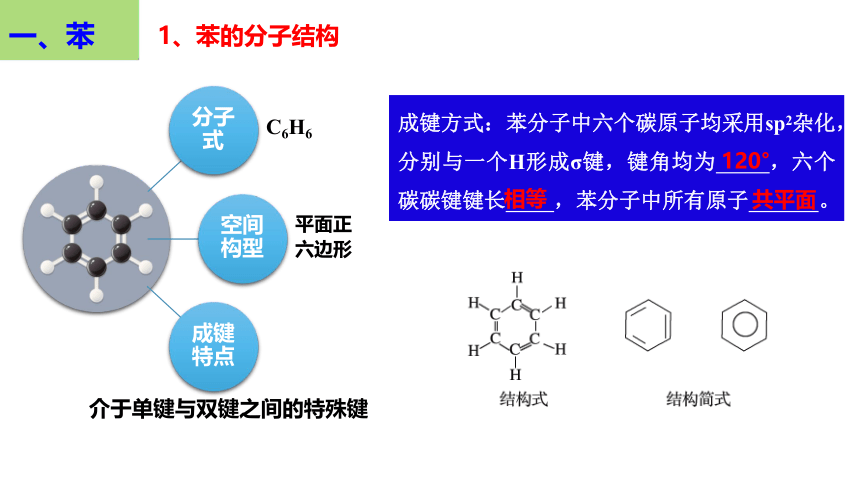
分子式
C6H6
空间构型
平面正
六边形
成键特点
介于单键与双键之间的特殊键
成键方式:苯分子中六个碳原子均采用sp2杂化,分别与一个H形成σ键,键角均为 ,六个碳碳键键长 ,苯分子中所有原子 。
120°
相等
共平面
一、苯
1、苯的分子结构
苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的键。苯分子中六个碳原子等效,六个氢原子等效。
思考1:苯分子中的大π键是如何形成的?与碳碳双键中的π键有什么不同?
一、苯
1、苯的分子结构
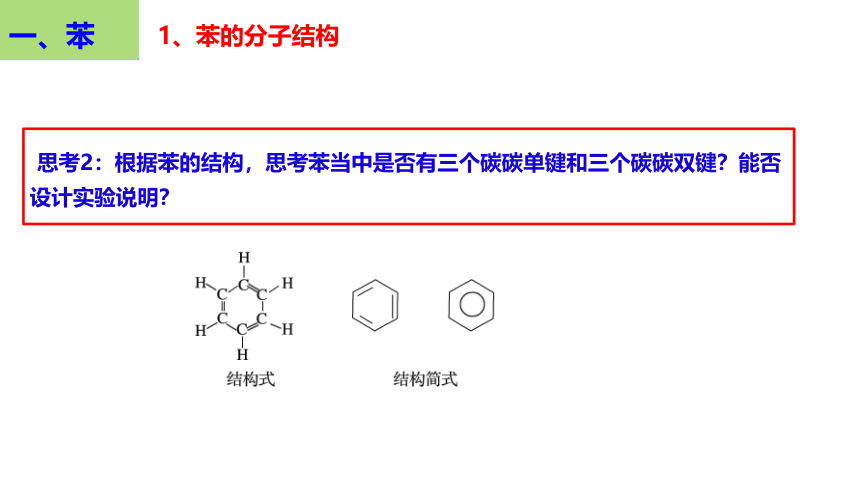
思考2:根据苯的结构,思考苯当中是否有三个碳碳单键和三个碳碳双键?能否设计实验说明?
一、苯
1、苯的分子结构
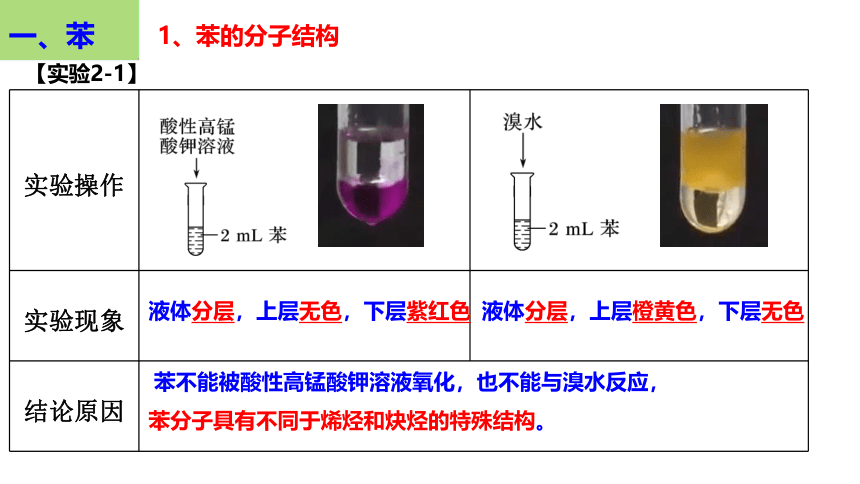
实验操作
实验现象
结论原因 液体分层,上层无色,下层紫红色
液体分层,上层橙黄色,下层无色
苯不能被酸性高锰酸钾溶液氧化,也不能与溴水反应,
苯分子具有不同于烯烃和炔烃的特殊结构。
【实验2-1】
一、苯
1、苯的分子结构
水层显紫色,没有褪色
苯层显黄色,苯能萃取溴水中Br2
(1)为什么两支试管溶液都发生了分层?
苯不溶于水,密度比水小。
(2)右侧试管中上层溶液显黄色,说明苯对Br2溶解有什么规律?
溴能在苯中溶解且溶解度大于水溶液中,苯能萃取溴水中的溴。
【实验2-1】
一、苯
1、苯的分子结构
思考3:根据已学知识,你认为下列结构是否为同一物质?
一、苯
1、苯的分子结构
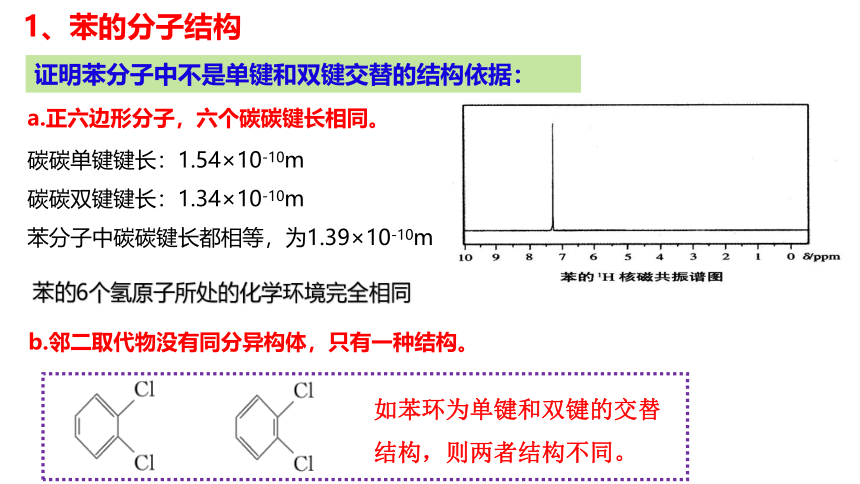
b.邻二取代物没有同分异构体,只有一种结构。
如苯环为单键和双键的交替结构,则两者结构不同。
碳碳单键键长:1.54×10-10m
碳碳双键键长:1.34×10-10m
苯分子中碳碳键长都相等,为1.39×10-10m
a.正六边形分子,六个碳碳键长相同。
证明苯分子中不是单键和双键交替的结构依据:
苯的6个氢原子所处的化学环境完全相同
1、苯的分子结构
二:苯的性质
颜色状态 密度、溶解性 毒性 熔、沸点 挥发性
色 体 溶于水且密度比水___ 毒 较低 易挥发
1.苯的物理性质
无
液
不
小
有
2.苯的化学性质
(1)氧化反应——可燃性
化学方程式:_______________________________(火焰明亮,带有黑烟)。
(2)取代反应
①溴代反应:_________________________________;纯净的溴苯是一种_____液体,有 的气味, 溶于水,密度比水的 。
+Br2 +HBr↑
溴苯
无色
特殊
不
大
1.苯的化学性质
苯分子中的大π键比较稳定,在通常情况下不易发生烯烃和炔烃所容易发生的加成反应
二:苯的性质
① 烧瓶中充满红棕色气体,导管口有白雾(HBr遇水蒸气形成)
② 向锥形瓶中加入AgNO3溶液出现浅黄色沉淀AgBr。
③ 烧瓶底部有褐色(溶有Br2)不溶于水液体生成。
①苯与液溴制取溴苯
问题2:溴苯不是无色的吗?
单质溴溶于溴苯使无色的溴苯呈褐色。
长导管的作用:导气、冷凝回流。
注意:①必须是纯溴。
②锥形瓶中的导管不能伸入到液面以下,防止HBr极易溶于水发生倒吸。
2Fe + 3Br2 = 2FeBr3
问题1:Fe屑的作用是什么?
与溴反应生成催化剂
溴苯的制取实验装置
实验现象:
二:苯的性质
分液
除去溴苯中的溴可加入NaOH溶液,振荡,再用分液漏斗分液
用水洗涤,除去溴苯中能溶于水的杂质(如FeBr3、HBr及Br2等)
用10%NaOH溶液洗涤:除去溴苯中未反应的Br2,转化成可溶于水的物质
用水洗涤,除去NaOH及生成的盐NaBr和NaBrO
用H2SO4吸水干燥,除去水
使溴苯和苯进行分离,除去溴苯中的苯
提纯方法
Br2 + 2NaOH = NaBr + NaBrO + H2O
问题2:如何提纯溴苯?
二:苯的性质
问题3.哪些现象说明发生了取代反应而不是加成反应?
苯与溴反应生成溴苯的同时有溴化氢生成,说明它们发生了取代反应而非加成反应。因加成反应不会生成溴化氢。
苯和液溴 —— 取代 —— 化学反应
苯和溴水 —— 萃取 —— 物理变化
二:苯的性质
溴苯的实验改进
创新装置的优点:
①有分液漏斗,可控制液溴的量。
②加装一个用CCl4除溴蒸气的装置。
③倒扣的漏斗可以防倒吸,还有利于尾气吸收。
思考与讨论:根据上述实验的分析,你认为溴苯的制备实验还可以怎样改进?
二:苯的性质
+HO—NO2 +H2O
硝基苯
2.苯的化学性质
(2)取代反应
②硝化反应:在浓硫酸作用下,苯在50~60℃与浓硝酸发生取代反应。
(2)纯净的硝基苯是一种无色油状液体,有苦杏仁气味,不溶于水,密度比水大。
易溶于有机溶剂。遇明火、高热会燃烧、爆炸。硝基苯蒸气有毒性。
(1)浓硫酸(催化剂、吸水剂)
(3)本实验中硝基苯因溶有少量NO2而呈黄色
注:
二:苯的性质
① 反应温度控制在50-60℃,需水浴加热
② 苯分子中H被-NO2(硝基)取代的反应叫硝化反应
注意事项:
① 温度计水银球的在水浴中,且不能触底;
② 长导管的作用—冷凝回流;
③ 浓硫酸的作用—催化剂和吸水剂。
苯
浓HNO3
浓H2SO4
硝基苯的制取实验装置
实验现象:瓶底生成不溶于水的无色油状液体
②苯的硝化反应
拓展:“水浴加热”容易控制恒温,且易使被加热物受热均匀。需要加热,且要控制在100℃以下的实验,均可采用水浴加热。如果超过100 ℃,还可采用油浴(0~300℃)、沙浴温度更高。
长导管的作用:冷凝回流。
二:苯的性质
用5%NaOH溶液洗涤:除去硝基苯中的硝酸、硫酸及NO2
用蒸馏水洗涤:除去氢氧化钠溶液及与其反应生成的盐
用无水氯化钙干燥,除去水
使硝基苯和苯进行分离,除去硝基苯中的苯
用蒸馏水洗涤:除去硝基苯中的硝酸、硫酸及NO2
分液
问题:如何提硝基苯?
提纯方法
③苯的磺化反应:___________________________________________;
苯磺酸 溶于水,是一种 酸,可以看作硫酸分子里的一个 被苯环取代的产物。
易
强
羟基
+HO—SO3H +H2O
苯磺酸
2.苯的化学性质
(2)取代反应
二:苯的性质
2.苯的化学性质
(3)加成反应
苯的大π键比较稳定,通常状态下不易发生加成反应,在Pt、Ni等催化剂并
加热的条件下,苯能与氢气发生加成反应:_______________________。
+3H2
环己烷
二:苯的性质
小结
苯兼有饱和烃和不饱和烃的性质
难氧化,易取代,能加成
1.苯环实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有
①苯的间位二取代物只有一种 ②苯的邻位二取代物只有一种 ③苯分子中碳碳键的键长均相等 ④苯不能使酸性KMnO4溶液褪色 ⑤苯在加热和催化剂存在条件下,与氢气发生加成反应 ⑥苯在FeBr3存在的条件下,与液溴发生取代反应,但不能因化学变化而使溴水褪色
A.①②③④ B.②③④⑥ C.③④⑤⑥ D.全部
应用体验
B
2.下列关于苯的叙述正确的是
A.反应①为取代反应,有机产物与水混合浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子中含有
三个碳碳双键
B
3.实验室制取硝基苯的反应装置如图所示,关于实验操作或叙述错误的是
A.试剂加入顺序:先加浓硝酸,再加浓硫酸,最后加入苯
B.实验时,水浴温度需控制在50~60 ℃
C.长玻璃导管兼起冷凝回流苯和硝酸的作用,以提高反应物
的转化率
D.反应后的混合液经水洗、碱溶液洗涤、结晶,得到硝基苯
D
4.下列实验操作中正确的是
A.将溴水、FeBr3和苯混合加热即可制得溴苯
B.除去溴苯中红棕色的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液
C.苯和浓HNO3在浓H2SO4催化下反应制取硝基苯时需水浴加热,温度计
水银球应放在混合液中
D.制取硝基苯时,应先加2 mL浓H2SO4,再加入1.5 mL浓HNO3,然后再
滴入约1 mL苯,最后放在水浴中加热
B
D
B
A
学习
目标
第1课时
苯的结构与性质
PART
01
PART
02
从化学键的特殊性了解苯的结构特点,进而理解苯性质的特殊性,培养宏观辨识与微观探析的能力。
通过回顾苯的发现史,了解研究有机物的一般过程。根据“结构决定性质”,预测苯的化学性质,并能设计实验进行验证
柑橘类水果的果皮中含有芳香烃化合物,这种化合物对橡胶的溶解性很强,可瞬间溶解橡胶。
芳香烃:
分子中含一个或多个苯环的碳氢化合物,最简单的芳香烃为苯。
分子式
C6H6
空间构型
平面正
六边形
成键特点
介于单键与双键之间的特殊键
成键方式:苯分子中六个碳原子均采用sp2杂化,分别与一个H形成σ键,键角均为 ,六个碳碳键键长 ,苯分子中所有原子 。
120°
相等
共平面
一、苯
1、苯的分子结构
苯分子中的碳碳键是介于碳碳单键和碳碳双键之间的特殊的键。苯分子中六个碳原子等效,六个氢原子等效。
思考1:苯分子中的大π键是如何形成的?与碳碳双键中的π键有什么不同?
一、苯
1、苯的分子结构
思考2:根据苯的结构,思考苯当中是否有三个碳碳单键和三个碳碳双键?能否设计实验说明?
一、苯
1、苯的分子结构
实验操作
实验现象
结论原因 液体分层,上层无色,下层紫红色
液体分层,上层橙黄色,下层无色
苯不能被酸性高锰酸钾溶液氧化,也不能与溴水反应,
苯分子具有不同于烯烃和炔烃的特殊结构。
【实验2-1】
一、苯
1、苯的分子结构
水层显紫色,没有褪色
苯层显黄色,苯能萃取溴水中Br2
(1)为什么两支试管溶液都发生了分层?
苯不溶于水,密度比水小。
(2)右侧试管中上层溶液显黄色,说明苯对Br2溶解有什么规律?
溴能在苯中溶解且溶解度大于水溶液中,苯能萃取溴水中的溴。
【实验2-1】
一、苯
1、苯的分子结构
思考3:根据已学知识,你认为下列结构是否为同一物质?
一、苯
1、苯的分子结构
b.邻二取代物没有同分异构体,只有一种结构。
如苯环为单键和双键的交替结构,则两者结构不同。
碳碳单键键长:1.54×10-10m
碳碳双键键长:1.34×10-10m
苯分子中碳碳键长都相等,为1.39×10-10m
a.正六边形分子,六个碳碳键长相同。
证明苯分子中不是单键和双键交替的结构依据:
苯的6个氢原子所处的化学环境完全相同
1、苯的分子结构
二:苯的性质
颜色状态 密度、溶解性 毒性 熔、沸点 挥发性
色 体 溶于水且密度比水___ 毒 较低 易挥发
1.苯的物理性质
无
液
不
小
有
2.苯的化学性质
(1)氧化反应——可燃性
化学方程式:_______________________________(火焰明亮,带有黑烟)。
(2)取代反应
①溴代反应:_________________________________;纯净的溴苯是一种_____液体,有 的气味, 溶于水,密度比水的 。
+Br2 +HBr↑
溴苯
无色
特殊
不
大
1.苯的化学性质
苯分子中的大π键比较稳定,在通常情况下不易发生烯烃和炔烃所容易发生的加成反应
二:苯的性质
① 烧瓶中充满红棕色气体,导管口有白雾(HBr遇水蒸气形成)
② 向锥形瓶中加入AgNO3溶液出现浅黄色沉淀AgBr。
③ 烧瓶底部有褐色(溶有Br2)不溶于水液体生成。
①苯与液溴制取溴苯
问题2:溴苯不是无色的吗?
单质溴溶于溴苯使无色的溴苯呈褐色。
长导管的作用:导气、冷凝回流。
注意:①必须是纯溴。
②锥形瓶中的导管不能伸入到液面以下,防止HBr极易溶于水发生倒吸。
2Fe + 3Br2 = 2FeBr3
问题1:Fe屑的作用是什么?
与溴反应生成催化剂
溴苯的制取实验装置
实验现象:
二:苯的性质
分液
除去溴苯中的溴可加入NaOH溶液,振荡,再用分液漏斗分液
用水洗涤,除去溴苯中能溶于水的杂质(如FeBr3、HBr及Br2等)
用10%NaOH溶液洗涤:除去溴苯中未反应的Br2,转化成可溶于水的物质
用水洗涤,除去NaOH及生成的盐NaBr和NaBrO
用H2SO4吸水干燥,除去水
使溴苯和苯进行分离,除去溴苯中的苯
提纯方法
Br2 + 2NaOH = NaBr + NaBrO + H2O
问题2:如何提纯溴苯?
二:苯的性质
问题3.哪些现象说明发生了取代反应而不是加成反应?
苯与溴反应生成溴苯的同时有溴化氢生成,说明它们发生了取代反应而非加成反应。因加成反应不会生成溴化氢。
苯和液溴 —— 取代 —— 化学反应
苯和溴水 —— 萃取 —— 物理变化
二:苯的性质
溴苯的实验改进
创新装置的优点:
①有分液漏斗,可控制液溴的量。
②加装一个用CCl4除溴蒸气的装置。
③倒扣的漏斗可以防倒吸,还有利于尾气吸收。
思考与讨论:根据上述实验的分析,你认为溴苯的制备实验还可以怎样改进?
二:苯的性质
+HO—NO2 +H2O
硝基苯
2.苯的化学性质
(2)取代反应
②硝化反应:在浓硫酸作用下,苯在50~60℃与浓硝酸发生取代反应。
(2)纯净的硝基苯是一种无色油状液体,有苦杏仁气味,不溶于水,密度比水大。
易溶于有机溶剂。遇明火、高热会燃烧、爆炸。硝基苯蒸气有毒性。
(1)浓硫酸(催化剂、吸水剂)
(3)本实验中硝基苯因溶有少量NO2而呈黄色
注:
二:苯的性质
① 反应温度控制在50-60℃,需水浴加热
② 苯分子中H被-NO2(硝基)取代的反应叫硝化反应
注意事项:
① 温度计水银球的在水浴中,且不能触底;
② 长导管的作用—冷凝回流;
③ 浓硫酸的作用—催化剂和吸水剂。
苯
浓HNO3
浓H2SO4
硝基苯的制取实验装置
实验现象:瓶底生成不溶于水的无色油状液体
②苯的硝化反应
拓展:“水浴加热”容易控制恒温,且易使被加热物受热均匀。需要加热,且要控制在100℃以下的实验,均可采用水浴加热。如果超过100 ℃,还可采用油浴(0~300℃)、沙浴温度更高。
长导管的作用:冷凝回流。
二:苯的性质
用5%NaOH溶液洗涤:除去硝基苯中的硝酸、硫酸及NO2
用蒸馏水洗涤:除去氢氧化钠溶液及与其反应生成的盐
用无水氯化钙干燥,除去水
使硝基苯和苯进行分离,除去硝基苯中的苯
用蒸馏水洗涤:除去硝基苯中的硝酸、硫酸及NO2
分液
问题:如何提硝基苯?
提纯方法
③苯的磺化反应:___________________________________________;
苯磺酸 溶于水,是一种 酸,可以看作硫酸分子里的一个 被苯环取代的产物。
易
强
羟基
+HO—SO3H +H2O
苯磺酸
2.苯的化学性质
(2)取代反应
二:苯的性质
2.苯的化学性质
(3)加成反应
苯的大π键比较稳定,通常状态下不易发生加成反应,在Pt、Ni等催化剂并
加热的条件下,苯能与氢气发生加成反应:_______________________。
+3H2
环己烷
二:苯的性质
小结
苯兼有饱和烃和不饱和烃的性质
难氧化,易取代,能加成
1.苯环实际上不具有碳碳单键和碳碳双键的简单交替结构,可以作为证据的事实有
①苯的间位二取代物只有一种 ②苯的邻位二取代物只有一种 ③苯分子中碳碳键的键长均相等 ④苯不能使酸性KMnO4溶液褪色 ⑤苯在加热和催化剂存在条件下,与氢气发生加成反应 ⑥苯在FeBr3存在的条件下,与液溴发生取代反应,但不能因化学变化而使溴水褪色
A.①②③④ B.②③④⑥ C.③④⑤⑥ D.全部
应用体验
B
2.下列关于苯的叙述正确的是
A.反应①为取代反应,有机产物与水混合浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并带有浓烟
C.反应③为取代反应,有机产物是一种烃
D.反应④中1 mol苯最多与3 mol H2发生加成反应,是因为苯分子中含有
三个碳碳双键
B
3.实验室制取硝基苯的反应装置如图所示,关于实验操作或叙述错误的是
A.试剂加入顺序:先加浓硝酸,再加浓硫酸,最后加入苯
B.实验时,水浴温度需控制在50~60 ℃
C.长玻璃导管兼起冷凝回流苯和硝酸的作用,以提高反应物
的转化率
D.反应后的混合液经水洗、碱溶液洗涤、结晶,得到硝基苯
D
4.下列实验操作中正确的是
A.将溴水、FeBr3和苯混合加热即可制得溴苯
B.除去溴苯中红棕色的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液
C.苯和浓HNO3在浓H2SO4催化下反应制取硝基苯时需水浴加热,温度计
水银球应放在混合液中
D.制取硝基苯时,应先加2 mL浓H2SO4,再加入1.5 mL浓HNO3,然后再
滴入约1 mL苯,最后放在水浴中加热
B
D
B
A
