实验活动 4 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 实验活动 4 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 39.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-05 00:00:00 | ||
图片预览


文档简介
实验活动 4 金属的物理性质和某些化学性质 同步练习
一、单选题
1.下列说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.赤铁矿、磁铁矿是重要的金属资源
C.铝比铁活泼,所以铁比铝耐腐蚀
D.纯铜的熔点小于铜锌合金
2.向一定量CuSO4溶液中加入过量铁粉,充分反应后过滤得到滤渣和滤液,下列判断正确的是( )
A.得到的滤液呈蓝色
B.所得滤渣的质量比加入铁粉的大
C.向滤渣中滴加稀盐酸无气泡产生
D.滤液中一定有FeSO4,可能有CuSO4
3.下列关于家庭小实验的说法正确的是( )
A.淬火的钢针弯曲制成鱼钩
B.用食盐除去热水瓶内胆壁上的水垢
C.用10%的烧碱溶液自制“叶脉书签”
D.制作简易净水器时,为了达到好的净水效果,活性炭应该放在最上层
4.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粒,充分反应后过滤,往滤渣中加入稀盐酸,无气泡产生。你能得出的结论是( )
A.滤渣中一定有Zn B.滤渣中一定有Ag和Cu
C.滤渣中可能有Cu D.滤液中一定有Ag+和Cu2+
5.在下列溶液中分别放入锌粒,一段时间后把锌粒取出,溶液质量减少的是()
A.MgCl2溶液 B.盐酸 C.稀硫酸 D.AgNO3溶液
6.不能跟稀盐酸反应产生氢气的是( )
A.锌 B.银 C.铝 D.镁
7.将等质量的镁、铝、铁、锌分别与足量的稀盐酸反应,产生氢气最多的是( )
A.镁 B.铝 C.锌 D.一 样 多
8.小明同学按如下步骤对金属X,Y,Z进行探究:(1)取样,分别加入到CuSO4溶液中,发现X,Z表面出现红色物质,而Y没有;(2)取大小相同的X,Z颗粒,分别接入到溶质质量分数相等的稀硫酸中,发现X表面产生气泡的速率比Z快.则X,Y,Z的金属活动性由强到弱依次为( )
A.X>Z>Y B.Z>Y>X C.X>Y>Z D.Z>X>Y
9.下列实验现象描述正确的是( )
A.硫在空气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热
B.加热通入足量二氧化碳后的石蕊溶液:溶液由红色变为紫色
C.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热
D.把铁钉放在硫酸铜溶液中:银白色固体表面有铜析出,溶液由蓝色变为浅绿色
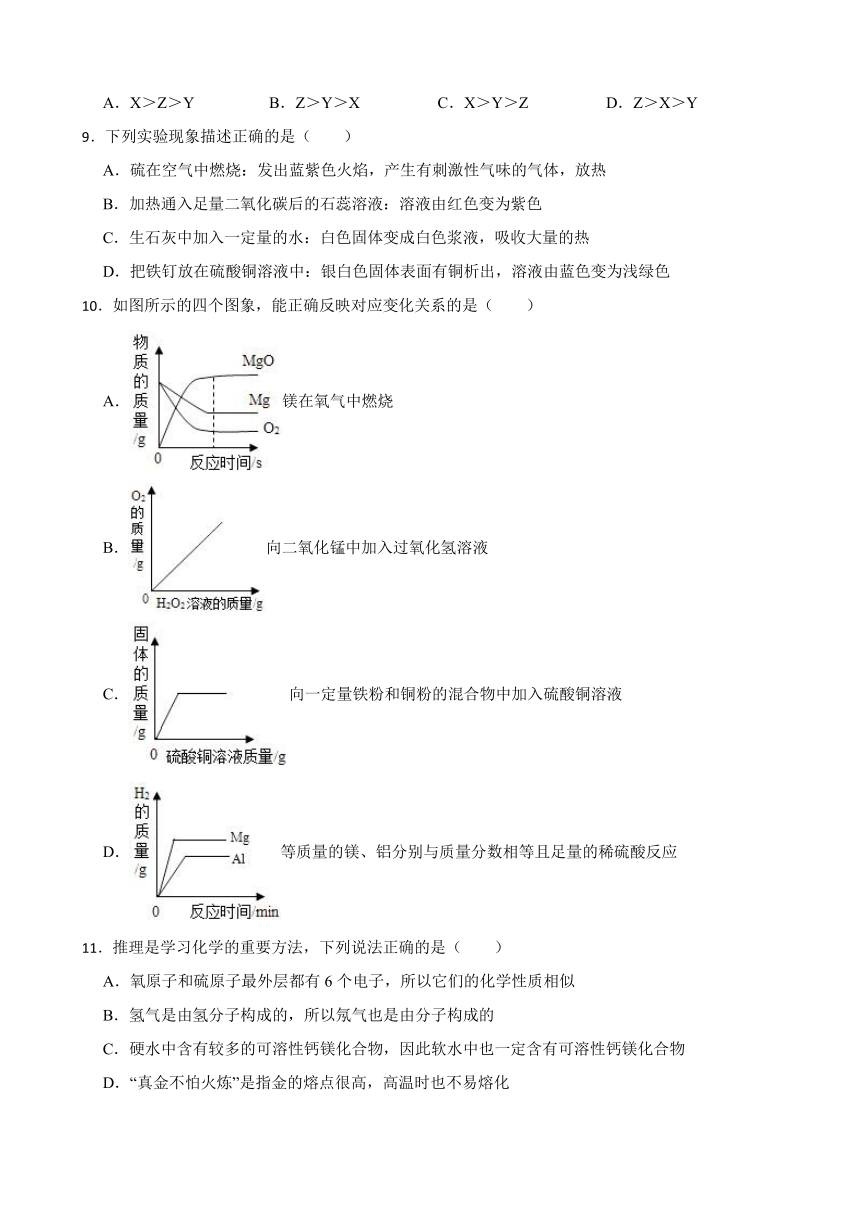
10.如图所示的四个图象,能正确反映对应变化关系的是( )
A.镁在氧气中燃烧
B.向二氧化锰中加入过氧化氢溶液
C.向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
11.推理是学习化学的重要方法,下列说法正确的是( )
A.氧原子和硫原子最外层都有6个电子,所以它们的化学性质相似
B.氢气是由氢分子构成的,所以氖气也是由分子构成的
C.硬水中含有较多的可溶性钙镁化合物,因此软水中也一定含有可溶性钙镁化合物
D.“真金不怕火炼”是指金的熔点很高,高温时也不易熔化
12.科学家发明了一种“碳纳米管温度计”,这种温度计被认定为世界上最小的温度计,研究人员在长约10-6m,直径为10-7m的碳纳米管中充入液态的金属镓。当温度升高时,管中的镓就会膨胀,通过电子显微镜就能读取温度值,这种温度计测量的温度范围为18 ℃~490 ℃,精确度较高,所以它可以用于检查电子线路是否异常,测定毛细血管的温度等许多方面。根据以上信息,判断下列推测错误的是( )
A.碳纳米管的体积在18 ℃~490 ℃之间随温度变化很小,可忽略不计
B.金属镓的熔点很低,沸点很高
C.金属镓体积在18 ℃~490 ℃之间随温度变化比较均匀
D.金属镓的体积在18 ℃~490 ℃之间随温度变化很小,可忽略不计
二、填空题
13.将一定量的铁加入到硝酸铝、硝酸银和硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。滤液中一定含有的物质化学式是 ,反应后溶液的质量比原混合溶液的质量 (填“大”或“小”)。
14.将一定量的镁粉和铁粉同时放入硝酸铜溶液中,充分反应后,过滤得滤渣和无色滤液。
(1)请写出一个该实验过程中发生反应的化学方程式 。
(2)滤渣中一定含有哪种物质?
15.在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,使之充分反应后铁有剩余,过滤,则滤液中有 ,固体残渣中一定含有 .
16.用下列物质的字母序号填空:
A.活性炭 B.二氧化硫 C.高分子材料 D.食醋 E.金属铝 F.氯化钾
(1)可形成酸雨的是 ;
(2)可用于生产食品包装袋的是 ;
(3)可用作钾肥的是 ;
(4)可用于填充防毒面具的是 ;
(5)可用于生产炊具的是 ;
(6)可用于除去水垢的是 .
17.在Cu(NO3)2、Al(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生.则反应后所得溶液中含有的金属离子有 ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);有关反应的化学方程式为 (写出一个即可).
18.将一定量的Zn加入含有Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中,充分反应后过滤,可以得到固体和溶液。其中会导致溶液质量减小的化学反应方程式为 ;若反应后溶液呈蓝色,此时溶液中一定含有的金属离子有 ,可能含有的金属离子有 。
三、综合题
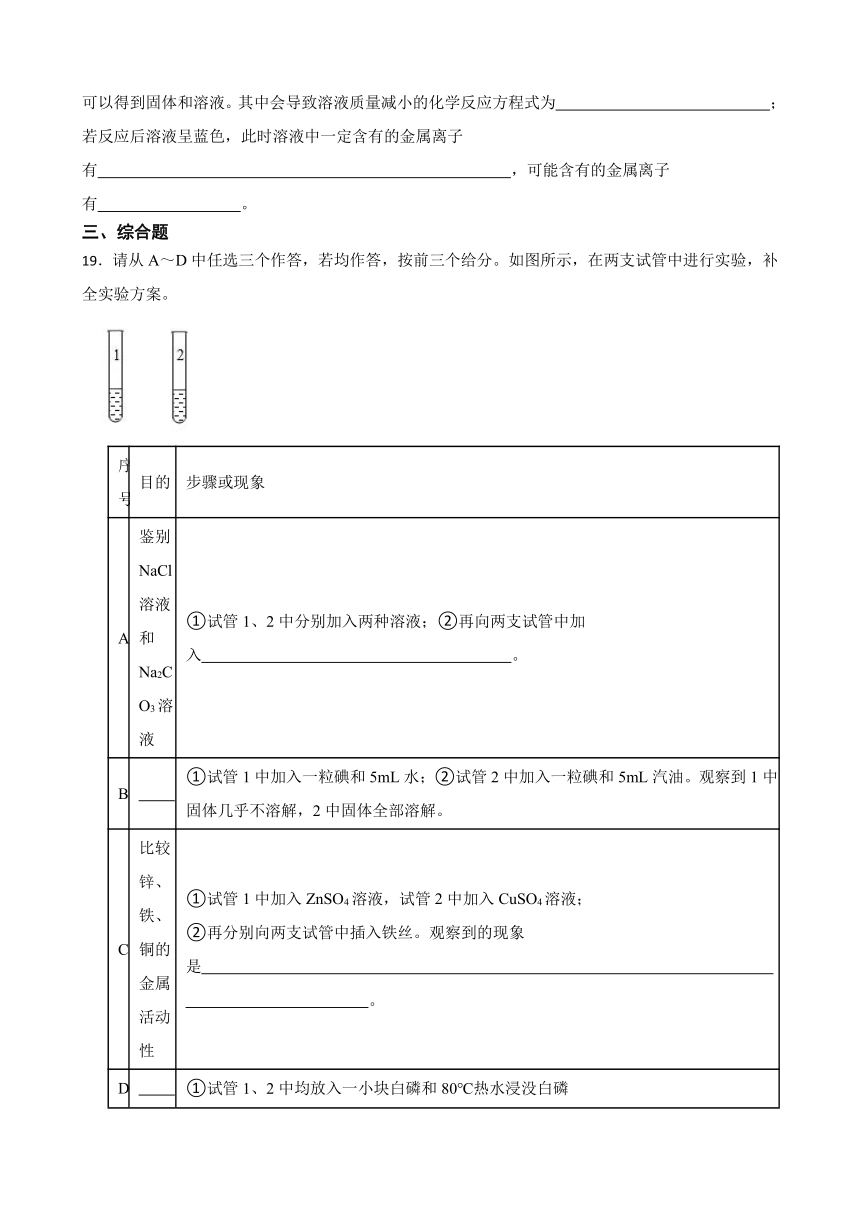
19.请从A~D中任选三个作答,若均作答,按前三个给分。如图所示,在两支试管中进行实验,补全实验方案。
序号 目的 步骤或现象
A 鉴别NaCl溶液和Na2CO3溶液 ①试管1、2中分别加入两种溶液;②再向两支试管中加入 。
B ①试管1中加入一粒碘和5mL水;②试管2中加入一粒碘和5mL汽油。观察到1中固体几乎不溶解,2中固体全部溶解。
C 比较锌、铁、铜的金属活动性 ①试管1中加入ZnSO4溶液,试管2中加入CuSO4溶液; ②再分别向两支试管中插入铁丝。观察到的现象是 。
D ①试管1、2中均放入一小块白磷和80℃热水浸没白磷 ②用导管对准试管2中白磷通入氧气。
20.人类拥有丰富的水资源。
(1)水的组成。如图为电解水的实验,请回答:
①若a管中气体体积为4mL,则b管中气体体积约为 mL。
②电解水的实验,说明水由 组成。
(2)水的净化。实验室常用 的方法除去水中不溶性杂质。
(3)水的利用。双氧水(H2O2的水溶液)是常用的消毒剂。双氧水属于 (填“混合物”或“纯净物”)。H2O2不稳定,易分解。H2O2分解的化学符号表达式为 。用3%的H2O2溶液对不同金属进行腐蚀性实验,结果如下:
金属种类 不锈钢片 铝片 铜片
腐蚀速度(mg/h) 0.001 0.010 0.404
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是 (填序号)。
A.不锈钢锅 B.铝盆 C.铜火锅
21.从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:
(1)图中“操作①”的名称是 。该操作中用到的玻璃仪器有 。
(2)滤液A中除水之外的主要成分的物质名称是 。
(3)写出所得贵重金属中任意一种成分的化学式 。
(4)任写一个①中发生的化学方程式 。
22.2017年5月5日,我国首架大型客机C919首飞成功,实现了我国航空领域的新突破。
(1)制造飞机大量使用铝锂合金、钛合金等合金,原因是 。
(2)在空气中,铝比铁具有更好的抗腐蚀性,原因是 (用化学方程式表示)。
(3)飞机起飞升空时,机翼下方气流的流速比机翼上方的小,则机翼下方的气流对机翼的压强 (选填“大于”、“等于”或“小于”)机翼上方的气流对机翼的压强。
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】C
4.【答案】C
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】A
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】Fe(NO3)2、Al(NO3)3;小
14.【答案】(1)
(2)铁和铜
15.【答案】ZnSO4、FeSO4、H2O;Fe和Cu
16.【答案】B;C;F;A;E;D
17.【答案】Al3+ 和Fe2+;小;Fe+Cu(NO3)2=Fe(NO3)2+Cu(或Fe+2AgNO3=Fe(NO3)2+2Ag)
18.【答案】;Al3+ 、Zn2+ 、Cu2+ (或铝离子、锌离子、铜离子);Ag+(银离子)
19.【答案】氯化钙溶液或澄清石灰水(合理给分);比较碘在水和汽油中的溶解性;试管1中无明显现象;试管2中溶液由蓝色变为浅绿色(或者溶液颜色变浅),铁丝表面有红色固体析出;证明可燃物燃烧需要与氧气接触
20.【答案】(1)2;氢元素、氧元素
(2)蒸馏
(3)混合物;;C
21.【答案】(1)过滤;烧杯、漏斗、玻璃棒
(2)硫酸亚铁和硫酸铝
(3)Au或Pt
(4)Fe+H2SO4=FeSO4+H2↑或2Al+3H2SO4=Al2(SO4)3+3H2↑
22.【答案】(1)合金具有更高的强度、硬度和更好的抗腐蚀性
(2)4Al + 3O 2 =2Al2O3
(3)大于
一、单选题
1.下列说法中,正确的是( )
A.地壳中含量最多的金属元素是铁
B.赤铁矿、磁铁矿是重要的金属资源
C.铝比铁活泼,所以铁比铝耐腐蚀
D.纯铜的熔点小于铜锌合金
2.向一定量CuSO4溶液中加入过量铁粉,充分反应后过滤得到滤渣和滤液,下列判断正确的是( )
A.得到的滤液呈蓝色
B.所得滤渣的质量比加入铁粉的大
C.向滤渣中滴加稀盐酸无气泡产生
D.滤液中一定有FeSO4,可能有CuSO4
3.下列关于家庭小实验的说法正确的是( )
A.淬火的钢针弯曲制成鱼钩
B.用食盐除去热水瓶内胆壁上的水垢
C.用10%的烧碱溶液自制“叶脉书签”
D.制作简易净水器时,为了达到好的净水效果,活性炭应该放在最上层
4.往AgNO3和Cu(NO3)2的混合溶液中加入一定量的锌粒,充分反应后过滤,往滤渣中加入稀盐酸,无气泡产生。你能得出的结论是( )
A.滤渣中一定有Zn B.滤渣中一定有Ag和Cu
C.滤渣中可能有Cu D.滤液中一定有Ag+和Cu2+
5.在下列溶液中分别放入锌粒,一段时间后把锌粒取出,溶液质量减少的是()
A.MgCl2溶液 B.盐酸 C.稀硫酸 D.AgNO3溶液
6.不能跟稀盐酸反应产生氢气的是( )
A.锌 B.银 C.铝 D.镁
7.将等质量的镁、铝、铁、锌分别与足量的稀盐酸反应,产生氢气最多的是( )
A.镁 B.铝 C.锌 D.一 样 多
8.小明同学按如下步骤对金属X,Y,Z进行探究:(1)取样,分别加入到CuSO4溶液中,发现X,Z表面出现红色物质,而Y没有;(2)取大小相同的X,Z颗粒,分别接入到溶质质量分数相等的稀硫酸中,发现X表面产生气泡的速率比Z快.则X,Y,Z的金属活动性由强到弱依次为( )
A.X>Z>Y B.Z>Y>X C.X>Y>Z D.Z>X>Y
9.下列实验现象描述正确的是( )
A.硫在空气中燃烧:发出蓝紫色火焰,产生有刺激性气味的气体,放热
B.加热通入足量二氧化碳后的石蕊溶液:溶液由红色变为紫色
C.生石灰中加入一定量的水:白色固体变成白色浆液,吸收大量的热
D.把铁钉放在硫酸铜溶液中:银白色固体表面有铜析出,溶液由蓝色变为浅绿色
10.如图所示的四个图象,能正确反映对应变化关系的是( )
A.镁在氧气中燃烧
B.向二氧化锰中加入过氧化氢溶液
C.向一定量铁粉和铜粉的混合物中加入硫酸铜溶液
D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
11.推理是学习化学的重要方法,下列说法正确的是( )
A.氧原子和硫原子最外层都有6个电子,所以它们的化学性质相似
B.氢气是由氢分子构成的,所以氖气也是由分子构成的
C.硬水中含有较多的可溶性钙镁化合物,因此软水中也一定含有可溶性钙镁化合物
D.“真金不怕火炼”是指金的熔点很高,高温时也不易熔化
12.科学家发明了一种“碳纳米管温度计”,这种温度计被认定为世界上最小的温度计,研究人员在长约10-6m,直径为10-7m的碳纳米管中充入液态的金属镓。当温度升高时,管中的镓就会膨胀,通过电子显微镜就能读取温度值,这种温度计测量的温度范围为18 ℃~490 ℃,精确度较高,所以它可以用于检查电子线路是否异常,测定毛细血管的温度等许多方面。根据以上信息,判断下列推测错误的是( )
A.碳纳米管的体积在18 ℃~490 ℃之间随温度变化很小,可忽略不计
B.金属镓的熔点很低,沸点很高
C.金属镓体积在18 ℃~490 ℃之间随温度变化比较均匀
D.金属镓的体积在18 ℃~490 ℃之间随温度变化很小,可忽略不计
二、填空题
13.将一定量的铁加入到硝酸铝、硝酸银和硝酸铜的混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。滤液中一定含有的物质化学式是 ,反应后溶液的质量比原混合溶液的质量 (填“大”或“小”)。
14.将一定量的镁粉和铁粉同时放入硝酸铜溶液中,充分反应后,过滤得滤渣和无色滤液。
(1)请写出一个该实验过程中发生反应的化学方程式 。
(2)滤渣中一定含有哪种物质?
15.在硫酸铜、硫酸锌和稀硫酸的混合溶液中,加入一定量的铁粉,使之充分反应后铁有剩余,过滤,则滤液中有 ,固体残渣中一定含有 .
16.用下列物质的字母序号填空:
A.活性炭 B.二氧化硫 C.高分子材料 D.食醋 E.金属铝 F.氯化钾
(1)可形成酸雨的是 ;
(2)可用于生产食品包装袋的是 ;
(3)可用作钾肥的是 ;
(4)可用于填充防毒面具的是 ;
(5)可用于生产炊具的是 ;
(6)可用于除去水垢的是 .
17.在Cu(NO3)2、Al(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生.则反应后所得溶液中含有的金属离子有 ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);有关反应的化学方程式为 (写出一个即可).
18.将一定量的Zn加入含有Cu(NO3)2、AgNO3和Al(NO3)3的混合溶液中,充分反应后过滤,可以得到固体和溶液。其中会导致溶液质量减小的化学反应方程式为 ;若反应后溶液呈蓝色,此时溶液中一定含有的金属离子有 ,可能含有的金属离子有 。
三、综合题
19.请从A~D中任选三个作答,若均作答,按前三个给分。如图所示,在两支试管中进行实验,补全实验方案。
序号 目的 步骤或现象
A 鉴别NaCl溶液和Na2CO3溶液 ①试管1、2中分别加入两种溶液;②再向两支试管中加入 。
B ①试管1中加入一粒碘和5mL水;②试管2中加入一粒碘和5mL汽油。观察到1中固体几乎不溶解,2中固体全部溶解。
C 比较锌、铁、铜的金属活动性 ①试管1中加入ZnSO4溶液,试管2中加入CuSO4溶液; ②再分别向两支试管中插入铁丝。观察到的现象是 。
D ①试管1、2中均放入一小块白磷和80℃热水浸没白磷 ②用导管对准试管2中白磷通入氧气。
20.人类拥有丰富的水资源。
(1)水的组成。如图为电解水的实验,请回答:
①若a管中气体体积为4mL,则b管中气体体积约为 mL。
②电解水的实验,说明水由 组成。
(2)水的净化。实验室常用 的方法除去水中不溶性杂质。
(3)水的利用。双氧水(H2O2的水溶液)是常用的消毒剂。双氧水属于 (填“混合物”或“纯净物”)。H2O2不稳定,易分解。H2O2分解的化学符号表达式为 。用3%的H2O2溶液对不同金属进行腐蚀性实验,结果如下:
金属种类 不锈钢片 铝片 铜片
腐蚀速度(mg/h) 0.001 0.010 0.404
下列金属制品用该溶液浸泡消毒时,最易被腐蚀的是 (填序号)。
A.不锈钢锅 B.铝盆 C.铜火锅
21.从某废旧电子产品中可以提炼贵重金属,并得到硫酸铜溶液。其工艺流程如图所示:
(1)图中“操作①”的名称是 。该操作中用到的玻璃仪器有 。
(2)滤液A中除水之外的主要成分的物质名称是 。
(3)写出所得贵重金属中任意一种成分的化学式 。
(4)任写一个①中发生的化学方程式 。
22.2017年5月5日,我国首架大型客机C919首飞成功,实现了我国航空领域的新突破。
(1)制造飞机大量使用铝锂合金、钛合金等合金,原因是 。
(2)在空气中,铝比铁具有更好的抗腐蚀性,原因是 (用化学方程式表示)。
(3)飞机起飞升空时,机翼下方气流的流速比机翼上方的小,则机翼下方的气流对机翼的压强 (选填“大于”、“等于”或“小于”)机翼上方的气流对机翼的压强。
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】C
4.【答案】C
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】A
9.【答案】B
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】Fe(NO3)2、Al(NO3)3;小
14.【答案】(1)
(2)铁和铜
15.【答案】ZnSO4、FeSO4、H2O;Fe和Cu
16.【答案】B;C;F;A;E;D
17.【答案】Al3+ 和Fe2+;小;Fe+Cu(NO3)2=Fe(NO3)2+Cu(或Fe+2AgNO3=Fe(NO3)2+2Ag)
18.【答案】;Al3+ 、Zn2+ 、Cu2+ (或铝离子、锌离子、铜离子);Ag+(银离子)
19.【答案】氯化钙溶液或澄清石灰水(合理给分);比较碘在水和汽油中的溶解性;试管1中无明显现象;试管2中溶液由蓝色变为浅绿色(或者溶液颜色变浅),铁丝表面有红色固体析出;证明可燃物燃烧需要与氧气接触
20.【答案】(1)2;氢元素、氧元素
(2)蒸馏
(3)混合物;;C
21.【答案】(1)过滤;烧杯、漏斗、玻璃棒
(2)硫酸亚铁和硫酸铝
(3)Au或Pt
(4)Fe+H2SO4=FeSO4+H2↑或2Al+3H2SO4=Al2(SO4)3+3H2↑
22.【答案】(1)合金具有更高的强度、硬度和更好的抗腐蚀性
(2)4Al + 3O 2 =2Al2O3
(3)大于
同课章节目录
