10.2 酸和碱的中和反应 同步练习 (含答案)2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 10.2 酸和碱的中和反应 同步练习 (含答案)2022-2023学年人教版九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 111.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-05 00:00:00 | ||
图片预览



文档简介
10.2 酸和碱的中和反应 同步练习
一、单选题
1.下列说法不正确的是( )
A.等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14
B.将溶质质量分数为98%的浓硫酸稀释为49%的硫酸,加水的体积与所取浓硫酸的体积一定相等
C.等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D.等质量的质量分数均为4%氢氧化钠溶液与稀硫酸充分反应后,所得溶液显碱性
2.某同学用pH试纸测定日常生活中的一些液体的pH.他的实验记录一定错误的是( )
A.肥皂水pH=10 B.纯碱溶液pH=11
C.橘子汁pH=4 D.食醋pH=7
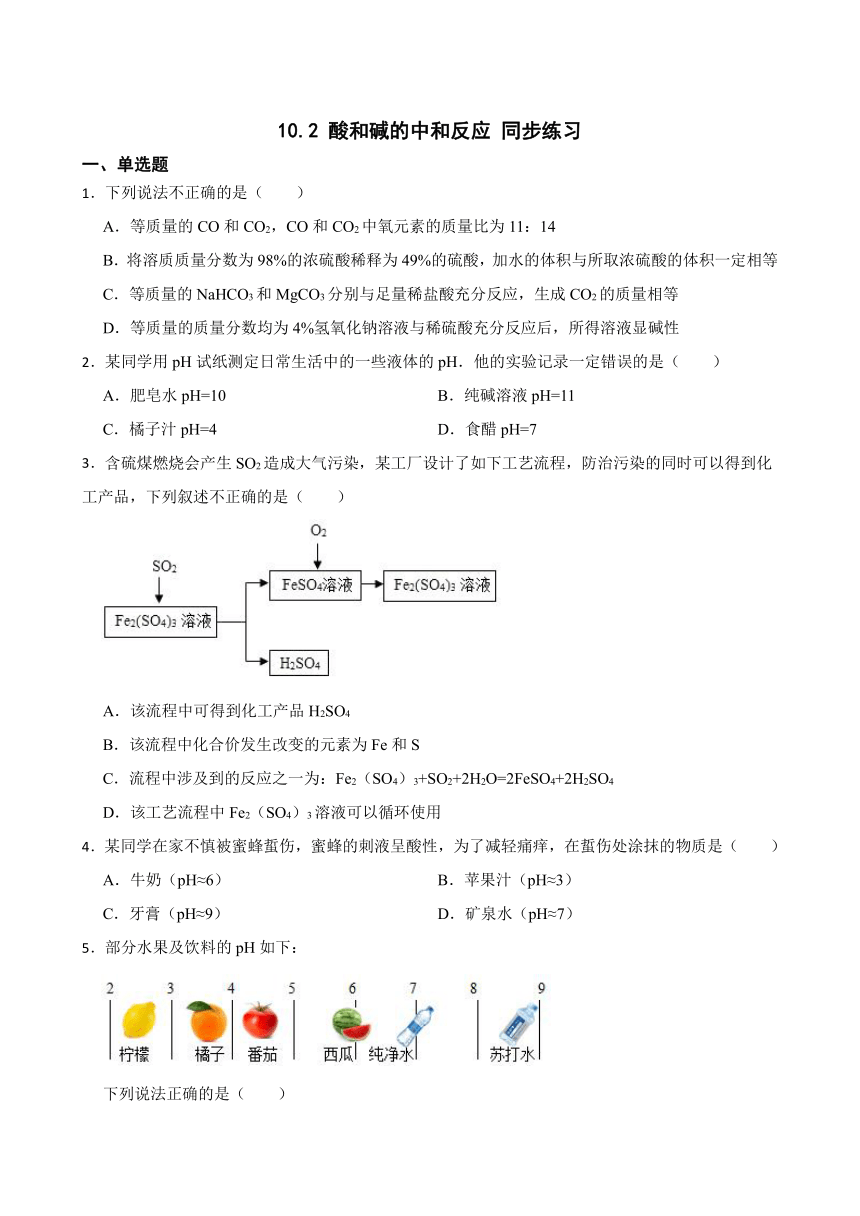
3.含硫煤燃烧会产生SO2造成大气污染,某工厂设计了如下工艺流程,防治污染的同时可以得到化工产品,下列叙述不正确的是( )
A.该流程中可得到化工产品H2SO4
B.该流程中化合价发生改变的元素为Fe和S
C.流程中涉及到的反应之一为:Fe2(SO4)3+SO2+2H2O=2FeSO4+2H2SO4
D.该工艺流程中Fe2(SO4)3溶液可以循环使用
4.某同学在家不慎被蜜蜂蜇伤,蜜蜂的刺液呈酸性,为了减轻痛痒,在蜇伤处涂抹的物质是( )
A.牛奶(pH≈6) B.苹果汁(pH≈3)
C.牙膏(pH≈9) D.矿泉水(pH≈7)
5.部分水果及饮料的pH如下:
下列说法正确的是( )
A.西瓜汁显碱性 B.橘子汁中滴入酚酞,溶液变红
C.苏打水显酸性 D.胃酸过多的人应该少饮柠檬水
6.柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈现酸性,主要用于制造香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )
A.Mg B.Fe2O3 C.CO2 D.Fe
7.用pH试纸测溶液的pH,是今年我市化学实验操作考查的题目之一,下列有关pH试纸的使用说法正确的是( )
A.把pH试纸浸入待测液
B.用湿润的玻璃棒蘸取待测液
C.把显色的pH试纸与标准比色卡对照读数
D.测出石灰水的pH为12.4
8.已知生活用品中厕所清洁剂的pH=1,厨房清洁剂的pH=12,下列说法错误的是( )
A.厕所清洁剂加水稀释,溶液pH升高
B.厨房清洁剂可能含有氢氧化钠
C.两者混合使用能提高清洁效果
D.厕所清洁剂可能使铁制下水道腐蚀
9.实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
A.A点时的溶液不能使酚酞溶液变色
B.该实验是将氢氧化钠溶液滴入盐酸中
C.B点表示盐酸和氢氧化钠溶液恰好完全反应
D.C点时,溶液中溶质只有氯化氢
10.下列排序正确的是( )
A.空气中物质含量:
B.溶液pH:
C.金属活动性顺序:
D.硫元素质量分数:
11.下列说法正确的是( )
A.质子数相同的微粒一定是同种元素
B.酸性溶液一定是酸的溶液
C.某温度下的浓溶液一定是饱和溶液
D.生铁比纯铁硬
12.下列是部分饮品的近似pH范围,其中酸性最强的是( )
A.苹果汁(2.9~3.3) B.番茄汁(4.0~4.4)
C.牛奶(6.3~6.6) D.豆浆(7.4~7.9)
二、填空题
13. 和 排放到空气中形成了酸雨.防止空气污染的措施:(写出两条) ; .
14.正常雨水显酸性,pH≈5.6,原因是 (填化学方程式),
将雨水放在太阳下暴晒,pH会变 (填大”或“小”)
15.下图表示的是一些物质在常温下的近似pH,回答下列问题:
(1)厨房清洁剂显 性,在少量厨房清洁剂中滴入几滴酚酞,溶液呈 色;
(2)酸雨的酸性比正常雨水的酸性 (填“强”或“弱”);
(3)测量苹果汁pH时,pH试纸是否需要先用蒸馏水润湿 (填“是”或“否”)。
16.A,B,C,D,E是初中化学常见的物质,其中C为最常见的液体,物质间的转化关系如图所示。
若反应①为置换反应,且D为紫红色固体单质,则A为 ,反应③的化学方程式为 ;
若A能使紫色石蕊溶液变红,D为蓝色溶液,且反应①②为中和反应,反应③有沉淀生成,则反应③的化学方程式为 。
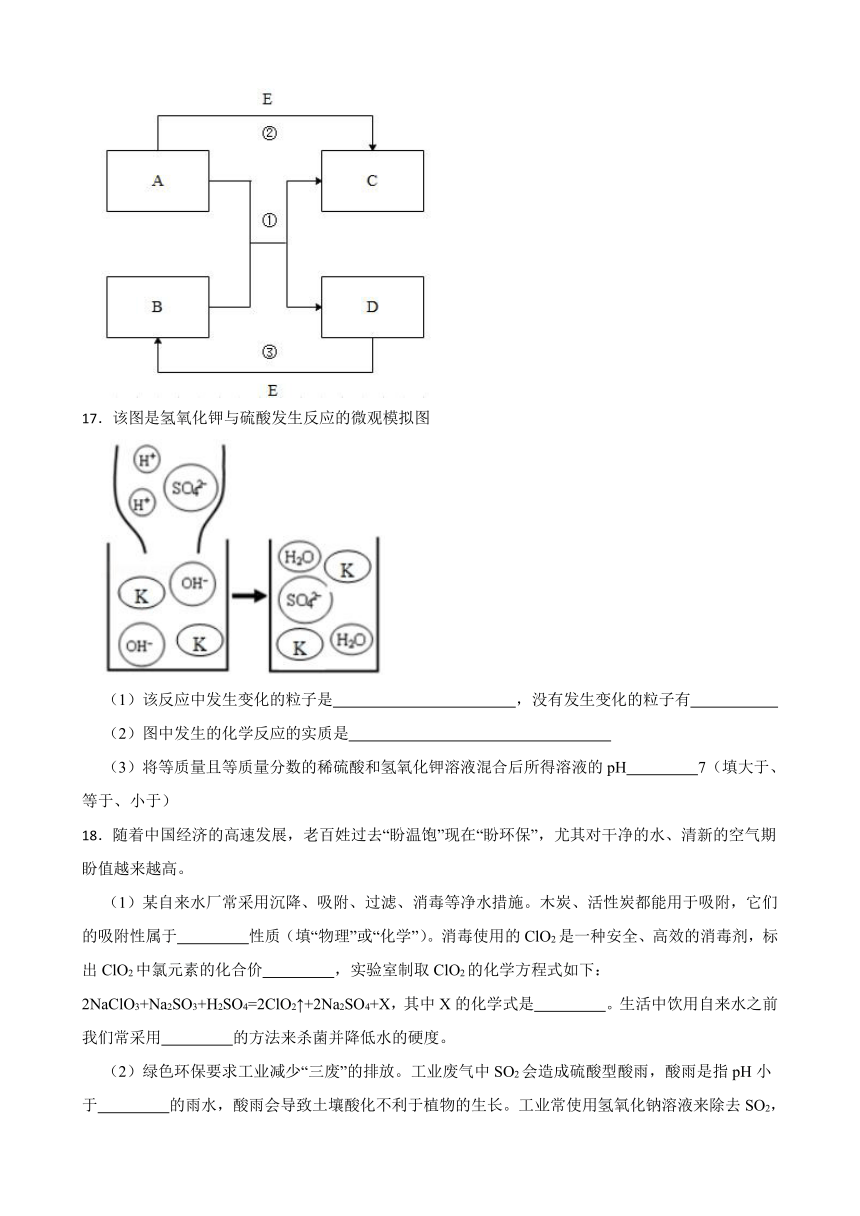
17.该图是氢氧化钾与硫酸发生反应的微观模拟图
(1)该反应中发生变化的粒子是 ,没有发生变化的粒子有
(2)图中发生的化学反应的实质是
(3)将等质量且等质量分数的稀硫酸和氢氧化钾溶液混合后所得溶液的pH 7(填大于、等于、小于)
18.随着中国经济的高速发展,老百姓过去“盼温饱”现在“盼环保”,尤其对干净的水、清新的空气期盼值越来越高。
(1)某自来水厂常采用沉降、吸附、过滤、消毒等净水措施。木炭、活性炭都能用于吸附,它们的吸附性属于 性质(填“物理”或“化学”)。消毒使用的ClO2是一种安全、高效的消毒剂,标出ClO2中氯元素的化合价 ,实验室制取ClO2的化学方程式如下:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+X,其中X的化学式是 。生活中饮用自来水之前我们常采用 的方法来杀菌并降低水的硬度。
(2)绿色环保要求工业减少“三废”的排放。工业废气中SO2会造成硫酸型酸雨,酸雨是指pH小于 的雨水,酸雨会导致土壤酸化不利于植物的生长。工业常使用氢氧化钠溶液来除去SO2,写出发生反应的化学方程式 ,农业常使用 改良酸性土壤。
三、综合题
19.从近来经常发生的雾霾天气来看,治理污染刻不容级。
(1)煤燃烧时排放出会形成酸雨的气体是 (写一种物质的名称即可);
(2)PM2.5是指大气中微粒直径小于2.5微米的颗粒物。下列物质中,不会形成PM2.5的是 (选填字母序号);
A.焚烧秸秆 B.汽车尾气排放 C.太阳能发电
(3)下列做法中,不符合“低碳”要求的是 (选填字母序号)。
A.节约纸张 B.大量使用化石燃料
C.提倡使用节约技术和节能产品 D.尽量乘坐公交车
20.室温下,将氢氧化钠溶液慢慢滴入装有稀盐酸的烧杯中,用温度计测量出烧杯中溶液的温度,溶液温度随加入氢氧化钠溶液的质量而变化的曲线如图:
(1)由图可知,两溶液发生的反应是 (填“放热”或“吸热”)反应;
(2)从A到B过程中,烧杯中溶液的pH逐渐 ;
(3) 点时恰好完全反应,C点的溶液中含有的溶质为 。
21.构建思维导图是一种重要的学习方法。请根据酸和碱的化学性质思维导图,回答下列问题。(“一”表示相连的两类物质之间可以发生化学反应)
(1)请写出图中甲表示的物质类别 。
(2)酸与碱作用生成盐和水的反应,叫做中和反应。请写出一个中和反应的化学方程式 。
(3)酸和碱能与指示剂反应,而使指示剂显示不同的颜色。如NaOH溶液能使无色酚酞变成 色。
22.利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数.
下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
(1)根据下图曲线可以判断实验中是向 (填“酸”或“碱”,下同)溶液(待测液)中滴加 溶液(标准液).
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到 ,则证明中和反应正好完成.
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数.
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】B
4.【答案】C
5.【答案】D
6.【答案】C
7.【答案】C
8.【答案】C
9.【答案】C
10.【答案】D
11.【答案】D
12.【答案】A
13.【答案】SO2 ;NO2;使用脱硫煤;使用清洁能源
14.【答案】CO2+H2O═H2CO3;大
15.【答案】(1)碱;红
(2)强
(3)否
16.【答案】氢气(或H2);;
17.【答案】(1)氢离子和氢氧根离子;钾离子和硫酸根离子
(2)氢离子和氢根离子结合生成了水
(3)小于
18.【答案】(1)物理;;H2O;煮沸
(2)5.6;SO2+2NaOH =Na2SO3+H2O;熟石灰(消石灰或Ca(OH)2)
19.【答案】(1)二氧化硫(或二氧化氮)
(2)C
(3)B
20.【答案】(1)放热
(2)增大
(3)B;氯化钠和氢氧化钠
21.【答案】(1)金属氧化物
(2)
(3)红
22.【答案】(1)碱;酸
(2)碱溶液的红色刚好褪去
(3)解:消耗掉的H2SO4质量:24.5mL×1.0g/mL=24.5g
消耗掉的H2SO4溶液中溶质的质量:24.5g×4.5%=1.10g
故答案为:
解:设待测液溶质的质量分数为x
2NaOH+ H2SO4 =Na2SO4+2H2O
80 98
25mL×1.0g/mL x 1.10g
x=3.6%
答:待测液溶质的质量分数为3.6%.
一、单选题
1.下列说法不正确的是( )
A.等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14
B.将溶质质量分数为98%的浓硫酸稀释为49%的硫酸,加水的体积与所取浓硫酸的体积一定相等
C.等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量相等
D.等质量的质量分数均为4%氢氧化钠溶液与稀硫酸充分反应后,所得溶液显碱性
2.某同学用pH试纸测定日常生活中的一些液体的pH.他的实验记录一定错误的是( )
A.肥皂水pH=10 B.纯碱溶液pH=11
C.橘子汁pH=4 D.食醋pH=7
3.含硫煤燃烧会产生SO2造成大气污染,某工厂设计了如下工艺流程,防治污染的同时可以得到化工产品,下列叙述不正确的是( )
A.该流程中可得到化工产品H2SO4
B.该流程中化合价发生改变的元素为Fe和S
C.流程中涉及到的反应之一为:Fe2(SO4)3+SO2+2H2O=2FeSO4+2H2SO4
D.该工艺流程中Fe2(SO4)3溶液可以循环使用
4.某同学在家不慎被蜜蜂蜇伤,蜜蜂的刺液呈酸性,为了减轻痛痒,在蜇伤处涂抹的物质是( )
A.牛奶(pH≈6) B.苹果汁(pH≈3)
C.牙膏(pH≈9) D.矿泉水(pH≈7)
5.部分水果及饮料的pH如下:
下列说法正确的是( )
A.西瓜汁显碱性 B.橘子汁中滴入酚酞,溶液变红
C.苏打水显酸性 D.胃酸过多的人应该少饮柠檬水
6.柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈现酸性,主要用于制造香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )
A.Mg B.Fe2O3 C.CO2 D.Fe
7.用pH试纸测溶液的pH,是今年我市化学实验操作考查的题目之一,下列有关pH试纸的使用说法正确的是( )
A.把pH试纸浸入待测液
B.用湿润的玻璃棒蘸取待测液
C.把显色的pH试纸与标准比色卡对照读数
D.测出石灰水的pH为12.4
8.已知生活用品中厕所清洁剂的pH=1,厨房清洁剂的pH=12,下列说法错误的是( )
A.厕所清洁剂加水稀释,溶液pH升高
B.厨房清洁剂可能含有氢氧化钠
C.两者混合使用能提高清洁效果
D.厕所清洁剂可能使铁制下水道腐蚀
9.实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
A.A点时的溶液不能使酚酞溶液变色
B.该实验是将氢氧化钠溶液滴入盐酸中
C.B点表示盐酸和氢氧化钠溶液恰好完全反应
D.C点时,溶液中溶质只有氯化氢
10.下列排序正确的是( )
A.空气中物质含量:
B.溶液pH:
C.金属活动性顺序:
D.硫元素质量分数:
11.下列说法正确的是( )
A.质子数相同的微粒一定是同种元素
B.酸性溶液一定是酸的溶液
C.某温度下的浓溶液一定是饱和溶液
D.生铁比纯铁硬
12.下列是部分饮品的近似pH范围,其中酸性最强的是( )
A.苹果汁(2.9~3.3) B.番茄汁(4.0~4.4)
C.牛奶(6.3~6.6) D.豆浆(7.4~7.9)
二、填空题
13. 和 排放到空气中形成了酸雨.防止空气污染的措施:(写出两条) ; .
14.正常雨水显酸性,pH≈5.6,原因是 (填化学方程式),
将雨水放在太阳下暴晒,pH会变 (填大”或“小”)
15.下图表示的是一些物质在常温下的近似pH,回答下列问题:
(1)厨房清洁剂显 性,在少量厨房清洁剂中滴入几滴酚酞,溶液呈 色;
(2)酸雨的酸性比正常雨水的酸性 (填“强”或“弱”);
(3)测量苹果汁pH时,pH试纸是否需要先用蒸馏水润湿 (填“是”或“否”)。
16.A,B,C,D,E是初中化学常见的物质,其中C为最常见的液体,物质间的转化关系如图所示。
若反应①为置换反应,且D为紫红色固体单质,则A为 ,反应③的化学方程式为 ;
若A能使紫色石蕊溶液变红,D为蓝色溶液,且反应①②为中和反应,反应③有沉淀生成,则反应③的化学方程式为 。
17.该图是氢氧化钾与硫酸发生反应的微观模拟图
(1)该反应中发生变化的粒子是 ,没有发生变化的粒子有
(2)图中发生的化学反应的实质是
(3)将等质量且等质量分数的稀硫酸和氢氧化钾溶液混合后所得溶液的pH 7(填大于、等于、小于)
18.随着中国经济的高速发展,老百姓过去“盼温饱”现在“盼环保”,尤其对干净的水、清新的空气期盼值越来越高。
(1)某自来水厂常采用沉降、吸附、过滤、消毒等净水措施。木炭、活性炭都能用于吸附,它们的吸附性属于 性质(填“物理”或“化学”)。消毒使用的ClO2是一种安全、高效的消毒剂,标出ClO2中氯元素的化合价 ,实验室制取ClO2的化学方程式如下:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+X,其中X的化学式是 。生活中饮用自来水之前我们常采用 的方法来杀菌并降低水的硬度。
(2)绿色环保要求工业减少“三废”的排放。工业废气中SO2会造成硫酸型酸雨,酸雨是指pH小于 的雨水,酸雨会导致土壤酸化不利于植物的生长。工业常使用氢氧化钠溶液来除去SO2,写出发生反应的化学方程式 ,农业常使用 改良酸性土壤。
三、综合题
19.从近来经常发生的雾霾天气来看,治理污染刻不容级。
(1)煤燃烧时排放出会形成酸雨的气体是 (写一种物质的名称即可);
(2)PM2.5是指大气中微粒直径小于2.5微米的颗粒物。下列物质中,不会形成PM2.5的是 (选填字母序号);
A.焚烧秸秆 B.汽车尾气排放 C.太阳能发电
(3)下列做法中,不符合“低碳”要求的是 (选填字母序号)。
A.节约纸张 B.大量使用化石燃料
C.提倡使用节约技术和节能产品 D.尽量乘坐公交车
20.室温下,将氢氧化钠溶液慢慢滴入装有稀盐酸的烧杯中,用温度计测量出烧杯中溶液的温度,溶液温度随加入氢氧化钠溶液的质量而变化的曲线如图:
(1)由图可知,两溶液发生的反应是 (填“放热”或“吸热”)反应;
(2)从A到B过程中,烧杯中溶液的pH逐渐 ;
(3) 点时恰好完全反应,C点的溶液中含有的溶质为 。
21.构建思维导图是一种重要的学习方法。请根据酸和碱的化学性质思维导图,回答下列问题。(“一”表示相连的两类物质之间可以发生化学反应)
(1)请写出图中甲表示的物质类别 。
(2)酸与碱作用生成盐和水的反应,叫做中和反应。请写出一个中和反应的化学方程式 。
(3)酸和碱能与指示剂反应,而使指示剂显示不同的颜色。如NaOH溶液能使无色酚酞变成 色。
22.利用中和反应可以测定酸或碱溶液中溶质的质量分数.例如,在一定量的待测酸(或碱)溶液中逐滴加入已知质量分数的碱(或酸)溶液(标准溶液),直到酸、碱正好完全反应,根据消耗标准碱(或酸)溶液的多少即可求算出待测酸(或碱)溶液的质量分数.
下图为某次测定过程中,溶液的pH随所滴加的某标准溶液体积的变化而变化的关系图.
(1)根据下图曲线可以判断实验中是向 (填“酸”或“碱”,下同)溶液(待测液)中滴加 溶液(标准液).
(2)在这次测定中,为了指示中和反应刚好完全,用酚酞作指示剂,即在待测溶液中先滴入几滴酚酞试液,若看到 ,则证明中和反应正好完成.
(3)如果实验中使用的酸是硫酸,碱是氢氧化钠,且待测液和标准液的密度均以1.0g/mL计.若测定中取用待测液25mL,标准液溶质的质量分数为4.5%,根据图中数据,计算待测液溶质的质量分数.
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】B
4.【答案】C
5.【答案】D
6.【答案】C
7.【答案】C
8.【答案】C
9.【答案】C
10.【答案】D
11.【答案】D
12.【答案】A
13.【答案】SO2 ;NO2;使用脱硫煤;使用清洁能源
14.【答案】CO2+H2O═H2CO3;大
15.【答案】(1)碱;红
(2)强
(3)否
16.【答案】氢气(或H2);;
17.【答案】(1)氢离子和氢氧根离子;钾离子和硫酸根离子
(2)氢离子和氢根离子结合生成了水
(3)小于
18.【答案】(1)物理;;H2O;煮沸
(2)5.6;SO2+2NaOH =Na2SO3+H2O;熟石灰(消石灰或Ca(OH)2)
19.【答案】(1)二氧化硫(或二氧化氮)
(2)C
(3)B
20.【答案】(1)放热
(2)增大
(3)B;氯化钠和氢氧化钠
21.【答案】(1)金属氧化物
(2)
(3)红
22.【答案】(1)碱;酸
(2)碱溶液的红色刚好褪去
(3)解:消耗掉的H2SO4质量:24.5mL×1.0g/mL=24.5g
消耗掉的H2SO4溶液中溶质的质量:24.5g×4.5%=1.10g
故答案为:
解:设待测液溶质的质量分数为x
2NaOH+ H2SO4 =Na2SO4+2H2O
80 98
25mL×1.0g/mL x 1.10g
x=3.6%
答:待测液溶质的质量分数为3.6%.
同课章节目录
