6.1 金属材料的物理特性 同步练习 (含答案) 2022-2023学年科粤版九年级下册化学
文档属性
| 名称 | 6.1 金属材料的物理特性 同步练习 (含答案) 2022-2023学年科粤版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 447.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-06 00:00:00 | ||
图片预览




文档简介
6.1 金属材料的物理特性 同步练习
一、单选题
1.金属材料在生活、生产中应用广泛,下列说法正确的是( )
A.不锈钢碗筷比普通铁锅耐腐蚀
B.焊锡(锡铅合金)的熔点大于铅的熔点
C.银导电性最好,常用作电线
D.铁制品只要与水接触就会生锈
2.下列事实和相应的解释不一致的是( )
A.切洋葱时可闻到刺激性气味——分子在不停地运动
B.CO2通入紫色石蕊溶液中,溶液变红——CO2能使紫色石蕊变红
C.水分解生成氢气和氧气——水是由氢元素和氧元素组成的
D.金刚石坚硬而石墨很软——碳原子的排列方式不同
3.下列金属制品中,利用金属导电性的是( )
A.黄金首饰 B.铝蒸锅
C.铜导线 D.金属乐器
4.下列关于金属的说法正确的是( )
A.铝元素在地壳中含量最多,使用也最早
B.不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C.灯泡里的灯丝常用钨制成
D.地球上金属矿物资源储量有限,可再生
5.化学与生产生活密切相关。下列说法错误的是( )
A.pH<5.6的降雨称为酸雨 B.石油属于可再生能源
C.PM2.5属于大气污染物 D.铝合金的硬度比纯铝大
6.2021年7月,三星堆3号坑再次出土一件青铜神树。下列关于青铜的说法正确的是( )
A.青铜属于合成材料 B.青铜的熔点比纯铜高
C.青铜的化学性质比较稳定 D.青铜的硬度比纯铜小
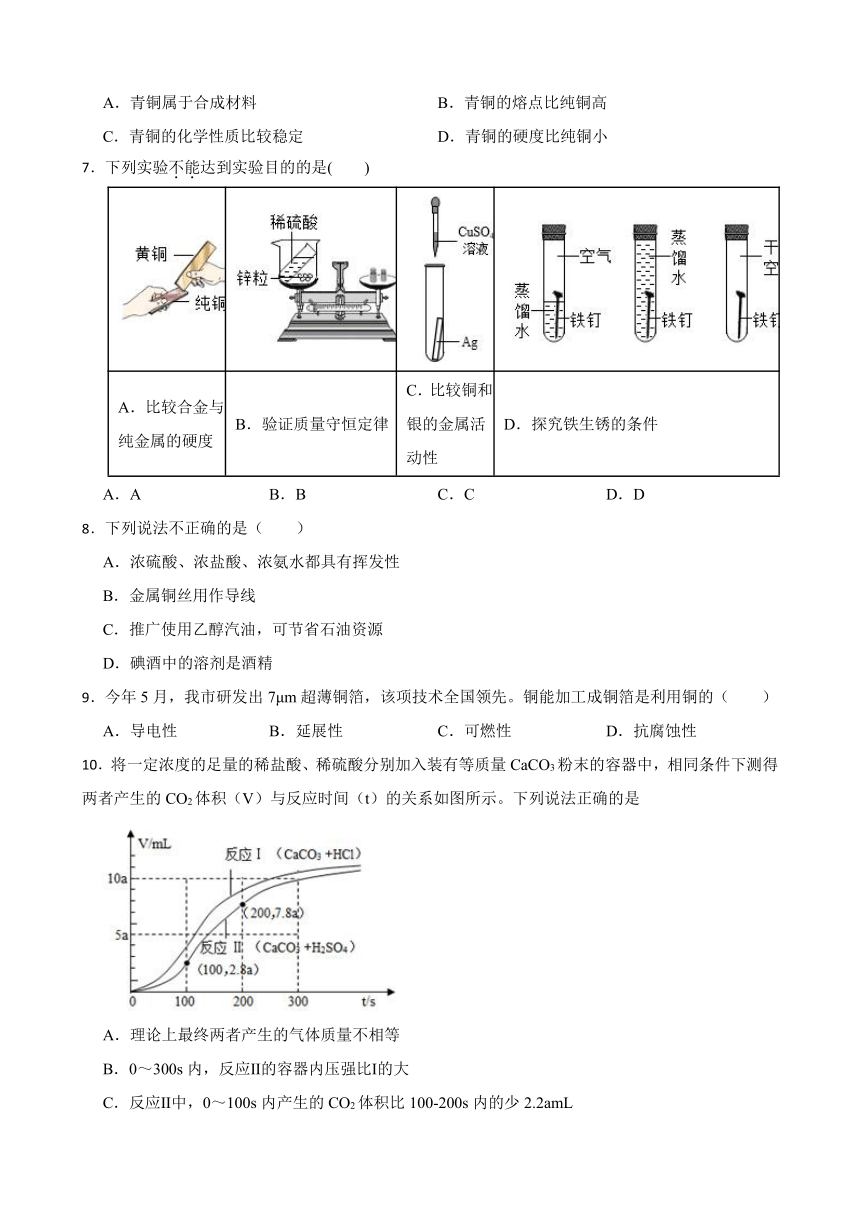
7.下列实验不能达到实验目的的是( )
A.比较合金与纯金属的硬度 B.验证质量守恒定律 C.比较铜和银的金属活动性 D.探究铁生锈的条件
A.A B.B C.C D.D
8.下列说法不正确的是( )
A.浓硫酸、浓盐酸、浓氨水都具有挥发性
B.金属铜丝用作导线
C.推广使用乙醇汽油,可节省石油资源
D.碘酒中的溶剂是酒精
9.今年5月,我市研发出7μm超薄铜箔,该项技术全国领先。铜能加工成铜箔是利用铜的( )
A.导电性 B.延展性 C.可燃性 D.抗腐蚀性
10.将一定浓度的足量的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如图所示。下列说法正确的是
A.理论上最终两者产生的气体质量不相等
B.0~300s内,反应Ⅱ的容器内压强比Ⅰ的大
C.反应Ⅱ中,0~100s内产生的CO2体积比100-200s内的少2.2amL
D.反应Ⅱ比反应Ⅰ的速率快
11.我国生产出仅有A4纸四分之一厚度的“手撕钢”(如图所示),其厚度只有0.02mm,这是目前中国最薄的不锈钢。下列有关“手撕钢”的说法错误的是( )
A.“手撕钢”不易生锈
B.“手撕钢”属于金属材料
C.“手撕钢”的含碳量比生铁高
D.普通钢材可以加工成“手撕钢”是因为金属具有延展性
12.《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。下列有关合金叙述不正确的是()
A.合金的熔点一般比其组分低
B.合金属于金属材料
C.合金的抗腐蚀性一般比其组分强
D.合金的硬度一般比其组分小
二、填空题
13.化学课上我们曾经观察过如图所示的实验.
(1)实验中,铜片上的白磷很快燃烧,其化学反应方程式为 .
(2)该实验主要利用了铜片良好的 性.
(3)烧杯中的水在实验中没有起到的作用是 (填序号).
A.作反应物 B.隔绝空气 C.升高温度.
14.中国手机厂商中兴推出了极具创新式的折叠手机-Axon m,如图是中兴可折叠手机,请回答下列问题。
(1)图中所示部件中属于有机合成材料的是
(2)用铝合金作手机外壳的优点是 。
(3)不锈钢属于 (填“纯净物”或“混合物”),请写出一个能证明铝金属活动性比铜强的化学反应方程式: 。
15.在日常生活、工农业生产和科学研究中,大量使用的金属材料常常不是纯金属,而是它们的合金,原因是:①合金的硬度比纯金属 (选填“大”或“小”);②合金的熔点比纯金属 (选填“高”或“低”);③合金的抗腐蚀性比纯金属 (选填“强”或“弱”).
16.金属材料在国防建设中起着重要的作用,歼﹣15飞机在辽宁舰上起飞.
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 ;
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 ;
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性 的金属.
17.铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有很好的抗腐蚀性能的原因是 。
(2)用铜制作导线主要是利用铜具有良好的 性;
(3)焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为 。
18.我国研制的“天问一号”飞船载着“祝融”号火星车成功着陆火星的乌托邦平原,标志着中国航天探索再创里程碑。
①火星车采用钛合金、铝合金、复合记忆纤维等材料制造,钛合金和铝合金属于 (选填“合成材料”、“复合材料”或“金属材料”)。
②工业制钛过程中的一个反应: ,X的化学式为 。
③下图是工业制硅反应的微观示意图:
写出该反应的化学方程式 ;硅片太阳能电池是将太阳能转化成电能,请说明太阳能电池的优点 (写出一点即可)。
三、综合题
19.材料是人类赖以生存和发展的物质基础。
(1)(一)C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,又会分解放出H2。
C60属于________(填字母序号)。
A.单质
B.化合物
C.混合物
(2)求算C60的相对分子质量的计算式为 。
(3)C60可用作吸氢材料是利用了其 (填“物理”或“化学”)性质。
(4)(二)铝是目前最经济实用的材料之一。
由铝制成的铝箔厚度仅为0.01 mm,广泛用于食品包装等。铝能制成铝箔,主要利用的铝的性质是 。
(5)铝箔表面有一层致密的氧化膜。用化学方程式表示 。
(6)某小组同学用铝箔做了如下实验:将铝箔在酒精灯上加热,发现铝箔逐渐变软,中间有液体被外面的固体包裹住。由此可以推测氧化铝的熔点比金属铝 (填“高”或“低”)。
20.海洋是巨大的资源宝库,从化学的视角看:
(1)元素资源:海水中含量最高的金属元素是 (填元素符号);从物质在水中溶解的规律和水天然循环的角度看,该元素含量最高的原因是 .
(2)淡水资源:淡化海水可以用 (填字母代号);
A.吸附法 B.蒸馏法 C.过滤法 D.电解法
该过程是 (填“化学变化”或“物理变化”).
(3)矿产资源:海底蕴藏着大量的“可燃冰”(含甲烷),甲烷燃烧的化学反应方程式为 .
(4)你还知道海洋中有哪些资源? (写一种)
21.2021年10月20日上午,冬奥会火种欢迎仪式在北京奥林匹克塔举行。
(1)从希腊采集的冬奥火种,通过火种灯来到北京,火种可点燃火炬内的燃料,火种为燃料燃烧提供的条件是 ;
(2)设计者在火种灯内外灯罩之间设计了一个导流通道,能够让燃料在燃烧时不至于产生黑烟和异味,保持火种灯外观清洁、透亮。从促进燃料充分燃烧角度看,导流通道的作用是 ;
(3)火种灯的外壳由铝合金制成,铝合金的硬度比纯铝的硬度 (填“大”或“小”);
(4)火种灯内的燃料是丙烷(C3H8)气体,完全燃烧生成二氧化碳和水,丙烷燃烧用化学方程式表示为 。
22.铅蓄电池在生产、生活中使用广泛.其构造示意图如图1,回答下列问题:
(1)铅蓄电池充电时是将电能转化为 (填序号)
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断 (填“增大”、“减小”或“不变”).
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类 材料.
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是 .
③如表是一些金属熔点的数据:
金属 锡 铅 铋 镉
熔点∕℃ 231.9 327.5 271.3 320.9
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 (填序号)
A.300﹣320℃
B.230﹣250℃
C.60﹣80℃
D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质 CaCO3 Ca(OH)2 NH3 NaOH
市场参考价(元/kg ) 1.8 2.0 6.5 11.5
已知:2NH3+H2SO4═(NH4)SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择 (填序号).
a、CaCO3b、Ca(OH)2c、NH3d、NaOH.
答案解析部分
1.【答案】A
2.【答案】B
3.【答案】C
4.【答案】C
5.【答案】B
6.【答案】C
7.【答案】B
8.【答案】A
9.【答案】B
10.【答案】C
11.【答案】C
12.【答案】D
13.【答案】4P+5O22P2O5;导热;A
14.【答案】(1)塑料贴膜
(2)质轻、硬度大、耐腐蚀等
(3)混合物;2Al+3Cu(NO3)2=2Al(NO3)3 +3Cu
15.【答案】大;低;强
16.【答案】(1)强度大、质量轻
(2)水和氧气;Fe2O3+6HCl=2FeCl3+3H2O
(3)强
17.【答案】(1)铝能和氧气反应生成一层致密的氧化膜,阻止铝继续腐蚀
(2)导电
(3)
18.【答案】金属材料;SO3;;无污染或绿色环保或节能(答案合理即可)
19.【答案】(1)A
(2)12×60
(3)化学
(4)延展性
(5)4Al+3O2 = 2Al2O3
(6)高
20.【答案】(1)Na;含有钠元素的碱、盐都是易溶于水的,通过水的天然循环,土壤中的含有钠元素的物质随水进入海洋
(2)B;物理变化
(3)CH4+2O2 CO2+2H2O
(4)海洋中含有溴
21.【答案】(1)使温度达到燃料的着火点
(2)提供充足的空气(或氧气)
(3)大
(4)
22.【答案】(1)c
(2)增大
(3)有机合成;Ca(H2PO4)2;C;b
一、单选题
1.金属材料在生活、生产中应用广泛,下列说法正确的是( )
A.不锈钢碗筷比普通铁锅耐腐蚀
B.焊锡(锡铅合金)的熔点大于铅的熔点
C.银导电性最好,常用作电线
D.铁制品只要与水接触就会生锈
2.下列事实和相应的解释不一致的是( )
A.切洋葱时可闻到刺激性气味——分子在不停地运动
B.CO2通入紫色石蕊溶液中,溶液变红——CO2能使紫色石蕊变红
C.水分解生成氢气和氧气——水是由氢元素和氧元素组成的
D.金刚石坚硬而石墨很软——碳原子的排列方式不同
3.下列金属制品中,利用金属导电性的是( )
A.黄金首饰 B.铝蒸锅
C.铜导线 D.金属乐器
4.下列关于金属的说法正确的是( )
A.铝元素在地壳中含量最多,使用也最早
B.不锈钢的抗腐蚀性强于纯铁,硬度小于纯铁
C.灯泡里的灯丝常用钨制成
D.地球上金属矿物资源储量有限,可再生
5.化学与生产生活密切相关。下列说法错误的是( )
A.pH<5.6的降雨称为酸雨 B.石油属于可再生能源
C.PM2.5属于大气污染物 D.铝合金的硬度比纯铝大
6.2021年7月,三星堆3号坑再次出土一件青铜神树。下列关于青铜的说法正确的是( )
A.青铜属于合成材料 B.青铜的熔点比纯铜高
C.青铜的化学性质比较稳定 D.青铜的硬度比纯铜小
7.下列实验不能达到实验目的的是( )
A.比较合金与纯金属的硬度 B.验证质量守恒定律 C.比较铜和银的金属活动性 D.探究铁生锈的条件
A.A B.B C.C D.D
8.下列说法不正确的是( )
A.浓硫酸、浓盐酸、浓氨水都具有挥发性
B.金属铜丝用作导线
C.推广使用乙醇汽油,可节省石油资源
D.碘酒中的溶剂是酒精
9.今年5月,我市研发出7μm超薄铜箔,该项技术全国领先。铜能加工成铜箔是利用铜的( )
A.导电性 B.延展性 C.可燃性 D.抗腐蚀性
10.将一定浓度的足量的稀盐酸、稀硫酸分别加入装有等质量CaCO3粉末的容器中,相同条件下测得两者产生的CO2体积(V)与反应时间(t)的关系如图所示。下列说法正确的是
A.理论上最终两者产生的气体质量不相等
B.0~300s内,反应Ⅱ的容器内压强比Ⅰ的大
C.反应Ⅱ中,0~100s内产生的CO2体积比100-200s内的少2.2amL
D.反应Ⅱ比反应Ⅰ的速率快
11.我国生产出仅有A4纸四分之一厚度的“手撕钢”(如图所示),其厚度只有0.02mm,这是目前中国最薄的不锈钢。下列有关“手撕钢”的说法错误的是( )
A.“手撕钢”不易生锈
B.“手撕钢”属于金属材料
C.“手撕钢”的含碳量比生铁高
D.普通钢材可以加工成“手撕钢”是因为金属具有延展性
12.《吕氏春秋》记载“金(即铜单质)柔锡(即锡单质)柔,合两柔则刚(即坚硬)”。下列有关合金叙述不正确的是()
A.合金的熔点一般比其组分低
B.合金属于金属材料
C.合金的抗腐蚀性一般比其组分强
D.合金的硬度一般比其组分小
二、填空题
13.化学课上我们曾经观察过如图所示的实验.
(1)实验中,铜片上的白磷很快燃烧,其化学反应方程式为 .
(2)该实验主要利用了铜片良好的 性.
(3)烧杯中的水在实验中没有起到的作用是 (填序号).
A.作反应物 B.隔绝空气 C.升高温度.
14.中国手机厂商中兴推出了极具创新式的折叠手机-Axon m,如图是中兴可折叠手机,请回答下列问题。
(1)图中所示部件中属于有机合成材料的是
(2)用铝合金作手机外壳的优点是 。
(3)不锈钢属于 (填“纯净物”或“混合物”),请写出一个能证明铝金属活动性比铜强的化学反应方程式: 。
15.在日常生活、工农业生产和科学研究中,大量使用的金属材料常常不是纯金属,而是它们的合金,原因是:①合金的硬度比纯金属 (选填“大”或“小”);②合金的熔点比纯金属 (选填“高”或“低”);③合金的抗腐蚀性比纯金属 (选填“强”或“弱”).
16.金属材料在国防建设中起着重要的作用,歼﹣15飞机在辽宁舰上起飞.
(1)铝合金用于制造飞机的外壳,铝合金材质的主要优点是 ;
(2)改装前的辽宁舰舰身锈迹斑斑,钢铁的锈蚀主要是铁与空气中的 共同作用的结果.工业生产中常用稀盐酸除去铁制品表面的铁锈,该反应的化学方程式为 ;
(3)为了避免轮船的钢质外壳被腐蚀,通常在轮船外壳上镶嵌比铁活动性 的金属.
17.铝、铜、铁是生活中常见的金属。
(1)铝在空气中具有很好的抗腐蚀性能的原因是 。
(2)用铜制作导线主要是利用铜具有良好的 性;
(3)焊接铁制品时,通常先用稀盐酸除去其表面的铁锈,反应的化学方程式为 。
18.我国研制的“天问一号”飞船载着“祝融”号火星车成功着陆火星的乌托邦平原,标志着中国航天探索再创里程碑。
①火星车采用钛合金、铝合金、复合记忆纤维等材料制造,钛合金和铝合金属于 (选填“合成材料”、“复合材料”或“金属材料”)。
②工业制钛过程中的一个反应: ,X的化学式为 。
③下图是工业制硅反应的微观示意图:
写出该反应的化学方程式 ;硅片太阳能电池是将太阳能转化成电能,请说明太阳能电池的优点 (写出一点即可)。
三、综合题
19.材料是人类赖以生存和发展的物质基础。
(1)(一)C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,又会分解放出H2。
C60属于________(填字母序号)。
A.单质
B.化合物
C.混合物
(2)求算C60的相对分子质量的计算式为 。
(3)C60可用作吸氢材料是利用了其 (填“物理”或“化学”)性质。
(4)(二)铝是目前最经济实用的材料之一。
由铝制成的铝箔厚度仅为0.01 mm,广泛用于食品包装等。铝能制成铝箔,主要利用的铝的性质是 。
(5)铝箔表面有一层致密的氧化膜。用化学方程式表示 。
(6)某小组同学用铝箔做了如下实验:将铝箔在酒精灯上加热,发现铝箔逐渐变软,中间有液体被外面的固体包裹住。由此可以推测氧化铝的熔点比金属铝 (填“高”或“低”)。
20.海洋是巨大的资源宝库,从化学的视角看:
(1)元素资源:海水中含量最高的金属元素是 (填元素符号);从物质在水中溶解的规律和水天然循环的角度看,该元素含量最高的原因是 .
(2)淡水资源:淡化海水可以用 (填字母代号);
A.吸附法 B.蒸馏法 C.过滤法 D.电解法
该过程是 (填“化学变化”或“物理变化”).
(3)矿产资源:海底蕴藏着大量的“可燃冰”(含甲烷),甲烷燃烧的化学反应方程式为 .
(4)你还知道海洋中有哪些资源? (写一种)
21.2021年10月20日上午,冬奥会火种欢迎仪式在北京奥林匹克塔举行。
(1)从希腊采集的冬奥火种,通过火种灯来到北京,火种可点燃火炬内的燃料,火种为燃料燃烧提供的条件是 ;
(2)设计者在火种灯内外灯罩之间设计了一个导流通道,能够让燃料在燃烧时不至于产生黑烟和异味,保持火种灯外观清洁、透亮。从促进燃料充分燃烧角度看,导流通道的作用是 ;
(3)火种灯的外壳由铝合金制成,铝合金的硬度比纯铝的硬度 (填“大”或“小”);
(4)火种灯内的燃料是丙烷(C3H8)气体,完全燃烧生成二氧化碳和水,丙烷燃烧用化学方程式表示为 。
22.铅蓄电池在生产、生活中使用广泛.其构造示意图如图1,回答下列问题:
(1)铅蓄电池充电时是将电能转化为 (填序号)
a、机械能 b、热能 c、化学能
(2)铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断 (填“增大”、“减小”或“不变”).
(3)如图2是回收废铅蓄电池的一种工艺流程:
①从材料分类角度看,塑料是一类 材料.
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是 .
③如表是一些金属熔点的数据:
金属 锡 铅 铋 镉
熔点∕℃ 231.9 327.5 271.3 320.9
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为 (填序号)
A.300﹣320℃
B.230﹣250℃
C.60﹣80℃
D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质 CaCO3 Ca(OH)2 NH3 NaOH
市场参考价(元/kg ) 1.8 2.0 6.5 11.5
已知:2NH3+H2SO4═(NH4)SO4,如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择 (填序号).
a、CaCO3b、Ca(OH)2c、NH3d、NaOH.
答案解析部分
1.【答案】A
2.【答案】B
3.【答案】C
4.【答案】C
5.【答案】B
6.【答案】C
7.【答案】B
8.【答案】A
9.【答案】B
10.【答案】C
11.【答案】C
12.【答案】D
13.【答案】4P+5O22P2O5;导热;A
14.【答案】(1)塑料贴膜
(2)质轻、硬度大、耐腐蚀等
(3)混合物;2Al+3Cu(NO3)2=2Al(NO3)3 +3Cu
15.【答案】大;低;强
16.【答案】(1)强度大、质量轻
(2)水和氧气;Fe2O3+6HCl=2FeCl3+3H2O
(3)强
17.【答案】(1)铝能和氧气反应生成一层致密的氧化膜,阻止铝继续腐蚀
(2)导电
(3)
18.【答案】金属材料;SO3;;无污染或绿色环保或节能(答案合理即可)
19.【答案】(1)A
(2)12×60
(3)化学
(4)延展性
(5)4Al+3O2 = 2Al2O3
(6)高
20.【答案】(1)Na;含有钠元素的碱、盐都是易溶于水的,通过水的天然循环,土壤中的含有钠元素的物质随水进入海洋
(2)B;物理变化
(3)CH4+2O2 CO2+2H2O
(4)海洋中含有溴
21.【答案】(1)使温度达到燃料的着火点
(2)提供充足的空气(或氧气)
(3)大
(4)
22.【答案】(1)c
(2)增大
(3)有机合成;Ca(H2PO4)2;C;b
