到实验室去 探究金属的性质 同步练习 (含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 到实验室去 探究金属的性质 同步练习 (含答案) 2022-2023学年鲁教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 61.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-06 00:00:00 | ||
图片预览



文档简介
到实验室去 探究金属的性质 同步练习
一、单选题
1.2021年,长沙市将启动地铁7号线一期工程建设,地铁的制造需要大量使用金属材料。下列有关金属的说法中正确的是( )
A.常温下所有金属都是固体
B.铜常用作导线,是因为铜有良好的导电性
C.所有金属元素在自然界中都是以化合物的形式存在
D.地壳中含量最高的金属元素是铁元素
2.铁、铝、铜是生活中常用的金属。下列有关说法或者做法正确的是( )
A.铁的利用要比铜和铝晚得多
B.钢是很纯的铁
C.可以用铁制容器配制波尔多液
D.铝在空气中有很好的抗腐蚀性能
3.下列化学方程式表示的反应,符合实验事实并书写正确的是()
A.铜丝插入硝酸银溶液中:Cu+2AgNO3=2Ag+Cu(NO3)2
B.硝酸钾溶液和氯化镁溶液混合:2KNO3+MgCl2=Mg(NO3)2↓+2KCl
C.一氧化碳还原氧化铁:3CO+Fe2O3=2Fe+3CO2↑
D.铁粉放入稀硫酸中:2Fe+H2SO4=Fe2(SO4)3+3H2↑
4.要出去物质中所含的少量杂质,下列实验设计不合理的是( )
选项 物质 杂质 所选试剂或方法
A CaO CaCO3 稀盐酸
B NaCl溶液 MgCl2 适量NaOH溶液
C O2 水蒸气 浓硫酸
D Cu粉 Fe粉 磁铁吸引
A.A B.B C.C D.D
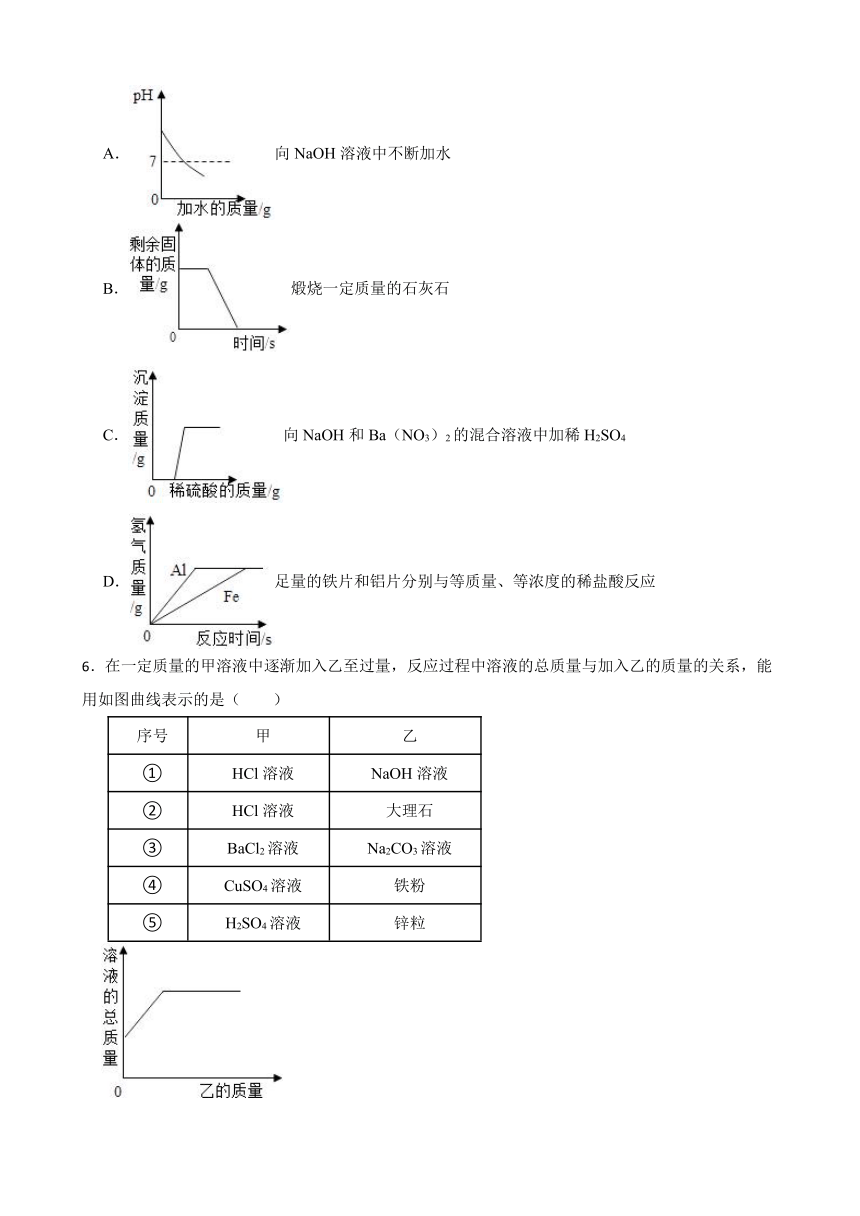
5.下列四个图象的变化趋势,能正确描述对应操作的是( )
A.向NaOH溶液中不断加水
B.煅烧一定质量的石灰石
C.向NaOH和Ba(NO3)2的混合溶液中加稀H2SO4
D.足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应
6.在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系,能用如图曲线表示的是( )
序号 甲 乙
① HCl溶液 NaOH溶液
② HCl溶液 大理石
③ BaCl2溶液 Na2CO3溶液
④ CuSO4溶液 铁粉
⑤ H2SO4溶液 锌粒
A.①② B.③④ C.①⑤ D.②⑤
7.2.5g镁和M的混合物与足量的稀盐酸反应,生成0.2g的氢气,则M不可能是( )
A.铁 B.锌 C.铜 D.铝
8.中华传统文化蕴含丰富的化学知识。从化学视角对下列俗语、诗词的解释不正确的是( )
A.“金入于猛火,色不夺精光”---金在加热的条件下能与氧气反应
B.“百炼成钢”---降低生铁中碳元素的含量
C.“只要功夫深,铁杵磨成针”---发生的是物理变化
D.“满架蔷薇一院香”---分子在不断地运动
9.下列有关金属材料的说法正确的是( )
A.生铁比纯铁硬度小
B.不锈钢的抗腐蚀性比纯铁的好
C.钢的含碳量比生铁的含碳量高
D.锡铅合金制作的保险丝的熔点比锡和铅的熔点都高
10.李伟同学将铝丝放入CuSO4溶液中,发现铝丝表面有红色物质析出的同时还有少量无色气体产生。对于产生气体这一“异常”现象,下列分析没有科学道理的是( )
A.产生的气体可能是氢气
B.CuSO4溶液pH可能小于7
C.若用银粉代替铝丝也可能会产生相同的现象
D.产生的气体也有可能是SO2
11.现有含铁和锌的样品 12.1g,加入到 200g 质量分数为 10%的稀盐酸中充分反应,反应后得到211.7g 溶液,则样品中铁的质量为( )
A.2.8g B.5.6g C.6.5g D.8.4g
12.最近科学家研制出一种新型防弹衣,它是由“剪切增稠液体”和凯夫拉纤维结合而成,这种“剪切增稠液体”是由微小而硬度极高的硅颗粒和聚乙二醇混合而成,当受外力打击时这些小颗粒迅速沉积形成一层坚硬阻挡层.关于硅的说法正确的是( )
A.硅能导电,是一种金属单质
B.硅颗粒溶合到聚乙二醇中是化学变化
C.硅元素在地壳中的含量最高
D.硅原子与碳原子最外层电子数相同
二、填空题
13.向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,得滤渣A和滤液B.向滤渣A中加入稀盐酸,有气泡冒出.则滤渣A中一定有 ;滤液B中一定有的金属离子是 ,一定没有的金属离子是 .
14.人类的生活与生产都离不开金属和金属材料。
(1)铝的金属活动性比铁强,但为什么生活中常在铁制品表面涂刷铝粉来防止铁制品锈蚀?
(2)向某硝酸银、硝酸汞混合溶液中逐渐加入锌粉,溶液质量与加入锌粉的质量关系如图所示。
①写出a~b段发生反应的化学方程式: 。
②写出c点时溶液中溶质的化学式: 。
15.对于下列金属:铝、铜、锌、钛、铁、钙.
①可用来冶炼高熔点得金属是 .
②可用于制干电池的是 .
③白铁表面所镀的金属是 .
④广泛用于制电线、电缆的是 .
⑤广泛应用于航空工业、制造工业的是 .
16.金属制品与我们的日常生活密不可分。
(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是 。
(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成 。
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是 (用序号①②③填空)
①Zn、CuSO4溶液、Ag ②ZnSO4溶液、Cu、AgNO3溶液 ③Zn、Cu、AgNO3溶液
(4)由所学知识可知,活泼性Fe>Cu, 。非金属与金属类似,活泼性Cl2>Br2>l2,请写出将Cl2通入NaBr溶液中发生反应的化学方程式 。
17.铁锭可以拉成铁丝是利用了其良好的 ;铁锁的表面刷油漆能防止腐蚀,其原因是 ;铁锁锁身生锈(主要成分Fe2O3)用硫酸除去的化学方程式为 ;
18.某学生在探究活动中,把少量的生铁放入烧杯中并注入一定量的稀硫酸中,能观察到的现象有: ①生铁表面有 产生,②溶液逐渐变 ,完全反应后烧杯底部有 出现。
请写出有关化学方程式
三、综合题
19.汽车是现代生活中重要的交通工具。请回答下列问题:
(1)汽车电路中的导线一般为铜芯线,这是利用了金属铜的良好导电性和 性。
(2)下列各类汽车在使用时,对空气污染最小的
①汽油车②柴油车③新能源纯电动汽车
(3)汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是 。
(4)为了安全起见,汽车内需配备小型灭火器,其灭火原理是 。
20.钢铁是重要的金属材料.
(1)下列铁制品话的用途中,利用金属导热性的是 .(填字母,下同).
(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 .
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(3)为防止水龙头生锈.其表面镀有一层铬.铁生锈的条件是 .
21.现在有以下物质:①氮气②氧气③稀有气体④二氧化碳⑤酒精⑥钨.请用序号回答问题:
(1)占空气体积78%的是 ;
(2)植物光合作用的原料是 ;
(3)医疗急救应选用 ;
(4)通电时发出有色光的是 ;
(5)化学实验常用的燃料是 ;
(6)可用于灯泡中灯丝的是 。
22.下列关于物质性质及用途的说法是否正确 正确的在括号中打“√”,错误的打“x”。
(1)稀有气体通电时发出不同颜色可以用作霓虹灯电光源。
(2)金属钨具有极高熔点,常用作电池的电极。
(3)酒精是一种溶剂,可以用于溶解中草药中的有效成分。
(4)液氧具有助燃性,可用作火箭发射的助燃剂。
(5)甲烷燃烧放出热量可用于高温切割和焊接金属。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】A
4.【答案】A
5.【答案】D
6.【答案】D
7.【答案】D
8.【答案】A
9.【答案】B
10.【答案】C
11.【答案】B
12.【答案】D
13.【答案】Ag、Cu、Fe;Zn2+;Ag+、Cu2+
14.【答案】(1)铝比较活泼,能和空气中的氧气反应生成氧化铝保护膜
(2)Zn+2AgNO3=Zn(NO3)2+2Ag;Zn(NO3)2
15.【答案】铝;锌;锌;铜、铝;钛
16.【答案】(1)Cu或铜
(2)致密氧化膜
(3)③
(4)
17.【答案】延展性;能够隔绝空气(或氧气)和水;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
18.【答案】气泡产生;浅绿色的溶液;残渣;Fe + H2SO4 = FeSO4 +H2↑
19.【答案】(1)延展
(2)③
(3)隔绝水和氧气(合理即可)
(4)隔绝空气(或降低温度到着火点以下或隔绝空气和降低温度到着火点以下)
20.【答案】(1)B
(2)A
(3)与水和氧气同时接触
21.【答案】(1)①
(2)④
(3)②
(4)③
(5)⑤
(6)⑥
22.【答案】(1)√
(2)
(3)√
(4)√
(5)
一、单选题
1.2021年,长沙市将启动地铁7号线一期工程建设,地铁的制造需要大量使用金属材料。下列有关金属的说法中正确的是( )
A.常温下所有金属都是固体
B.铜常用作导线,是因为铜有良好的导电性
C.所有金属元素在自然界中都是以化合物的形式存在
D.地壳中含量最高的金属元素是铁元素
2.铁、铝、铜是生活中常用的金属。下列有关说法或者做法正确的是( )
A.铁的利用要比铜和铝晚得多
B.钢是很纯的铁
C.可以用铁制容器配制波尔多液
D.铝在空气中有很好的抗腐蚀性能
3.下列化学方程式表示的反应,符合实验事实并书写正确的是()
A.铜丝插入硝酸银溶液中:Cu+2AgNO3=2Ag+Cu(NO3)2
B.硝酸钾溶液和氯化镁溶液混合:2KNO3+MgCl2=Mg(NO3)2↓+2KCl
C.一氧化碳还原氧化铁:3CO+Fe2O3=2Fe+3CO2↑
D.铁粉放入稀硫酸中:2Fe+H2SO4=Fe2(SO4)3+3H2↑
4.要出去物质中所含的少量杂质,下列实验设计不合理的是( )
选项 物质 杂质 所选试剂或方法
A CaO CaCO3 稀盐酸
B NaCl溶液 MgCl2 适量NaOH溶液
C O2 水蒸气 浓硫酸
D Cu粉 Fe粉 磁铁吸引
A.A B.B C.C D.D
5.下列四个图象的变化趋势,能正确描述对应操作的是( )
A.向NaOH溶液中不断加水
B.煅烧一定质量的石灰石
C.向NaOH和Ba(NO3)2的混合溶液中加稀H2SO4
D.足量的铁片和铝片分别与等质量、等浓度的稀盐酸反应
6.在一定质量的甲溶液中逐渐加入乙至过量,反应过程中溶液的总质量与加入乙的质量的关系,能用如图曲线表示的是( )
序号 甲 乙
① HCl溶液 NaOH溶液
② HCl溶液 大理石
③ BaCl2溶液 Na2CO3溶液
④ CuSO4溶液 铁粉
⑤ H2SO4溶液 锌粒
A.①② B.③④ C.①⑤ D.②⑤
7.2.5g镁和M的混合物与足量的稀盐酸反应,生成0.2g的氢气,则M不可能是( )
A.铁 B.锌 C.铜 D.铝
8.中华传统文化蕴含丰富的化学知识。从化学视角对下列俗语、诗词的解释不正确的是( )
A.“金入于猛火,色不夺精光”---金在加热的条件下能与氧气反应
B.“百炼成钢”---降低生铁中碳元素的含量
C.“只要功夫深,铁杵磨成针”---发生的是物理变化
D.“满架蔷薇一院香”---分子在不断地运动
9.下列有关金属材料的说法正确的是( )
A.生铁比纯铁硬度小
B.不锈钢的抗腐蚀性比纯铁的好
C.钢的含碳量比生铁的含碳量高
D.锡铅合金制作的保险丝的熔点比锡和铅的熔点都高
10.李伟同学将铝丝放入CuSO4溶液中,发现铝丝表面有红色物质析出的同时还有少量无色气体产生。对于产生气体这一“异常”现象,下列分析没有科学道理的是( )
A.产生的气体可能是氢气
B.CuSO4溶液pH可能小于7
C.若用银粉代替铝丝也可能会产生相同的现象
D.产生的气体也有可能是SO2
11.现有含铁和锌的样品 12.1g,加入到 200g 质量分数为 10%的稀盐酸中充分反应,反应后得到211.7g 溶液,则样品中铁的质量为( )
A.2.8g B.5.6g C.6.5g D.8.4g
12.最近科学家研制出一种新型防弹衣,它是由“剪切增稠液体”和凯夫拉纤维结合而成,这种“剪切增稠液体”是由微小而硬度极高的硅颗粒和聚乙二醇混合而成,当受外力打击时这些小颗粒迅速沉积形成一层坚硬阻挡层.关于硅的说法正确的是( )
A.硅能导电,是一种金属单质
B.硅颗粒溶合到聚乙二醇中是化学变化
C.硅元素在地壳中的含量最高
D.硅原子与碳原子最外层电子数相同
二、填空题
13.向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,得滤渣A和滤液B.向滤渣A中加入稀盐酸,有气泡冒出.则滤渣A中一定有 ;滤液B中一定有的金属离子是 ,一定没有的金属离子是 .
14.人类的生活与生产都离不开金属和金属材料。
(1)铝的金属活动性比铁强,但为什么生活中常在铁制品表面涂刷铝粉来防止铁制品锈蚀?
(2)向某硝酸银、硝酸汞混合溶液中逐渐加入锌粉,溶液质量与加入锌粉的质量关系如图所示。
①写出a~b段发生反应的化学方程式: 。
②写出c点时溶液中溶质的化学式: 。
15.对于下列金属:铝、铜、锌、钛、铁、钙.
①可用来冶炼高熔点得金属是 .
②可用于制干电池的是 .
③白铁表面所镀的金属是 .
④广泛用于制电线、电缆的是 .
⑤广泛应用于航空工业、制造工业的是 .
16.金属制品与我们的日常生活密不可分。
(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是 。
(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成 。
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是 (用序号①②③填空)
①Zn、CuSO4溶液、Ag ②ZnSO4溶液、Cu、AgNO3溶液 ③Zn、Cu、AgNO3溶液
(4)由所学知识可知,活泼性Fe>Cu, 。非金属与金属类似,活泼性Cl2>Br2>l2,请写出将Cl2通入NaBr溶液中发生反应的化学方程式 。
17.铁锭可以拉成铁丝是利用了其良好的 ;铁锁的表面刷油漆能防止腐蚀,其原因是 ;铁锁锁身生锈(主要成分Fe2O3)用硫酸除去的化学方程式为 ;
18.某学生在探究活动中,把少量的生铁放入烧杯中并注入一定量的稀硫酸中,能观察到的现象有: ①生铁表面有 产生,②溶液逐渐变 ,完全反应后烧杯底部有 出现。
请写出有关化学方程式
三、综合题
19.汽车是现代生活中重要的交通工具。请回答下列问题:
(1)汽车电路中的导线一般为铜芯线,这是利用了金属铜的良好导电性和 性。
(2)下列各类汽车在使用时,对空气污染最小的
①汽油车②柴油车③新能源纯电动汽车
(3)汽车表面喷漆,可以延缓汽车的锈蚀,其防锈原理是 。
(4)为了安全起见,汽车内需配备小型灭火器,其灭火原理是 。
20.钢铁是重要的金属材料.
(1)下列铁制品话的用途中,利用金属导热性的是 .(填字母,下同).
(2)目前世界上已有50%以上的废钢铁得到回收利用,其目的是 .
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(3)为防止水龙头生锈.其表面镀有一层铬.铁生锈的条件是 .
21.现在有以下物质:①氮气②氧气③稀有气体④二氧化碳⑤酒精⑥钨.请用序号回答问题:
(1)占空气体积78%的是 ;
(2)植物光合作用的原料是 ;
(3)医疗急救应选用 ;
(4)通电时发出有色光的是 ;
(5)化学实验常用的燃料是 ;
(6)可用于灯泡中灯丝的是 。
22.下列关于物质性质及用途的说法是否正确 正确的在括号中打“√”,错误的打“x”。
(1)稀有气体通电时发出不同颜色可以用作霓虹灯电光源。
(2)金属钨具有极高熔点,常用作电池的电极。
(3)酒精是一种溶剂,可以用于溶解中草药中的有效成分。
(4)液氧具有助燃性,可用作火箭发射的助燃剂。
(5)甲烷燃烧放出热量可用于高温切割和焊接金属。
答案解析部分
1.【答案】B
2.【答案】D
3.【答案】A
4.【答案】A
5.【答案】D
6.【答案】D
7.【答案】D
8.【答案】A
9.【答案】B
10.【答案】C
11.【答案】B
12.【答案】D
13.【答案】Ag、Cu、Fe;Zn2+;Ag+、Cu2+
14.【答案】(1)铝比较活泼,能和空气中的氧气反应生成氧化铝保护膜
(2)Zn+2AgNO3=Zn(NO3)2+2Ag;Zn(NO3)2
15.【答案】铝;锌;锌;铜、铝;钛
16.【答案】(1)Cu或铜
(2)致密氧化膜
(3)③
(4)
17.【答案】延展性;能够隔绝空气(或氧气)和水;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O
18.【答案】气泡产生;浅绿色的溶液;残渣;Fe + H2SO4 = FeSO4 +H2↑
19.【答案】(1)延展
(2)③
(3)隔绝水和氧气(合理即可)
(4)隔绝空气(或降低温度到着火点以下或隔绝空气和降低温度到着火点以下)
20.【答案】(1)B
(2)A
(3)与水和氧气同时接触
21.【答案】(1)①
(2)④
(3)②
(4)③
(5)⑤
(6)⑥
22.【答案】(1)√
(2)
(3)√
(4)√
(5)
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
