第三章第一节卤代烃课件(共42张PPT)2022-2023学年高二化学下学期人教版(2019)选择性必修3
文档属性
| 名称 | 第三章第一节卤代烃课件(共42张PPT)2022-2023学年高二化学下学期人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 23.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-07 00:00:00 | ||
图片预览











文档简介
(共42张PPT)
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第一节 卤代烃
学习
目标
第1课时
卤代烃
PART
01
PART
02
通过从卤代烃的官能团及其转化角度认识卤代烃取代反应、消去反应的特点和规律,了解有机反应类型与有机化合物分子结构特点之间的关系。
掌握卤代烃在有机合成中的桥梁作用,培养“科学探究与社会责任”的核心素养
烃分子中的氢原子被不同官能团取代后,就能生成一系列新的不同类别的有机化
合物,如卤代烃、醇、酚、醛、羧酸和酯等。从结构角度看都可以看作是由烃衍生而
来的,所以被称为烃的衍生物。
烃的衍生物
CH3CH2Br
烃的衍生物具有与烃不同的性质,这些性质主要由其分子中的官能团
决定。
认识卤代烃
阅读教材54页,思考下列问题:
(1)什么是卤代烃?有哪些分类?
(2)第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
(3)卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
烃分子中的氢原子被卤素原子取代生成的化合物。一元卤代烃可表示为:R-X
1. 概念:
C X 碳卤键
元素组成:一定含C、X(H不一定)
官能团:
如CCl4
2. 分类
卤代烃分类
按卤素原
子数目分
单卤代烃
多卤代烃
按卤素原
子种类分
氟代烃
氯代烃
溴代烃
碘代烃
一卤代烃、多卤代烃
按卤素原子数目
饱和卤代烃、不饱和卤代烃
按烃基是否饱和
脂肪卤代烃、芳香卤代烃
按是否含有苯环
认识卤代烃
①甲烷和氯气
②苯与溴
③乙烯和溴
④乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
3.烃转化为卤代烃的途径
认识卤代烃
选主链
定编号
写名称
选择含官能团的最长碳链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,
有碳碳双键时从距离碳碳双键近的一端开始编号
从简入繁
4.卤代烃的命名
3-甲基-3-溴-1-丁烯
卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
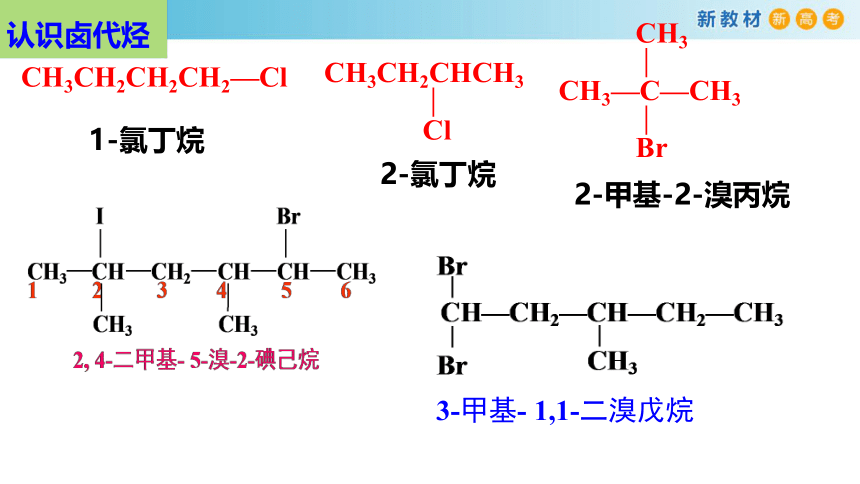
认识卤代烃
CH3CH2CH2CH2—Cl
CH3CH2CHCH3
Cl
—
CH3—C—CH3
Br
—
—
CH3
1-氯丁烷
2-氯丁烷
2-甲基-2-溴丙烷
3-甲基- 1,1-二溴戊烷
认识卤代烃
名称 结构简式 液态时密度/(g·cm-3) 沸点/℃
一氯甲烷 CH3Cl 0.916 -24
一氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
以氯代烃的密度和沸点为例,同时结合烷烃的物理性质的变化规律,总结卤代烃的物理性质。
认识卤代烃
常温下除一氯甲烷、氯乙烷、氯乙烯等少数是气体外,
大多数为液体或固体。
除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。
一般随着烃基中碳原子数目的增加而减小。
卤代烃不溶于水,可溶于有机溶剂,某些卤代烃本身就是有机溶剂
熔沸点大于同碳个数的烃,随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。
状态
沸点
密度
溶解性
1.物理性质
阅读52页教材,并结合P30烷烃的物理性质,
分析表3-1,总结卤代烃的物理性质及其递变规律。
认识卤代烃
(1)卤代烃是一类特殊的烃。 ( )
提示:卤代烃含卤族元素,不是烃。
(2)卤代烃中一定含有的元素为C、H和卤素。( )
提示:卤代烃不一定含H元素,如CCl4。
(3)卤代烃不一定是由烃分子和卤素单质发生取代反应得到的。( )
提示:
卤代烃可以由烃分子发生加成反应得到,如乙烯与溴水发生加成反应得到1,2-二溴乙烷。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
√
×
×
认识卤代烃
2.溴乙烷中混有杂质乙醇,除去乙醇的方法是( )
A.加热蒸发 B.过滤 C.加水、萃取、分液 D.加苯、萃取、分液
解析:溴乙烷难溶于水,而乙醇可与水以任意比例互溶,故可向混合液中加水进行萃取,然后分液即可除去乙醇。
C
3.下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
解析:A项,卤代烃的密度比水的大,错;B项,卤代烃的沸点比相应烃的高,错;D项,前者大,错。
C
认识卤代烃
C2H5Br
CH3CH2Br 或 C2H5Br
分子式:
结构式:
结构简式:
官能团:
C—Br
核磁共振氢谱图
(碳溴键)
球棍模型
空间填充模型
电子式:
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
【以溴乙烷为例】学习卤代烃的性质:
1、溴乙烷的组成和结构
认识卤代烃
颜 色:
状 态:
密 度:
溶解性:
沸 点:
无色透明
油状液体
比水大
不溶于水,
易溶于有机溶剂
沸点38.4℃
易挥发
2. C2H5Br物理性质
对 比
无色
气体
-88.6 ℃
不溶于水
CH3CH3
比水小
>
卤代烃的熔沸点大于同C原子数的烃!
【以溴乙烷为例】学习卤代烃的性质:
认识卤代烃
分析卤代烃的结构特点,推测卤代烃具有怎样的化学性质。
卤代烃中卤素原子吸引电子能力较强,共用电子对偏向卤素原子,使C—X键具有较强的极性,所以卤代烃具有较强的反应活性,易发生取代反应和消去反应。
碳卤键
官能团:
X
C
δ—
δ+
例:溴乙烷和乙烷的结构相似,区别在于C-H键与C-Br键的不同。C-Br键为极性键,由于溴原子吸引电子能力强,C-Br键易断裂,使溴原子易被取代。
【思考】
提出问题1:
对CH3CH2Br化学性质的探索
溴乙烷CH3CH2Br 在水中能否电离出Br-?
它是否为电解质?请设计实验证明。
实验:
溴乙烷
HNO3酸化后的AgNO3溶液
无明显变化
溴乙烷不是电解质,不能电离出Br-。
提出问题2:CH3CH3+水→不反应, CH3CH2Br+H2O →
科学猜测:若反应,可能有 产生。
怎样证明有Br-产生?
资料卡片:
C2H5Br与水的反应要在碱性环境下才容易进行
Br-
实验装置
实验现象 ①中溶液_____ ;②中有机层厚度减小;④中有 生成
实验解释 溴乙烷与NaOH溶液共热产生了______
分层
淡黄色沉淀
Br-
溴乙烷与NaOH溶液共热的化学方程式为______________________________________。反应类型为 。
取代反应
CH3CH2Br+NaOH CH3CH2OH+NaBr
1.取代反应
【实验3-1】课文P55
(以溴乙烷为例)
卤代烃的化学性质
CH3CH2—Br + Na—OH CH3CH2—OH + NaBr
H2O
从平衡移动的角度看,NaOH不断中和氢溴酸,促进溴乙烷的水解;加热的目的是提高反应速率,且水解是吸热反应,升高温度也有利于平衡右移。水相当于是催化剂
卤代烃的化学性质
1.取代反应(水解反应)
反应条件:
NaOH水溶液、加热
反应原理:
羟基取代溴原子
C2H5—Br + H--OH C2H5—OH + HBr
△
NaOH + HBr == NaBr + H2O
总反应:
(以溴乙烷为例)
推广:所有卤代烃在碱性水溶液中都会发生水解反应
(1)在实验中加入过量稀硝酸的目的是什么?
①中和过量的NaOH溶液 ②检验生成的沉淀是否溶于稀HNO3
(3)检验卤代烃中的卤原子一般流程:
AgNO3溶液
NaOH溶液
水解
HNO3溶液
酸化
R-X
AgCl 白色沉淀
AgBr 浅黄色沉淀
AgI 黄色沉淀
该步骤必不可少
卤代烃的化学性质
1.取代反应(水解反应)
(以溴乙烷为例)
思考:
(2)若不加稀硝酸,直接滴加AgNO3(aq),将会看到什么现象?
过量的NaOH与AgNO3反应,产生黑褐色的Ag2O↓
NaOH+AgNO3 = AgOH↓+NaNO3
2AgOH = Ag2O↓ +H2O
【练习】请写出下列卤代烃水解的方程式:
思考:CH3CH2Br+NaCN(aq)反应的产物?
CH3 C CH2Br
CH3
CH3
Br
CH3CH CH2CH3
Br
①所有卤代烃在一定条件下都能发生水解。
②卤素原子直接与苯环相连的卤代芳香烃水解反应条件比较苛刻
R-X + NaOH R-OH + NaX
水
△
在卤代烃分子中,由于卤原子的吸电子作用,不仅使得α-C带部分正电荷,也使β-C带有更少量的正电荷,从而使β-H的活泼性增强,能在强碱的作用下,失去一分子卤化氢,生成烯烃,这就是卤代烃的消去反应。
C
C
Br
H
H
H
H
H
Br
δ+
δ-
δ++
现象:
高锰酸钾酸性溶液褪色
实验:
结论:
生成的气体分子中含有不饱和碳碳键
溴乙烷与NaOH的乙醇混合液
反应原理:
CH2—CH2 +NaOH CH2=CH2↑ +NaBr +H2O
Br
H
乙醇
△
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而形成不饱和键(双键或三键)的化合物的反应。。
消去反应:
2.消去反应(消除反应)
如果将溴乙烷与强碱(如NaOH或KOH)的乙醇溶液共热,溴乙烷可以从分子中脱去HBr,生成乙烯。
溴乙烷的消去反应(消除反应)
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
思考:下列卤代烃能否发生消去反应?
①CH3I
CH2Br
③
Br
CH3CH CHCH3
Br
⑤
Br
⑥
CH3 C CH2Br
CH3
CH3
②
CH3CHBr2
④
由此你能得出什么结论?
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
发生消去反应的条件:
①烃中碳原子数≥2
②连卤原子的相邻碳原子上有氢原子
1、反应条件:
+NaOH
— C— C—
H
X
醇
C=C
+NaX+H2O
HX+NaOH ===NaX +H2O
强碱的醇溶液、加热
2、物质结构条件:
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
思考:在溴乙烷与NaOH的醇溶液的反应中,如何检验气体产物
(1)分析反应产生的气体中可能含有哪些杂质?
(2)为什么要在气体通入酸性KMnO4溶液前
加一个盛有水的试管?
溴乙烷、乙醇、水蒸气
①水能除去挥发出来的乙醇,乙醇也能使酸性高锰酸钾溶液褪色,干扰乙烯的检验。
②产生的气体乙烯(含 等杂质气体)
(3)除酸性高锰酸钾溶液外还可以用什么来检验乙烯,此时气体还用先通入水中吗?理由是?
溴水或溴的四氯化碳溶液。
不用;乙醇与溴不反应,不会干扰乙烯的检验。
乙醇、溴乙烷、水蒸气
2.消去反应(消除反应)
反应类型 消去反应 水解(取代)反应
反应条件
卤代烃的 断键规律
结构特点
产物特征
归纳总结
卤代烃的消去反应与取代(水解)反应的比较
NaOH醇溶液、加热
NaOH水溶液、加热
与X相连的C的邻位C上有H原子
含C—X键即可
消去HX,引入碳碳双键或碳碳三键
在碳上引入—OH,生成含—OH的有机物(醇)
运用第一章所学的波谱方法检验取代产物1-丁醇
【实验探究P56】
生成醇
生成烯烃
CH3CH2CH2CH2Br
CH3CH2CH2CH2Br
CH3CH2CH2CH2OH、NaBr
CH3CH2CH=CH2、NaBr、H2O
+ 水
NaOH水溶液,加热
NaOH醇溶液,加热
1-溴丁烷和NaOH在不同条件下发生不同类型的反应
【实验探究P56】
还可以利用溴水、溴的CCl4溶液检验丁烯。
此时不需要先通入水中。
因受热而挥发的乙醇也能使高锰酸钾褪色,所以要先通过水除去乙醇,防止干扰实验。
乙醇与溴不反应,不会干扰乙烯的检验。
【实验探究P56】
2-丁烯
CH3-CH-CH2-CH3
Br
CH3-CH=CH-CH3
CH3-CH2-CH=CH2
(主产物)
1-丁烯
消去反应规则:当有多个产物时,以消H少的C原子上的H为主
“雪上加霜”
【实验探究P56】
卤代烯烃的某些化学性质与烯烃的相似,能发生加成反应和加聚反应。
聚氯乙烯和聚四氟乙烯都是用途广泛的高分子材料。
3、加成和加聚反应
特富龙(Teflon)是美国杜邦公司对其研发的所有碳氢树脂的总称,包括聚四氟乙烯、聚全氟乙丙烯及各种共聚物。由于其独特优异的耐热(180℃-260℃)、耐低温(-200℃)、自润滑性及化学稳定性能等,而被称为“拒腐蚀、永不粘的特富龙”。
聚四氟乙烯不粘锅
聚四氟乙烯,俗称塑料王,具有最佳的耐热性和耐化学性,显示了独特的不粘性和润滑性。
运动场上的“化学大夫”
氯乙烷
液态的氯乙烷汽化时大量吸热,具有冷冻麻醉作用,可在身体局部产生快速镇痛效果。因此,常用氯乙烷与其他药物制成“复方氯乙烷气雾剂”,用于运动中的急性损伤,如肌肉拉伤、关节扭伤等的镇痛。
【资料卡片】P55
聚氯乙烯
[ CH-CH2 ]n
Cl
生活中的卤代烃
生活中的保鲜膜
既可用于冰箱保鲜(-60℃),也可用于微波炉(+140℃)。
PVDC保鲜膜
聚偏二氯乙烯
PE保鲜膜
聚乙烯
PVC保鲜膜
聚氯乙烯
虽可用于食品包装,但在生产过程中需添加塑化剂。如在生产过程中添加了有毒塑化剂DEHA,则危害很大。
生活中的卤代烃
【科学-技术-社会】P57
卤代烃的功与过
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
氟氯烃——造成臭氧空洞的“罪魁祸首”
卤代烃的“功”:
1)作溶剂:CHCl3(氯仿);CCl4;CH2Cl2
2)农药: “六六六”, DDT
3)制冷剂:氟氯代烷(商品名氟利昂) CHClF2、CCl2F2(冰箱用)
4)灭火剂: CCl4灭火剂 (电器类起火)
5)麻醉剂: CHCl3、氯乙烷
6)塑料: 聚四氟乙烯 (塑料王)、聚氯乙烯(PVC)
【科学-技术-社会】P57
→危害:氟氯烃——造成臭氧空洞的“罪魁祸首”
→卤代烃破坏臭氧层原理(了解):氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为
卤代烃的“过”:
→实际上氯原子起了催化作用。
【科学-技术-社会】P57
作业多多
老是写错
找到帮手
身体不适
医院就医
明白事因
涂改液中含有二氯乙烷、三氯乙烷、四氯乙烷等有机氯化合物对眼睛有明显胡刺激作用,严重时会导恶心、呕吐、浑身不舒服等。
原来如此
课堂小结
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第一节 卤代烃
学习
目标
第1课时
卤代烃
PART
01
PART
02
通过从卤代烃的官能团及其转化角度认识卤代烃取代反应、消去反应的特点和规律,了解有机反应类型与有机化合物分子结构特点之间的关系。
掌握卤代烃在有机合成中的桥梁作用,培养“科学探究与社会责任”的核心素养
烃分子中的氢原子被不同官能团取代后,就能生成一系列新的不同类别的有机化
合物,如卤代烃、醇、酚、醛、羧酸和酯等。从结构角度看都可以看作是由烃衍生而
来的,所以被称为烃的衍生物。
烃的衍生物
CH3CH2Br
烃的衍生物具有与烃不同的性质,这些性质主要由其分子中的官能团
决定。
认识卤代烃
阅读教材54页,思考下列问题:
(1)什么是卤代烃?有哪些分类?
(2)第二章我们学习了烃,想想通过哪些反应可以将烃转化为卤代烃?
(3)卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
烃分子中的氢原子被卤素原子取代生成的化合物。一元卤代烃可表示为:R-X
1. 概念:
C X 碳卤键
元素组成:一定含C、X(H不一定)
官能团:
如CCl4
2. 分类
卤代烃分类
按卤素原
子数目分
单卤代烃
多卤代烃
按卤素原
子种类分
氟代烃
氯代烃
溴代烃
碘代烃
一卤代烃、多卤代烃
按卤素原子数目
饱和卤代烃、不饱和卤代烃
按烃基是否饱和
脂肪卤代烃、芳香卤代烃
按是否含有苯环
认识卤代烃
①甲烷和氯气
②苯与溴
③乙烯和溴
④乙炔和氯化氢
取代反应
取代反应
加成反应
加成反应
3.烃转化为卤代烃的途径
认识卤代烃
选主链
定编号
写名称
选择含官能团的最长碳链
将卤素原子看做取代基,编号时从距简单取代基近的一端编号,
有碳碳双键时从距离碳碳双键近的一端开始编号
从简入繁
4.卤代烃的命名
3-甲基-3-溴-1-丁烯
卤代烃如何命名?根据资料卡片,结合烃类物质的命名,请你总结出卤代烃的命名原则。
认识卤代烃
CH3CH2CH2CH2—Cl
CH3CH2CHCH3
Cl
—
CH3—C—CH3
Br
—
—
CH3
1-氯丁烷
2-氯丁烷
2-甲基-2-溴丙烷
3-甲基- 1,1-二溴戊烷
认识卤代烃
名称 结构简式 液态时密度/(g·cm-3) 沸点/℃
一氯甲烷 CH3Cl 0.916 -24
一氯乙烷 CH3CH2Cl 0.898 12
1-氯丙烷 CH3CH2CH2Cl 0.890 46
1-氯丁烷 CH3CH2CH2CH2Cl 0.886 78
1-氯戊烷 CH3CH2CH2CH2CH2Cl 0.882 108
以氯代烃的密度和沸点为例,同时结合烷烃的物理性质的变化规律,总结卤代烃的物理性质。
认识卤代烃
常温下除一氯甲烷、氯乙烷、氯乙烯等少数是气体外,
大多数为液体或固体。
除脂肪烃的一氟代物和一氯代物外,其余卤代烃密度都比水大。
一般随着烃基中碳原子数目的增加而减小。
卤代烃不溶于水,可溶于有机溶剂,某些卤代烃本身就是有机溶剂
熔沸点大于同碳个数的烃,随碳原子数增多,沸点依次升高(碳原子数相同时,支链越多沸点越低)。
状态
沸点
密度
溶解性
1.物理性质
阅读52页教材,并结合P30烷烃的物理性质,
分析表3-1,总结卤代烃的物理性质及其递变规律。
认识卤代烃
(1)卤代烃是一类特殊的烃。 ( )
提示:卤代烃含卤族元素,不是烃。
(2)卤代烃中一定含有的元素为C、H和卤素。( )
提示:卤代烃不一定含H元素,如CCl4。
(3)卤代烃不一定是由烃分子和卤素单质发生取代反应得到的。( )
提示:
卤代烃可以由烃分子发生加成反应得到,如乙烯与溴水发生加成反应得到1,2-二溴乙烷。
1.判断正误(对的在括号内打“√”,错的在括号内打“×”。)
√
×
×
认识卤代烃
2.溴乙烷中混有杂质乙醇,除去乙醇的方法是( )
A.加热蒸发 B.过滤 C.加水、萃取、分液 D.加苯、萃取、分液
解析:溴乙烷难溶于水,而乙醇可与水以任意比例互溶,故可向混合液中加水进行萃取,然后分液即可除去乙醇。
C
3.下列关于卤代烃的叙述中正确的是 ( )
A.所有卤代烃都是难溶于水,密度比水小的液体
B.所有卤代烃的沸点比相应烃的沸点低
C.CH3CH2Cl与CH3CH2CH2Cl的沸点前者低
D.CH3CH2Cl与CH3CH2CH2Cl的密度前者小
解析:A项,卤代烃的密度比水的大,错;B项,卤代烃的沸点比相应烃的高,错;D项,前者大,错。
C
认识卤代烃
C2H5Br
CH3CH2Br 或 C2H5Br
分子式:
结构式:
结构简式:
官能团:
C—Br
核磁共振氢谱图
(碳溴键)
球棍模型
空间填充模型
电子式:
有2种化学环境的H原子,则核磁共振有2组峰,强度比为3:2
【以溴乙烷为例】学习卤代烃的性质:
1、溴乙烷的组成和结构
认识卤代烃
颜 色:
状 态:
密 度:
溶解性:
沸 点:
无色透明
油状液体
比水大
不溶于水,
易溶于有机溶剂
沸点38.4℃
易挥发
2. C2H5Br物理性质
对 比
无色
气体
-88.6 ℃
不溶于水
CH3CH3
比水小
>
卤代烃的熔沸点大于同C原子数的烃!
【以溴乙烷为例】学习卤代烃的性质:
认识卤代烃
分析卤代烃的结构特点,推测卤代烃具有怎样的化学性质。
卤代烃中卤素原子吸引电子能力较强,共用电子对偏向卤素原子,使C—X键具有较强的极性,所以卤代烃具有较强的反应活性,易发生取代反应和消去反应。
碳卤键
官能团:
X
C
δ—
δ+
例:溴乙烷和乙烷的结构相似,区别在于C-H键与C-Br键的不同。C-Br键为极性键,由于溴原子吸引电子能力强,C-Br键易断裂,使溴原子易被取代。
【思考】
提出问题1:
对CH3CH2Br化学性质的探索
溴乙烷CH3CH2Br 在水中能否电离出Br-?
它是否为电解质?请设计实验证明。
实验:
溴乙烷
HNO3酸化后的AgNO3溶液
无明显变化
溴乙烷不是电解质,不能电离出Br-。
提出问题2:CH3CH3+水→不反应, CH3CH2Br+H2O →
科学猜测:若反应,可能有 产生。
怎样证明有Br-产生?
资料卡片:
C2H5Br与水的反应要在碱性环境下才容易进行
Br-
实验装置
实验现象 ①中溶液_____ ;②中有机层厚度减小;④中有 生成
实验解释 溴乙烷与NaOH溶液共热产生了______
分层
淡黄色沉淀
Br-
溴乙烷与NaOH溶液共热的化学方程式为______________________________________。反应类型为 。
取代反应
CH3CH2Br+NaOH CH3CH2OH+NaBr
1.取代反应
【实验3-1】课文P55
(以溴乙烷为例)
卤代烃的化学性质
CH3CH2—Br + Na—OH CH3CH2—OH + NaBr
H2O
从平衡移动的角度看,NaOH不断中和氢溴酸,促进溴乙烷的水解;加热的目的是提高反应速率,且水解是吸热反应,升高温度也有利于平衡右移。水相当于是催化剂
卤代烃的化学性质
1.取代反应(水解反应)
反应条件:
NaOH水溶液、加热
反应原理:
羟基取代溴原子
C2H5—Br + H--OH C2H5—OH + HBr
△
NaOH + HBr == NaBr + H2O
总反应:
(以溴乙烷为例)
推广:所有卤代烃在碱性水溶液中都会发生水解反应
(1)在实验中加入过量稀硝酸的目的是什么?
①中和过量的NaOH溶液 ②检验生成的沉淀是否溶于稀HNO3
(3)检验卤代烃中的卤原子一般流程:
AgNO3溶液
NaOH溶液
水解
HNO3溶液
酸化
R-X
AgCl 白色沉淀
AgBr 浅黄色沉淀
AgI 黄色沉淀
该步骤必不可少
卤代烃的化学性质
1.取代反应(水解反应)
(以溴乙烷为例)
思考:
(2)若不加稀硝酸,直接滴加AgNO3(aq),将会看到什么现象?
过量的NaOH与AgNO3反应,产生黑褐色的Ag2O↓
NaOH+AgNO3 = AgOH↓+NaNO3
2AgOH = Ag2O↓ +H2O
【练习】请写出下列卤代烃水解的方程式:
思考:CH3CH2Br+NaCN(aq)反应的产物?
CH3 C CH2Br
CH3
CH3
Br
CH3CH CH2CH3
Br
①所有卤代烃在一定条件下都能发生水解。
②卤素原子直接与苯环相连的卤代芳香烃水解反应条件比较苛刻
R-X + NaOH R-OH + NaX
水
△
在卤代烃分子中,由于卤原子的吸电子作用,不仅使得α-C带部分正电荷,也使β-C带有更少量的正电荷,从而使β-H的活泼性增强,能在强碱的作用下,失去一分子卤化氢,生成烯烃,这就是卤代烃的消去反应。
C
C
Br
H
H
H
H
H
Br
δ+
δ-
δ++
现象:
高锰酸钾酸性溶液褪色
实验:
结论:
生成的气体分子中含有不饱和碳碳键
溴乙烷与NaOH的乙醇混合液
反应原理:
CH2—CH2 +NaOH CH2=CH2↑ +NaBr +H2O
Br
H
乙醇
△
有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而形成不饱和键(双键或三键)的化合物的反应。。
消去反应:
2.消去反应(消除反应)
如果将溴乙烷与强碱(如NaOH或KOH)的乙醇溶液共热,溴乙烷可以从分子中脱去HBr,生成乙烯。
溴乙烷的消去反应(消除反应)
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
思考:下列卤代烃能否发生消去反应?
①CH3I
CH2Br
③
Br
CH3CH CHCH3
Br
⑤
Br
⑥
CH3 C CH2Br
CH3
CH3
②
CH3CHBr2
④
由此你能得出什么结论?
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
发生消去反应的条件:
①烃中碳原子数≥2
②连卤原子的相邻碳原子上有氢原子
1、反应条件:
+NaOH
— C— C—
H
X
醇
C=C
+NaX+H2O
HX+NaOH ===NaX +H2O
强碱的醇溶液、加热
2、物质结构条件:
卤代烃的化学性质
(以溴乙烷为例)
2.消去反应(消除反应)
思考:在溴乙烷与NaOH的醇溶液的反应中,如何检验气体产物
(1)分析反应产生的气体中可能含有哪些杂质?
(2)为什么要在气体通入酸性KMnO4溶液前
加一个盛有水的试管?
溴乙烷、乙醇、水蒸气
①水能除去挥发出来的乙醇,乙醇也能使酸性高锰酸钾溶液褪色,干扰乙烯的检验。
②产生的气体乙烯(含 等杂质气体)
(3)除酸性高锰酸钾溶液外还可以用什么来检验乙烯,此时气体还用先通入水中吗?理由是?
溴水或溴的四氯化碳溶液。
不用;乙醇与溴不反应,不会干扰乙烯的检验。
乙醇、溴乙烷、水蒸气
2.消去反应(消除反应)
反应类型 消去反应 水解(取代)反应
反应条件
卤代烃的 断键规律
结构特点
产物特征
归纳总结
卤代烃的消去反应与取代(水解)反应的比较
NaOH醇溶液、加热
NaOH水溶液、加热
与X相连的C的邻位C上有H原子
含C—X键即可
消去HX,引入碳碳双键或碳碳三键
在碳上引入—OH,生成含—OH的有机物(醇)
运用第一章所学的波谱方法检验取代产物1-丁醇
【实验探究P56】
生成醇
生成烯烃
CH3CH2CH2CH2Br
CH3CH2CH2CH2Br
CH3CH2CH2CH2OH、NaBr
CH3CH2CH=CH2、NaBr、H2O
+ 水
NaOH水溶液,加热
NaOH醇溶液,加热
1-溴丁烷和NaOH在不同条件下发生不同类型的反应
【实验探究P56】
还可以利用溴水、溴的CCl4溶液检验丁烯。
此时不需要先通入水中。
因受热而挥发的乙醇也能使高锰酸钾褪色,所以要先通过水除去乙醇,防止干扰实验。
乙醇与溴不反应,不会干扰乙烯的检验。
【实验探究P56】
2-丁烯
CH3-CH-CH2-CH3
Br
CH3-CH=CH-CH3
CH3-CH2-CH=CH2
(主产物)
1-丁烯
消去反应规则:当有多个产物时,以消H少的C原子上的H为主
“雪上加霜”
【实验探究P56】
卤代烯烃的某些化学性质与烯烃的相似,能发生加成反应和加聚反应。
聚氯乙烯和聚四氟乙烯都是用途广泛的高分子材料。
3、加成和加聚反应
特富龙(Teflon)是美国杜邦公司对其研发的所有碳氢树脂的总称,包括聚四氟乙烯、聚全氟乙丙烯及各种共聚物。由于其独特优异的耐热(180℃-260℃)、耐低温(-200℃)、自润滑性及化学稳定性能等,而被称为“拒腐蚀、永不粘的特富龙”。
聚四氟乙烯不粘锅
聚四氟乙烯,俗称塑料王,具有最佳的耐热性和耐化学性,显示了独特的不粘性和润滑性。
运动场上的“化学大夫”
氯乙烷
液态的氯乙烷汽化时大量吸热,具有冷冻麻醉作用,可在身体局部产生快速镇痛效果。因此,常用氯乙烷与其他药物制成“复方氯乙烷气雾剂”,用于运动中的急性损伤,如肌肉拉伤、关节扭伤等的镇痛。
【资料卡片】P55
聚氯乙烯
[ CH-CH2 ]n
Cl
生活中的卤代烃
生活中的保鲜膜
既可用于冰箱保鲜(-60℃),也可用于微波炉(+140℃)。
PVDC保鲜膜
聚偏二氯乙烯
PE保鲜膜
聚乙烯
PVC保鲜膜
聚氯乙烯
虽可用于食品包装,但在生产过程中需添加塑化剂。如在生产过程中添加了有毒塑化剂DEHA,则危害很大。
生活中的卤代烃
【科学-技术-社会】P57
卤代烃的功与过
溶剂
卤代烃
致冷剂
医用
灭火剂
麻醉剂
农药
氟氯烃——造成臭氧空洞的“罪魁祸首”
卤代烃的“功”:
1)作溶剂:CHCl3(氯仿);CCl4;CH2Cl2
2)农药: “六六六”, DDT
3)制冷剂:氟氯代烷(商品名氟利昂) CHClF2、CCl2F2(冰箱用)
4)灭火剂: CCl4灭火剂 (电器类起火)
5)麻醉剂: CHCl3、氯乙烷
6)塑料: 聚四氟乙烯 (塑料王)、聚氯乙烯(PVC)
【科学-技术-社会】P57
→危害:氟氯烃——造成臭氧空洞的“罪魁祸首”
→卤代烃破坏臭氧层原理(了解):氟利昂可在强烈的紫外线作用下分解,产生的氯原子自由基会对臭氧层产生长久的破坏作用。以CCl3F为例,它破坏臭氧层的反应过程可表示为
卤代烃的“过”:
→实际上氯原子起了催化作用。
【科学-技术-社会】P57
作业多多
老是写错
找到帮手
身体不适
医院就医
明白事因
涂改液中含有二氯乙烷、三氯乙烷、四氯乙烷等有机氯化合物对眼睛有明显胡刺激作用,严重时会导恶心、呕吐、浑身不舒服等。
原来如此
课堂小结
