化学人教版(2019)必修第二册7.3.1乙醇(共24张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.1乙醇(共24张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 24.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-07 16:05:00 | ||
图片预览






文档简介
(共24张PPT)
第三节 乙醇与乙酸
(第1课时 乙醇)
化妆品
啤酒
酒文化博大精深,源远流长,早在几千年前,人类就掌握了发酵法酿酒的技术,酒精在生活中也很常见。
白酒
消毒液
含酒精:3% - 5%
含酒精:75%
含酒精:38% - 65%
你在生活中还有那些地方用到了酒精,体现了乙醇哪些物理性质?
(以上均为体积分数)
洗手液:做溶剂、杀菌
酒精的作用
去除油渍、油漆
中药材里的药引子
酒精的作用
75%的医用酒精可外科消毒
物理降温
(幼儿慎用)
基本有机化工原料:乙醇可用来制取乙醛、乙醚、乙酸乙酯、乙胺等化工原料,也是制取染料、涂料、洗涤剂等产品的原料。
酒精的作用
乙醇汽油:90%的普通汽油+10%的燃料乙醇
它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
乙醇(俗称酒精)
颜色:
状态:
气味:
沸点:
密度:
溶解度:
一、乙醇的物理性质
无色透明
特殊香味
液体
比水小 20℃时,密度是0.7893g/ml
跟水以任意比互溶,能够溶解多种有机物,
是重要的有机溶剂。
78.5℃(易挥发)
?
分子式:
结构式:
结构简式:
二、乙醇的分子结构
1、乙醇的分子结构
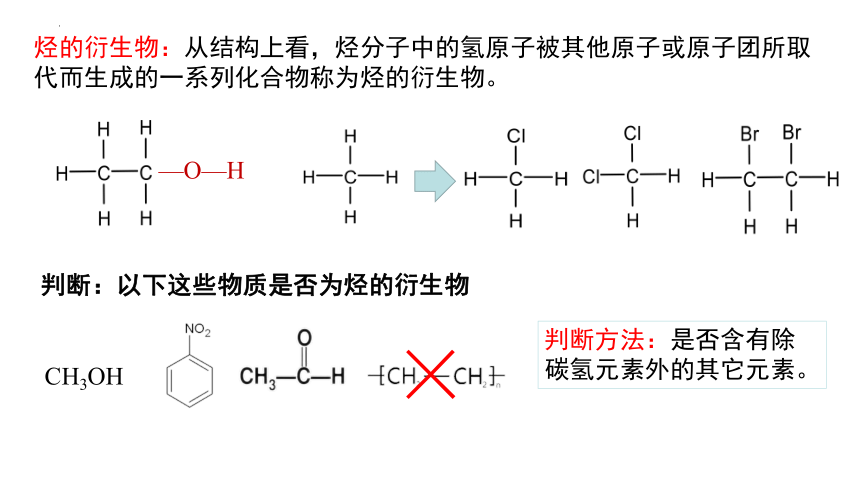
烃的衍生物:从结构上看,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
判断:以下这些物质是否为烃的衍生物
判断方法:是否含有除碳氢元素外的其它元素。
—O—H
CH3OH
×
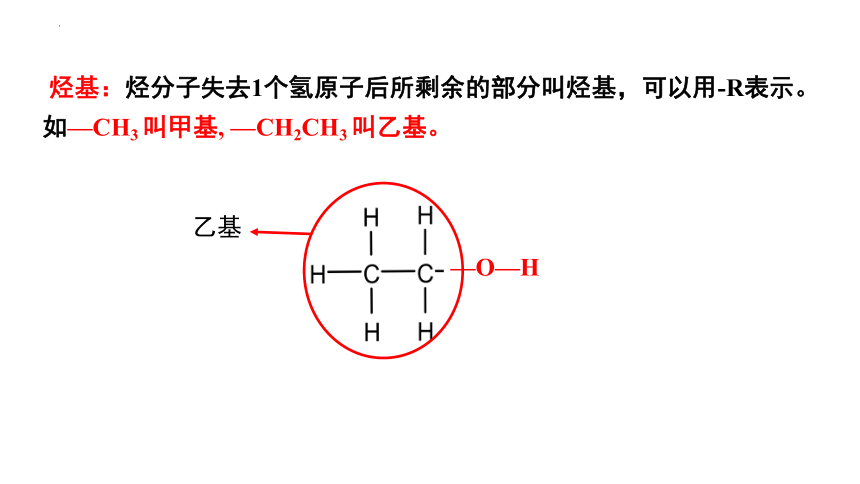
乙基
烃基:烃分子失去1个氢原子后所剩余的部分叫烃基,可以用-R表示。如—CH3 叫甲基, —CH2CH3 叫乙基。
—O—H
实验现象 实验结论
点燃生成的气体,产生淡蓝色火焰,烧杯内壁有水雾,澄清石灰水不变浑浊。
钠表面有气泡产生,随后逐渐浮到水面上,慢慢消失
钠先沉入液体底部
钠的密度比乙醇的大
反应缓慢,产生气体
有氢气生成
实验7-4:乙醇与钠反应
乙醇与钠反应过程中,哪里发生了断键?
回顾所学知识:①钠能保存在煤油中(煤油是主要成分为C10-C16烷烃,主要含C-H)
②钠与H2O反应
序号 钠与水 反应的现象 钠与乙醇 反应的现象 结论
1 浮 沉 ρ乙醇<ρ水
2 熔化成小球 剧烈,四处游动 块状,未熔化 氢原子活泼性:
水分子>乙醇的羟基
三、乙醇的化学性质
1、与活泼金属(如Na)反应
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
H H
│ │
H─ C ─ C─ O─ H
│ │
H H
乙醇钠
思考:根据钠与乙醇、水反应的现象,比较氧氢键中氢的活泼性。
钠与水反应比钠与乙醇反应更剧烈。所以乙醇氧氢键中的氢原子不如水分子中的氢原子活泼
官能团:决定有机化合物的化学特性的原子或原子团
碳碳双键
碳碳三键
H—C≡C—H
羟基,写作-OH
氧 氢
羟 qiǎng
—O—H
羟基与氢氧根离子的比较
羟基 氢氧根离子
电子式
电子数
电性
稳定程度
存在
O:H
: :
·
:O:H
: :
[ ]
9e 10e
不显电性
显电性
不稳定
较稳定
不能单独存在,必须与其他基团结合在一起
能独立存在
2. 氧化反应
(1)乙醇的燃烧
点燃
CH3CH2OH + 3O2 2CO2 + 3H2O
产物检验:点燃酒精灯,将一个干燥烧杯罩在火焰上,烧杯内壁有水珠,燃烧产物有水。将一个用澄清石灰水润湿内壁的烧杯罩在火焰上,内壁附着的石灰水变浑浊,说明有二氧化碳生成。
写出乙醇燃烧的化学方程式,如何检验燃烧产物?
固态酒精
三、乙醇的化学性质
焊接银器、铜器时,表面会生成发黑的氧化膜,如果马上蘸一下酒精,铜银会光亮如初!这是何原理?
操作 现象 转化
将下端绕成螺旋状的铜丝在酒精灯上灼烧
将表面变黑的铜丝灼热后立即插入盛有无水乙醇的试管中,反复操作几次
铜丝由红色变为黑色
乙醇沸腾,铜丝表面恢复红亮,闻到刺激性气味
2. 氧化反应
Cu→CuO
CuO→Cu
CH3CH2OH→CH3CHO
乙醛
活动:在纸上画出结构式,表示乙醇催化氧化的过程,说说反应中哪些化学键发生了变化
羟基与其直接相连的碳原子变成碳氧双键
(2)乙醇的催化氧化
2Cu+O2 = 2CuO
2 2 2 2 2
CuO + CH3CH2OH Cu + CH3CHO + H2O
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
H C C H
H
O H
H
H
H C C H
O
H
H
2 +O2 2 +2H2O
Cu
氧化反应:有机物“去氢”或“得氧”的反应
还原反应:有机物“得氧”或“去氢”的反应
(3)乙醇被强氧化剂氧化
酸性高锰酸钾溶液
酸性重铬酸钾溶液
CH3CH2OH
CH3COOH
K2Cr2O7(橙黄色)
Cr2(SO4)3(蓝绿色)
C2H5OH
C2H5OH CH3CHO CH3COOH
[O]
[O]
强氧化剂
生活解密:乙醇在人体内究竟发生了哪些化学变化 喝酒上脸的人真能喝吗?“喝酒脸红不伤肝,喝酒脸白才伤肝”是真的吗?为何女性更容易喝醉?究竟谁才是真正的酒神?
乙醇
乙醛
乙酸
乙醇脱氢酶
CO2+H2O
乙醛脱氢酶
(ALDH)
人饮酒后大部分在肝内氧化分解。乙醇先经醇脱氢酶的氧化,被氧化为乙醛,然后在醛脱氢酶的作用下氧化为乙酸,参加体内正常的乙酸代谢,最后生成CO2和H2O,释放出能量。乙醛氧化为乙酸的速度较快,因此在一般饮酒量不多的情况下,乙醛不致于在体内积蓄,但如果大量饮酒,即可发生乙醛积蓄,乙醛的毒性是乙醇的三十倍以上,肝细胞内乙醛浓度增加会导致肝脏受损伤,所以常喝酒会伤肝,也会给人带来其他疾病。
四、乙醇的用途
③用作酒精灯、火锅、内燃机等的燃料
④用作重要的有机化工原料和溶剂
②医疗上常用体积分数为75%的乙醇溶液作消毒剂
①用于生产饮品
二、乙醇的分子结构
一、乙醇的物理性质
三、乙醇的化学性质
1.与活泼金属(K、Ca、Na)反应
2.氧化反应(燃烧、催化氧化、与强氧化剂)
乙醇
四、乙醇的用途
H H
│ │
H─ C ─ C─ O─ H
│ │
H H
第三节 乙醇与乙酸
(第1课时 乙醇)
化妆品
啤酒
酒文化博大精深,源远流长,早在几千年前,人类就掌握了发酵法酿酒的技术,酒精在生活中也很常见。
白酒
消毒液
含酒精:3% - 5%
含酒精:75%
含酒精:38% - 65%
你在生活中还有那些地方用到了酒精,体现了乙醇哪些物理性质?
(以上均为体积分数)
洗手液:做溶剂、杀菌
酒精的作用
去除油渍、油漆
中药材里的药引子
酒精的作用
75%的医用酒精可外科消毒
物理降温
(幼儿慎用)
基本有机化工原料:乙醇可用来制取乙醛、乙醚、乙酸乙酯、乙胺等化工原料,也是制取染料、涂料、洗涤剂等产品的原料。
酒精的作用
乙醇汽油:90%的普通汽油+10%的燃料乙醇
它可以改善油品的性能和质量,降低一氧化碳、碳氢化合物等主要污染物排放。
乙醇(俗称酒精)
颜色:
状态:
气味:
沸点:
密度:
溶解度:
一、乙醇的物理性质
无色透明
特殊香味
液体
比水小 20℃时,密度是0.7893g/ml
跟水以任意比互溶,能够溶解多种有机物,
是重要的有机溶剂。
78.5℃(易挥发)
?
分子式:
结构式:
结构简式:
二、乙醇的分子结构
1、乙醇的分子结构
烃的衍生物:从结构上看,烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。
判断:以下这些物质是否为烃的衍生物
判断方法:是否含有除碳氢元素外的其它元素。
—O—H
CH3OH
×
乙基
烃基:烃分子失去1个氢原子后所剩余的部分叫烃基,可以用-R表示。如—CH3 叫甲基, —CH2CH3 叫乙基。
—O—H
实验现象 实验结论
点燃生成的气体,产生淡蓝色火焰,烧杯内壁有水雾,澄清石灰水不变浑浊。
钠表面有气泡产生,随后逐渐浮到水面上,慢慢消失
钠先沉入液体底部
钠的密度比乙醇的大
反应缓慢,产生气体
有氢气生成
实验7-4:乙醇与钠反应
乙醇与钠反应过程中,哪里发生了断键?
回顾所学知识:①钠能保存在煤油中(煤油是主要成分为C10-C16烷烃,主要含C-H)
②钠与H2O反应
序号 钠与水 反应的现象 钠与乙醇 反应的现象 结论
1 浮 沉 ρ乙醇<ρ水
2 熔化成小球 剧烈,四处游动 块状,未熔化 氢原子活泼性:
水分子>乙醇的羟基
三、乙醇的化学性质
1、与活泼金属(如Na)反应
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
H H
│ │
H─ C ─ C─ O─ H
│ │
H H
乙醇钠
思考:根据钠与乙醇、水反应的现象,比较氧氢键中氢的活泼性。
钠与水反应比钠与乙醇反应更剧烈。所以乙醇氧氢键中的氢原子不如水分子中的氢原子活泼
官能团:决定有机化合物的化学特性的原子或原子团
碳碳双键
碳碳三键
H—C≡C—H
羟基,写作-OH
氧 氢
羟 qiǎng
—O—H
羟基与氢氧根离子的比较
羟基 氢氧根离子
电子式
电子数
电性
稳定程度
存在
O:H
: :
·
:O:H
: :
[ ]
9e 10e
不显电性
显电性
不稳定
较稳定
不能单独存在,必须与其他基团结合在一起
能独立存在
2. 氧化反应
(1)乙醇的燃烧
点燃
CH3CH2OH + 3O2 2CO2 + 3H2O
产物检验:点燃酒精灯,将一个干燥烧杯罩在火焰上,烧杯内壁有水珠,燃烧产物有水。将一个用澄清石灰水润湿内壁的烧杯罩在火焰上,内壁附着的石灰水变浑浊,说明有二氧化碳生成。
写出乙醇燃烧的化学方程式,如何检验燃烧产物?
固态酒精
三、乙醇的化学性质
焊接银器、铜器时,表面会生成发黑的氧化膜,如果马上蘸一下酒精,铜银会光亮如初!这是何原理?
操作 现象 转化
将下端绕成螺旋状的铜丝在酒精灯上灼烧
将表面变黑的铜丝灼热后立即插入盛有无水乙醇的试管中,反复操作几次
铜丝由红色变为黑色
乙醇沸腾,铜丝表面恢复红亮,闻到刺激性气味
2. 氧化反应
Cu→CuO
CuO→Cu
CH3CH2OH→CH3CHO
乙醛
活动:在纸上画出结构式,表示乙醇催化氧化的过程,说说反应中哪些化学键发生了变化
羟基与其直接相连的碳原子变成碳氧双键
(2)乙醇的催化氧化
2Cu+O2 = 2CuO
2 2 2 2 2
CuO + CH3CH2OH Cu + CH3CHO + H2O
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
H C C H
H
O H
H
H
H C C H
O
H
H
2 +O2 2 +2H2O
Cu
氧化反应:有机物“去氢”或“得氧”的反应
还原反应:有机物“得氧”或“去氢”的反应
(3)乙醇被强氧化剂氧化
酸性高锰酸钾溶液
酸性重铬酸钾溶液
CH3CH2OH
CH3COOH
K2Cr2O7(橙黄色)
Cr2(SO4)3(蓝绿色)
C2H5OH
C2H5OH CH3CHO CH3COOH
[O]
[O]
强氧化剂
生活解密:乙醇在人体内究竟发生了哪些化学变化 喝酒上脸的人真能喝吗?“喝酒脸红不伤肝,喝酒脸白才伤肝”是真的吗?为何女性更容易喝醉?究竟谁才是真正的酒神?
乙醇
乙醛
乙酸
乙醇脱氢酶
CO2+H2O
乙醛脱氢酶
(ALDH)
人饮酒后大部分在肝内氧化分解。乙醇先经醇脱氢酶的氧化,被氧化为乙醛,然后在醛脱氢酶的作用下氧化为乙酸,参加体内正常的乙酸代谢,最后生成CO2和H2O,释放出能量。乙醛氧化为乙酸的速度较快,因此在一般饮酒量不多的情况下,乙醛不致于在体内积蓄,但如果大量饮酒,即可发生乙醛积蓄,乙醛的毒性是乙醇的三十倍以上,肝细胞内乙醛浓度增加会导致肝脏受损伤,所以常喝酒会伤肝,也会给人带来其他疾病。
四、乙醇的用途
③用作酒精灯、火锅、内燃机等的燃料
④用作重要的有机化工原料和溶剂
②医疗上常用体积分数为75%的乙醇溶液作消毒剂
①用于生产饮品
二、乙醇的分子结构
一、乙醇的物理性质
三、乙醇的化学性质
1.与活泼金属(K、Ca、Na)反应
2.氧化反应(燃烧、催化氧化、与强氧化剂)
乙醇
四、乙醇的用途
H H
│ │
H─ C ─ C─ O─ H
│ │
H H
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
