专题7 第3单元 含氮化合物的合理使用 课件(共39张PPT) 2022-2023学年高一下学期化学苏教版(2019)必修第二册
文档属性
| 名称 | 专题7 第3单元 含氮化合物的合理使用 课件(共39张PPT) 2022-2023学年高一下学期化学苏教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-08 15:05:01 | ||
图片预览










文档简介
(共39张PPT)
专题7
氮与社会可持续发展
第三单元 含氮化合物的合理使用
学 习 目 标
活 动 方 案
阅读教材,什么是铵盐?大多数铵盐有什么共同的物理性质?
【答案】 通常把由铵根离子与酸根离子形成的离子化合物称为铵盐。
铵盐大多为无色、易溶于水的晶体。
活动一:学习铵盐的物理性质
1. 靠近NH4HCO3,闻到什么气味?为什么?
【答案】 闻到刺激性气味,说明碳酸氢铵发生分解反应生成了具有刺激性气味的气体。
活动二:探究铵盐的化学性质
2. 实验探究铵盐的性质。
【实验1】 取少量氯化铵和碳酸氢铵,分别放入两支试管中,在酒精灯火焰上微热,观察发生的现象。
【实验2】 将少量氯化铵与少量氢氧化钙混合后放入试管中,在酒精灯火焰上微热,用湿润的红色石蕊试纸检验反应产生的气体。
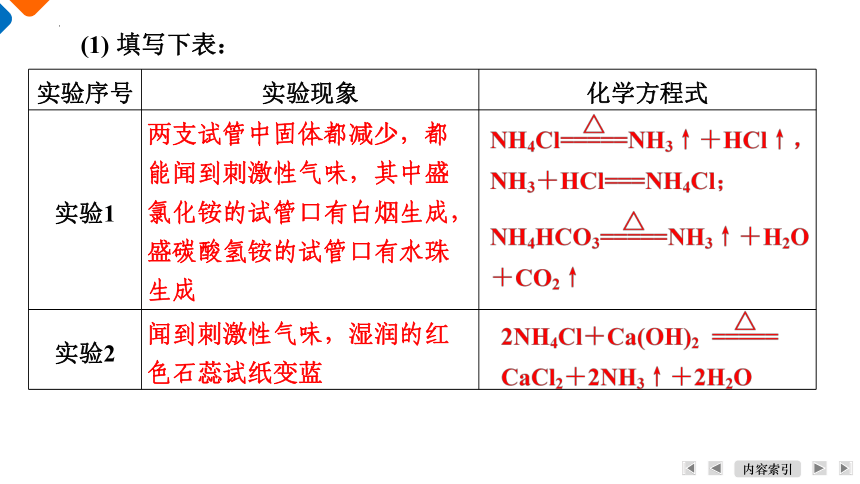
(1) 填写下表:
实验序号 实验现象 化学方程式
实验1
实验2
两支试管中固体都减少,都能闻到刺激性气味,其中盛氯化铵的试管口有白烟生成,盛碳酸氢铵的试管口有水珠生成
闻到刺激性气味,湿润的红色石蕊试纸变蓝
(2) 怎样检验铵盐中含有的铵根离子?
【答案】 滴加浓碱溶液,加热,用湿润的红色石蕊试纸检验生成的气体,若试纸变蓝,说明生成氨气,原物质中含有铵根离子。
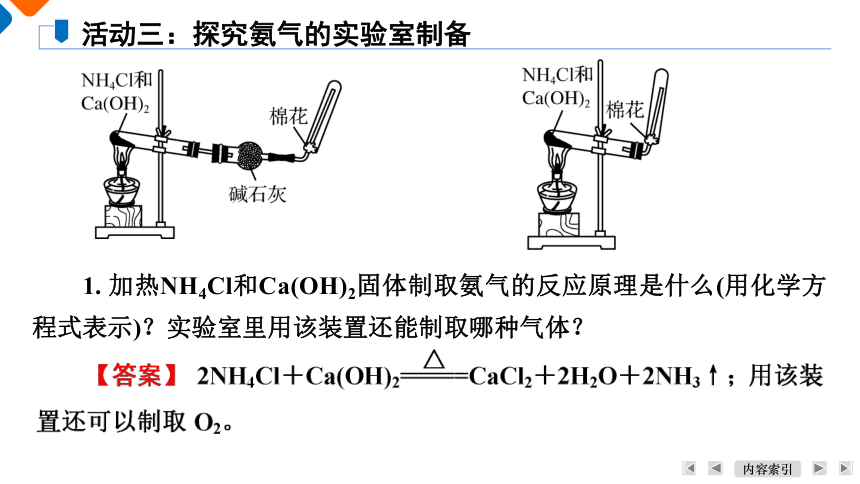
1. 加热NH4Cl和Ca(OH)2固体制取氨气的反应原理是什么(用化学方程式表示)?实验室里用该装置还能制取哪种气体?
活动三:探究氨气的实验室制备
2. 干燥管中的碱石灰是干燥氨的,能用无水CaCl2、P2O5代替碱石灰作干燥剂吗?
【答案】 不能,CaCl2能和NH3发生反应生成CaCl2·8NH3,P2O5为酸性干燥剂,也能和NH3反应。
3. 用什么方法收集氨气?怎样吸收尾气?
【答案】 用向下排空气法收集,尾气可用水吸收(注意防倒吸)。
4. 在制取氨的实验装置中,使用棉花的作用是什么?
【答案】 若为干燥的棉花,则起到减缓氨与空气对流的作用;若为蘸有水或稀硫酸的棉花,则还可以吸收多余的NH3。
5. 如何检验氨气已经收集满?
【答案】 把湿润的红色石蕊试纸置于试管口,试纸变蓝色;或将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生。
6. 直接加热分解氯化铵,然后用碱石灰吸收HCl能否得到氨气?
【答案】 不能,因为生成的氨气和氯化氢在常温下化合又生成氯化铵。
7. 氨是化学实验室常需制取的气体。实验室也可以用下面的两种方法快速制备NH3。
方法一:加热浓氨水。
方法二:将浓氨水滴入生石灰(或碱石灰)固体中。
(1) 请写出上述两种方法中发生反应的化学方程式:_____________ _____________________________________________________________________________________________。
方法一:
(2) 根据上述原理,该小组欲用下列装置制取氨气,方法一应选择______(填字母,下同),方法二应选择______。
D
C
(3) 下图是该小组设计收集氨气的几种装置,其中可行的是______,集气的原理是___________________________________________________ ____________。
d
NH3的密度小于空气,采用短管进氨气,长管出空气的
方法收集
1. 氮肥主要包括哪几种?
【答案】 氮肥主要有铵态氮肥、硝态氮肥和尿素。
2. 铵态氮肥使用时要注意什么?
【答案】 低温保存,深施盖土,避免受热;不可以跟碱性物质(如草木灰等)混合使用。
活动四:常用氮肥及其使用
3. 为什么硝态氮肥易被植物吸收?什么情况下会导致硝态氮肥损失?
4. 请根据氮肥的特性回答问题。
(1) 为什么硝态氮肥不宜在高温天气、多雨的水田区施用,而多用于冷凉的旱地?
【答案】 高温天气,硝态氮肥高温下易分解变质,多雨的水田地区易流失,所以硝态氮肥多用于冷凉的旱地。
(2) 为什么适应在pH较高的碱性土壤中生长的植物优先使用硝态氮肥,而适应在酸性土壤中生长的植物优先使用铵态氮肥?
【答案】 pH较高的碱性土壤使用硝态氮肥,不会因硝酸挥发而使氮肥损失,所以可优先使用硝态氮肥,若使用铵态氮肥,则会生成氨气使氮肥损失;而pH较低的酸性土壤应优先使用铵态氮肥,若使用硝态氮肥,则会因硝酸挥发而导致肥效降低。
5. 为什么尿素是使用量最大的一种氮肥?
【答案】 尿素是一种中性肥料,适用于各种土壤和作物。施用尿素后,土壤中的微生物将其吸收,使其水解成碳酸铵或碳酸氢铵,缓慢释放氨气被作物吸收利用。因此,通常在作物需肥期前4~8天施用。由于尿素肥效高、易保存、使用方便,长期使用对土壤的破坏作用小,所以它是目前使用量最大的一种氮肥。
6. 长期使用化肥会引起哪些环境问题?
【答案】 长期使用化肥的土壤容易酸化、板结。雨水冲刷使肥料离开土壤,进入溪水、河水和湖泊。水中的肥料会使细菌和藻类迅速生长,并消耗水中的氧气,严重时导致水中含氧量减少,许多水生生物随之死亡、腐烂,水质下降。
1943年,美国洛杉矶市发生严重的光化学烟雾事件,持续数十天之久,这种烟雾使人眼睛发红、咽喉疼痛、呼吸憋闷、头昏、头痛,不少老人因呼吸衰竭而死亡。光化学烟雾还使远离城市100 km 以外的高山上的大片松林枯死,柑橘减产。之后世界上的许多地区,如日本的东京、英国的伦敦,加拿大、澳大利亚、荷兰等国的大城市,以及我国的某些地区也曾出现过光化学烟雾。
1. 氮氧化物污染的来源有哪些?
【答案】 化石燃料的燃烧、硝酸生产等产生的工业废气处理不当和日益增多的机动车辆尾气排放,使得大量氮氧化物排放到空气中,给空气带来了一定程度的污染。
活动五:氮氧化物的无害化处理
2. 氮的氧化物NO2有哪些危害?光化学烟雾是怎样形成的?
【答案】 NO2不但会形成酸雨,在日光照射下,二氧化氮还能使氧气经过复杂的反应生成臭氧(O3)。臭氧与空气中的氮氧化物和一些碳氢化合物在紫外线的照射下发生作用后,产生了一种有毒的烟雾,人们称它为光化学烟雾。光化学烟雾具有特殊气味,刺激眼睛,对人体健康、植物生长等都有很大的危害。
3. 为了预防和控制氮氧化物的污染,人们给汽车安装了净化处理装置。净化装置中含有钯(Pd)等金属元素催化剂,尾气通过净化装置后,有害气体NO、CO转化为无害气体,写出该反应的化学方程式。
课 堂 反 馈
2
4
5
1
3
7
6
8
1. 下列关于铵盐的叙述正确的是( )
①铵盐是易溶于水的晶体 ②铵盐中的氮元素均为-3价 ③铵盐受热易分解 ④铵盐只能跟碱反应 ⑤铵态氮肥不宜跟草木灰混合施用 ⑥铵盐都能与酸反应
A. ①②③④⑤ B. ①③⑤
C. ③④⑤ D. ①③④⑤⑥
2
4
5
1
3
7
6
8
【解析】 ①铵盐均为无色或白色晶体,都易溶于水,正确;②硝酸铵中的氮元素为-3价和+5价,错误;③铵盐不稳定,所有铵盐受热均易分解,正确;④铵盐能跟碱反应生成氨气,碳酸铵能与酸反应,错误;⑤铵态氮肥不应跟碱性物质(如草木灰)混合使用,铵盐遇碱生成氨气,降低肥效,正确;⑥氯化铵与盐酸不反应,错误。
【答案】 B
2
4
5
1
3
7
6
8
2. (2022·南通高一下联考)下列有关氮及其化合物的性质与用途具有对应关系的是( )
A. 氨水具有碱性,可用于去除烟气中的SO2
B. NH3易溶于水,可用作制冷剂
C. 浓硝酸具有酸性,可用于钝化铁、铝
D. HNO3具有氧化性,可用于生产氮肥NH4NO3
【解析】 NH3易液化,液氨汽化时从环境吸收热量,用作制冷剂,与易溶于水无关,B错误;浓硝酸因有强氧化性,可钝化铁、铝,与酸性无关,C错误;HNO3生成NH4NO3,体现其酸性,与氧化性无关,D错误。
【答案】 A
2
4
5
3
7
6
8
3. (2022·无锡高一下期末)实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
1
A. 用装置甲制备氨气
B. 用装置乙除去氨气中的少量水蒸气
C. 用装置丙收集氨气
D. 用装置丁吸收多余的氨气
2
4
5
3
7
6
8
1
【解析】 氯化铵在试管底部分解成NH3和HCl,在试管口附近温度降低,又生成NH4Cl,A错误;NH3能被浓硫酸吸收,B错误;装置丁中液体会倒吸,D错误。
【答案】 C
2
4
5
3
7
6
8
1
2
4
5
3
7
6
8
1
【解析】 酸性HNO3>H2CO3,所以CO2与NH4NO3溶液反应不能生成(NH4)2CO3,C错误。
【答案】 C
2
4
5
3
7
6
8
5. 为检验一种氮肥的成分,某学习小组的同学进行了以下实验:
①加热氮肥样品生成两种气体,其中一种有刺激性气味的气体能使湿润的红色石蕊试纸变蓝,另一种无色无味气体能使澄清石灰水变浑浊。
②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。
由此可知该氮肥的主要成分是( )
A. NH4HCO3 B. NH4Cl
C. (NH4)2CO3 D. NH4NO3
1
2
4
5
3
7
6
8
1
【解析】 加热氮肥样品生成两种气体,其中一种有刺激性气味的气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种无色无味气体能使澄清石灰水变浑浊,说明含有碳酸根离子或碳酸氢根离子;取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸根离子,则该氮肥中含有铵根离子和碳酸氢根离子,所以该氮肥的主要成分是NH4HCO3,故选A。
【答案】 A
2
4
5
3
7
6
8
6. 下列化合物既能与硫酸反应,又能与氢氧化钠反应的是( )
①NaHCO3 ②NaHSO4 ③(NH4)2CO3 ④NaNO3 ⑤NH4HCO3
A. 只有① B. 只有③
C. ①②③ D. ①③⑤
1
2
4
5
3
7
6
8
1
【解析】 碳酸氢钠既能与硫酸反应生成硫酸钠、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠和水,①正确;硫酸氢钠只与氢氧化钠反应生成硫酸钠和水,②错误;碳酸铵既能与硫酸反应生成硫酸铵、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠和一水合氨(或放出氨),③正确;硝酸钠与硫酸、氢氧化钠都不反应,④错误;碳酸氢铵既能与硫酸反应生成硫酸铵、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠、水和一水合氨(或放出氨),⑤正确。
【答案】 D
2
4
5
3
7
6
8
7. 某化学小组欲制取氨气设计了如图所示装置(另有橡胶管若干可选用)。
1
2
4
5
3
7
6
8
(1) A中制氨气的化学方程式是_________________________________ ___________________。
(2) B中应装__________,作用是____________。
(3) 收集氨气时,B装置的a口应连接C装置的______(填“b”或“c”)口;证明氨气已集满的操作和现象是____________________________ ______________________________________________________。
1
2NH3↑+2H2O
碱石灰
干燥氨气
c
将湿润的红色石蕊试纸靠近
出气口b,若试纸变蓝,则说明氨气已集满(答案合理即可)
2
4
5
3
7
6
8
8. 实验室制取氨气通常有以下两种方法:
方法一:固体氢氧化钙与氯化铵共热;方法二:固体氢氧化钠与浓氨水反应。
1
2
4
5
3
7
6
8
(1) 某化学研究性学习小组欲用方法二制取氨气并验证其性质,上面的装置A、B中,应选用装置______(填字母,下同)制取气体,在制取装置后面连接干燥装置,应选用装置C、D中的______。
(2) 装置E连接在干燥装置的后面,用以验证氨气的性质,装置E中的现象是________________。
(3) 为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是______(填“F”或“G”)。
1
B
D
试纸变成蓝色
F
谢谢观看
Thank you for watching
专题7
氮与社会可持续发展
第三单元 含氮化合物的合理使用
学 习 目 标
活 动 方 案
阅读教材,什么是铵盐?大多数铵盐有什么共同的物理性质?
【答案】 通常把由铵根离子与酸根离子形成的离子化合物称为铵盐。
铵盐大多为无色、易溶于水的晶体。
活动一:学习铵盐的物理性质
1. 靠近NH4HCO3,闻到什么气味?为什么?
【答案】 闻到刺激性气味,说明碳酸氢铵发生分解反应生成了具有刺激性气味的气体。
活动二:探究铵盐的化学性质
2. 实验探究铵盐的性质。
【实验1】 取少量氯化铵和碳酸氢铵,分别放入两支试管中,在酒精灯火焰上微热,观察发生的现象。
【实验2】 将少量氯化铵与少量氢氧化钙混合后放入试管中,在酒精灯火焰上微热,用湿润的红色石蕊试纸检验反应产生的气体。
(1) 填写下表:
实验序号 实验现象 化学方程式
实验1
实验2
两支试管中固体都减少,都能闻到刺激性气味,其中盛氯化铵的试管口有白烟生成,盛碳酸氢铵的试管口有水珠生成
闻到刺激性气味,湿润的红色石蕊试纸变蓝
(2) 怎样检验铵盐中含有的铵根离子?
【答案】 滴加浓碱溶液,加热,用湿润的红色石蕊试纸检验生成的气体,若试纸变蓝,说明生成氨气,原物质中含有铵根离子。
1. 加热NH4Cl和Ca(OH)2固体制取氨气的反应原理是什么(用化学方程式表示)?实验室里用该装置还能制取哪种气体?
活动三:探究氨气的实验室制备
2. 干燥管中的碱石灰是干燥氨的,能用无水CaCl2、P2O5代替碱石灰作干燥剂吗?
【答案】 不能,CaCl2能和NH3发生反应生成CaCl2·8NH3,P2O5为酸性干燥剂,也能和NH3反应。
3. 用什么方法收集氨气?怎样吸收尾气?
【答案】 用向下排空气法收集,尾气可用水吸收(注意防倒吸)。
4. 在制取氨的实验装置中,使用棉花的作用是什么?
【答案】 若为干燥的棉花,则起到减缓氨与空气对流的作用;若为蘸有水或稀硫酸的棉花,则还可以吸收多余的NH3。
5. 如何检验氨气已经收集满?
【答案】 把湿润的红色石蕊试纸置于试管口,试纸变蓝色;或将蘸有浓盐酸的玻璃棒置于试管口,有白烟产生。
6. 直接加热分解氯化铵,然后用碱石灰吸收HCl能否得到氨气?
【答案】 不能,因为生成的氨气和氯化氢在常温下化合又生成氯化铵。
7. 氨是化学实验室常需制取的气体。实验室也可以用下面的两种方法快速制备NH3。
方法一:加热浓氨水。
方法二:将浓氨水滴入生石灰(或碱石灰)固体中。
(1) 请写出上述两种方法中发生反应的化学方程式:_____________ _____________________________________________________________________________________________。
方法一:
(2) 根据上述原理,该小组欲用下列装置制取氨气,方法一应选择______(填字母,下同),方法二应选择______。
D
C
(3) 下图是该小组设计收集氨气的几种装置,其中可行的是______,集气的原理是___________________________________________________ ____________。
d
NH3的密度小于空气,采用短管进氨气,长管出空气的
方法收集
1. 氮肥主要包括哪几种?
【答案】 氮肥主要有铵态氮肥、硝态氮肥和尿素。
2. 铵态氮肥使用时要注意什么?
【答案】 低温保存,深施盖土,避免受热;不可以跟碱性物质(如草木灰等)混合使用。
活动四:常用氮肥及其使用
3. 为什么硝态氮肥易被植物吸收?什么情况下会导致硝态氮肥损失?
4. 请根据氮肥的特性回答问题。
(1) 为什么硝态氮肥不宜在高温天气、多雨的水田区施用,而多用于冷凉的旱地?
【答案】 高温天气,硝态氮肥高温下易分解变质,多雨的水田地区易流失,所以硝态氮肥多用于冷凉的旱地。
(2) 为什么适应在pH较高的碱性土壤中生长的植物优先使用硝态氮肥,而适应在酸性土壤中生长的植物优先使用铵态氮肥?
【答案】 pH较高的碱性土壤使用硝态氮肥,不会因硝酸挥发而使氮肥损失,所以可优先使用硝态氮肥,若使用铵态氮肥,则会生成氨气使氮肥损失;而pH较低的酸性土壤应优先使用铵态氮肥,若使用硝态氮肥,则会因硝酸挥发而导致肥效降低。
5. 为什么尿素是使用量最大的一种氮肥?
【答案】 尿素是一种中性肥料,适用于各种土壤和作物。施用尿素后,土壤中的微生物将其吸收,使其水解成碳酸铵或碳酸氢铵,缓慢释放氨气被作物吸收利用。因此,通常在作物需肥期前4~8天施用。由于尿素肥效高、易保存、使用方便,长期使用对土壤的破坏作用小,所以它是目前使用量最大的一种氮肥。
6. 长期使用化肥会引起哪些环境问题?
【答案】 长期使用化肥的土壤容易酸化、板结。雨水冲刷使肥料离开土壤,进入溪水、河水和湖泊。水中的肥料会使细菌和藻类迅速生长,并消耗水中的氧气,严重时导致水中含氧量减少,许多水生生物随之死亡、腐烂,水质下降。
1943年,美国洛杉矶市发生严重的光化学烟雾事件,持续数十天之久,这种烟雾使人眼睛发红、咽喉疼痛、呼吸憋闷、头昏、头痛,不少老人因呼吸衰竭而死亡。光化学烟雾还使远离城市100 km 以外的高山上的大片松林枯死,柑橘减产。之后世界上的许多地区,如日本的东京、英国的伦敦,加拿大、澳大利亚、荷兰等国的大城市,以及我国的某些地区也曾出现过光化学烟雾。
1. 氮氧化物污染的来源有哪些?
【答案】 化石燃料的燃烧、硝酸生产等产生的工业废气处理不当和日益增多的机动车辆尾气排放,使得大量氮氧化物排放到空气中,给空气带来了一定程度的污染。
活动五:氮氧化物的无害化处理
2. 氮的氧化物NO2有哪些危害?光化学烟雾是怎样形成的?
【答案】 NO2不但会形成酸雨,在日光照射下,二氧化氮还能使氧气经过复杂的反应生成臭氧(O3)。臭氧与空气中的氮氧化物和一些碳氢化合物在紫外线的照射下发生作用后,产生了一种有毒的烟雾,人们称它为光化学烟雾。光化学烟雾具有特殊气味,刺激眼睛,对人体健康、植物生长等都有很大的危害。
3. 为了预防和控制氮氧化物的污染,人们给汽车安装了净化处理装置。净化装置中含有钯(Pd)等金属元素催化剂,尾气通过净化装置后,有害气体NO、CO转化为无害气体,写出该反应的化学方程式。
课 堂 反 馈
2
4
5
1
3
7
6
8
1. 下列关于铵盐的叙述正确的是( )
①铵盐是易溶于水的晶体 ②铵盐中的氮元素均为-3价 ③铵盐受热易分解 ④铵盐只能跟碱反应 ⑤铵态氮肥不宜跟草木灰混合施用 ⑥铵盐都能与酸反应
A. ①②③④⑤ B. ①③⑤
C. ③④⑤ D. ①③④⑤⑥
2
4
5
1
3
7
6
8
【解析】 ①铵盐均为无色或白色晶体,都易溶于水,正确;②硝酸铵中的氮元素为-3价和+5价,错误;③铵盐不稳定,所有铵盐受热均易分解,正确;④铵盐能跟碱反应生成氨气,碳酸铵能与酸反应,错误;⑤铵态氮肥不应跟碱性物质(如草木灰)混合使用,铵盐遇碱生成氨气,降低肥效,正确;⑥氯化铵与盐酸不反应,错误。
【答案】 B
2
4
5
1
3
7
6
8
2. (2022·南通高一下联考)下列有关氮及其化合物的性质与用途具有对应关系的是( )
A. 氨水具有碱性,可用于去除烟气中的SO2
B. NH3易溶于水,可用作制冷剂
C. 浓硝酸具有酸性,可用于钝化铁、铝
D. HNO3具有氧化性,可用于生产氮肥NH4NO3
【解析】 NH3易液化,液氨汽化时从环境吸收热量,用作制冷剂,与易溶于水无关,B错误;浓硝酸因有强氧化性,可钝化铁、铝,与酸性无关,C错误;HNO3生成NH4NO3,体现其酸性,与氧化性无关,D错误。
【答案】 A
2
4
5
3
7
6
8
3. (2022·无锡高一下期末)实验室制取少量干燥的氨气涉及下列装置,其中正确的是( )
1
A. 用装置甲制备氨气
B. 用装置乙除去氨气中的少量水蒸气
C. 用装置丙收集氨气
D. 用装置丁吸收多余的氨气
2
4
5
3
7
6
8
1
【解析】 氯化铵在试管底部分解成NH3和HCl,在试管口附近温度降低,又生成NH4Cl,A错误;NH3能被浓硫酸吸收,B错误;装置丁中液体会倒吸,D错误。
【答案】 C
2
4
5
3
7
6
8
1
2
4
5
3
7
6
8
1
【解析】 酸性HNO3>H2CO3,所以CO2与NH4NO3溶液反应不能生成(NH4)2CO3,C错误。
【答案】 C
2
4
5
3
7
6
8
5. 为检验一种氮肥的成分,某学习小组的同学进行了以下实验:
①加热氮肥样品生成两种气体,其中一种有刺激性气味的气体能使湿润的红色石蕊试纸变蓝,另一种无色无味气体能使澄清石灰水变浑浊。
②取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化。
由此可知该氮肥的主要成分是( )
A. NH4HCO3 B. NH4Cl
C. (NH4)2CO3 D. NH4NO3
1
2
4
5
3
7
6
8
1
【解析】 加热氮肥样品生成两种气体,其中一种有刺激性气味的气体能使湿润的红色石蕊试纸变蓝,该气体为氨气,说明含有铵根离子,另一种无色无味气体能使澄清石灰水变浑浊,说明含有碳酸根离子或碳酸氢根离子;取少量该氮肥样品溶于水,并加入少量BaCl2溶液,没有明显变化,说明没有碳酸根离子,则该氮肥中含有铵根离子和碳酸氢根离子,所以该氮肥的主要成分是NH4HCO3,故选A。
【答案】 A
2
4
5
3
7
6
8
6. 下列化合物既能与硫酸反应,又能与氢氧化钠反应的是( )
①NaHCO3 ②NaHSO4 ③(NH4)2CO3 ④NaNO3 ⑤NH4HCO3
A. 只有① B. 只有③
C. ①②③ D. ①③⑤
1
2
4
5
3
7
6
8
1
【解析】 碳酸氢钠既能与硫酸反应生成硫酸钠、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠和水,①正确;硫酸氢钠只与氢氧化钠反应生成硫酸钠和水,②错误;碳酸铵既能与硫酸反应生成硫酸铵、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠和一水合氨(或放出氨),③正确;硝酸钠与硫酸、氢氧化钠都不反应,④错误;碳酸氢铵既能与硫酸反应生成硫酸铵、二氧化碳和水,又能与氢氧化钠反应生成碳酸钠、水和一水合氨(或放出氨),⑤正确。
【答案】 D
2
4
5
3
7
6
8
7. 某化学小组欲制取氨气设计了如图所示装置(另有橡胶管若干可选用)。
1
2
4
5
3
7
6
8
(1) A中制氨气的化学方程式是_________________________________ ___________________。
(2) B中应装__________,作用是____________。
(3) 收集氨气时,B装置的a口应连接C装置的______(填“b”或“c”)口;证明氨气已集满的操作和现象是____________________________ ______________________________________________________。
1
2NH3↑+2H2O
碱石灰
干燥氨气
c
将湿润的红色石蕊试纸靠近
出气口b,若试纸变蓝,则说明氨气已集满(答案合理即可)
2
4
5
3
7
6
8
8. 实验室制取氨气通常有以下两种方法:
方法一:固体氢氧化钙与氯化铵共热;方法二:固体氢氧化钠与浓氨水反应。
1
2
4
5
3
7
6
8
(1) 某化学研究性学习小组欲用方法二制取氨气并验证其性质,上面的装置A、B中,应选用装置______(填字母,下同)制取气体,在制取装置后面连接干燥装置,应选用装置C、D中的______。
(2) 装置E连接在干燥装置的后面,用以验证氨气的性质,装置E中的现象是________________。
(3) 为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是______(填“F”或“G”)。
1
B
D
试纸变成蓝色
F
谢谢观看
Thank you for watching
