专题9 第1单元 金属的冶炼方法 课件(共32张PPT) 2022-2023学年高一下学期化学苏教版(2019)必修第二册
文档属性
| 名称 | 专题9 第1单元 金属的冶炼方法 课件(共32张PPT) 2022-2023学年高一下学期化学苏教版(2019)必修第二册 |  | |
| 格式 | pptx | ||
| 文件大小 | 566.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-08 15:09:19 | ||
图片预览











文档简介
(共32张PPT)
专题9
金属与人类文明
第一单元 金属的冶炼方法
学 习 目 标
1. 能用金属活动性解释人类利用金属的顺序和比较金属冶炼的方法,说明金属冶炼的本质。
2. 认识我国古代文明与金属冶炼的关系,认识化学在自然资源综合利用方面的重要价值。
3. 感受物质制备中的科学思想。
活 动 方 案
从青铜器时代开始,人类就开始用金属制作各种各样的工具。与传统的陶瓷和石器材料相比,金属材料既有良好的可塑性,坚固耐用,而且还有导电、导热等诸多优良性能,因而具有广泛的应用。大量的金属元素存在于地壳的矿石中,我们必须把它们提炼出来,才能更好地加以利用。
活动一:了解金属在自然界中的存在形式
1. 根据你的经验和所掌握的知识,举例说明什么样的金属在自然界以单质(游离态)形式存在?什么样的金属在自然界以化合物(化合态)形式存在?
【答案】 自然金和自然银等少数化学性质不活泼的金属,在自然界中以单质形式存在;多数金属如钠、镁、铁(陨铁除外)等化学性质比较活泼的金属,在自然界中以化合态形式存在。
2. 阅读下面的材料,回答问题。
从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事。一般认为,人类知道的第一种金属是金,其次是铜。最初人们用石斧把自然界中的天然铜砍下来,锤打成多种器物。随着生产的发展,人们找到了从铜矿中取得铜的方法。含铜的矿物比较多见,例如黄铜矿(CuFeS2)、孔雀石[Cu2(OH)2CO3]、石青[2CuCO3·Cu(OH)2]等,这些矿石在空气中焙烧后形成氧化铜,再用碳还原,就得到金属铜。
(1) 铜元素在自然界中的存在形式是什么?
【答案】 既有游离态,又有化合态。
(2) 铜、铁、铝发现的先后顺序取决于什么因素?
【答案】 金属活动性顺序,金属冶炼的难易程度,金属在自然界中储量等。
(3) 写出将孔雀石投入炭火中焙烧分解,并将其还原为金属铜的化学方程式。
1. 阅读教材,什么是金属的冶炼?从氧化还原的角度看,金属冶炼的原理是什么?
【答案】 利用化学反应使金属元素从化合态变为游离态的过程称为金属的冶炼。从氧化还原的角度看,金属冶炼即通过氧化还原反应将正价态的金属还原为金属单质。
活动二:认识金属的冶炼
2. 查阅资料,写出下列金属冶炼原理的化学方程式。
金属 冶炼原理的化学方程式
(1) Na
(2) Mg
(3) Al
金属 冶炼原理的化学方程式
(4) Fe
(5) Hg
(6) Ag
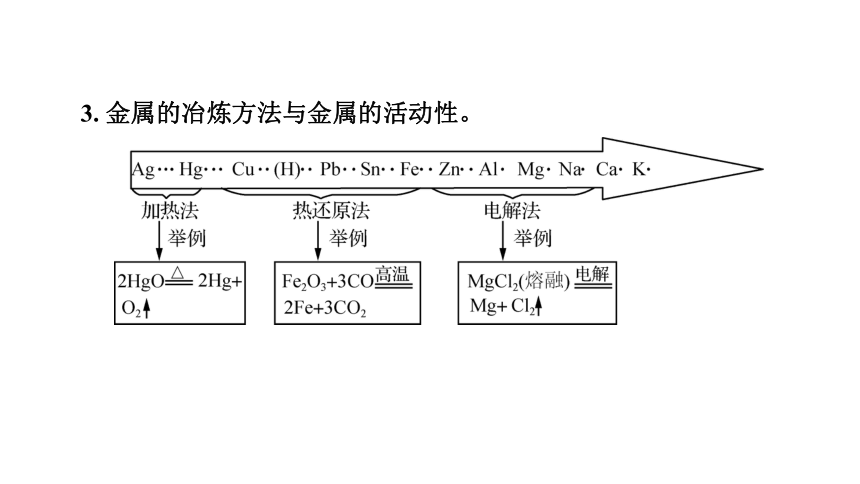
3. 金属的冶炼方法与金属的活动性。
(2) 铁的冶炼。
①高炉炼铁(高温还原法)。
工业上冶炼铁的原料是铁矿石、焦炭和石灰石等,该反应在高炉中进行,又被称为高炉炼铁。冶炼的基本过程:从高炉下方通入热空气,原料从高炉上方的传送带送入炉中,焦炭先与热空气中的氧气反应生成二氧化碳,并放出大量的热;二氧化碳再与灼热的焦炭反应,生成一氧化碳;一氧化碳在高温下将氧化铁还原为液态的金属铁,并从高炉中分离出来。
思考:高炉炼铁的过程中加入石灰石的作用是什么?
【答案】 造渣,除去二氧化硅。
【答案】 该放热反应需要高温引发反应,该反应可用于野外焊接钢轨。
(3) 铝的冶炼(电解法)。
铝元素是地壳中含量最多的金属元素,主要以铝土矿形式存在(主要成分是Al2O3)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝。
工艺流程:
写出向铝土矿中加入氢氧化钠溶液发生反应的化学方程式、向偏铝酸钠溶液中通入过量CO2发生反应的化学方程式和电解氧化铝发生反应的化学方程式。
从矿石中提取人们想要的元素需要经历非常复杂的变化过程。其中最关键的是根据目标产物选择合适的化学反应,以实现物质的转化。冶炼得到的金属有时仍含有较多杂质,需要经过进一步的精炼提纯,以满足实际使用。在金属冶炼的过程中,必须坚持绿色环保、循环利用和节约成本等原则。
活动三:体验金属冶炼中的原理与原则
课 堂 反 馈
2
4
5
1
3
7
6
1. 从本质上讲,工业上冶炼金属的反应一定都属于( )
A. 氧化还原反应 B. 置换反应
C. 分解反应 D. 复分解反应
【解析】 金属冶炼的本质是金属阳离子得电子被还原生成金属单质,因此一定属于氧化还原反应。
【答案】 A
2
4
5
1
3
7
6
2. 能用铝作原料来冶炼难熔的金属是因为( )
A. 铝的密度小,熔点较低
B. 铝在空气中燃烧放出大量的热
C. 铝在金属活动性顺序中排在较前面
D. 铝具有还原性,铝热反应放热
【解析】 利用铝来冶炼难熔的金属是利用铝热反应来进行的。在铝热反应中,铝表现出还原性,可置换出其他金属;另外铝热反应还有一个特点就是反应能放出大量的热,可使置换出的金属熔化,达到冶炼的目的。
【答案】 D
2
4
5
3
7
6
3. (2021·苏州期末)从石器时代到青铜器时代,再到铁器时代,金属的冶炼体现了人类文明的发展历程和水平。下列关于金属冶炼的说法正确的是( )
A. 制铝:将Al(OH)3溶于盐酸中,电解所得AlCl3溶液
B. 制铜:“曾青(CuSO4)得铁,则化为铜”的过程发生复分解反应
C. 炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
D. 制钠:高温分解NaCl制备Na
1
2
4
5
3
7
6
1
【答案】 C
2
4
5
3
7
6
1
2
4
5
3
7
6
1
【解析】 Hg是不活泼金属,可采用直接加热分解其氧化物的方法冶炼,A正确;Mn的金属性小于Al,且熔点大于Al,所以V、Cr、Mn、W等高熔点金属可利用铝热反应产生的高温来冶炼,B正确;Mg是活泼金属,MgO的熔点较高、氯化镁的熔点较低,所以工业上为减少资源消耗,采用电解熔融氯化镁的方法冶炼镁,C错误;在金属活动性顺序中,Fe是处于中间位置的金属,可利用还原剂将Fe从其化合物中还原出来,D正确。
【答案】 C
2
4
5
3
7
6
5. 下列说法不正确的是( )
A. 金属的冶炼就是运用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来
B. 冶炼金属时,必须加入一种物质作还原剂
C. 金属由化合态变为游离态,一定是被还原
D. 金属单质被发现和应用得越早,其活动性越弱
1
2
4
5
3
7
6
1
【解析】 金属的冶炼是指将金属化合物转化为金属单质,A正确;某些金属化合物在发生氧化还原反应冶炼金属单质时,自身既作氧化剂又作还原剂,不需要另加还原剂,如HgO,B错误;金属元素在化合物中一定显正价,当变成金属单质后,化合价就变为0价,金属元素被还原,C正确;金属被发现和应用得越早,说明该金属越容易被还原,其活动性一般是较弱的,D正确。
【答案】 B
2
4
5
3
7
6
6. 金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1) 金属的冶炼一般有下列方法:
a. 焦炭法 b. 水煤气(氢气和一氧化碳)法
c. 活泼金属置换法 d. 电解法
请从上述四种方法中选择相应的字母填入下表中:
1
高炉炼铁 湿法炼铜 铝热法炼铬 工业上冶炼铝
a c c d
写出Al与Cr2O3反应的化学方程式:__________________________。
2
4
5
3
7
6
(2) 铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:__________________________________
_____________________________________________________________。
1
2
4
5
3
7
6
7. 铝热反应的实验装置如图所示。
(1) 该实验装置中还缺________,在试剂使用正确且符合要求的情况下引发铝热反应的操作为______________________________________ _____________。化学方程式为_______________________________。
1
镁条
在混合物中间插一根用砂纸打磨过的镁条,
然后点燃镁条
2
4
5
3
7
6
(2) 若将氧化铁换成氧化镁,该反应________(填“能”或“不能”)发生,理由是______________________________。
(3) 若将所得产品置于足量的NaOH溶液中,可能看到的现象是____________________________,写出铝热反应的一种主要用途:________________________________________________________。
(4) 假设铝足量且反应充分,设计一种实验方案,证明本实验中有单质铁生成:____________________________________________________ ____________________________________________________。
1
不能
镁比铝活泼,铝不能置换出镁
部分固体溶解,有气泡产生
野外焊接钢轨(或冶炼某些熔点高的金属,答案合理即可)
取适量反应后的固体混合物,先用NaOH溶液除去铝和Al2O3,再加入稀硫酸,若有气泡产生,则说明有铁生成
谢谢观看
Thank you for watching
专题9
金属与人类文明
第一单元 金属的冶炼方法
学 习 目 标
1. 能用金属活动性解释人类利用金属的顺序和比较金属冶炼的方法,说明金属冶炼的本质。
2. 认识我国古代文明与金属冶炼的关系,认识化学在自然资源综合利用方面的重要价值。
3. 感受物质制备中的科学思想。
活 动 方 案
从青铜器时代开始,人类就开始用金属制作各种各样的工具。与传统的陶瓷和石器材料相比,金属材料既有良好的可塑性,坚固耐用,而且还有导电、导热等诸多优良性能,因而具有广泛的应用。大量的金属元素存在于地壳的矿石中,我们必须把它们提炼出来,才能更好地加以利用。
活动一:了解金属在自然界中的存在形式
1. 根据你的经验和所掌握的知识,举例说明什么样的金属在自然界以单质(游离态)形式存在?什么样的金属在自然界以化合物(化合态)形式存在?
【答案】 自然金和自然银等少数化学性质不活泼的金属,在自然界中以单质形式存在;多数金属如钠、镁、铁(陨铁除外)等化学性质比较活泼的金属,在自然界中以化合态形式存在。
2. 阅读下面的材料,回答问题。
从金属利用的历史来看,先是青铜器时代,而后是铁器时代,铝的利用是近百年的事。一般认为,人类知道的第一种金属是金,其次是铜。最初人们用石斧把自然界中的天然铜砍下来,锤打成多种器物。随着生产的发展,人们找到了从铜矿中取得铜的方法。含铜的矿物比较多见,例如黄铜矿(CuFeS2)、孔雀石[Cu2(OH)2CO3]、石青[2CuCO3·Cu(OH)2]等,这些矿石在空气中焙烧后形成氧化铜,再用碳还原,就得到金属铜。
(1) 铜元素在自然界中的存在形式是什么?
【答案】 既有游离态,又有化合态。
(2) 铜、铁、铝发现的先后顺序取决于什么因素?
【答案】 金属活动性顺序,金属冶炼的难易程度,金属在自然界中储量等。
(3) 写出将孔雀石投入炭火中焙烧分解,并将其还原为金属铜的化学方程式。
1. 阅读教材,什么是金属的冶炼?从氧化还原的角度看,金属冶炼的原理是什么?
【答案】 利用化学反应使金属元素从化合态变为游离态的过程称为金属的冶炼。从氧化还原的角度看,金属冶炼即通过氧化还原反应将正价态的金属还原为金属单质。
活动二:认识金属的冶炼
2. 查阅资料,写出下列金属冶炼原理的化学方程式。
金属 冶炼原理的化学方程式
(1) Na
(2) Mg
(3) Al
金属 冶炼原理的化学方程式
(4) Fe
(5) Hg
(6) Ag
3. 金属的冶炼方法与金属的活动性。
(2) 铁的冶炼。
①高炉炼铁(高温还原法)。
工业上冶炼铁的原料是铁矿石、焦炭和石灰石等,该反应在高炉中进行,又被称为高炉炼铁。冶炼的基本过程:从高炉下方通入热空气,原料从高炉上方的传送带送入炉中,焦炭先与热空气中的氧气反应生成二氧化碳,并放出大量的热;二氧化碳再与灼热的焦炭反应,生成一氧化碳;一氧化碳在高温下将氧化铁还原为液态的金属铁,并从高炉中分离出来。
思考:高炉炼铁的过程中加入石灰石的作用是什么?
【答案】 造渣,除去二氧化硅。
【答案】 该放热反应需要高温引发反应,该反应可用于野外焊接钢轨。
(3) 铝的冶炼(电解法)。
铝元素是地壳中含量最多的金属元素,主要以铝土矿形式存在(主要成分是Al2O3)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝。
工艺流程:
写出向铝土矿中加入氢氧化钠溶液发生反应的化学方程式、向偏铝酸钠溶液中通入过量CO2发生反应的化学方程式和电解氧化铝发生反应的化学方程式。
从矿石中提取人们想要的元素需要经历非常复杂的变化过程。其中最关键的是根据目标产物选择合适的化学反应,以实现物质的转化。冶炼得到的金属有时仍含有较多杂质,需要经过进一步的精炼提纯,以满足实际使用。在金属冶炼的过程中,必须坚持绿色环保、循环利用和节约成本等原则。
活动三:体验金属冶炼中的原理与原则
课 堂 反 馈
2
4
5
1
3
7
6
1. 从本质上讲,工业上冶炼金属的反应一定都属于( )
A. 氧化还原反应 B. 置换反应
C. 分解反应 D. 复分解反应
【解析】 金属冶炼的本质是金属阳离子得电子被还原生成金属单质,因此一定属于氧化还原反应。
【答案】 A
2
4
5
1
3
7
6
2. 能用铝作原料来冶炼难熔的金属是因为( )
A. 铝的密度小,熔点较低
B. 铝在空气中燃烧放出大量的热
C. 铝在金属活动性顺序中排在较前面
D. 铝具有还原性,铝热反应放热
【解析】 利用铝来冶炼难熔的金属是利用铝热反应来进行的。在铝热反应中,铝表现出还原性,可置换出其他金属;另外铝热反应还有一个特点就是反应能放出大量的热,可使置换出的金属熔化,达到冶炼的目的。
【答案】 D
2
4
5
3
7
6
3. (2021·苏州期末)从石器时代到青铜器时代,再到铁器时代,金属的冶炼体现了人类文明的发展历程和水平。下列关于金属冶炼的说法正确的是( )
A. 制铝:将Al(OH)3溶于盐酸中,电解所得AlCl3溶液
B. 制铜:“曾青(CuSO4)得铁,则化为铜”的过程发生复分解反应
C. 炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中铁的氧化物
D. 制钠:高温分解NaCl制备Na
1
2
4
5
3
7
6
1
【答案】 C
2
4
5
3
7
6
1
2
4
5
3
7
6
1
【解析】 Hg是不活泼金属,可采用直接加热分解其氧化物的方法冶炼,A正确;Mn的金属性小于Al,且熔点大于Al,所以V、Cr、Mn、W等高熔点金属可利用铝热反应产生的高温来冶炼,B正确;Mg是活泼金属,MgO的熔点较高、氯化镁的熔点较低,所以工业上为减少资源消耗,采用电解熔融氯化镁的方法冶炼镁,C错误;在金属活动性顺序中,Fe是处于中间位置的金属,可利用还原剂将Fe从其化合物中还原出来,D正确。
【答案】 C
2
4
5
3
7
6
5. 下列说法不正确的是( )
A. 金属的冶炼就是运用氧化还原反应原理,在一定条件下将金属从其化合物中还原出来
B. 冶炼金属时,必须加入一种物质作还原剂
C. 金属由化合态变为游离态,一定是被还原
D. 金属单质被发现和应用得越早,其活动性越弱
1
2
4
5
3
7
6
1
【解析】 金属的冶炼是指将金属化合物转化为金属单质,A正确;某些金属化合物在发生氧化还原反应冶炼金属单质时,自身既作氧化剂又作还原剂,不需要另加还原剂,如HgO,B错误;金属元素在化合物中一定显正价,当变成金属单质后,化合价就变为0价,金属元素被还原,C正确;金属被发现和应用得越早,说明该金属越容易被还原,其活动性一般是较弱的,D正确。
【答案】 B
2
4
5
3
7
6
6. 金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1) 金属的冶炼一般有下列方法:
a. 焦炭法 b. 水煤气(氢气和一氧化碳)法
c. 活泼金属置换法 d. 电解法
请从上述四种方法中选择相应的字母填入下表中:
1
高炉炼铁 湿法炼铜 铝热法炼铬 工业上冶炼铝
a c c d
写出Al与Cr2O3反应的化学方程式:__________________________。
2
4
5
3
7
6
(2) 铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:__________________________________
_____________________________________________________________。
1
2
4
5
3
7
6
7. 铝热反应的实验装置如图所示。
(1) 该实验装置中还缺________,在试剂使用正确且符合要求的情况下引发铝热反应的操作为______________________________________ _____________。化学方程式为_______________________________。
1
镁条
在混合物中间插一根用砂纸打磨过的镁条,
然后点燃镁条
2
4
5
3
7
6
(2) 若将氧化铁换成氧化镁,该反应________(填“能”或“不能”)发生,理由是______________________________。
(3) 若将所得产品置于足量的NaOH溶液中,可能看到的现象是____________________________,写出铝热反应的一种主要用途:________________________________________________________。
(4) 假设铝足量且反应充分,设计一种实验方案,证明本实验中有单质铁生成:____________________________________________________ ____________________________________________________。
1
不能
镁比铝活泼,铝不能置换出镁
部分固体溶解,有气泡产生
野外焊接钢轨(或冶炼某些熔点高的金属,答案合理即可)
取适量反应后的固体混合物,先用NaOH溶液除去铝和Al2O3,再加入稀硫酸,若有气泡产生,则说明有铁生成
谢谢观看
Thank you for watching
