7.1 酸及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 7.1 酸及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 60.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-08 00:00:00 | ||
图片预览

文档简介
7.1 酸及其性质 同步练习
一、单选题
1.某同学设计的制备氯化铁的方案中,分别采用下列物品,其中能实现的是( )
A.氢氧化亚铁和盐酸 B.铁和盐酸
C.氧化亚铁和盐酸 D.氢氧化铁和盐酸
2.下列有关盐酸的说法正确的是( )
A.稀盐酸的溶质是一种气体
B.打开浓盐酸瓶塞,可看到大量白烟
C.镁和稀盐酸的反应是一个吸热反应
D.向稀盐酸中逐滴加入氢氧化钠溶液,溶液的pH先增大后减小
3.下列药品未经密封保存,敞口放置一段时间后,质量增加并发生化学反应的是( )
①苛性钠 ②碳酸 ③浓盐酸 ④浓硫酸 ⑤熟石灰
A.①③ B.②④ C.①⑤ D.④⑤
4.下列关于浓硫酸的描述中不正确的是( )
A.有强烈的腐蚀性
B.溶于水时放出大量的热
C.稀释浓硫酸时,将浓硫酸慢慢注入水里,并不断搅拌
D.如果不慎沾到皮肤上,立即用大量水冲洗,再涂上氢氧化钠溶液
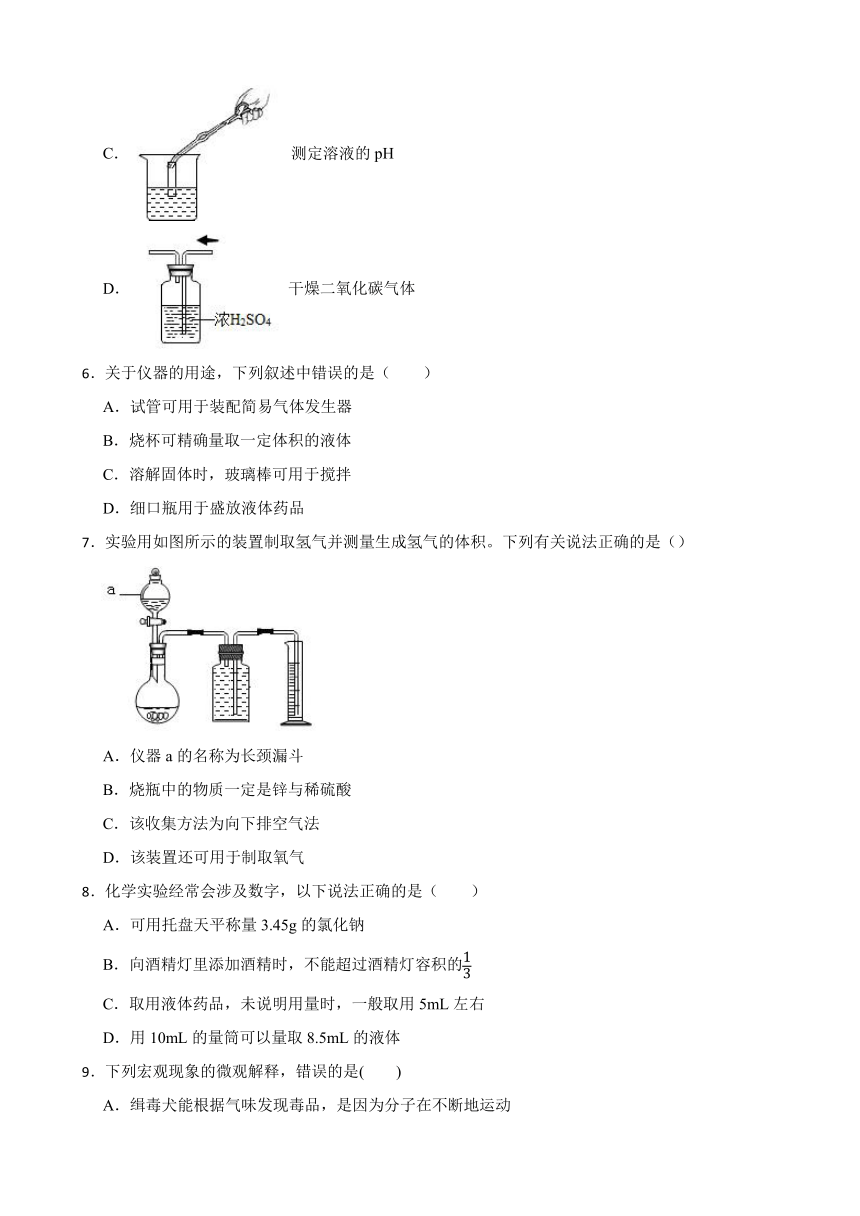
5.如图图示的实验操作,正确的是()
A. 稀释浓硫酸
B. 配制NaCl溶液
C. 测定溶液的pH
D. 干燥二氧化碳气体
6.关于仪器的用途,下列叙述中错误的是( )
A.试管可用于装配简易气体发生器
B.烧杯可精确量取一定体积的液体
C.溶解固体时,玻璃棒可用于搅拌
D.细口瓶用于盛放液体药品
7.实验用如图所示的装置制取氢气并测量生成氢气的体积。下列有关说法正确的是()
A.仪器a的名称为长颈漏斗
B.烧瓶中的物质一定是锌与稀硫酸
C.该收集方法为向下排空气法
D.该装置还可用于制取氧气
8.化学实验经常会涉及数字,以下说法正确的是( )
A.可用托盘天平称量3.45g的氯化钠
B.向酒精灯里添加酒精时,不能超过酒精灯容积的
C.取用液体药品,未说明用量时,一般取用5mL左右
D.用10mL的量筒可以量取8.5mL的液体
9.下列宏观现象的微观解释,错误的是( )
A.缉毒犬能根据气味发现毒品,是因为分子在不断地运动
B.温度计受热时水银柱上升,是因为汞原子受热时体积变大
C.稀盐酸和稀硫酸都能使紫色石蕊溶液变红,是因为它们的溶液中都含H+
D.20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔
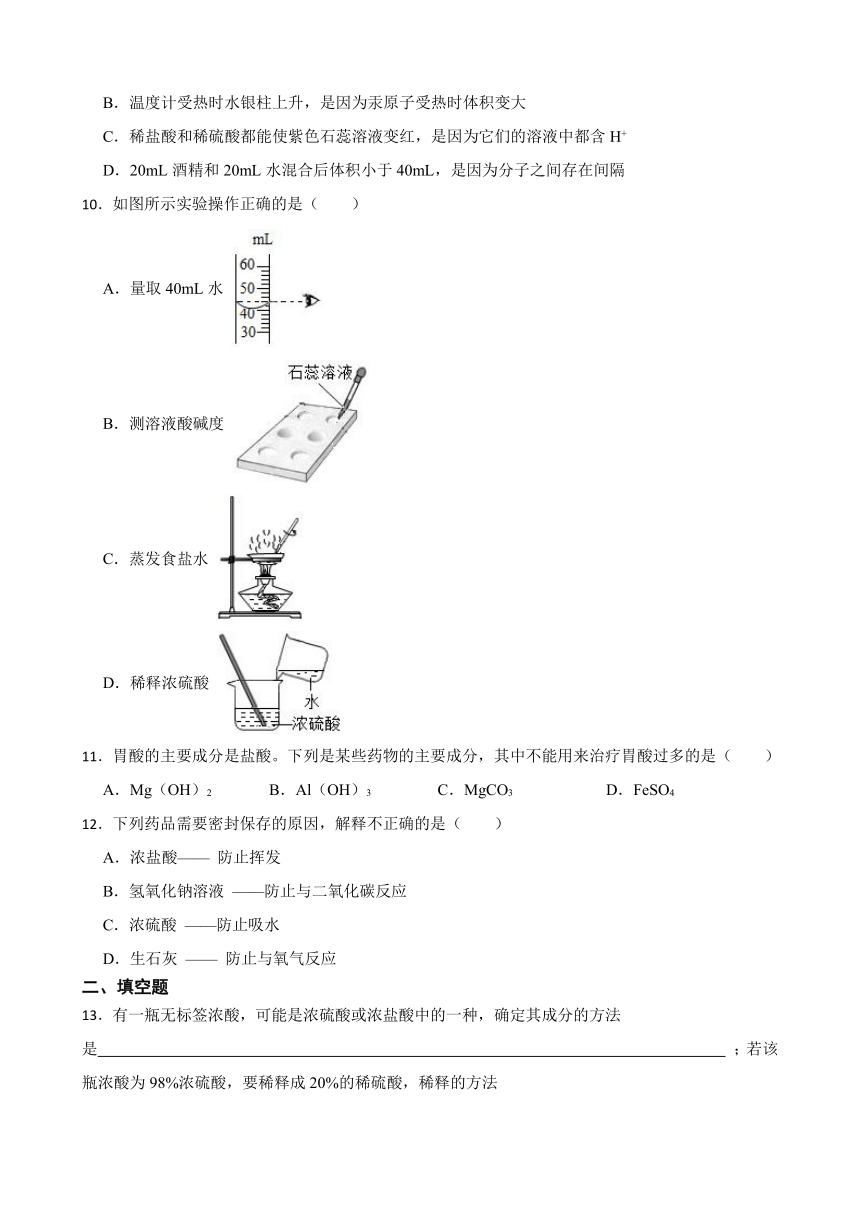
10.如图所示实验操作正确的是( )
A.量取40mL水
B.测溶液酸碱度
C.蒸发食盐水
D.稀释浓硫酸
11.胃酸的主要成分是盐酸。下列是某些药物的主要成分,其中不能用来治疗胃酸过多的是( )
A.Mg(OH)2 B.Al(OH)3 C.MgCO3 D.FeSO4
12.下列药品需要密封保存的原因,解释不正确的是( )
A.浓盐酸—— 防止挥发
B.氢氧化钠溶液 ——防止与二氧化碳反应
C.浓硫酸 ——防止吸水
D.生石灰 —— 防止与氧气反应
二、填空题
13.有一瓶无标签浓酸,可能是浓硫酸或浓盐酸中的一种,确定其成分的方法是 ;若该瓶浓酸为98%浓硫酸,要稀释成20%的稀硫酸,稀释的方法是 ;在该实验中具有搅拌作用的仪器在其他实验中也经常用到,请举一例利用该仪器其他作用的实验名称 .
14.浓盐酸放在空气中质量变 ,质量分数变 ,原因是 .浓硫酸放在空气中质量变 ,质量分数变 ,原因是 .
15.
(1)在实验室常用的仪器①试管、②集气瓶、③蒸发皿、④量筒、⑤烧杯、⑥燃烧匙中,可以在酒精灯上直接加热的是 (填序号);
(2)稀释浓硫酸时,先往烧杯中倾倒的液体为 ;
(3)实验室用高锰酸钾氧气,实验结束时应先 (填字母序号)。
A
将导气管从水槽中移出 B 熄灭酒精灯
16.稀释浓硫酸时,一定要将 慢慢注入水中,用 不断地搅拌,使热量迅速扩散,切不可将水注入浓硫酸中.
17.水是一种重要的资源,根据你所学的知识回答下列问题。
(1)在日常生活中,人们常用 来区分硬软水。
(2)自来水厂常用活性炭来净水,活性炭净水是利用活性炭的 作用。
(3)水电解过程中发生变化的微粒是 。
(4)实验室稀释浓硫酸时,应将 沿烧杯壁缓缓地注入盛有 的烧杯中。
(5)用湿抹布扑盖实验桌上燃烧的酒精,其主要灭火原理是 。
18.浓盐酸打开瓶子,瓶口有 ,这是因为浓盐酸具有 ,挥发出的 气体与空气中的 结合形成 .
三、综合题
19.盐酸、硫酸是两种重要的酸,回答与它们有关的下列问题。
(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是 ;
(2)它们都能除铁锈,写出硫酸与铁锈主要成分反应的化学方程式 ;
(3)稀盐酸和稀硫酸具有相似化学性质的微观本质是 。
20.请根据所学的化学知识填空:
(1)在抗震救灾中,国家给救援人员配备了活性炭口罩,活性炭起 作用。
(2)生活中为降低水的硬度,可采用的方法是 。
(3)若要除去热水瓶中的水垢[主要成分是CaCO3],可选用厨房中的 。
(4)电解水制取氢气和氧气实验说明分子在化学反应中 ,该反应的化学方程式为 。
(5)我国第一艘国产航母下水,该航母采用了大量钢铁作为原材料,钢铁生锈的条件是铁与 (填化学式)接触。工业上常用赤铁矿和一氧化碳在高温条件下来炼铁,该反应的化学方程式 。
21.如图是某浓盐酸试剂瓶上标签的部分内容.
(1)将浓盐酸敞口放置,其质量分数会变小,这是由于浓盐酸具有较强的 ,所以浓盐酸必须密封保存;
(2)将该瓶浓盐酸全部配制成溶质质量分数为11.8%(密度约为1.06g/mL)的盐酸,需加入水 mL(ρ水=1g/mL);
(3)含杂质40%的石灰石100g与足量稀盐酸充分反应,理论上可得到CO2多少克?(假设杂质不与稀盐酸反应)
22.某兴趣小组做以下实验探究分子有运动。请回答实验中的有关问题。
(1)实验I:在盛有少量蒸馏水的小烧杯中先滴入2—3滴酚酞试液,再向其中滴加浓氨水。总结出实验现象及结论:
(2)实验Ⅱ(如图甲所示):烧杯B中的现象是 ;产生这一现象的原因是 。
(3)为使实验结论准确可靠,兴趣小组成设计实验Ⅲ(如图乙所示)作为对比实验。你认为有无必要? ,理由是
答案解析部分
1.【答案】D
2.【答案】A
3.【答案】C
4.【答案】D
5.【答案】D
6.【答案】B
7.【答案】D
8.【答案】D
9.【答案】B
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】打开瓶盖,瓶口出现白雾的是浓盐酸,且闻到刺激性气体,浓硫酸不挥发,无此现象;把浓硫酸沿容器壁慢慢注入水里,并不断搅拌;过滤
14.【答案】小;小;浓盐酸具有挥发性;大;小;浓硫酸具有吸水性
15.【答案】(1)①③⑥
(2)水(或H2O)
(3)A
16.【答案】浓硫酸;玻璃棒
17.【答案】(1)肥皂水
(2)吸附
(3)水分子
(4)浓硫酸;水
(5)隔绝氧气
18.【答案】白雾;挥发性;氯化氢气体;水蒸气;盐酸小液滴
19.【答案】(1)浓盐酸
(2)Fe2O3+3H2SO4 =Fe2(SO4)3 + 3H2O
(3)都能电离出H+
20.【答案】(1)吸附
(2)煮沸
(3)食醋
(4)可以再分;
(5)O2 和 H2O;
21.【答案】(1)挥发性
(2)1210
(3)解:根据碳酸钙与盐酸反应的化学方程式,已知碳酸钙的质量可求出二氧化碳的质量
设可得到二氧化碳的质量为x
CaCO3+2HCl═CaCl2+H2O+ CO2↑
100 44
100g×(1﹣40%) x
= x=26.4g
22.【答案】(1)酚酞试液由无色变红色,酚酞试液遇蒸馏水不变色,遇浓氨水变红色
(2)无色变为红色;浓氨水具有极强的挥发性,挥发出的氨分子不断运动,与烧杯B内水发生反应生成氨水,呈碱性,使无色酚酞变为红色
(3)不必要;烧杯D中原本就含有蒸馏水
一、单选题
1.某同学设计的制备氯化铁的方案中,分别采用下列物品,其中能实现的是( )
A.氢氧化亚铁和盐酸 B.铁和盐酸
C.氧化亚铁和盐酸 D.氢氧化铁和盐酸
2.下列有关盐酸的说法正确的是( )
A.稀盐酸的溶质是一种气体
B.打开浓盐酸瓶塞,可看到大量白烟
C.镁和稀盐酸的反应是一个吸热反应
D.向稀盐酸中逐滴加入氢氧化钠溶液,溶液的pH先增大后减小
3.下列药品未经密封保存,敞口放置一段时间后,质量增加并发生化学反应的是( )
①苛性钠 ②碳酸 ③浓盐酸 ④浓硫酸 ⑤熟石灰
A.①③ B.②④ C.①⑤ D.④⑤
4.下列关于浓硫酸的描述中不正确的是( )
A.有强烈的腐蚀性
B.溶于水时放出大量的热
C.稀释浓硫酸时,将浓硫酸慢慢注入水里,并不断搅拌
D.如果不慎沾到皮肤上,立即用大量水冲洗,再涂上氢氧化钠溶液
5.如图图示的实验操作,正确的是()
A. 稀释浓硫酸
B. 配制NaCl溶液
C. 测定溶液的pH
D. 干燥二氧化碳气体
6.关于仪器的用途,下列叙述中错误的是( )
A.试管可用于装配简易气体发生器
B.烧杯可精确量取一定体积的液体
C.溶解固体时,玻璃棒可用于搅拌
D.细口瓶用于盛放液体药品
7.实验用如图所示的装置制取氢气并测量生成氢气的体积。下列有关说法正确的是()
A.仪器a的名称为长颈漏斗
B.烧瓶中的物质一定是锌与稀硫酸
C.该收集方法为向下排空气法
D.该装置还可用于制取氧气
8.化学实验经常会涉及数字,以下说法正确的是( )
A.可用托盘天平称量3.45g的氯化钠
B.向酒精灯里添加酒精时,不能超过酒精灯容积的
C.取用液体药品,未说明用量时,一般取用5mL左右
D.用10mL的量筒可以量取8.5mL的液体
9.下列宏观现象的微观解释,错误的是( )
A.缉毒犬能根据气味发现毒品,是因为分子在不断地运动
B.温度计受热时水银柱上升,是因为汞原子受热时体积变大
C.稀盐酸和稀硫酸都能使紫色石蕊溶液变红,是因为它们的溶液中都含H+
D.20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔
10.如图所示实验操作正确的是( )
A.量取40mL水
B.测溶液酸碱度
C.蒸发食盐水
D.稀释浓硫酸
11.胃酸的主要成分是盐酸。下列是某些药物的主要成分,其中不能用来治疗胃酸过多的是( )
A.Mg(OH)2 B.Al(OH)3 C.MgCO3 D.FeSO4
12.下列药品需要密封保存的原因,解释不正确的是( )
A.浓盐酸—— 防止挥发
B.氢氧化钠溶液 ——防止与二氧化碳反应
C.浓硫酸 ——防止吸水
D.生石灰 —— 防止与氧气反应
二、填空题
13.有一瓶无标签浓酸,可能是浓硫酸或浓盐酸中的一种,确定其成分的方法是 ;若该瓶浓酸为98%浓硫酸,要稀释成20%的稀硫酸,稀释的方法是 ;在该实验中具有搅拌作用的仪器在其他实验中也经常用到,请举一例利用该仪器其他作用的实验名称 .
14.浓盐酸放在空气中质量变 ,质量分数变 ,原因是 .浓硫酸放在空气中质量变 ,质量分数变 ,原因是 .
15.
(1)在实验室常用的仪器①试管、②集气瓶、③蒸发皿、④量筒、⑤烧杯、⑥燃烧匙中,可以在酒精灯上直接加热的是 (填序号);
(2)稀释浓硫酸时,先往烧杯中倾倒的液体为 ;
(3)实验室用高锰酸钾氧气,实验结束时应先 (填字母序号)。
A
将导气管从水槽中移出 B 熄灭酒精灯
16.稀释浓硫酸时,一定要将 慢慢注入水中,用 不断地搅拌,使热量迅速扩散,切不可将水注入浓硫酸中.
17.水是一种重要的资源,根据你所学的知识回答下列问题。
(1)在日常生活中,人们常用 来区分硬软水。
(2)自来水厂常用活性炭来净水,活性炭净水是利用活性炭的 作用。
(3)水电解过程中发生变化的微粒是 。
(4)实验室稀释浓硫酸时,应将 沿烧杯壁缓缓地注入盛有 的烧杯中。
(5)用湿抹布扑盖实验桌上燃烧的酒精,其主要灭火原理是 。
18.浓盐酸打开瓶子,瓶口有 ,这是因为浓盐酸具有 ,挥发出的 气体与空气中的 结合形成 .
三、综合题
19.盐酸、硫酸是两种重要的酸,回答与它们有关的下列问题。
(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是 ;
(2)它们都能除铁锈,写出硫酸与铁锈主要成分反应的化学方程式 ;
(3)稀盐酸和稀硫酸具有相似化学性质的微观本质是 。
20.请根据所学的化学知识填空:
(1)在抗震救灾中,国家给救援人员配备了活性炭口罩,活性炭起 作用。
(2)生活中为降低水的硬度,可采用的方法是 。
(3)若要除去热水瓶中的水垢[主要成分是CaCO3],可选用厨房中的 。
(4)电解水制取氢气和氧气实验说明分子在化学反应中 ,该反应的化学方程式为 。
(5)我国第一艘国产航母下水,该航母采用了大量钢铁作为原材料,钢铁生锈的条件是铁与 (填化学式)接触。工业上常用赤铁矿和一氧化碳在高温条件下来炼铁,该反应的化学方程式 。
21.如图是某浓盐酸试剂瓶上标签的部分内容.
(1)将浓盐酸敞口放置,其质量分数会变小,这是由于浓盐酸具有较强的 ,所以浓盐酸必须密封保存;
(2)将该瓶浓盐酸全部配制成溶质质量分数为11.8%(密度约为1.06g/mL)的盐酸,需加入水 mL(ρ水=1g/mL);
(3)含杂质40%的石灰石100g与足量稀盐酸充分反应,理论上可得到CO2多少克?(假设杂质不与稀盐酸反应)
22.某兴趣小组做以下实验探究分子有运动。请回答实验中的有关问题。
(1)实验I:在盛有少量蒸馏水的小烧杯中先滴入2—3滴酚酞试液,再向其中滴加浓氨水。总结出实验现象及结论:
(2)实验Ⅱ(如图甲所示):烧杯B中的现象是 ;产生这一现象的原因是 。
(3)为使实验结论准确可靠,兴趣小组成设计实验Ⅲ(如图乙所示)作为对比实验。你认为有无必要? ,理由是
答案解析部分
1.【答案】D
2.【答案】A
3.【答案】C
4.【答案】D
5.【答案】D
6.【答案】B
7.【答案】D
8.【答案】D
9.【答案】B
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】打开瓶盖,瓶口出现白雾的是浓盐酸,且闻到刺激性气体,浓硫酸不挥发,无此现象;把浓硫酸沿容器壁慢慢注入水里,并不断搅拌;过滤
14.【答案】小;小;浓盐酸具有挥发性;大;小;浓硫酸具有吸水性
15.【答案】(1)①③⑥
(2)水(或H2O)
(3)A
16.【答案】浓硫酸;玻璃棒
17.【答案】(1)肥皂水
(2)吸附
(3)水分子
(4)浓硫酸;水
(5)隔绝氧气
18.【答案】白雾;挥发性;氯化氢气体;水蒸气;盐酸小液滴
19.【答案】(1)浓盐酸
(2)Fe2O3+3H2SO4 =Fe2(SO4)3 + 3H2O
(3)都能电离出H+
20.【答案】(1)吸附
(2)煮沸
(3)食醋
(4)可以再分;
(5)O2 和 H2O;
21.【答案】(1)挥发性
(2)1210
(3)解:根据碳酸钙与盐酸反应的化学方程式,已知碳酸钙的质量可求出二氧化碳的质量
设可得到二氧化碳的质量为x
CaCO3+2HCl═CaCl2+H2O+ CO2↑
100 44
100g×(1﹣40%) x
= x=26.4g
22.【答案】(1)酚酞试液由无色变红色,酚酞试液遇蒸馏水不变色,遇浓氨水变红色
(2)无色变为红色;浓氨水具有极强的挥发性,挥发出的氨分子不断运动,与烧杯B内水发生反应生成氨水,呈碱性,使无色酚酞变为红色
(3)不必要;烧杯D中原本就含有蒸馏水
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
