8.2 常见的酸和碱 同步练习(含答案) 2022-2023学年粤教版九年级下册化学
文档属性
| 名称 | 8.2 常见的酸和碱 同步练习(含答案) 2022-2023学年粤教版九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 102.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-09 00:00:00 | ||
图片预览


文档简介
8.2 常见的酸和碱 同步练习 2022-2023学年粤教版九年级下册化学
一、单选题
1.在盛有稀硫酸的烧杯中,分别加入下列物质,最终只存在无色液体的是( )
A.Na2CO3溶液、KOH溶液 B.BaCl2溶液、NaOH溶液
C.Fe2(SO4)3溶液、NaNO3溶液 D.Cu片、Na2SO4溶液
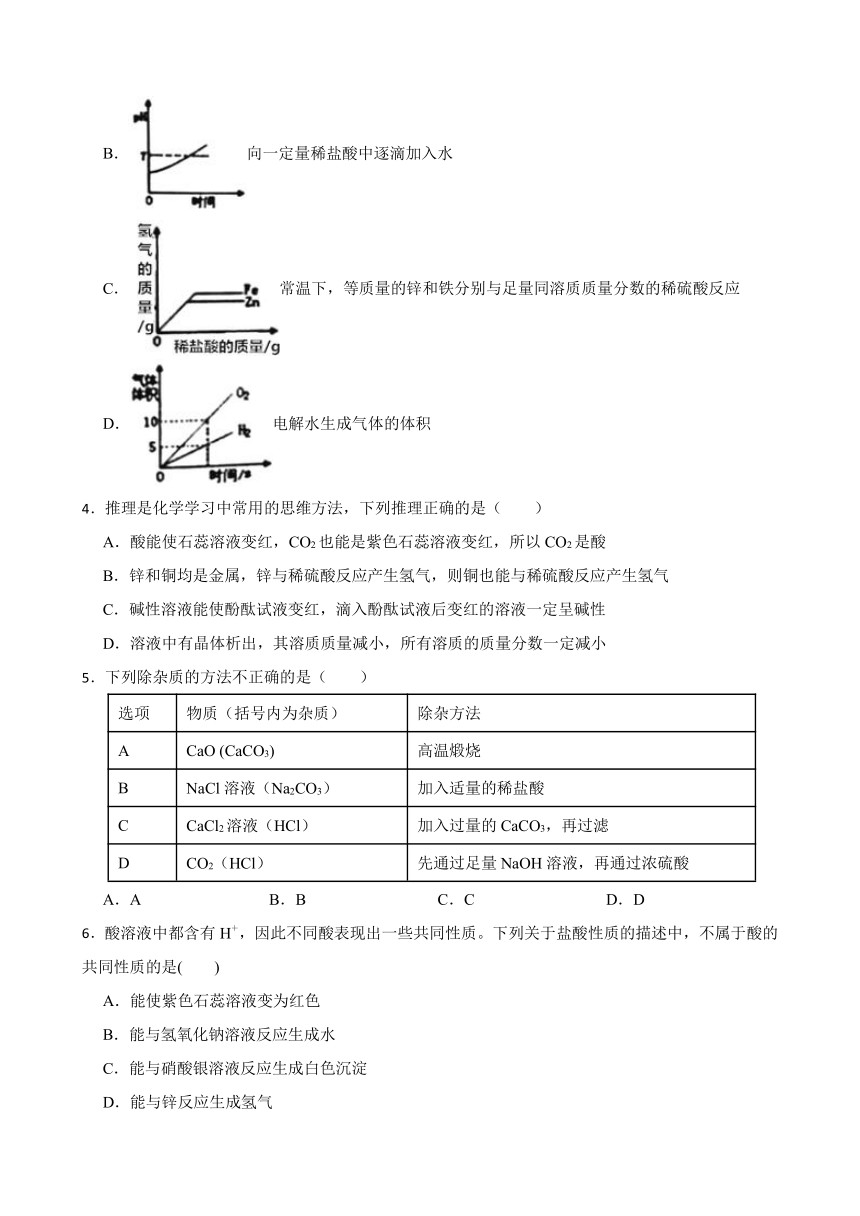
2.能反映相关实验过程中量的变化的图象是( )
A.大理石投入足量盐酸中
B.稀盐酸滴入Na2CO3溶液中
C.稀释NaCl溶液
D.稀H2SO4中滴入BaCl2溶液
3.下列图象分别与选项中的实验过程相对应,其中正确的是( )
A.向部分变质的氢氧化钠溶液中滴加稀盐酸
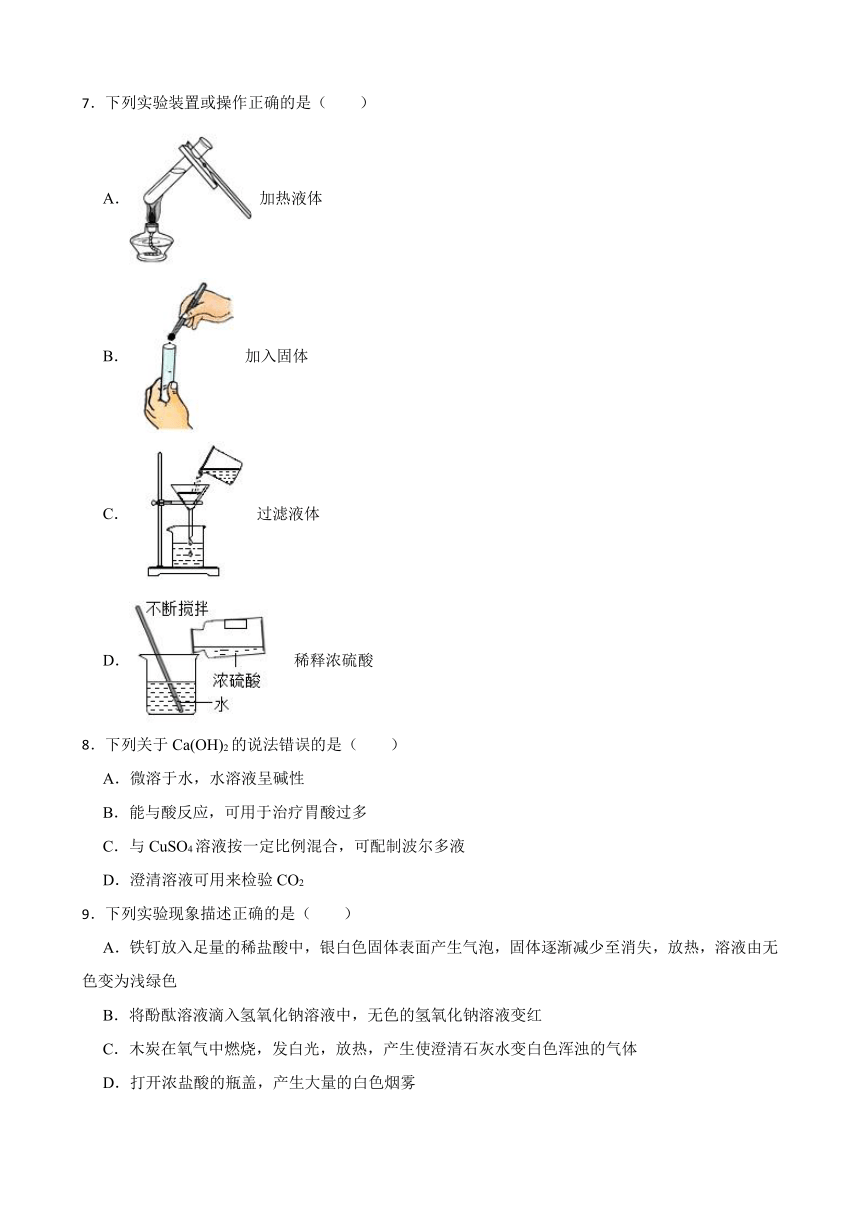
B.向一定量稀盐酸中逐滴加入水
C.常温下,等质量的锌和铁分别与足量同溶质质量分数的稀硫酸反应
D.电解水生成气体的体积
4.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.酸能使石蕊溶液变红,CO2也能是紫色石蕊溶液变红,所以CO2是酸
B.锌和铜均是金属,锌与稀硫酸反应产生氢气,则铜也能与稀硫酸反应产生氢气
C.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D.溶液中有晶体析出,其溶质质量减小,所有溶质的质量分数一定减小
5.下列除杂质的方法不正确的是( )
选项 物质(括号内为杂质) 除杂方法
A CaO (CaCO3) 高温煅烧
B NaCl溶液(Na2CO3) 加入适量的稀盐酸
C CaCl2溶液(HCl) 加入过量的CaCO3,再过滤
D CO2(HCl) 先通过足量NaOH溶液,再通过浓硫酸
A.A B.B C.C D.D
6.酸溶液中都含有H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊溶液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
7.下列实验装置或操作正确的是( )
A. 加热液体
B. 加入固体
C. 过滤液体
D. 稀释浓硫酸
8.下列关于Ca(OH)2的说法错误的是( )
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
9.下列实验现象描述正确的是( )
A.铁钉放入足量的稀盐酸中,银白色固体表面产生气泡,固体逐渐减少至消失,放热,溶液由无色变为浅绿色
B.将酚酞溶液滴入氢氧化钠溶液中,无色的氢氧化钠溶液变红
C.木炭在氧气中燃烧,发白光,放热,产生使澄清石灰水变白色浑浊的气体
D.打开浓盐酸的瓶盖,产生大量的白色烟雾
10.有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是 ( )
A.硫酸铁、硝酸铁 B.硫酸、氯化铁
C.盐酸、氯化铁 D.盐酸、硫酸铁
11.下列实验方案中,设计不合理的是()
A.鉴别硫酸铜溶液和稀盐酸:分别观察溶液颜色
B.鉴别氯化铵和尿素:分别加熟石灰粉末研磨,闻气味
C.鉴别硝酸铵和氯化钠:分别加适量水,用手触摸容器壁
D.鉴别烧碱溶液和石灰水:分别滴加酚酞试液,观察颜色变化
12.下列有关实验现象的描述正确的是( )
A.红磷在空气中燃烧产生大量白色烟雾
B.氢气在空气中燃烧发出明亮的蓝色火焰
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.向硫酸铜溶液中滴加氢氧化钠溶液,有蓝色絮状沉淀生成,加热后可变成黑色
二、填空题
13.镍(Ni)是一种用途广泛的金属,常用于电镀工业和制造电池,硫酸镍溶液显绿色,氢氧化镍为难溶于水的绿色固体,在这些化合物中镍元素都显+2价.
(1)氢氧化镍的化学式为 .
(2)将硫酸镍溶液加入试管中,再滴加足量氢氧化钠溶液,充分振荡后静置.
①反应的化学方程式为 .
②预测反应现象: .
14.氧气和水是重要的化学物质,应用它们的化学知识回答问题。
(1)二者在组成上的共同点是都含有 ;
(2)超市里的一些食品采用真空包装,其原理是除去袋内的空气,使微生物因缺少 而受到抑制,达到防腐作用;
(3)在过滤、吸附和蒸馏三种净水方法中,单一操作相对净化程度最高的是 ;
(4)某条河的附近有一硫酸厂,欲检验该厂废水呈酸性,一般可选用下列药品中的________(填字母序号)。
A.Ca(OH)2 B.Mg
C.CaO D.AgNO3 E NaCO3
15.硫酸、盐酸是重要的化工原料.
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性.
(2)写出下列反应的化学方程式:
①用熟石灰中和硫酸厂排出的废水
②将生锈铁钉加入稀硫酸中一段时间后铁锈消失铁钉表面有气泡: ; .
③稀硫酸与碳酸钠溶液反应:
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
16.稀释浓硫酸时,一定要把 沿器壁慢慢注入 中,并不断 ,使产生的 迅速地扩散.这是因为浓硫酸溶于水时 ,而且浓硫酸具有很强的 性.如果不慎将浓硫酸溅到皮肤上,必须先用 ,再用 .
17.铁锈的主要成分是 ,用稀盐酸除去将铁锈的化学方程式为 ;反应的现象为 .
18.在NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3四种碱中,
(1)属于微溶于水的是 ;水溶液能使酚酞试液变红的是 ;
(2)不溶于水,但能溶于酸的是 ;
(3)与酸反应溶液呈蓝色的是 ;
(4)水溶液通入CO2后有浑浊或沉淀出现的是 .
三、综合题
19.下图是某钙片的部分标签,根据图示回答下列问题。
咀嚼钙片
本品以碳酸钙为主要原料
[配料表]碳酸钙、淀粉、乳糖
[适用人群]缺钙人群
[贮存方法]密封,阴凉、干燥处
(1)碳酸钙中碳元素的化合价为 价:
(2)W液的主要成分有盐酸,服用该保健品后有时会出现腹胀、打嗝等反应,出现这种反应的原因是(用化学方程式表示) 。
20.根据如图所示的实验操作图示回答问题.
(1)下列图示①、②、③、④操作中有错误的是 ,共有 处错误.
(2)若用⑤收集下列气体,从a通入气体可以收集 (填字母代号,下同);从b通入气体可以收集 .
A、NH3; B、CO2; C、CH4; D、SO2.
21.在牙膏中,常用轻质碳酸钙粉末作摩擦剂。轻质碳酸钙是以石灰石为原料,经过提纯后得到的高纯度碳酸钙。其生产流程如图。
(1)石灰石在石灰窑中发生反应的化学方程式为: 。其反应类型是 (填基本反应类型)。
(2)消化池反应后得到的主要产物是 (填化学式),反应过程会 (填“吸收”或“放出”)热量。
(3)过筛的目的是除去块状残渣,下列实验操作原理与过筛相似的是____(填字母)。
A.加热 B.蒸馏 C.过滤 D.研碎
(4)碳化塔中发生反应的化学方程式为: ,从企业生产的角度看,该生产流程将产生的CO2通入碳化塔循环利用的优点是 。
四、实验探究题
22.一般不用K、Ca、Na等活泼金属来置换盐溶液中的其他金属元素,这是教科书上的一句话.小科对此进行了思考,并查阅资料,对金属钠和硫酸铜溶液的反应进行探究.
【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O═2NaOH+H2↑
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成.
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜.
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示
实验编号 钠块大小 硫酸铜溶液 实验中产生沉淀的现象
① 绿豆大小 稀溶液10mL 产生蓝绿色沉淀
② 绿豆大小 浓溶液10mL 产生蓝色絮状沉淀
③ 豌豆大小 稀溶液10mL 产生蓝色絮状沉淀
④ 豌豆大小 浓溶液10mL 产生蓝色絮状沉淀,并出现黑色固体
小科咨询老师后得知蓝绿色沉淀为碱式铜盐.
(1)【实验结论】上述实验中均未观察到 色固体生成,由此判断猜想一错误.
实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误.
(2)【实验反思】
实验中生成氢氧化铜沉淀的原理是 .
由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有 .
(3)为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热.
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热.
请从两个方案中选出合理的方案,并说明理由. .
答案解析部分
1.【答案】A
2.【答案】A
3.【答案】C
4.【答案】C
5.【答案】D
6.【答案】C
7.【答案】D
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】Ni(OH)2;NiSO4+2NaOH═Ni(OH)2↓+Na2SO4;有绿色固体生成,溶液从绿色变成无色
14.【答案】(1)氧元素
(2)氧气
(3)蒸馏
(4)B
15.【答案】吸水;Ca(OH)2+H2SO4═CaSO4+2H2O;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4═FeSO4+H2↑;Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;②③
16.【答案】浓硫酸;水;搅拌;热量;放热;腐蚀;抹布擦掉;大量水冲洗
17.【答案】氧化铁;Fe2O3+6HCl═2FeCl3+3H2O;铁锈消失,溶液变为黄色
18.【答案】(1)Ca(OH)2;NaOH、Ca(OH)2
(2)Cu(OH)2、Fe(OH)3
(3)Cu(OH)2
(4)Ca(OH)2.
19.【答案】(1)+4
(2)CaCO3+2HCl =CaCl2+ H2O + CO2↑
20.【答案】(1)④;2
(2)BD;AC
21.【答案】(1);分解反应
(2)Ca(OH)2;放出
(3)C
(4);节约原料,降低成本
22.【答案】(1)红
(2)钠和水先反应生成氢氧化钠,生成的氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀;钠块的大小、硫酸铜溶液的浓度
(3)方案二;隔绝空气加热,能避免钠在空气中被氧化
一、单选题
1.在盛有稀硫酸的烧杯中,分别加入下列物质,最终只存在无色液体的是( )
A.Na2CO3溶液、KOH溶液 B.BaCl2溶液、NaOH溶液
C.Fe2(SO4)3溶液、NaNO3溶液 D.Cu片、Na2SO4溶液
2.能反映相关实验过程中量的变化的图象是( )
A.大理石投入足量盐酸中
B.稀盐酸滴入Na2CO3溶液中
C.稀释NaCl溶液
D.稀H2SO4中滴入BaCl2溶液
3.下列图象分别与选项中的实验过程相对应,其中正确的是( )
A.向部分变质的氢氧化钠溶液中滴加稀盐酸
B.向一定量稀盐酸中逐滴加入水
C.常温下,等质量的锌和铁分别与足量同溶质质量分数的稀硫酸反应
D.电解水生成气体的体积
4.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.酸能使石蕊溶液变红,CO2也能是紫色石蕊溶液变红,所以CO2是酸
B.锌和铜均是金属,锌与稀硫酸反应产生氢气,则铜也能与稀硫酸反应产生氢气
C.碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性
D.溶液中有晶体析出,其溶质质量减小,所有溶质的质量分数一定减小
5.下列除杂质的方法不正确的是( )
选项 物质(括号内为杂质) 除杂方法
A CaO (CaCO3) 高温煅烧
B NaCl溶液(Na2CO3) 加入适量的稀盐酸
C CaCl2溶液(HCl) 加入过量的CaCO3,再过滤
D CO2(HCl) 先通过足量NaOH溶液,再通过浓硫酸
A.A B.B C.C D.D
6.酸溶液中都含有H+,因此不同酸表现出一些共同性质。下列关于盐酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊溶液变为红色
B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀
D.能与锌反应生成氢气
7.下列实验装置或操作正确的是( )
A. 加热液体
B. 加入固体
C. 过滤液体
D. 稀释浓硫酸
8.下列关于Ca(OH)2的说法错误的是( )
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
9.下列实验现象描述正确的是( )
A.铁钉放入足量的稀盐酸中,银白色固体表面产生气泡,固体逐渐减少至消失,放热,溶液由无色变为浅绿色
B.将酚酞溶液滴入氢氧化钠溶液中,无色的氢氧化钠溶液变红
C.木炭在氧气中燃烧,发白光,放热,产生使澄清石灰水变白色浑浊的气体
D.打开浓盐酸的瓶盖,产生大量的白色烟雾
10.有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是 ( )
A.硫酸铁、硝酸铁 B.硫酸、氯化铁
C.盐酸、氯化铁 D.盐酸、硫酸铁
11.下列实验方案中,设计不合理的是()
A.鉴别硫酸铜溶液和稀盐酸:分别观察溶液颜色
B.鉴别氯化铵和尿素:分别加熟石灰粉末研磨,闻气味
C.鉴别硝酸铵和氯化钠:分别加适量水,用手触摸容器壁
D.鉴别烧碱溶液和石灰水:分别滴加酚酞试液,观察颜色变化
12.下列有关实验现象的描述正确的是( )
A.红磷在空气中燃烧产生大量白色烟雾
B.氢气在空气中燃烧发出明亮的蓝色火焰
C.细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
D.向硫酸铜溶液中滴加氢氧化钠溶液,有蓝色絮状沉淀生成,加热后可变成黑色
二、填空题
13.镍(Ni)是一种用途广泛的金属,常用于电镀工业和制造电池,硫酸镍溶液显绿色,氢氧化镍为难溶于水的绿色固体,在这些化合物中镍元素都显+2价.
(1)氢氧化镍的化学式为 .
(2)将硫酸镍溶液加入试管中,再滴加足量氢氧化钠溶液,充分振荡后静置.
①反应的化学方程式为 .
②预测反应现象: .
14.氧气和水是重要的化学物质,应用它们的化学知识回答问题。
(1)二者在组成上的共同点是都含有 ;
(2)超市里的一些食品采用真空包装,其原理是除去袋内的空气,使微生物因缺少 而受到抑制,达到防腐作用;
(3)在过滤、吸附和蒸馏三种净水方法中,单一操作相对净化程度最高的是 ;
(4)某条河的附近有一硫酸厂,欲检验该厂废水呈酸性,一般可选用下列药品中的________(填字母序号)。
A.Ca(OH)2 B.Mg
C.CaO D.AgNO3 E NaCO3
15.硫酸、盐酸是重要的化工原料.
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性.
(2)写出下列反应的化学方程式:
①用熟石灰中和硫酸厂排出的废水
②将生锈铁钉加入稀硫酸中一段时间后铁锈消失铁钉表面有气泡: ; .
③稀硫酸与碳酸钠溶液反应:
(3)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填编号)
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH.
16.稀释浓硫酸时,一定要把 沿器壁慢慢注入 中,并不断 ,使产生的 迅速地扩散.这是因为浓硫酸溶于水时 ,而且浓硫酸具有很强的 性.如果不慎将浓硫酸溅到皮肤上,必须先用 ,再用 .
17.铁锈的主要成分是 ,用稀盐酸除去将铁锈的化学方程式为 ;反应的现象为 .
18.在NaOH、Ca(OH)2、Cu(OH)2、Fe(OH)3四种碱中,
(1)属于微溶于水的是 ;水溶液能使酚酞试液变红的是 ;
(2)不溶于水,但能溶于酸的是 ;
(3)与酸反应溶液呈蓝色的是 ;
(4)水溶液通入CO2后有浑浊或沉淀出现的是 .
三、综合题
19.下图是某钙片的部分标签,根据图示回答下列问题。
咀嚼钙片
本品以碳酸钙为主要原料
[配料表]碳酸钙、淀粉、乳糖
[适用人群]缺钙人群
[贮存方法]密封,阴凉、干燥处
(1)碳酸钙中碳元素的化合价为 价:
(2)W液的主要成分有盐酸,服用该保健品后有时会出现腹胀、打嗝等反应,出现这种反应的原因是(用化学方程式表示) 。
20.根据如图所示的实验操作图示回答问题.
(1)下列图示①、②、③、④操作中有错误的是 ,共有 处错误.
(2)若用⑤收集下列气体,从a通入气体可以收集 (填字母代号,下同);从b通入气体可以收集 .
A、NH3; B、CO2; C、CH4; D、SO2.
21.在牙膏中,常用轻质碳酸钙粉末作摩擦剂。轻质碳酸钙是以石灰石为原料,经过提纯后得到的高纯度碳酸钙。其生产流程如图。
(1)石灰石在石灰窑中发生反应的化学方程式为: 。其反应类型是 (填基本反应类型)。
(2)消化池反应后得到的主要产物是 (填化学式),反应过程会 (填“吸收”或“放出”)热量。
(3)过筛的目的是除去块状残渣,下列实验操作原理与过筛相似的是____(填字母)。
A.加热 B.蒸馏 C.过滤 D.研碎
(4)碳化塔中发生反应的化学方程式为: ,从企业生产的角度看,该生产流程将产生的CO2通入碳化塔循环利用的优点是 。
四、实验探究题
22.一般不用K、Ca、Na等活泼金属来置换盐溶液中的其他金属元素,这是教科书上的一句话.小科对此进行了思考,并查阅资料,对金属钠和硫酸铜溶液的反应进行探究.
【查阅资料】钠常温下就能与水发生剧烈反应,反应方程式为:2Na+2H2O═2NaOH+H2↑
【提出猜想】猜想一:金属钠和硫酸铜溶液反应会有铜生成.
猜想二:金属钠和硫酸铜溶液反应,生成的沉淀只有氢氧化铜.
【实验及现象】切取不同大小的钠块分别投入到两种不同浓度的硫酸铜溶液中,有关产生沉淀的现象如表所示
实验编号 钠块大小 硫酸铜溶液 实验中产生沉淀的现象
① 绿豆大小 稀溶液10mL 产生蓝绿色沉淀
② 绿豆大小 浓溶液10mL 产生蓝色絮状沉淀
③ 豌豆大小 稀溶液10mL 产生蓝色絮状沉淀
④ 豌豆大小 浓溶液10mL 产生蓝色絮状沉淀,并出现黑色固体
小科咨询老师后得知蓝绿色沉淀为碱式铜盐.
(1)【实验结论】上述实验中均未观察到 色固体生成,由此判断猜想一错误.
实验①中观察到的沉淀是蓝绿色的,由此判断猜想二也错误.
(2)【实验反思】
实验中生成氢氧化铜沉淀的原理是 .
由上述实验可知,导致钠和硫酸铜溶液反应的产物不同的因素有 .
(3)为了用钠置换硫酸铜中的铜元素,小科设计了如下实验方案
方案一:把钠块和无水硫酸铜直接混合,在干燥的空气中加热.
方案二:把钠块和无水硫酸铜直接混合,隔绝空气加热.
请从两个方案中选出合理的方案,并说明理由. .
答案解析部分
1.【答案】A
2.【答案】A
3.【答案】C
4.【答案】C
5.【答案】D
6.【答案】C
7.【答案】D
8.【答案】B
9.【答案】C
10.【答案】C
11.【答案】D
12.【答案】D
13.【答案】Ni(OH)2;NiSO4+2NaOH═Ni(OH)2↓+Na2SO4;有绿色固体生成,溶液从绿色变成无色
14.【答案】(1)氧元素
(2)氧气
(3)蒸馏
(4)B
15.【答案】吸水;Ca(OH)2+H2SO4═CaSO4+2H2O;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;Fe+H2SO4═FeSO4+H2↑;Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;②③
16.【答案】浓硫酸;水;搅拌;热量;放热;腐蚀;抹布擦掉;大量水冲洗
17.【答案】氧化铁;Fe2O3+6HCl═2FeCl3+3H2O;铁锈消失,溶液变为黄色
18.【答案】(1)Ca(OH)2;NaOH、Ca(OH)2
(2)Cu(OH)2、Fe(OH)3
(3)Cu(OH)2
(4)Ca(OH)2.
19.【答案】(1)+4
(2)CaCO3+2HCl =CaCl2+ H2O + CO2↑
20.【答案】(1)④;2
(2)BD;AC
21.【答案】(1);分解反应
(2)Ca(OH)2;放出
(3)C
(4);节约原料,降低成本
22.【答案】(1)红
(2)钠和水先反应生成氢氧化钠,生成的氢氧化钠与硫酸铜溶液反应生成氢氧化铜蓝色沉淀;钠块的大小、硫酸铜溶液的浓度
(3)方案二;隔绝空气加热,能避免钠在空气中被氧化
