7.1 酸及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学
文档属性
| 名称 | 7.1 酸及其性质 同步练习(含答案) 2022-2023学年鲁教版九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 238.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-09 00:00:00 | ||
图片预览

文档简介
7.1 酸及其性质 同步练习 2022-2023学年鲁教版九年级下册化学
一、单选题
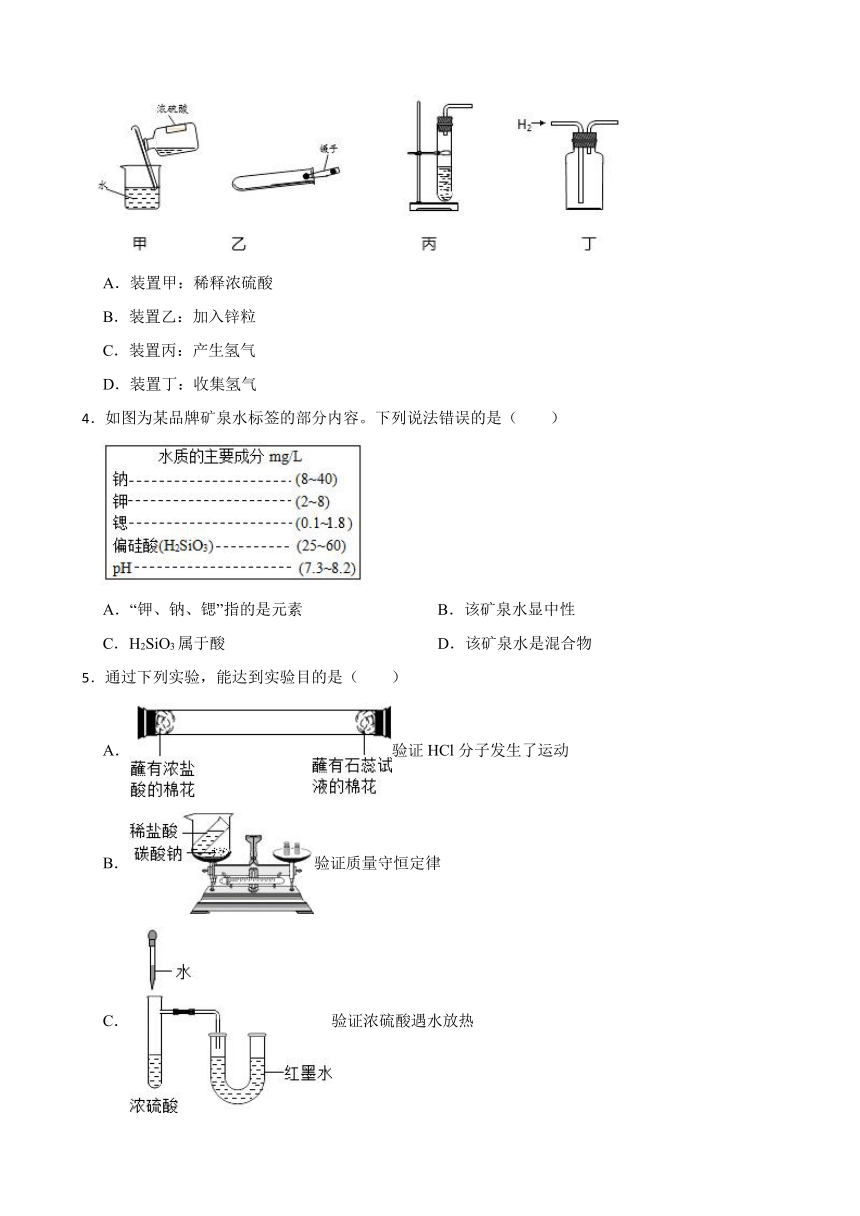
1.下列曲线正确的是( )
A. 向稀硝酸中加水
B. 双氧水分解
C. 向等体积、等浓度的稀盐酸中加金属
D. 向稀硫酸中滴BaCl2溶液
2.检验某溶液是否为酸溶液,下列四种方案中错误的是( )
A.向该溶液中滴加碳酸钠溶液,看是否有气泡产生
B.向该溶液中滴加紫色石蕊溶液,看是否变红
C.向该溶液中滴加无色酚酞溶液,看是否变色
D.向该溶液中加锌粒,看是否有气泡产生
3.实验室用锌和稀硫酸制取氢气,下列操作错误的是( )
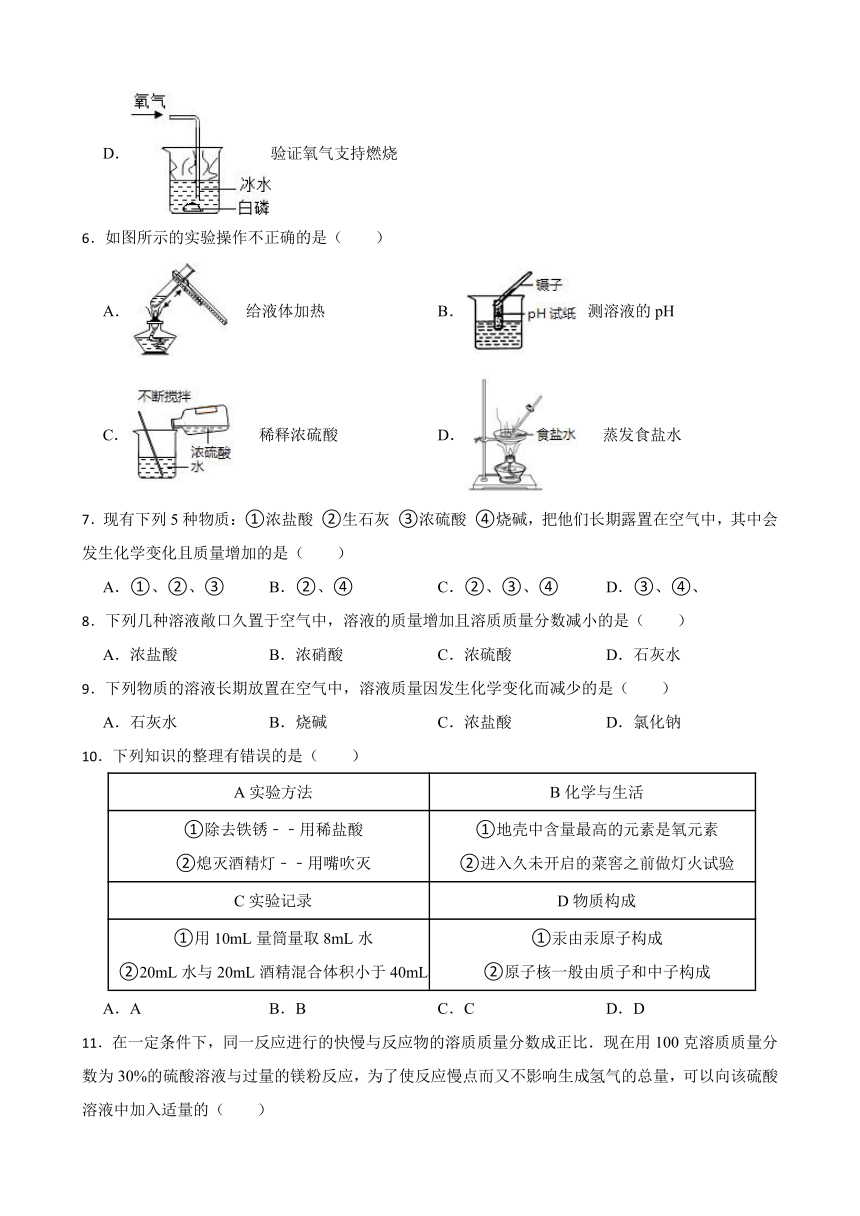
A.装置甲:稀释浓硫酸
B.装置乙:加入锌粒
C.装置丙:产生氢气
D.装置丁:收集氢气
4.如图为某品牌矿泉水标签的部分内容。下列说法错误的是( )
A.“钾、钠、锶”指的是元素 B.该矿泉水显中性
C.H2SiO3属于酸 D.该矿泉水是混合物
5.通过下列实验,能达到实验目的是( )
A.验证HCl分子发生了运动
B.验证质量守恒定律
C.验证浓硫酸遇水放热
D.验证氧气支持燃烧
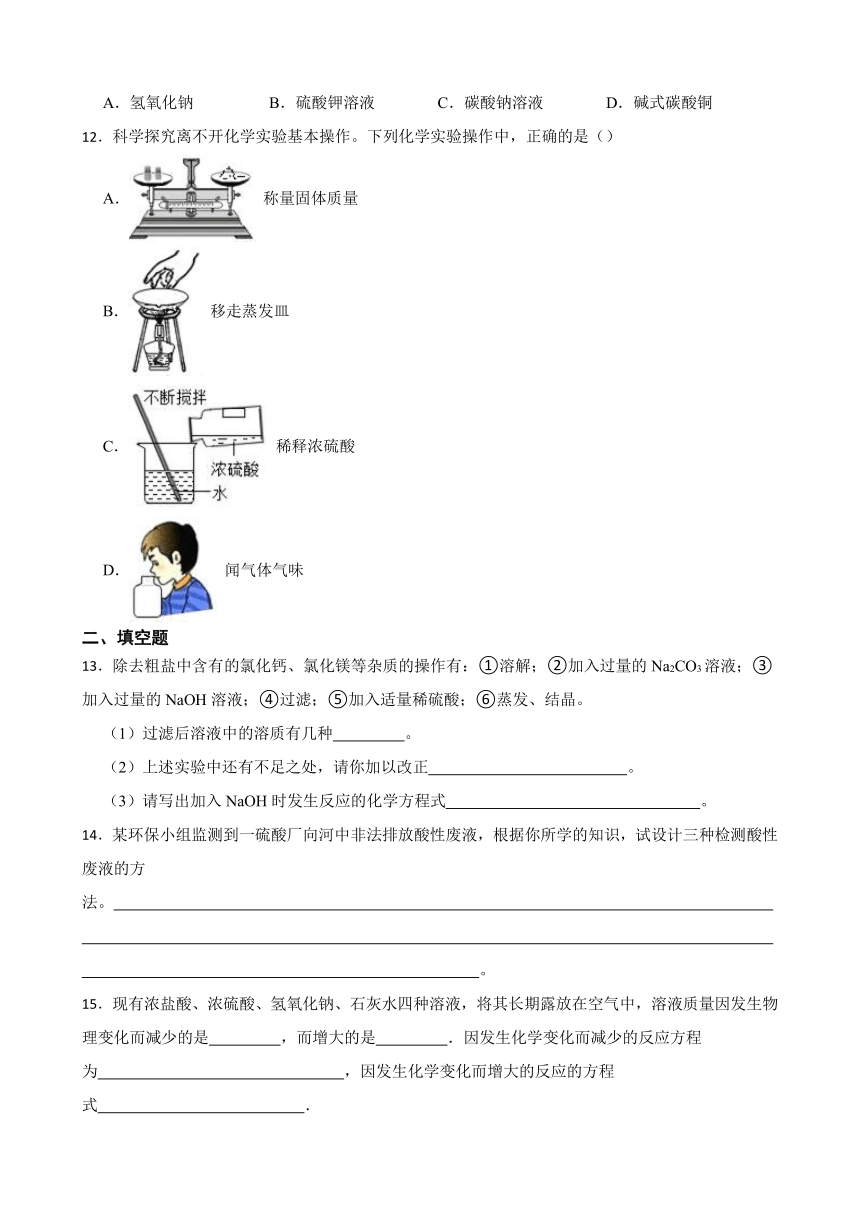
6.如图所示的实验操作不正确的是( )
A. 给液体加热 B. 测溶液的pH
C. 稀释浓硫酸 D. 蒸发食盐水
7.现有下列5种物质:①浓盐酸 ②生石灰 ③浓硫酸 ④烧碱,把他们长期露置在空气中,其中会发生化学变化且质量增加的是( )
A.①、②、③ B.②、④ C.②、③、④ D.③、④、
8.下列几种溶液敞口久置于空气中,溶液的质量增加且溶质质量分数减小的是( )
A.浓盐酸 B.浓硝酸 C.浓硫酸 D.石灰水
9.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是( )
A.石灰水 B.烧碱 C.浓盐酸 D.氯化钠
10.下列知识的整理有错误的是( )
A实验方法 B化学与生活
①除去铁锈﹣﹣用稀盐酸 ②熄灭酒精灯﹣﹣用嘴吹灭 ①地壳中含量最高的元素是氧元素 ②进入久未开启的菜窖之前做灯火试验
C实验记录 D物质构成
①用10mL量筒量取8mL水 ②20mL水与20mL酒精混合体积小于40mL ①汞由汞原子构成 ②原子核一般由质子和中子构成
A.A B.B C.C D.D
11.在一定条件下,同一反应进行的快慢与反应物的溶质质量分数成正比.现在用100克溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点而又不影响生成氢气的总量,可以向该硫酸溶液中加入适量的( )
A.氢氧化钠 B.硫酸钾溶液 C.碳酸钠溶液 D.碱式碳酸铜
12.科学探究离不开化学实验基本操作。下列化学实验操作中,正确的是()
A. 称量固体质量
B. 移走蒸发皿
C. 稀释浓硫酸
D. 闻气体气味
二、填空题
13.除去粗盐中含有的氯化钙、氯化镁等杂质的操作有:①溶解;②加入过量的Na2CO3溶液;③加入过量的NaOH溶液;④过滤;⑤加入适量稀硫酸;⑥蒸发、结晶。
(1)过滤后溶液中的溶质有几种 。
(2)上述实验中还有不足之处,请你加以改正 。
(3)请写出加入NaOH时发生反应的化学方程式 。
14.某环保小组监测到一硫酸厂向河中非法排放酸性废液,根据你所学的知识,试设计三种检测酸性废液的方法。 。
15.现有浓盐酸、浓硫酸、氢氧化钠、石灰水四种溶液,将其长期露放在空气中,溶液质量因发生物理变化而减少的是 ,而增大的是 .因发生化学变化而减少的反应方程为 ,因发生化学变化而增大的反应的方程式 .
16.做化学实验时,应严格遵守实验室规则和操作规程.请仔细观察图,找出其中存在的安全隐患(任写两种):
① ;② .
17.如图表示五种不同类别物质间的关系.A是铁锈的主要成分,C俗称苛性钠,请结合图示回答问题.(图中“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质)
(1)A物质的化学式是 ,B物质是 .
(2)C物质的另一个俗称是 .它溶于水时会出现 (填“放热”或“吸热”)现象.
(3)在①、②、③、④四个反应中,不能体现酸的化学通性的是 (填序号).
18.“大理石”是常见的筑装饰材料,容易受到酸雨(含硫酸)的侵蚀,原因是(用化学方程式表示) 。
三、综合题
19.根据如图所示的实验操作图示回答问题.
(1)下列图示①、②、③、④操作中有错误的是 ,共有 处错误.
(2)若用⑤收集下列气体,从a通入气体可以收集 (填字母代号,下同);从b通入气体可以收集 .
A、NH3; B、CO2; C、CH4; D、SO2.
20.“宏观——微观——符号”三重表征是化学独特的表示物质及其变化的方法。请结合图示完成下列问题。
(1)Fe2O3、CO2和P2O5都含有 (填名称),且只含有两种元素,均属于氧化物。
(2)向装有一定量氧化铁粉末的试管中,加入适量稀硫酸,恰好完全反应后。
①可以观察到的现象是 。
②如图表示该反应前后溶液中存在的主要离子。请写出每种图形代表的离子(填离子符号):
。
③下列物质能与氧化铁反应,产生相似实验现象的是 (填选项)
A. 硫酸钠
B. 稀盐酸
C.食醋
D. 氢氧化钠
21.如图是稀释浓硫酸实验的示意图.
(1)量筒盛放的液体是 (填“水”或“浓硫酸”).
(2)玻璃棒搅拌的目的是 .
(3)稀释时若颠倒两种试剂的添加顺序,其后果是 .
四、实验探究题
22.如图,某同学做酸和碱的中和反应实验时,滴加盐酸前忘记先在氢氧化钠溶液中加入酚酞试液结果无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【提出猜想】①溶液可能呈中性; ②溶液可能呈酸性; ③溶液可能呈碱性。
(1)【实验探究】
实验操作 实验现象 实验结论
用试管取该溶液1-2mL,滴入1-2滴酚酞试液,振荡 溶液呈碱性
溶液颜色无明显变化 溶液呈酸性或中性
(2)【分析思考】
若溶液呈碱性,则溶液中的溶质为 (填写化学式)。
(3)若溶液颜色无明显变化,为进一步确定溶液的酸碱性,该同学提出了两种方案:
方案1:取样,用pH试纸测定,若pH<7,则溶液呈酸性;若pH=7,则呈中性。
方案2:取样,向其中加入 ,若观察到有气泡产生,则溶液呈酸性;若无明显现象,则呈中性。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】B
5.【答案】A
6.【答案】B
7.【答案】B
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】C
13.【答案】(1)三种
(2)⑤中应加入适量稀盐酸
(3)
14.【答案】方法一:取废液少许,滴入紫色石蕊,溶液变成红色,说明显酸性,不变色,说明不显酸性。方法二:取锌粒,加入废液,有气泡生成证明是酸性溶液。方法三:用玻璃棒蘸取废液滴在pH试纸能测出溶液的pH值,若小于7,证明溶液是酸性溶液。
15.【答案】浓盐酸;浓硫酸;Ca(OH)2+CO2=CaCO3↓+H2O;2NaOH+CO2═Na2CO3+H2O
16.【答案】不应在实验室里打闹;不能在实验室里吃喝食物
17.【答案】Fe2O3;铁;火碱;放热;④
18.【答案】CaCO3+H2SO4 = CaSO4+CO2↑+H2O
19.【答案】(1)④;2
(2)BD;AC
20.【答案】(1)氧元素(填名称)
(2)固体溶解,溶液由无色变黄色; H+; SO42-; Fe3+;BC
21.【答案】(1)浓硫酸
(2)加速热量的散失
(3)酸液飞溅
22.【答案】(1)溶液变红色
(2)NaCl、NaOH
(3)锌粒(其他合理答案亦可给分)
一、单选题
1.下列曲线正确的是( )
A. 向稀硝酸中加水
B. 双氧水分解
C. 向等体积、等浓度的稀盐酸中加金属
D. 向稀硫酸中滴BaCl2溶液
2.检验某溶液是否为酸溶液,下列四种方案中错误的是( )
A.向该溶液中滴加碳酸钠溶液,看是否有气泡产生
B.向该溶液中滴加紫色石蕊溶液,看是否变红
C.向该溶液中滴加无色酚酞溶液,看是否变色
D.向该溶液中加锌粒,看是否有气泡产生
3.实验室用锌和稀硫酸制取氢气,下列操作错误的是( )
A.装置甲:稀释浓硫酸
B.装置乙:加入锌粒
C.装置丙:产生氢气
D.装置丁:收集氢气
4.如图为某品牌矿泉水标签的部分内容。下列说法错误的是( )
A.“钾、钠、锶”指的是元素 B.该矿泉水显中性
C.H2SiO3属于酸 D.该矿泉水是混合物
5.通过下列实验,能达到实验目的是( )
A.验证HCl分子发生了运动
B.验证质量守恒定律
C.验证浓硫酸遇水放热
D.验证氧气支持燃烧
6.如图所示的实验操作不正确的是( )
A. 给液体加热 B. 测溶液的pH
C. 稀释浓硫酸 D. 蒸发食盐水
7.现有下列5种物质:①浓盐酸 ②生石灰 ③浓硫酸 ④烧碱,把他们长期露置在空气中,其中会发生化学变化且质量增加的是( )
A.①、②、③ B.②、④ C.②、③、④ D.③、④、
8.下列几种溶液敞口久置于空气中,溶液的质量增加且溶质质量分数减小的是( )
A.浓盐酸 B.浓硝酸 C.浓硫酸 D.石灰水
9.下列物质的溶液长期放置在空气中,溶液质量因发生化学变化而减少的是( )
A.石灰水 B.烧碱 C.浓盐酸 D.氯化钠
10.下列知识的整理有错误的是( )
A实验方法 B化学与生活
①除去铁锈﹣﹣用稀盐酸 ②熄灭酒精灯﹣﹣用嘴吹灭 ①地壳中含量最高的元素是氧元素 ②进入久未开启的菜窖之前做灯火试验
C实验记录 D物质构成
①用10mL量筒量取8mL水 ②20mL水与20mL酒精混合体积小于40mL ①汞由汞原子构成 ②原子核一般由质子和中子构成
A.A B.B C.C D.D
11.在一定条件下,同一反应进行的快慢与反应物的溶质质量分数成正比.现在用100克溶质质量分数为30%的硫酸溶液与过量的镁粉反应,为了使反应慢点而又不影响生成氢气的总量,可以向该硫酸溶液中加入适量的( )
A.氢氧化钠 B.硫酸钾溶液 C.碳酸钠溶液 D.碱式碳酸铜
12.科学探究离不开化学实验基本操作。下列化学实验操作中,正确的是()
A. 称量固体质量
B. 移走蒸发皿
C. 稀释浓硫酸
D. 闻气体气味
二、填空题
13.除去粗盐中含有的氯化钙、氯化镁等杂质的操作有:①溶解;②加入过量的Na2CO3溶液;③加入过量的NaOH溶液;④过滤;⑤加入适量稀硫酸;⑥蒸发、结晶。
(1)过滤后溶液中的溶质有几种 。
(2)上述实验中还有不足之处,请你加以改正 。
(3)请写出加入NaOH时发生反应的化学方程式 。
14.某环保小组监测到一硫酸厂向河中非法排放酸性废液,根据你所学的知识,试设计三种检测酸性废液的方法。 。
15.现有浓盐酸、浓硫酸、氢氧化钠、石灰水四种溶液,将其长期露放在空气中,溶液质量因发生物理变化而减少的是 ,而增大的是 .因发生化学变化而减少的反应方程为 ,因发生化学变化而增大的反应的方程式 .
16.做化学实验时,应严格遵守实验室规则和操作规程.请仔细观察图,找出其中存在的安全隐患(任写两种):
① ;② .
17.如图表示五种不同类别物质间的关系.A是铁锈的主要成分,C俗称苛性钠,请结合图示回答问题.(图中“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质)
(1)A物质的化学式是 ,B物质是 .
(2)C物质的另一个俗称是 .它溶于水时会出现 (填“放热”或“吸热”)现象.
(3)在①、②、③、④四个反应中,不能体现酸的化学通性的是 (填序号).
18.“大理石”是常见的筑装饰材料,容易受到酸雨(含硫酸)的侵蚀,原因是(用化学方程式表示) 。
三、综合题
19.根据如图所示的实验操作图示回答问题.
(1)下列图示①、②、③、④操作中有错误的是 ,共有 处错误.
(2)若用⑤收集下列气体,从a通入气体可以收集 (填字母代号,下同);从b通入气体可以收集 .
A、NH3; B、CO2; C、CH4; D、SO2.
20.“宏观——微观——符号”三重表征是化学独特的表示物质及其变化的方法。请结合图示完成下列问题。
(1)Fe2O3、CO2和P2O5都含有 (填名称),且只含有两种元素,均属于氧化物。
(2)向装有一定量氧化铁粉末的试管中,加入适量稀硫酸,恰好完全反应后。
①可以观察到的现象是 。
②如图表示该反应前后溶液中存在的主要离子。请写出每种图形代表的离子(填离子符号):
。
③下列物质能与氧化铁反应,产生相似实验现象的是 (填选项)
A. 硫酸钠
B. 稀盐酸
C.食醋
D. 氢氧化钠
21.如图是稀释浓硫酸实验的示意图.
(1)量筒盛放的液体是 (填“水”或“浓硫酸”).
(2)玻璃棒搅拌的目的是 .
(3)稀释时若颠倒两种试剂的添加顺序,其后果是 .
四、实验探究题
22.如图,某同学做酸和碱的中和反应实验时,滴加盐酸前忘记先在氢氧化钠溶液中加入酚酞试液结果无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【提出猜想】①溶液可能呈中性; ②溶液可能呈酸性; ③溶液可能呈碱性。
(1)【实验探究】
实验操作 实验现象 实验结论
用试管取该溶液1-2mL,滴入1-2滴酚酞试液,振荡 溶液呈碱性
溶液颜色无明显变化 溶液呈酸性或中性
(2)【分析思考】
若溶液呈碱性,则溶液中的溶质为 (填写化学式)。
(3)若溶液颜色无明显变化,为进一步确定溶液的酸碱性,该同学提出了两种方案:
方案1:取样,用pH试纸测定,若pH<7,则溶液呈酸性;若pH=7,则呈中性。
方案2:取样,向其中加入 ,若观察到有气泡产生,则溶液呈酸性;若无明显现象,则呈中性。
答案解析部分
1.【答案】C
2.【答案】C
3.【答案】D
4.【答案】B
5.【答案】A
6.【答案】B
7.【答案】B
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】C
13.【答案】(1)三种
(2)⑤中应加入适量稀盐酸
(3)
14.【答案】方法一:取废液少许,滴入紫色石蕊,溶液变成红色,说明显酸性,不变色,说明不显酸性。方法二:取锌粒,加入废液,有气泡生成证明是酸性溶液。方法三:用玻璃棒蘸取废液滴在pH试纸能测出溶液的pH值,若小于7,证明溶液是酸性溶液。
15.【答案】浓盐酸;浓硫酸;Ca(OH)2+CO2=CaCO3↓+H2O;2NaOH+CO2═Na2CO3+H2O
16.【答案】不应在实验室里打闹;不能在实验室里吃喝食物
17.【答案】Fe2O3;铁;火碱;放热;④
18.【答案】CaCO3+H2SO4 = CaSO4+CO2↑+H2O
19.【答案】(1)④;2
(2)BD;AC
20.【答案】(1)氧元素(填名称)
(2)固体溶解,溶液由无色变黄色; H+; SO42-; Fe3+;BC
21.【答案】(1)浓硫酸
(2)加速热量的散失
(3)酸液飞溅
22.【答案】(1)溶液变红色
(2)NaCl、NaOH
(3)锌粒(其他合理答案亦可给分)
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
