辽宁省重点高中沈阳市郊联体2022-2023学年高一上学期期末考试化学试题(Word版含答案)
文档属性
| 名称 | 辽宁省重点高中沈阳市郊联体2022-2023学年高一上学期期末考试化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 813.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-12 00:00:00 | ||
图片预览


文档简介
辽宁省重点高中沈阳市郊联体
2022-2023学年度上学期期末高一年级试题
化学
一、选择题(本题共15个小题,每小题3分,共45分。每小题只有1个选项符合题意)
1.2022年北京冬奥会是碳中和的试验场,这其中从清洁能源到环保材料,化学高科技所起到的作用功不可没,下列有关说法正确的是( )
A.冬奥村餐厅大部分料理由机器人完成,制作机器人芯片的基础材料是二氧化硅
B.场馆的照明采用光伏发电技术,可减少的排放,是导致酸雨的主要气体
C.麻黄碱是一种兴奋剂,运动员可长期服用,提高成绩
D.国家速滑馆采用二氧化碳制冰技术,比传统制冷剂氟利昂更加环保
2.下列化学用语描述正确的是( )
A.的电子式:
B.可用于考古断代的一种核素的符号:
C.的结构示意图:
D.、和互称为同位素
3.下列反应的离子方程式书写正确的是( )
A.金属铁与稀盐酸反应:
B.氢氧化铜与稀反应:
C.“84”消毒液和洁厕剂不能混用,原因是:
D.三氯化铁溶液中加入铜粉:
4.在化学研究中,可以根据物质的组成、结构和反应规律等,预测元素及其化合物的性质、可能发生的化学反应,下面表格中根据事实,预测不合理的是( )
选项 事实 预测
A 钠与钾是第ⅠA族元素,它们都能与水反应 铷与钠、钾属于同族元素,铷也能与水反应
B 与形成离子键,与形成共价键 与形成共价键
C 在1500℃时分解,在230℃时分解 的分解温度介于二者之间
D 随着核电荷数递增,第ⅠA族元素单质的沸点逐渐降低 随着核电荷数递增,第ⅦA族元素单质的沸点也逐渐降低
A.A B.B C.C D.D
5.过氧化氢()溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。能与反应生成,的分子结构如图所示。下列说法错误的是( )
A.的结构式为
B.为含有极性键和非极性键的共价化合物
C.与在水溶液中反应的离子方程式为
D.与反应过程中有共价键断裂,同时有共价键和离子键形成
6.下列为除去物质中的少量杂质所选试剂不正确的是( )
选项 物质(杂质) 试剂
A 浓硫酸
B 氢氧化钾溶液
C 水
D 品红溶液
A.A B.B C.C D.D
7.现有短周期主族元素X、Y、Z、W,其中X、Y、Z在元素周期表中的相对位置关系如图,且X、Y、Z的原子序数之和为32,W原子的最外层电子数是其次外层电子数的2倍,下列说法错误的是( )
X Z
Y
A.X、W的氧化物均不止一种
B.原子半径:
C.化合物中所有原子的最外层均达到8电子稳定结构
D.常温常压下X元素的最简单氢化物为液体
8.下列说法中正确的是( )
A.中的化合价为价
B.铁与水蒸气在高温条件下,生成红棕色固体
C.鉴别碳酸钠溶液与碳酸氢钠溶液,可以选用澄清的石灰水
D.向氯化铝溶液中加入过量氨水,可制得氢氧化铝
9.下列物质① ② ③ ④ ⑤ ⑥中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A.①③⑤⑥ B.③④⑤⑥ C.①②③④ D.②③⑤⑥
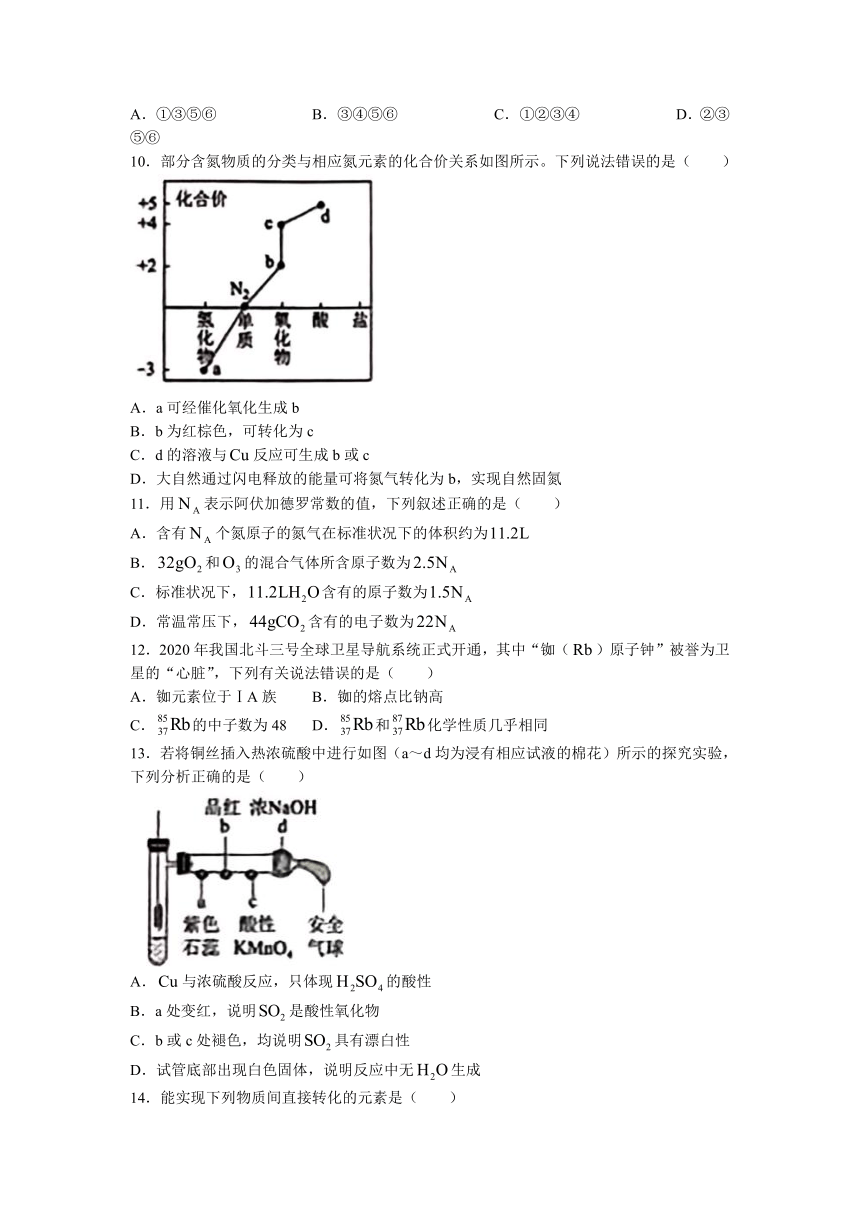
10.部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法错误的是( )
A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.d的溶液与反应可生成b或c
D.大自然通过闪电释放的能量可将氮气转化为b,实现自然固氮
11.用表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有个氮原子的氮气在标准状况下的体积约为
B.和的混合气体所含原子数为
C.标准状况下,含有的原子数为
D.常温常压下,含有的电子数为
12.2020年我国北斗三号全球卫星导航系统正式开通,其中“铷()原子钟”被誉为卫星的“心脏”,下列有关说法错误的是( )
A.铷元素位于ⅠA族 B.铷的熔点比钠高
C.的中子数为48 D.和化学性质几乎相同
13.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A.与浓硫酸反应,只体现的酸性
B.a处变红,说明是酸性氧化物
C.b或c处褪色,均说明具有漂白性
D.试管底部出现白色固体,说明反应中无生成
14.能实现下列物质间直接转化的元素是( )
A. B.S C. D.
15.溴化钾()可作为分析试剂、感光剂、神经镇静剂等,工业上制取溴化钾的方法之一为:先将尿素()加到溶液中,然后在不断搅拌下缓慢注入液溴,随即发生反应:。
下列有关此反应的说法正确的是( )
A.尿素作还原剂,、是氧化产物
B.若制取,转移电子数目为
C.此方法成本低,且制得的纯净
D.实验室中密封保存在无色广口瓶中
第Ⅱ卷 非选择题(共55分)
16.(14分)化学是一门实用性很强的科学,请根据题意填空:
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装__________(填“浓硫酸”或“浓盐酸”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是__________(填化学式)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的和反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:。
(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:
①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是__________(填字母序号).
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的__________(填“强”或“弱”),空气中,铝比铁具有更好的抗腐蚀性,原因是__________(用化学反应方程式解释)。
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(),该化合物中硅元素的化合价为__________。
17.(14分)为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”,元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素,请按题目要求回答下列问题:
(1)①~⑦对应元素中,非金属性最强的元素名称是__________;⑤在周期表中的位置为__________。
(2)②与③形成化合物的电子式为__________;①的最高价氧化物的结构式为__________。
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是__________(用化学式来回答)。
写出③、④两种元素最高价氧化物对应水化物反应的离子方程式__________。
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是__________(填对应的序号)。
18.(14分)人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产。某化学兴趣小组在实验室利用如图装置制备氨气并探究相关性质。
(1)该实验中A装置制备的化学方程式是__________。
(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是__________(填装置序号)。
(3)若将D与a相连,在E中产生白色沉淀,其化学式为:__________。若向a处单独通入__________(填下列气体字母编号),在E中也会产生白色沉淀。
A. B. C. D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体.
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:__________;若充分反应后红色固体有剩余,再加入下列的__________(填字母)试剂,固体又可以继续溶解。
A.稀 B.溶液 C.溶液 D.溶液
②已知也为红色固体,若反应前C中质量为,反应后C中红色固体质量为,则C中发生的总反应化学方程式为:__________.
19.(13分)我国近代化学工业的奠基人之一侯德榜发明的“侯氏制碱法”,将制碱技术发展到了一个新的水平,在此基础上,将工业纯碱(含、等杂质)进行提纯。工艺流程如下:
请回答下列问题。
(1)上述物质中属于酸式盐的是__________.
(2)“操作1”的名称是__________,需用到的玻璃仪器有烧杯、玻璃棒、__________。
(3)反应Ⅱ的化学方程式是__________.
(4)流程中加入除去的杂质离子是__________.
(5)结晶后的晶体表面附着有、等杂质.
①检验该晶体中是否含有氯离子杂质的操作方法是__________.
②取纯碱样品溶解后再加入足量稀硫酸,得到(全部逸出)。则样品中纯碱的质量分数为__________%(计算结果保留两位小数).
沈阳市郊联体2022-2023学年度上学期高一年级
期末考试化学试题答案
选择题1—15 DDCDD DDDAB DBBBC
每空2分,共14分
(1) 浓硫酸 (2)SiO2 (3)N2
(4) ①A ② 强 4Al+3O2=2Al2O3 ③+4
17. 每空2分,共14分
(1) 氟 第三周期ⅤⅠA族
(2) (全用“×”或全用“·”均可) O=C=O
(3)KOH>NaOH>Al(OH)3 Al(OH)3 +OH-=AlO2-+2H2O
(4)④、⑦
18. 每空2分,共14分
(1)Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O (条件不写扣1分,下同)
(2)②③
(3) AB
(4) ①(浓) (“浓”不写不给分 ) BD
②2NH3+4CuO2Cu+Cu2O+N2+3H2O
除注明外每空2分,共13分
(1) (2) 过滤 漏斗或普通漏斗(1分)
(3) (4)
(5) ①取少量该晶体于试管中,加入足量稀硝酸酸化,再加入2-3滴溶液,若无白色沉淀产生,说明不存在杂质,反之,存在
② 96.95
2022-2023学年度上学期期末高一年级试题
化学
一、选择题(本题共15个小题,每小题3分,共45分。每小题只有1个选项符合题意)
1.2022年北京冬奥会是碳中和的试验场,这其中从清洁能源到环保材料,化学高科技所起到的作用功不可没,下列有关说法正确的是( )
A.冬奥村餐厅大部分料理由机器人完成,制作机器人芯片的基础材料是二氧化硅
B.场馆的照明采用光伏发电技术,可减少的排放,是导致酸雨的主要气体
C.麻黄碱是一种兴奋剂,运动员可长期服用,提高成绩
D.国家速滑馆采用二氧化碳制冰技术,比传统制冷剂氟利昂更加环保
2.下列化学用语描述正确的是( )
A.的电子式:
B.可用于考古断代的一种核素的符号:
C.的结构示意图:
D.、和互称为同位素
3.下列反应的离子方程式书写正确的是( )
A.金属铁与稀盐酸反应:
B.氢氧化铜与稀反应:
C.“84”消毒液和洁厕剂不能混用,原因是:
D.三氯化铁溶液中加入铜粉:
4.在化学研究中,可以根据物质的组成、结构和反应规律等,预测元素及其化合物的性质、可能发生的化学反应,下面表格中根据事实,预测不合理的是( )
选项 事实 预测
A 钠与钾是第ⅠA族元素,它们都能与水反应 铷与钠、钾属于同族元素,铷也能与水反应
B 与形成离子键,与形成共价键 与形成共价键
C 在1500℃时分解,在230℃时分解 的分解温度介于二者之间
D 随着核电荷数递增,第ⅠA族元素单质的沸点逐渐降低 随着核电荷数递增,第ⅦA族元素单质的沸点也逐渐降低
A.A B.B C.C D.D
5.过氧化氢()溶液俗称双氧水,医疗上常用3%的双氧水进行伤口消毒。能与反应生成,的分子结构如图所示。下列说法错误的是( )
A.的结构式为
B.为含有极性键和非极性键的共价化合物
C.与在水溶液中反应的离子方程式为
D.与反应过程中有共价键断裂,同时有共价键和离子键形成
6.下列为除去物质中的少量杂质所选试剂不正确的是( )
选项 物质(杂质) 试剂
A 浓硫酸
B 氢氧化钾溶液
C 水
D 品红溶液
A.A B.B C.C D.D
7.现有短周期主族元素X、Y、Z、W,其中X、Y、Z在元素周期表中的相对位置关系如图,且X、Y、Z的原子序数之和为32,W原子的最外层电子数是其次外层电子数的2倍,下列说法错误的是( )
X Z
Y
A.X、W的氧化物均不止一种
B.原子半径:
C.化合物中所有原子的最外层均达到8电子稳定结构
D.常温常压下X元素的最简单氢化物为液体
8.下列说法中正确的是( )
A.中的化合价为价
B.铁与水蒸气在高温条件下,生成红棕色固体
C.鉴别碳酸钠溶液与碳酸氢钠溶液,可以选用澄清的石灰水
D.向氯化铝溶液中加入过量氨水,可制得氢氧化铝
9.下列物质① ② ③ ④ ⑤ ⑥中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A.①③⑤⑥ B.③④⑤⑥ C.①②③④ D.②③⑤⑥
10.部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法错误的是( )
A.a可经催化氧化生成b
B.b为红棕色,可转化为c
C.d的溶液与反应可生成b或c
D.大自然通过闪电释放的能量可将氮气转化为b,实现自然固氮
11.用表示阿伏加德罗常数的值,下列叙述正确的是( )
A.含有个氮原子的氮气在标准状况下的体积约为
B.和的混合气体所含原子数为
C.标准状况下,含有的原子数为
D.常温常压下,含有的电子数为
12.2020年我国北斗三号全球卫星导航系统正式开通,其中“铷()原子钟”被誉为卫星的“心脏”,下列有关说法错误的是( )
A.铷元素位于ⅠA族 B.铷的熔点比钠高
C.的中子数为48 D.和化学性质几乎相同
13.若将铜丝插入热浓硫酸中进行如图(a~d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是( )
A.与浓硫酸反应,只体现的酸性
B.a处变红,说明是酸性氧化物
C.b或c处褪色,均说明具有漂白性
D.试管底部出现白色固体,说明反应中无生成
14.能实现下列物质间直接转化的元素是( )
A. B.S C. D.
15.溴化钾()可作为分析试剂、感光剂、神经镇静剂等,工业上制取溴化钾的方法之一为:先将尿素()加到溶液中,然后在不断搅拌下缓慢注入液溴,随即发生反应:。
下列有关此反应的说法正确的是( )
A.尿素作还原剂,、是氧化产物
B.若制取,转移电子数目为
C.此方法成本低,且制得的纯净
D.实验室中密封保存在无色广口瓶中
第Ⅱ卷 非选择题(共55分)
16.(14分)化学是一门实用性很强的科学,请根据题意填空:
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装__________(填“浓硫酸”或“浓盐酸”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是__________(填化学式)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的和反应转化为无污染的物质,请完成一定条件下该反应的化学方程式:。
(4)“厉害了,我的国”,2017年4月:“天舟一号”成功对接,12月:大型客机C919(如下图)第二次在上海浦东机场试飞成功,实现了我国航空领域的新突破。
请回答下列问题:
①铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是__________(填字母序号).
A.密度小 强度好 B.密度大 硬度大 C.熔点低 硬度小
②铝的金属活动性比铁的__________(填“强”或“弱”),空气中,铝比铁具有更好的抗腐蚀性,原因是__________(用化学反应方程式解释)。
③高温结构陶瓷可用于制造汽车发动机,通常所用的材料是氮化硅(),该化合物中硅元素的化合价为__________。
17.(14分)为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”,元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素,请按题目要求回答下列问题:
(1)①~⑦对应元素中,非金属性最强的元素名称是__________;⑤在周期表中的位置为__________。
(2)②与③形成化合物的电子式为__________;①的最高价氧化物的结构式为__________。
(3)③、④、⑥三种元素最高价氧化物对应的水化物的碱性由强到弱的顺序是__________(用化学式来回答)。
写出③、④两种元素最高价氧化物对应水化物反应的离子方程式__________。
(4)①~⑦对应元素中,位于金属与非金属的分界线附近的是__________(填对应的序号)。
18.(14分)人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料生产。某化学兴趣小组在实验室利用如图装置制备氨气并探究相关性质。
(1)该实验中A装置制备的化学方程式是__________。
(2)D装置后接尾气吸收装置。下列能用来吸收尾气的装置是__________(填装置序号)。
(3)若将D与a相连,在E中产生白色沉淀,其化学式为:__________。若向a处单独通入__________(填下列气体字母编号),在E中也会产生白色沉淀。
A. B. C. D.
(4)实验发现C中粉末完全变红,D中无水硫酸铜变蓝,还产生一种单质气体.
①若红色固体为单质,实验后将C中固体与浓硫酸混合加热,其化学方程式为:__________;若充分反应后红色固体有剩余,再加入下列的__________(填字母)试剂,固体又可以继续溶解。
A.稀 B.溶液 C.溶液 D.溶液
②已知也为红色固体,若反应前C中质量为,反应后C中红色固体质量为,则C中发生的总反应化学方程式为:__________.
19.(13分)我国近代化学工业的奠基人之一侯德榜发明的“侯氏制碱法”,将制碱技术发展到了一个新的水平,在此基础上,将工业纯碱(含、等杂质)进行提纯。工艺流程如下:
请回答下列问题。
(1)上述物质中属于酸式盐的是__________.
(2)“操作1”的名称是__________,需用到的玻璃仪器有烧杯、玻璃棒、__________。
(3)反应Ⅱ的化学方程式是__________.
(4)流程中加入除去的杂质离子是__________.
(5)结晶后的晶体表面附着有、等杂质.
①检验该晶体中是否含有氯离子杂质的操作方法是__________.
②取纯碱样品溶解后再加入足量稀硫酸,得到(全部逸出)。则样品中纯碱的质量分数为__________%(计算结果保留两位小数).
沈阳市郊联体2022-2023学年度上学期高一年级
期末考试化学试题答案
选择题1—15 DDCDD DDDAB DBBBC
每空2分,共14分
(1) 浓硫酸 (2)SiO2 (3)N2
(4) ①A ② 强 4Al+3O2=2Al2O3 ③+4
17. 每空2分,共14分
(1) 氟 第三周期ⅤⅠA族
(2) (全用“×”或全用“·”均可) O=C=O
(3)KOH>NaOH>Al(OH)3 Al(OH)3 +OH-=AlO2-+2H2O
(4)④、⑦
18. 每空2分,共14分
(1)Ca(OH)2+2NH4ClCaCl2+2NH3↑+2H2O (条件不写扣1分,下同)
(2)②③
(3) AB
(4) ①(浓) (“浓”不写不给分 ) BD
②2NH3+4CuO2Cu+Cu2O+N2+3H2O
除注明外每空2分,共13分
(1) (2) 过滤 漏斗或普通漏斗(1分)
(3) (4)
(5) ①取少量该晶体于试管中,加入足量稀硝酸酸化,再加入2-3滴溶液,若无白色沉淀产生,说明不存在杂质,反之,存在
② 96.95
同课章节目录
