化学人教版(2019)选择性必修3 3.2.1醇 课件(共25张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.2.1醇 课件(共25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 524.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-12 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
第二章 烃和卤代烃
第二节 醇和酚
第1课时 醇
1.什么叫烃的衍生物 如果烃分子中的氢原子被-OH取代产物是什么
2.溴乙烷在氢氧化钠水溶液中加热生成
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
烃分子中的氢原子被含有氧的原子团取代得到的化合物称为烃的含氧衍生物。烃分子中的氢原子被-OH取代产物是醇
羟基化合物
醇
酚
链烃基与羟基相连而成
苯环与羟基直接相连而成
可分为一元羟基化合物和多元羟基化合物
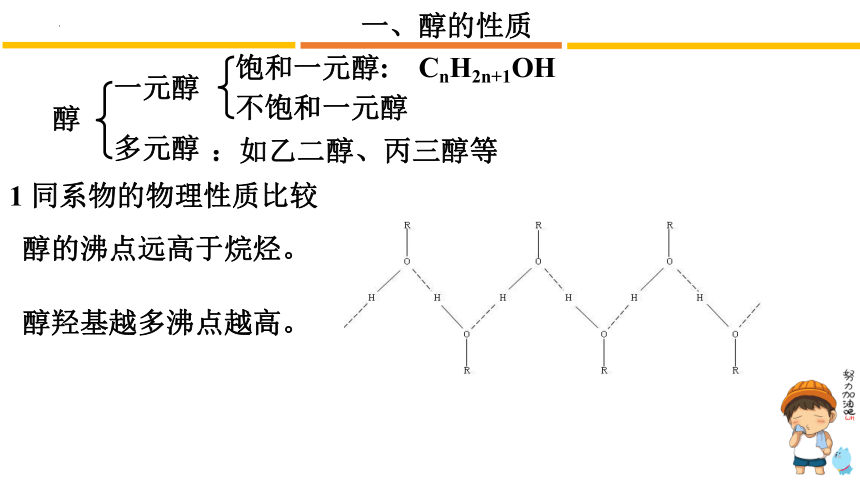
一、醇的性质
醇
一元醇
多元醇
饱和一元醇:
不饱和一元醇
CnH2n+1OH
:如乙二醇、丙三醇等
1 同系物的物理性质比较
醇的沸点远高于烷烃。
醇羟基越多沸点越高。
(1)沸点:b.饱和一元醇的沸点随分子中碳原子数的增加而逐渐升高
c.若同碳数时,羟基数越多沸点越高。
(2)溶解性:低级醇如甲醇、乙醇、丙醇能与水形成氢键,故与水可以任意比互溶,但随着碳原子数增大,烃基增大,羟基在分子中的比例减少,而不溶于水、易溶于有机溶剂。
(3)密度:饱和一元醇的密度比水的密度小。
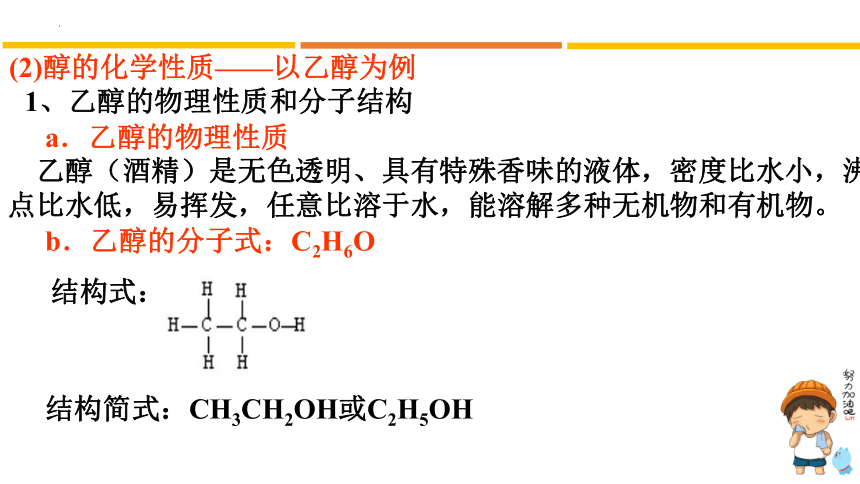
(2)醇的化学性质——以乙醇为例
1、乙醇的物理性质和分子结构
a.乙醇的物理性质
乙醇(酒精)是无色透明、具有特殊香味的液体,密度比水小,沸点比水低,易挥发,任意比溶于水,能溶解多种无机物和有机物。
b.乙醇的分子式:C2H6O
结构简式:CH3CH2OH或C2H5OH
结构式:
H
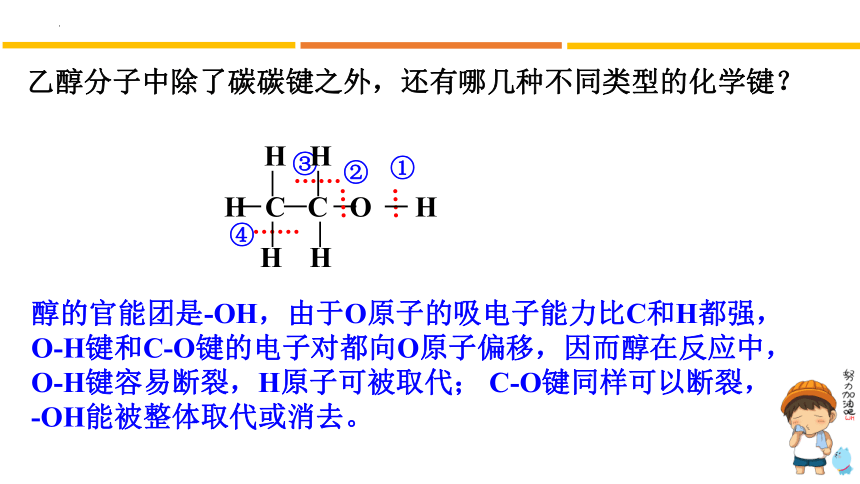
乙醇分子中除了碳碳键之外,还有哪几种不同类型的化学键?
②
①
③
④
醇的官能团是-OH,由于O原子的吸电子能力比C和H都强, O-H键和C-O键的电子对都向O原子偏移,因而醇在反应中, O-H键容易断裂,H原子可被取代; C-O键同样可以断裂,-OH能被整体取代或消去。
C C O H
H
H
H
H
2、乙醇的化学性质
2CH3CH2-OH +2Na →2CH3CH2ONa +H2↑
1) 乙醇与钠反应
产物乙醇钠在水中强烈水解
CH3CH2-ONa +H2O→CH3CH2OH +NaOH
练习:写出乙醇与K反应的化学方程式
现象:缓慢产生气泡,金属钠沉于底部或上下浮动。
活泼金属与醇类反应的规律
2-OH ~2Na ~H2
2CH3CH2-OH +2K →2CH3CH2OK +H2↑
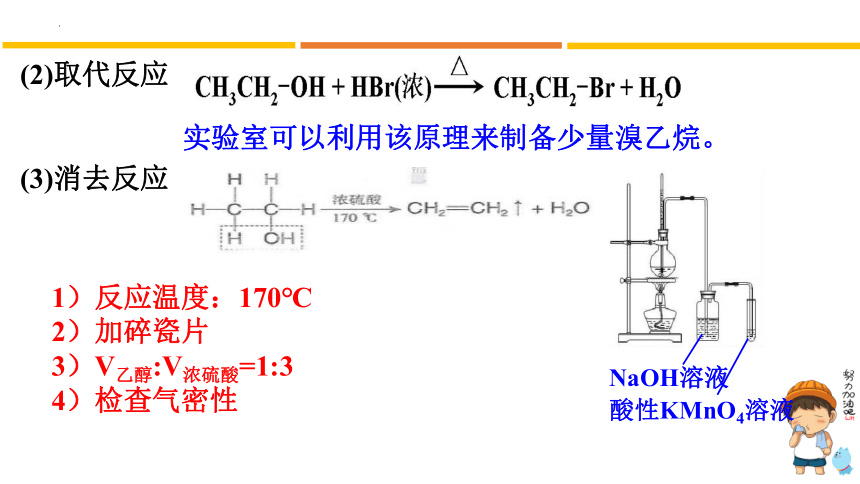
实验室可以利用该原理来制备少量溴乙烷。
(2)取代反应
(3)消去反应
1)反应温度:170℃
2)加碎瓷片
3)V乙醇:V浓硫酸=1:3
4)检查气密性
NaOH溶液
酸性KMnO4溶液
① 混合液颜色如何变化?为什么?
烧瓶中的液体逐渐变黑。因为浓硫酸有多种特性。在加热的条件下,无水酒精和浓硫酸混合物的反应除可生成乙烯等物质以外,浓硫酸还能将无水酒精氧化生成碳的单质等多种物质,碳的单质使烧瓶内的液体带上了黑色。
思考
②温度计的位置?
温度计感温泡要置于反应物的中央位置因为需要测量的是反应物的温度。
③有何杂质气体?如何除去?
由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通过碱石灰。
副反应:分子间脱水
2CH3CH2-OH CH3CH2-O-CH2CH3+H2O
140℃
浓H2SO4
拓展练习:—— 醇的消去反应及条件
1.写出下列化学反应方程式
CH3-CH2-CH-CH3
OH
浓硫酸
△
浓硫酸
△
CH2-CH2-CH2-CH2
OH
OH
结论:醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发生消去反应,外部条件:浓硫酸、加热到170℃
H2O+CH3-CH=CH-CH3↑
2H2O+CH2=CH-CH=CH2 ↑
(4)乙醇的氧化反应
2CO2 +3H2O
C2H5OH +3 O2
点燃
①燃烧氧化
②催化氧化
实验现象:
1、铜丝在酒精灯上灼烧后,铜丝变黑;
2、趁热伸入乙醇中发现铜丝变红;
3、反复多次,闻到刺激性气味。
拓展练习:—— 醇的催化氧化产物书写和条件
结论:羟基碳上有2个氢原子的醇被氧化成醛;羟基碳上有1个氢原子的醇被氧化成酮。羟基碳上没有氢原子的醇不能被氧化。
CHO
CH3-C-CH3
O
不反应
③被强氧化剂KMnO4或K2Cr2O7氧化
反应原理:CH3CH2OH→CH3CHO → CH3COOH
乙醇
乙醛
乙酸
实验现象:紫色褪去溶液或由橙黄色变为绿色
氧化反应:有机物分子中失去氢原子或加入氧原子的反应叫做氧化反应。
举例:
CH3CH2OH→CH3CHO ,失去氢原子;
CH3CHO→CH3COOH,加入氧原子。
还原反应:有机物分子中加入氢原子或失去氧原子的反应叫做还原反应。
举例:
CH3CHO→CH3CH2OH ,加入氢原子;
CH3COOH→CH3CHO ,失去氧原子。
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应
消去反应
催化氧化
小结
①
卤代烃和醇消去反应的比较
乙醇可以发生消去反应,醇类都有类似的性质。写出下列各醇发生消去反应的产物。
CH3-CH2-CH-CH3
OH
仲醇:
伯醇:CH3-CH2-CH2-CH2-OH
CH3-CH2-C-CH3
OH
CH3
叔醇:
CH3-CH2-CH=CH2
CH3-CH2-CH=CH2
CH3-CH=CH-CH3
CH3-CH2=C-CH3
CH3
CH3-CH2-C=CH2
CH3
C.将 与CH3CH2OH在浓H2SO4存在下加热,最多可生成 3种有机产物
D.醇类在一定条件下都能与氢卤酸反应生成卤代烃
例4 下列说法中,正确的是
A.醇类在一定条件下都能发生消去反应生成烯烃
B.CH3OH、CH3CH2OH、
都能在铜催化下发生氧化反应
D
醇类
1.醇的概念: R-OH
2. 饱和一元醇的化学通式 CnH2n+2O
多元醇的化学通式 CnH2n+2O2 CnH2n+2O3
知识小结
3.分类
饱和醇和不饱和醇
一元醇和多元醇
脂肪醇和芳香醇
4 几种重要的醇
⑴甲醇
⑵乙二醇
⑶丙三醇
俗称:木醇 有毒
无色、粘稠、有甜味的液体,
易溶于水,
凝固点低,可做内燃机的抗冻剂
俗称:甘油
无色、粘稠、有甜味的液体,吸湿性强
与水以任意比例混溶 可制成硝化甘油——烈性炸药,可做防冻剂、润滑剂
5、化学性质:
⑴与金属钠反应:
在反应中饱和一元醇和产生的氢气存在着怎样的定量关系呢?
CH2-OH
请写出 与金属钠反应的化学方程式
CH2-OH
CH2-OH CH2-ONa
+ 2Na → +H2↑
CH2-OH CH2-ONa
2(-OH ) → H2↑
⑵与HX反应:
⑶燃烧:
⑷催化氧化:
CnH2n+1OH + HX → CnH2n+1X + H2O
CnH2n+1OH + O2 → CO2 + H2O
(3n/2) n (n+1)
连有羟基的碳原子上连有二个氢原子被氧化成醛。
连有羟基的碳原子上连有一个氢原子被氧化成酮。
连有羟基的碳原子上连没有氢原子则不能被氧化。
⑸消去反应:
连有羟基的相邻碳原子上必需连有氢原子, 否则不能消去反应。
炔 醛
烯 卤代烃
醇
粮食 酯
引人-OH的方法——反应原理:
一卤代物生成二卤代物再生成二元醇;
【练习1】下列醇类物质不能发生催化氧化的是( )
A. CH3CH2CH2OH B. CH3OH
C. (CH3)2CHOH D. (CH3)3COH
D
【注意】 醇发生催化氧化的条件:和羟基相连的碳上必须有氢
第二章 烃和卤代烃
第二节 醇和酚
第1课时 醇
1.什么叫烃的衍生物 如果烃分子中的氢原子被-OH取代产物是什么
2.溴乙烷在氢氧化钠水溶液中加热生成
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
烃分子中的氢原子被含有氧的原子团取代得到的化合物称为烃的含氧衍生物。烃分子中的氢原子被-OH取代产物是醇
羟基化合物
醇
酚
链烃基与羟基相连而成
苯环与羟基直接相连而成
可分为一元羟基化合物和多元羟基化合物
一、醇的性质
醇
一元醇
多元醇
饱和一元醇:
不饱和一元醇
CnH2n+1OH
:如乙二醇、丙三醇等
1 同系物的物理性质比较
醇的沸点远高于烷烃。
醇羟基越多沸点越高。
(1)沸点:b.饱和一元醇的沸点随分子中碳原子数的增加而逐渐升高
c.若同碳数时,羟基数越多沸点越高。
(2)溶解性:低级醇如甲醇、乙醇、丙醇能与水形成氢键,故与水可以任意比互溶,但随着碳原子数增大,烃基增大,羟基在分子中的比例减少,而不溶于水、易溶于有机溶剂。
(3)密度:饱和一元醇的密度比水的密度小。
(2)醇的化学性质——以乙醇为例
1、乙醇的物理性质和分子结构
a.乙醇的物理性质
乙醇(酒精)是无色透明、具有特殊香味的液体,密度比水小,沸点比水低,易挥发,任意比溶于水,能溶解多种无机物和有机物。
b.乙醇的分子式:C2H6O
结构简式:CH3CH2OH或C2H5OH
结构式:
H
乙醇分子中除了碳碳键之外,还有哪几种不同类型的化学键?
②
①
③
④
醇的官能团是-OH,由于O原子的吸电子能力比C和H都强, O-H键和C-O键的电子对都向O原子偏移,因而醇在反应中, O-H键容易断裂,H原子可被取代; C-O键同样可以断裂,-OH能被整体取代或消去。
C C O H
H
H
H
H
2、乙醇的化学性质
2CH3CH2-OH +2Na →2CH3CH2ONa +H2↑
1) 乙醇与钠反应
产物乙醇钠在水中强烈水解
CH3CH2-ONa +H2O→CH3CH2OH +NaOH
练习:写出乙醇与K反应的化学方程式
现象:缓慢产生气泡,金属钠沉于底部或上下浮动。
活泼金属与醇类反应的规律
2-OH ~2Na ~H2
2CH3CH2-OH +2K →2CH3CH2OK +H2↑
实验室可以利用该原理来制备少量溴乙烷。
(2)取代反应
(3)消去反应
1)反应温度:170℃
2)加碎瓷片
3)V乙醇:V浓硫酸=1:3
4)检查气密性
NaOH溶液
酸性KMnO4溶液
① 混合液颜色如何变化?为什么?
烧瓶中的液体逐渐变黑。因为浓硫酸有多种特性。在加热的条件下,无水酒精和浓硫酸混合物的反应除可生成乙烯等物质以外,浓硫酸还能将无水酒精氧化生成碳的单质等多种物质,碳的单质使烧瓶内的液体带上了黑色。
思考
②温度计的位置?
温度计感温泡要置于反应物的中央位置因为需要测量的是反应物的温度。
③有何杂质气体?如何除去?
由于无水酒精和浓硫酸发生的氧化还原反应,反应制得的乙烯中往往混有H2O、CO2、SO2等气体。可将气体通过碱石灰。
副反应:分子间脱水
2CH3CH2-OH CH3CH2-O-CH2CH3+H2O
140℃
浓H2SO4
拓展练习:—— 醇的消去反应及条件
1.写出下列化学反应方程式
CH3-CH2-CH-CH3
OH
浓硫酸
△
浓硫酸
△
CH2-CH2-CH2-CH2
OH
OH
结论:醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,并且此相邻的碳原子上必须连有氢原子时,才可发生消去反应,外部条件:浓硫酸、加热到170℃
H2O+CH3-CH=CH-CH3↑
2H2O+CH2=CH-CH=CH2 ↑
(4)乙醇的氧化反应
2CO2 +3H2O
C2H5OH +3 O2
点燃
①燃烧氧化
②催化氧化
实验现象:
1、铜丝在酒精灯上灼烧后,铜丝变黑;
2、趁热伸入乙醇中发现铜丝变红;
3、反复多次,闻到刺激性气味。
拓展练习:—— 醇的催化氧化产物书写和条件
结论:羟基碳上有2个氢原子的醇被氧化成醛;羟基碳上有1个氢原子的醇被氧化成酮。羟基碳上没有氢原子的醇不能被氧化。
CHO
CH3-C-CH3
O
不反应
③被强氧化剂KMnO4或K2Cr2O7氧化
反应原理:CH3CH2OH→CH3CHO → CH3COOH
乙醇
乙醛
乙酸
实验现象:紫色褪去溶液或由橙黄色变为绿色
氧化反应:有机物分子中失去氢原子或加入氧原子的反应叫做氧化反应。
举例:
CH3CH2OH→CH3CHO ,失去氢原子;
CH3CHO→CH3COOH,加入氧原子。
还原反应:有机物分子中加入氢原子或失去氧原子的反应叫做还原反应。
举例:
CH3CHO→CH3CH2OH ,加入氢原子;
CH3COOH→CH3CHO ,失去氧原子。
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应
消去反应
催化氧化
小结
①
卤代烃和醇消去反应的比较
乙醇可以发生消去反应,醇类都有类似的性质。写出下列各醇发生消去反应的产物。
CH3-CH2-CH-CH3
OH
仲醇:
伯醇:CH3-CH2-CH2-CH2-OH
CH3-CH2-C-CH3
OH
CH3
叔醇:
CH3-CH2-CH=CH2
CH3-CH2-CH=CH2
CH3-CH=CH-CH3
CH3-CH2=C-CH3
CH3
CH3-CH2-C=CH2
CH3
C.将 与CH3CH2OH在浓H2SO4存在下加热,最多可生成 3种有机产物
D.醇类在一定条件下都能与氢卤酸反应生成卤代烃
例4 下列说法中,正确的是
A.醇类在一定条件下都能发生消去反应生成烯烃
B.CH3OH、CH3CH2OH、
都能在铜催化下发生氧化反应
D
醇类
1.醇的概念: R-OH
2. 饱和一元醇的化学通式 CnH2n+2O
多元醇的化学通式 CnH2n+2O2 CnH2n+2O3
知识小结
3.分类
饱和醇和不饱和醇
一元醇和多元醇
脂肪醇和芳香醇
4 几种重要的醇
⑴甲醇
⑵乙二醇
⑶丙三醇
俗称:木醇 有毒
无色、粘稠、有甜味的液体,
易溶于水,
凝固点低,可做内燃机的抗冻剂
俗称:甘油
无色、粘稠、有甜味的液体,吸湿性强
与水以任意比例混溶 可制成硝化甘油——烈性炸药,可做防冻剂、润滑剂
5、化学性质:
⑴与金属钠反应:
在反应中饱和一元醇和产生的氢气存在着怎样的定量关系呢?
CH2-OH
请写出 与金属钠反应的化学方程式
CH2-OH
CH2-OH CH2-ONa
+ 2Na → +H2↑
CH2-OH CH2-ONa
2(-OH ) → H2↑
⑵与HX反应:
⑶燃烧:
⑷催化氧化:
CnH2n+1OH + HX → CnH2n+1X + H2O
CnH2n+1OH + O2 → CO2 + H2O
(3n/2) n (n+1)
连有羟基的碳原子上连有二个氢原子被氧化成醛。
连有羟基的碳原子上连有一个氢原子被氧化成酮。
连有羟基的碳原子上连没有氢原子则不能被氧化。
⑸消去反应:
连有羟基的相邻碳原子上必需连有氢原子, 否则不能消去反应。
炔 醛
烯 卤代烃
醇
粮食 酯
引人-OH的方法——反应原理:
一卤代物生成二卤代物再生成二元醇;
【练习1】下列醇类物质不能发生催化氧化的是( )
A. CH3CH2CH2OH B. CH3OH
C. (CH3)2CHOH D. (CH3)3COH
D
【注意】 醇发生催化氧化的条件:和羟基相连的碳上必须有氢
