2.2 碱及其性质 同步练习 (含答案)2022-2023学年鲁教版(五四制)九年级全册化学
文档属性
| 名称 | 2.2 碱及其性质 同步练习 (含答案)2022-2023学年鲁教版(五四制)九年级全册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 105.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-11 16:37:00 | ||
图片预览



文档简介
2.2 碱及其性质 同步练习 2022-2023学年九年级全册化学
一、单选题
1.在实验室中,下列物质具有强烈腐蚀性的是( )
A.稀HCl B.NaCl溶液
C.KNO3溶液 D.98%的浓H2SO4
2.在化学实验中必须注意安全操作:① 在点燃H2、CO、CH4等可燃性气体前,必须检验气体的纯度② 在稀释浓硫酸时将水沿器壁慢慢注入浓硫酸中,并用玻璃棒搅拌③ 浓硫酸不慎滴到皮肤上,应立即用大量水冲洗,再用3-5%的NaHCO3溶液涂上④ 给试管中液体加热,液体一般不超过试管容积的1/3
⑤ 可以向燃着的酒精灯中添加酒精
上述说法中正确的是( )
A.①② B.②⑤ C.③⑤ D.①③④
3.为除去下列物质中的杂质(括号里为杂质),选用的试剂和操作方法都正确的是( )
序号 物质 选用试剂 操作方法
A CO2气体(HCl) NaOH溶液 洗气
B FeSO4(CuSO4) Al粉 加入过量Al粉,过滤
C KNO3固体(KOH) H2O、CuSO4溶液 溶解、过滤、蒸发结晶
D NaCl固体(MgCl2) H2O、NaOH溶液、盐酸 溶解、加过量NaOH溶液、过滤、加过量盐酸、蒸发结晶
A.A B.B C.C D.D
4.下列叙述正确的是()
A.氦气常用作保护气
B.氧化钙的俗称熟石灰
C.盐酸能用作厨房清洁剂
D.煤炉上放一盆水可以防止煤气中毒
5.下列物质的鉴别方法错误的是( )
A.用肥皂水鉴别软水和硬水
B.用带火星的木条鉴别空气和氧气
C.用灼烧法鉴别棉纤维和羊毛纤维
D.用酚酞溶液鉴别稀盐酸和稀硫酸
6.推理是化学学习中常用的思维方法,下面推理中正确的是( )
A.碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
B.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
C.酸中都有氢元素,所以含有氢元素的化合物一定是酸
D.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱反应
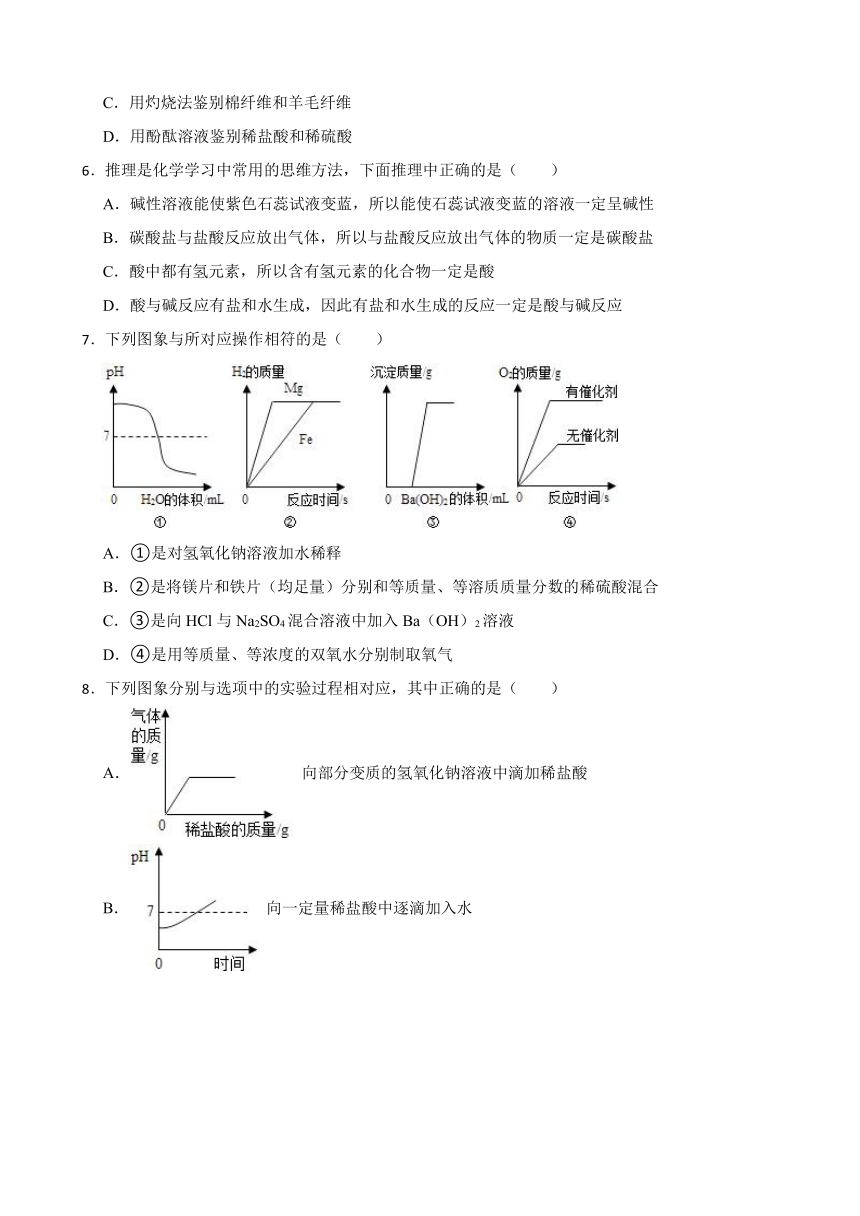
7.下列图象与所对应操作相符的是( )
A.①是对氢氧化钠溶液加水稀释
B.②是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.③是向HCl与Na2SO4混合溶液中加入Ba(OH)2溶液
D.④是用等质量、等浓度的双氧水分别制取氧气
8.下列图象分别与选项中的实验过程相对应,其中正确的是( )
A. 向部分变质的氢氧化钠溶液中滴加稀盐酸
B. 向一定量稀盐酸中逐滴加入水
C. 常温下,等质量的锌和铁分别与足量同溶质质量分数的稀硫酸反应
D. 电解水生成气体的体积
9.下列有关物质混合后的现象描述中,正确的是( )
A.在无色碘化钾溶液中滴加淀粉溶液,溶液变蓝
B.无色的氯化氢气体和氨气混合,产生白雾
C.在氢氧化钠稀溶液中滴加数滴硫酸铜溶液,产生蓝色絮状沉淀
D.铵盐与碱溶液混合加热,产生的气体使湿润的蓝色石蕊试纸变红
10.下列除杂设计(括号内为杂质)所选用试剂和操作都正确的是( )
序号 物 质 选用试剂 操作
A CO2(CO) O2 点燃
B NaOH溶液(Na2CO3) 稀盐酸 加入试剂至不再产生气泡
C KNO3溶液(KOH) CuSO4溶液 加入适量的试剂,充分反应后过滤
D NaCl固体(泥沙) H2O 溶解、过滤、洗涤、蒸发
A.A B.B C.C D.D
11.下列物质的应用中,不正确的是( )
A.将硝酸铵溶于水制作热敷袋
B.用汽油或加了洗涤剂的水都能除去衣服上的油污
C.把池水喷向空中,可以增加养鱼池水中氧气的溶解量
D.用Ca(OH)2改良酸性土壤
12.下列事实解释不正确的是( )
选项 事 实 解释
A NaOH 和Ca(OH)2的性质相似 Na+和Ca2+的性质相似
B 氢气、木炭、一氧化碳都可以冶炼金属 它们都具有还原性
C 给装满水的纸杯加热,开始时纸杯完好无损 温度没有达到纸的着火点
D 酒精灯不用时,需用灯帽盖好 防止酒精分子不断运动到空气中
A.A B.B C.C D.D
二、填空题
13.除杂(括号中为杂质):
NaOH溶液(Ca(OH)2) Na2SO4溶液(Na2CO3)
K2SO4溶液(CuSO4) KNO3溶液(CuSO4) .
14.小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.
资料:
物质 碳酸钠 碳酸氢钠
20℃溶解度/g 21.5 9.6
水溶液的pH 11 9
(1)纯碱的化学式为 .
(2)将紫甘蓝汁滴入溶液A中,紫甘蓝汁显红色,则A溶液是 .
(3)将B溶液滴入A中,无明显现象,由此得出的结论是 .
(4)将C溶液滴入D、E中,均有沉淀产生,该过程的反应之一是(用化学方程式表示) .
(5)为进一步区别D、E,小明试着向其溶液中分别通入CO2,观察到D中有沉淀产生,E中无明显现象,试推测D的成分并说明理由 .
15.如图是研究氢氧化钠溶解于水时是否放热的实验,它是利用 的变化引起了U形管内水位的变化,使 (填a或b)处的水位升高的,探究过程中,可能会发生反应的化学方程式为: 。
16.亮亮做家务时接触到下列用品.
用品 脱氧剂 洁厕灵 炉灶清洁剂
有效成分 还原铁粉 盐酸 氢氧化钠
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是 .
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理 .
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是 .
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是 (填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
17. 实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
(1)实验室用装置A来制取CO2,常用的药品是 和 ,写出两物质制取二氧化碳的化学反应方程式 。
(2)若要用装置B鉴定CO2,在B中应盛放的试剂名称是 ,当将标①和②的导管口连接时,B中看到的实验现象是 。
(3)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是 ,当将标①和③的导管口连接时,C中看到的实验现象是 。
(4)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是 。
18.请对以下方案及现象做出合理补充或解释:
(1)浓硫酸在溶于水中时,溶液温度会明显 (填“升高”或“降低”),所以稀释浓硫酸的方法是将 并不断搅拌.
(2)不能服用NaOH治疗胃酸过多,原因是NaOH具有 性.
(3)Ca(OH)2和NaOH都要密封保存的共同原因是 .
三、综合题
19.粗盐中含有Mg 、Ca 等杂质,工业提纯粗盐的工艺流程如图所示
(1)Ca(OH)2溶液的pH (填“>”、“=”或“<”)
(2)步骤①反应的化学方程式为 ;
(3)步骤④加入适量盐酸的目的是除去滤液中的 ;
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有 .
20.
(1)我国古代纺织业常用氢氧化钾作漂洗的洗涤剂。古人将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主要成分是碳酸钾)在水中相互作用,即可制得氢氧化钾,生产流程如下图所示∶
请用化学方程式表示过程②中发生的化学反应∶
在上述①一④的生产过程中,没有涉及到的化学反应类型是 反应。(填“化合”“置换” “分解”“复分解”之一)
(2)NaCl、KNO3、Ca(OH)2三物质的溶解度曲线图分别如图一、图二所示,请回答∶
①由图一可知,20℃ 时,100g 水中加入40gNaCl固体充分溶解,所得溶液的质量为 g。②由图一可知,50℃ 时,KNO3溶液的溶质质量分数 NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
③如图三所示,20℃ 时,将盛有饱和石灰水的小试管放入盛水的烧杯l中,向水中加入氢氧化钠固体,结合图二分析石灰水中可出现 的现象。
21.如图是自来水消毒过程中发生反应的示意图,产物D具有杀菌消毒作用.
(1)当A物质泄漏时,可闻到刺激性气味,这说明分子具有的性质是 .
(2)该反应中,没有发生变化的微粒是 (填微粒符号).
(3)C物质的水溶液能使紫色石蕊试液变成 色.
(4)D物质杀菌消毒的化学原理是
四、实验探究题
22.“对比实验”是化学学习中行之有效的思维方法.某化学学习小组的同学在学完相关化学知识后,走进实验室做了如下实验,请你参与并回答下列问题
A.燃烧的条件 B.铁钉生锈的条件 C.证明CO2与NaOH反应 D.分子运动的现象
(1)实验A,实验中使用铜片,是利用了铜的 性(填一条物理性质)
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与 直接接触.欲除去铁锈可用 洗的方法,除锈的反应方程式 ,铁制品除锈时不能长时间浸在除锈溶液中.原因(方程式)
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 .
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的.当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 .其中盐酸与NaOH反应的化学方程式为 ,属于 反应(填反应类型)
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】D
4.【答案】A
5.【答案】D
6.【答案】A
7.【答案】B
8.【答案】C
9.【答案】C
10.【答案】D
11.【答案】A
12.【答案】A
13.【答案】碳酸钠溶液;稀硫酸;氢氧化钾溶液;氢氧化钡溶液
14.【答案】Na2CO3;饮水机清洁剂;B是食盐水或石灰水;Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;D为碳酸钠,CO2+H2O+Na2CO3=2NaHCO3碳酸氢钠的溶解度较小从而析出
15.【答案】压强;b;
16.【答案】Fe与潮湿的空气接触;CaCO3+2HCl=CaCl2+H2O+CO2↑;NaOH有强腐蚀性;AB
17.【答案】石灰石或大理石;稀盐酸;CaCO3 + 2HCl = CO2↑+ H2O + CaCl2;澄清石灰水;澄清石灰水变浑浊;石蕊试液;石蕊溶液变红;两支蜡烛从下往上依次熄灭
18.【答案】升高;浓硫酸缓缓地沿器壁注入水中;腐蚀;均能与空气中的二氧化碳反应
19.【答案】(1)>
(2)Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓
(3)Na2CO3和NaOH
(4)CaCl2
20.【答案】(1)CaO+H2O=Ca(OH)2;置换
(2)136g;无法确定;溶液变浑浊
21.【答案】(1)不断运动的
(2)Cl、H、O
(3)红
(4)2HClO═2HCl+O2↑
22.【答案】(1)导热
(2)水、氧气;稀盐酸;Fe2O3+6HCl=2FeCl3+3H2O;Fe+2HCl=FeCl2+H2↑
(3)2NaOH+CO2═Na2CO3+H2O
(4)红;红色逐渐褪去变为无色;HCl+NaOH═NaCl+H2O;复分解
一、单选题
1.在实验室中,下列物质具有强烈腐蚀性的是( )
A.稀HCl B.NaCl溶液
C.KNO3溶液 D.98%的浓H2SO4
2.在化学实验中必须注意安全操作:① 在点燃H2、CO、CH4等可燃性气体前,必须检验气体的纯度② 在稀释浓硫酸时将水沿器壁慢慢注入浓硫酸中,并用玻璃棒搅拌③ 浓硫酸不慎滴到皮肤上,应立即用大量水冲洗,再用3-5%的NaHCO3溶液涂上④ 给试管中液体加热,液体一般不超过试管容积的1/3
⑤ 可以向燃着的酒精灯中添加酒精
上述说法中正确的是( )
A.①② B.②⑤ C.③⑤ D.①③④
3.为除去下列物质中的杂质(括号里为杂质),选用的试剂和操作方法都正确的是( )
序号 物质 选用试剂 操作方法
A CO2气体(HCl) NaOH溶液 洗气
B FeSO4(CuSO4) Al粉 加入过量Al粉,过滤
C KNO3固体(KOH) H2O、CuSO4溶液 溶解、过滤、蒸发结晶
D NaCl固体(MgCl2) H2O、NaOH溶液、盐酸 溶解、加过量NaOH溶液、过滤、加过量盐酸、蒸发结晶
A.A B.B C.C D.D
4.下列叙述正确的是()
A.氦气常用作保护气
B.氧化钙的俗称熟石灰
C.盐酸能用作厨房清洁剂
D.煤炉上放一盆水可以防止煤气中毒
5.下列物质的鉴别方法错误的是( )
A.用肥皂水鉴别软水和硬水
B.用带火星的木条鉴别空气和氧气
C.用灼烧法鉴别棉纤维和羊毛纤维
D.用酚酞溶液鉴别稀盐酸和稀硫酸
6.推理是化学学习中常用的思维方法,下面推理中正确的是( )
A.碱性溶液能使紫色石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性
B.碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐
C.酸中都有氢元素,所以含有氢元素的化合物一定是酸
D.酸与碱反应有盐和水生成,因此有盐和水生成的反应一定是酸与碱反应
7.下列图象与所对应操作相符的是( )
A.①是对氢氧化钠溶液加水稀释
B.②是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.③是向HCl与Na2SO4混合溶液中加入Ba(OH)2溶液
D.④是用等质量、等浓度的双氧水分别制取氧气
8.下列图象分别与选项中的实验过程相对应,其中正确的是( )
A. 向部分变质的氢氧化钠溶液中滴加稀盐酸
B. 向一定量稀盐酸中逐滴加入水
C. 常温下,等质量的锌和铁分别与足量同溶质质量分数的稀硫酸反应
D. 电解水生成气体的体积
9.下列有关物质混合后的现象描述中,正确的是( )
A.在无色碘化钾溶液中滴加淀粉溶液,溶液变蓝
B.无色的氯化氢气体和氨气混合,产生白雾
C.在氢氧化钠稀溶液中滴加数滴硫酸铜溶液,产生蓝色絮状沉淀
D.铵盐与碱溶液混合加热,产生的气体使湿润的蓝色石蕊试纸变红
10.下列除杂设计(括号内为杂质)所选用试剂和操作都正确的是( )
序号 物 质 选用试剂 操作
A CO2(CO) O2 点燃
B NaOH溶液(Na2CO3) 稀盐酸 加入试剂至不再产生气泡
C KNO3溶液(KOH) CuSO4溶液 加入适量的试剂,充分反应后过滤
D NaCl固体(泥沙) H2O 溶解、过滤、洗涤、蒸发
A.A B.B C.C D.D
11.下列物质的应用中,不正确的是( )
A.将硝酸铵溶于水制作热敷袋
B.用汽油或加了洗涤剂的水都能除去衣服上的油污
C.把池水喷向空中,可以增加养鱼池水中氧气的溶解量
D.用Ca(OH)2改良酸性土壤
12.下列事实解释不正确的是( )
选项 事 实 解释
A NaOH 和Ca(OH)2的性质相似 Na+和Ca2+的性质相似
B 氢气、木炭、一氧化碳都可以冶炼金属 它们都具有还原性
C 给装满水的纸杯加热,开始时纸杯完好无损 温度没有达到纸的着火点
D 酒精灯不用时,需用灯帽盖好 防止酒精分子不断运动到空气中
A.A B.B C.C D.D
二、填空题
13.除杂(括号中为杂质):
NaOH溶液(Ca(OH)2) Na2SO4溶液(Na2CO3)
K2SO4溶液(CuSO4) KNO3溶液(CuSO4) .
14.小明在家中自制紫甘蓝汁,并测试其在酸性、中性、碱性条件下颜色(如图).他找到饮水机清洁剂(含盐酸)、食盐水、纯碱水、小苏打水和石灰水,开始了他的家庭实践活动.
资料:
物质 碳酸钠 碳酸氢钠
20℃溶解度/g 21.5 9.6
水溶液的pH 11 9
(1)纯碱的化学式为 .
(2)将紫甘蓝汁滴入溶液A中,紫甘蓝汁显红色,则A溶液是 .
(3)将B溶液滴入A中,无明显现象,由此得出的结论是 .
(4)将C溶液滴入D、E中,均有沉淀产生,该过程的反应之一是(用化学方程式表示) .
(5)为进一步区别D、E,小明试着向其溶液中分别通入CO2,观察到D中有沉淀产生,E中无明显现象,试推测D的成分并说明理由 .
15.如图是研究氢氧化钠溶解于水时是否放热的实验,它是利用 的变化引起了U形管内水位的变化,使 (填a或b)处的水位升高的,探究过程中,可能会发生反应的化学方程式为: 。
16.亮亮做家务时接触到下列用品.
用品 脱氧剂 洁厕灵 炉灶清洁剂
有效成分 还原铁粉 盐酸 氢氧化钠
(1)他清理垃圾时发现一袋脱氧剂,拆开后看到还原铁粉已生锈,铁生锈的原因是 .
(2)他选用洁厕灵清除水垢(主要成分是碳酸钙),用化学方程式表示其原理 .
(3)他清洗炉灶时戴上橡胶手套,以防清洁剂与皮肤直接接触,其原因是 .
(4)做完家务,他用Vc泡腾片冲了一杯饮料.下列Vc泡腾片的主要成分中,属于有机物的是 (填字母序号).
A.维生素C(C6H8O6) B.柠檬酸(C6H8O7) C.碳酸氢钠(NaHCO3)
17. 实验室按下图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
(1)实验室用装置A来制取CO2,常用的药品是 和 ,写出两物质制取二氧化碳的化学反应方程式 。
(2)若要用装置B鉴定CO2,在B中应盛放的试剂名称是 ,当将标①和②的导管口连接时,B中看到的实验现象是 。
(3)若要用装置C证明CO2能与水反应生成碳酸,C中除有少量水外,应加入的试剂是 ,当将标①和③的导管口连接时,C中看到的实验现象是 。
(4)烧杯D中放有燃着的蜡烛如图所示,当将标①和④的导管口连接时,D中看到的实验现象是 。
18.请对以下方案及现象做出合理补充或解释:
(1)浓硫酸在溶于水中时,溶液温度会明显 (填“升高”或“降低”),所以稀释浓硫酸的方法是将 并不断搅拌.
(2)不能服用NaOH治疗胃酸过多,原因是NaOH具有 性.
(3)Ca(OH)2和NaOH都要密封保存的共同原因是 .
三、综合题
19.粗盐中含有Mg 、Ca 等杂质,工业提纯粗盐的工艺流程如图所示
(1)Ca(OH)2溶液的pH (填“>”、“=”或“<”)
(2)步骤①反应的化学方程式为 ;
(3)步骤④加入适量盐酸的目的是除去滤液中的 ;
(4)若步骤①和步骤②的顺序颠倒,则最后所得的精盐水中还含有 .
20.
(1)我国古代纺织业常用氢氧化钾作漂洗的洗涤剂。古人将贝壳(主要成分是碳酸钙)灼烧后的固体与草木灰(主要成分是碳酸钾)在水中相互作用,即可制得氢氧化钾,生产流程如下图所示∶
请用化学方程式表示过程②中发生的化学反应∶
在上述①一④的生产过程中,没有涉及到的化学反应类型是 反应。(填“化合”“置换” “分解”“复分解”之一)
(2)NaCl、KNO3、Ca(OH)2三物质的溶解度曲线图分别如图一、图二所示,请回答∶
①由图一可知,20℃ 时,100g 水中加入40gNaCl固体充分溶解,所得溶液的质量为 g。②由图一可知,50℃ 时,KNO3溶液的溶质质量分数 NaCl溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
③如图三所示,20℃ 时,将盛有饱和石灰水的小试管放入盛水的烧杯l中,向水中加入氢氧化钠固体,结合图二分析石灰水中可出现 的现象。
21.如图是自来水消毒过程中发生反应的示意图,产物D具有杀菌消毒作用.
(1)当A物质泄漏时,可闻到刺激性气味,这说明分子具有的性质是 .
(2)该反应中,没有发生变化的微粒是 (填微粒符号).
(3)C物质的水溶液能使紫色石蕊试液变成 色.
(4)D物质杀菌消毒的化学原理是
四、实验探究题
22.“对比实验”是化学学习中行之有效的思维方法.某化学学习小组的同学在学完相关化学知识后,走进实验室做了如下实验,请你参与并回答下列问题
A.燃烧的条件 B.铁钉生锈的条件 C.证明CO2与NaOH反应 D.分子运动的现象
(1)实验A,实验中使用铜片,是利用了铜的 性(填一条物理性质)
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与 直接接触.欲除去铁锈可用 洗的方法,除锈的反应方程式 ,铁制品除锈时不能长时间浸在除锈溶液中.原因(方程式)
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2 与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 .
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的.当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 .其中盐酸与NaOH反应的化学方程式为 ,属于 反应(填反应类型)
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】D
4.【答案】A
5.【答案】D
6.【答案】A
7.【答案】B
8.【答案】C
9.【答案】C
10.【答案】D
11.【答案】A
12.【答案】A
13.【答案】碳酸钠溶液;稀硫酸;氢氧化钾溶液;氢氧化钡溶液
14.【答案】Na2CO3;饮水机清洁剂;B是食盐水或石灰水;Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;D为碳酸钠,CO2+H2O+Na2CO3=2NaHCO3碳酸氢钠的溶解度较小从而析出
15.【答案】压强;b;
16.【答案】Fe与潮湿的空气接触;CaCO3+2HCl=CaCl2+H2O+CO2↑;NaOH有强腐蚀性;AB
17.【答案】石灰石或大理石;稀盐酸;CaCO3 + 2HCl = CO2↑+ H2O + CaCl2;澄清石灰水;澄清石灰水变浑浊;石蕊试液;石蕊溶液变红;两支蜡烛从下往上依次熄灭
18.【答案】升高;浓硫酸缓缓地沿器壁注入水中;腐蚀;均能与空气中的二氧化碳反应
19.【答案】(1)>
(2)Ca(OH)2+MgCl2═CaCl2+Mg(OH)2↓
(3)Na2CO3和NaOH
(4)CaCl2
20.【答案】(1)CaO+H2O=Ca(OH)2;置换
(2)136g;无法确定;溶液变浑浊
21.【答案】(1)不断运动的
(2)Cl、H、O
(3)红
(4)2HClO═2HCl+O2↑
22.【答案】(1)导热
(2)水、氧气;稀盐酸;Fe2O3+6HCl=2FeCl3+3H2O;Fe+2HCl=FeCl2+H2↑
(3)2NaOH+CO2═Na2CO3+H2O
(4)红;红色逐渐褪去变为无色;HCl+NaOH═NaCl+H2O;复分解
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
