9.2 溶解度 同步练习 (含答案)2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 9.2 溶解度 同步练习 (含答案)2022-2023学年人教版九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 145.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-12 00:00:00 | ||
图片预览


文档简介
9.2 溶解度 同步练习 2022-2023学年人教版九年级下册化学
一、单选题
1.甲、乙两种物质的溶解度曲线如下图所示。下列说法错误的是( )
A.t1℃时甲乙的溶解度相等
B.t2℃时,甲的饱和溶液中溶质的质量分数为40%
C.t2℃时,甲的饱和溶液的质量分数比乙的饱和溶液的质量分数大
D.将t2℃时甲、乙的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
2.现有一杯30℃的硝酸钾饱和溶液,在下列情.况下,溶液的质量不变的是( )。
A.温度不变,向溶液中加入一定量的硝酸钾晶体
B.温度不变,向溶液中加入氯化钾晶体
C.温度不变,向溶液中加入蒸馏水
D.降低温度
3.下图表示的是甲、乙两种物质的溶解度曲线,据图所示,下列说法正确的是( )
A.t2℃时,甲乙两物质饱和溶液中的溶质质量大小关系是甲>乙
B.若甲物质中混有少量的乙物质,可以采用降温结晶的方法提纯甲物质
C.t2℃时将30g乙物质加入到50g水中,所得溶液的质量为80g
D.将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,溶液中的溶质质量分数大小关系是甲>乙
4.盛有饱和石灰水溶液的烧杯敞口放置在空气中,较长时间后,石灰水表面形成了一层“白 膜”(假设水没有减少)。下列说法正确的是( )
A.“白膜”为反应生成的碳酸钙固体
B.此时该溶液仍为饱和溶液
C.因析出氢氧化钙固体而形成“白膜 ”
D.给饱和石灰水降温,溶液会变浑浊
5.如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )
A.降低温度可使接近饱和的甲溶液变成饱和溶液
B.10℃时甲、乙两种溶液的溶质质量分数一定相等
C.将甲、乙两种物质的饱和溶液从10℃升温到35℃时,两溶液的溶质质量分数都变大
D.35℃时,100g甲的溶液中含甲的质量60g
6.甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
A.甲的溶解度大于乙的溶解度
B.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数
C.40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等
D.分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会
7.下列有关饱和溶液的说法中,正确的是( )
A.饱和溶液的浓度一定比不饱和溶液的大
B.饱和溶液降温析出晶体后的溶液一定是不饱和溶液
C.任何饱和溶液升温后都会变成不饱和溶液
D.一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液
8.高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表,下列说法正确的是( )
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20℃时,将2g高氯酸钾溶解于98g水可配制2%的溶液
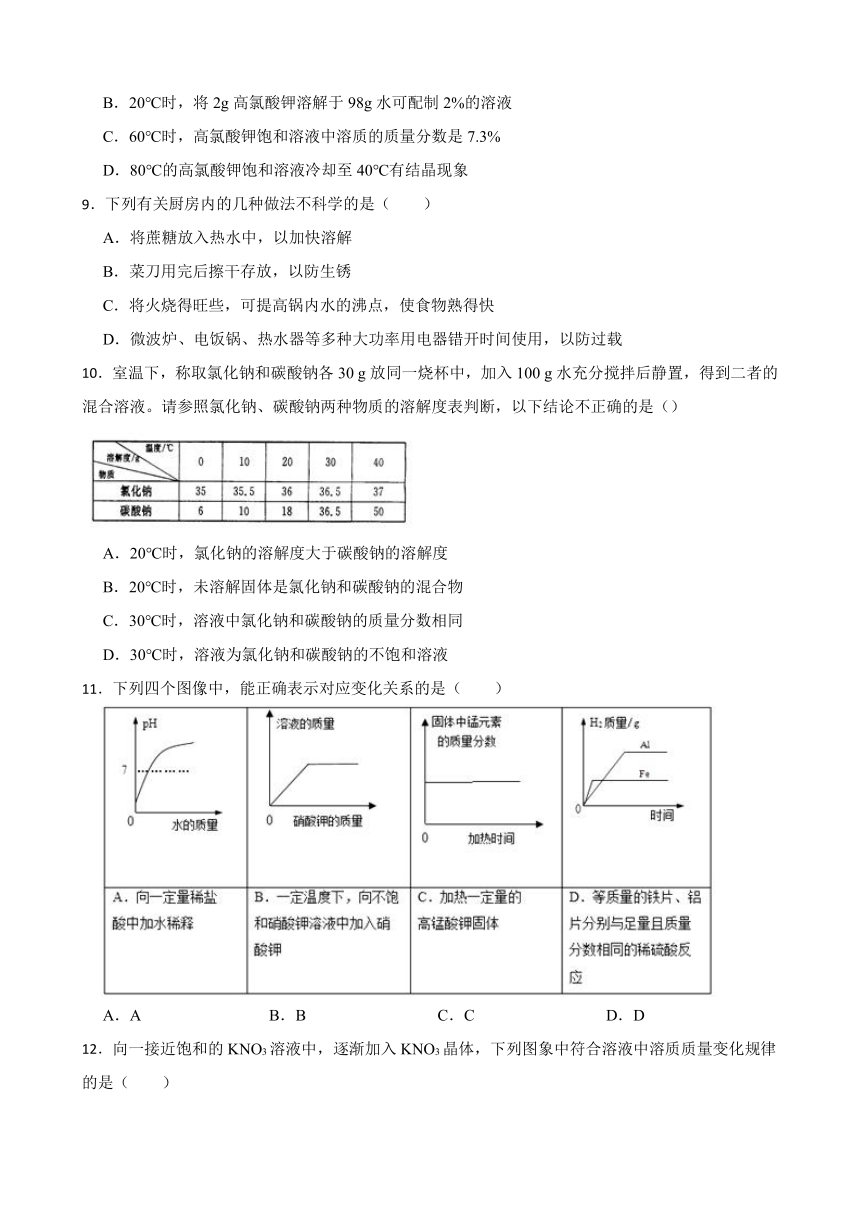
C.60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象
9.下列有关厨房内的几种做法不科学的是( )
A.将蔗糖放入热水中,以加快溶解
B.菜刀用完后擦干存放,以防生锈
C.将火烧得旺些,可提高锅内水的沸点,使食物熟得快
D.微波炉、电饭锅、热水器等多种大功率用电器错开时间使用,以防过载
10.室温下,称取氯化钠和碳酸钠各30 g放同一烧杯中,加入100 g水充分搅拌后静置,得到二者的混合溶液。请参照氯化钠、碳酸钠两种物质的溶解度表判断,以下结论不正确的是()
A.20℃时,氯化钠的溶解度大于碳酸钠的溶解度
B.20℃时,未溶解固体是氯化钠和碳酸钠的混合物
C.30℃时,溶液中氯化钠和碳酸钠的质量分数相同
D.30℃时,溶液为氯化钠和碳酸钠的不饱和溶液
11.下列四个图像中,能正确表示对应变化关系的是( )
A.A B.B C.C D.D
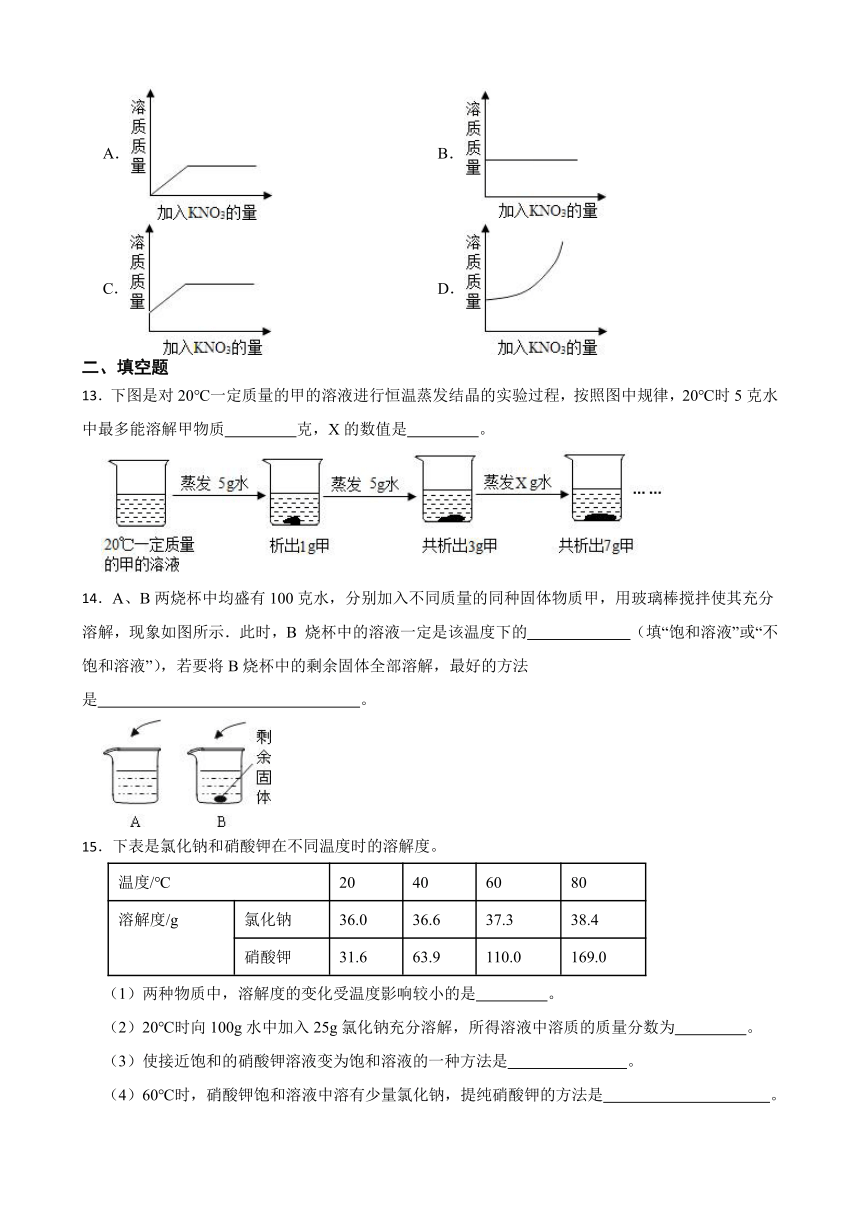
12.向一接近饱和的KNO3溶液中,逐渐加入KNO3晶体,下列图象中符合溶液中溶质质量变化规律的是( )
A. B.
C. D.
二、填空题
13.下图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,按照图中规律,20℃时5克水中最多能溶解甲物质 克,X的数值是 。
14.A、B两烧杯中均盛有100克水,分别加入不同质量的同种固体物质甲,用玻璃棒搅拌使其充分溶解,现象如图所示.此时,B 烧杯中的溶液一定是该温度下的 (填“饱和溶液”或“不饱和溶液”),若要将B烧杯中的剩余固体全部溶解,最好的方法是 。
15.下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ 20 40 60 80
溶解度/g 氯化钠 36.0 36.6 37.3 38.4
硝酸钾 31.6 63.9 110.0 169.0
(1)两种物质中,溶解度的变化受温度影响较小的是 。
(2)20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为 。
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是 。
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是 。
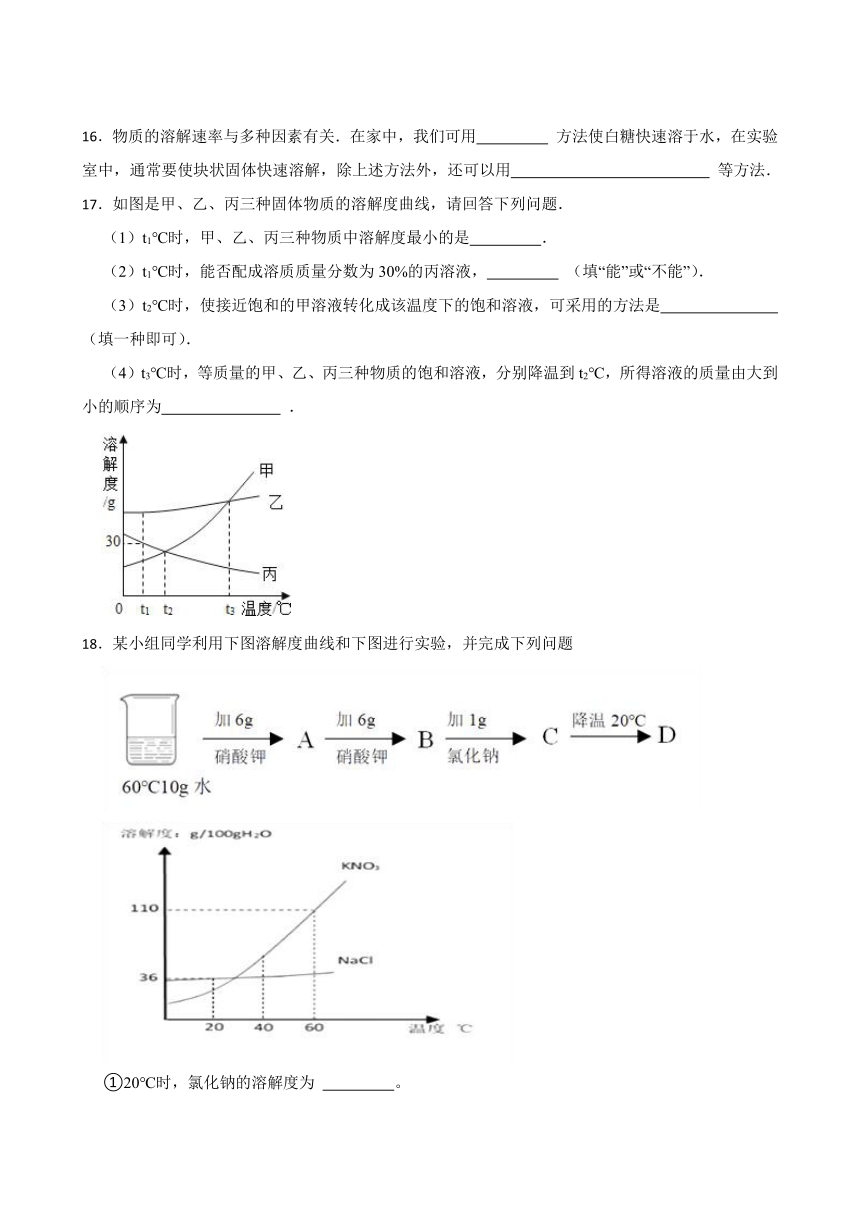
16.物质的溶解速率与多种因素有关.在家中,我们可用 方法使白糖快速溶于水,在实验室中,通常要使块状固体快速溶解,除上述方法外,还可以用 等方法.
17.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
(1)t1℃时,甲、乙、丙三种物质中溶解度最小的是 .
(2)t1℃时,能否配成溶质质量分数为30%的丙溶液, (填“能”或“不能”).
(3)t2℃时,使接近饱和的甲溶液转化成该温度下的饱和溶液,可采用的方法是 (填一种即可).
(4)t3℃时,等质量的甲、乙、丙三种物质的饱和溶液,分别降温到t2℃,所得溶液的质量由大到小的顺序为 .
18.某小组同学利用下图溶解度曲线和下图进行实验,并完成下列问题
①20℃时,氯化钠的溶解度为 。
②40℃时,硝酸钾的溶解度 氯化钠的溶解度(用“>”“<”“=”填空)
③A中溶液为60℃硝酸钾的 溶液(填“饱和”或“不饱和”)
④B中溶液的质量为 克
⑤将D过滤,下列有关所得晶体和溶液说法正确的是 (填字母)。
Ⅰ.析出的晶体中可能含有氯化钠 Ⅱ.所得溶液中一定含有硝酸钾和氯化钠
Ⅲ .C→D过程可以完全分离硝酸钾和氯化钠 Ⅳ.所得溶液一定是硝酸钾的饱和溶液
三、综合题
19.如图为A,B,C三种固体物质的溶解度曲线.
(1)根据题意判断,图中的横坐标和纵坐标分别表示 和 .
(2) ℃时,A,C两种物质的溶解度相等.
(3)把相等质量的A,B,C三种饱和溶液从 t2℃降至 t1℃时,析出晶体的质量最大的是 .
20.如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,A,B两种物质的溶解度是A B(填“>”、“<”或“=”,下同)。
(2)将t3℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
21.A、B、C三种物质的溶解度曲线如图所示.
(1)在t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 .其中,可能是气态物质的是
(2)P点表示t2℃时,完全溶解a g A物质最少需 g水.
(3)若B是KCl,则B溶液中的溶质粒子是(填符号) .
四、实验探究题
22.化学是一门以实验为基础的学科
【实验一】常见气体的制取.如图1所示
(1)仪器a的名称 .
(2)实验室用A装置制取氧气,从燃烧条件分析,加热过程中试管内的棉花没有燃烧的原因是 .选择E装置收集氧气的理由是 .
(3)实验室常用锌与稀硫酸来制取氢气,反应的化学方程式为 ,氢气验纯时,最好选用 方法来收集氢气,再点燃试验.
(4)【实验二】对比归纳是学习化学的重要方法.如图2所示
实验A:②中反应更剧烈,可知影响硫燃烧剧烈程度的因素是 .
(5)实验B:④中固体消失,③中固体几乎不溶,可知影响物质溶解性的因素是
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】B
4.【答案】A
5.【答案】A
6.【答案】C
7.【答案】D
8.【答案】D
9.【答案】C
10.【答案】B
11.【答案】B
12.【答案】C
13.【答案】2;10
14.【答案】饱和溶液;加水使剩余的甲物质全部溶解。
15.【答案】(1)氯化钠
(2)20%
(3)加入硝酸钾
(4)降温结晶,再过滤
16.【答案】搅拌;将固体研碎(或加热)
17.【答案】甲;不能;增加溶质或蒸发溶剂;丙>乙>甲
18.【答案】36g;>;不饱和;21;Ⅱ、Ⅳ
19.【答案】(1)温度;溶解度
(2)t1
(3)A
20.【答案】(1)<
(2)>
21.【答案】(1)C>B>A;C
(2)100
(3)K+、Cl﹣
22.【答案】(1)集气瓶
(2)温度没有达到着火点;氧气不易溶于水
(3)Zn+H2SO4═ZnSO4+H2↑;排水
(4)氧气的浓度
(5)溶剂的性质
一、单选题
1.甲、乙两种物质的溶解度曲线如下图所示。下列说法错误的是( )
A.t1℃时甲乙的溶解度相等
B.t2℃时,甲的饱和溶液中溶质的质量分数为40%
C.t2℃时,甲的饱和溶液的质量分数比乙的饱和溶液的质量分数大
D.将t2℃时甲、乙的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等
2.现有一杯30℃的硝酸钾饱和溶液,在下列情.况下,溶液的质量不变的是( )。
A.温度不变,向溶液中加入一定量的硝酸钾晶体
B.温度不变,向溶液中加入氯化钾晶体
C.温度不变,向溶液中加入蒸馏水
D.降低温度
3.下图表示的是甲、乙两种物质的溶解度曲线,据图所示,下列说法正确的是( )
A.t2℃时,甲乙两物质饱和溶液中的溶质质量大小关系是甲>乙
B.若甲物质中混有少量的乙物质,可以采用降温结晶的方法提纯甲物质
C.t2℃时将30g乙物质加入到50g水中,所得溶液的质量为80g
D.将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,溶液中的溶质质量分数大小关系是甲>乙
4.盛有饱和石灰水溶液的烧杯敞口放置在空气中,较长时间后,石灰水表面形成了一层“白 膜”(假设水没有减少)。下列说法正确的是( )
A.“白膜”为反应生成的碳酸钙固体
B.此时该溶液仍为饱和溶液
C.因析出氢氧化钙固体而形成“白膜 ”
D.给饱和石灰水降温,溶液会变浑浊
5.如图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是( )
A.降低温度可使接近饱和的甲溶液变成饱和溶液
B.10℃时甲、乙两种溶液的溶质质量分数一定相等
C.将甲、乙两种物质的饱和溶液从10℃升温到35℃时,两溶液的溶质质量分数都变大
D.35℃时,100g甲的溶液中含甲的质量60g
6.甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
A.甲的溶解度大于乙的溶解度
B.20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数
C.40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等
D.分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会
7.下列有关饱和溶液的说法中,正确的是( )
A.饱和溶液的浓度一定比不饱和溶液的大
B.饱和溶液降温析出晶体后的溶液一定是不饱和溶液
C.任何饱和溶液升温后都会变成不饱和溶液
D.一定温度下,向氯化钠饱和溶液中加入水后会变成不饱和溶液
8.高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表,下列说法正确的是( )
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20℃时,将2g高氯酸钾溶解于98g水可配制2%的溶液
C.60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象
9.下列有关厨房内的几种做法不科学的是( )
A.将蔗糖放入热水中,以加快溶解
B.菜刀用完后擦干存放,以防生锈
C.将火烧得旺些,可提高锅内水的沸点,使食物熟得快
D.微波炉、电饭锅、热水器等多种大功率用电器错开时间使用,以防过载
10.室温下,称取氯化钠和碳酸钠各30 g放同一烧杯中,加入100 g水充分搅拌后静置,得到二者的混合溶液。请参照氯化钠、碳酸钠两种物质的溶解度表判断,以下结论不正确的是()
A.20℃时,氯化钠的溶解度大于碳酸钠的溶解度
B.20℃时,未溶解固体是氯化钠和碳酸钠的混合物
C.30℃时,溶液中氯化钠和碳酸钠的质量分数相同
D.30℃时,溶液为氯化钠和碳酸钠的不饱和溶液
11.下列四个图像中,能正确表示对应变化关系的是( )
A.A B.B C.C D.D
12.向一接近饱和的KNO3溶液中,逐渐加入KNO3晶体,下列图象中符合溶液中溶质质量变化规律的是( )
A. B.
C. D.
二、填空题
13.下图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,按照图中规律,20℃时5克水中最多能溶解甲物质 克,X的数值是 。
14.A、B两烧杯中均盛有100克水,分别加入不同质量的同种固体物质甲,用玻璃棒搅拌使其充分溶解,现象如图所示.此时,B 烧杯中的溶液一定是该温度下的 (填“饱和溶液”或“不饱和溶液”),若要将B烧杯中的剩余固体全部溶解,最好的方法是 。
15.下表是氯化钠和硝酸钾在不同温度时的溶解度。
温度/℃ 20 40 60 80
溶解度/g 氯化钠 36.0 36.6 37.3 38.4
硝酸钾 31.6 63.9 110.0 169.0
(1)两种物质中,溶解度的变化受温度影响较小的是 。
(2)20℃时向100g水中加入25g氯化钠充分溶解,所得溶液中溶质的质量分数为 。
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是 。
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钠,提纯硝酸钾的方法是 。
16.物质的溶解速率与多种因素有关.在家中,我们可用 方法使白糖快速溶于水,在实验室中,通常要使块状固体快速溶解,除上述方法外,还可以用 等方法.
17.如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题.
(1)t1℃时,甲、乙、丙三种物质中溶解度最小的是 .
(2)t1℃时,能否配成溶质质量分数为30%的丙溶液, (填“能”或“不能”).
(3)t2℃时,使接近饱和的甲溶液转化成该温度下的饱和溶液,可采用的方法是 (填一种即可).
(4)t3℃时,等质量的甲、乙、丙三种物质的饱和溶液,分别降温到t2℃,所得溶液的质量由大到小的顺序为 .
18.某小组同学利用下图溶解度曲线和下图进行实验,并完成下列问题
①20℃时,氯化钠的溶解度为 。
②40℃时,硝酸钾的溶解度 氯化钠的溶解度(用“>”“<”“=”填空)
③A中溶液为60℃硝酸钾的 溶液(填“饱和”或“不饱和”)
④B中溶液的质量为 克
⑤将D过滤,下列有关所得晶体和溶液说法正确的是 (填字母)。
Ⅰ.析出的晶体中可能含有氯化钠 Ⅱ.所得溶液中一定含有硝酸钾和氯化钠
Ⅲ .C→D过程可以完全分离硝酸钾和氯化钠 Ⅳ.所得溶液一定是硝酸钾的饱和溶液
三、综合题
19.如图为A,B,C三种固体物质的溶解度曲线.
(1)根据题意判断,图中的横坐标和纵坐标分别表示 和 .
(2) ℃时,A,C两种物质的溶解度相等.
(3)把相等质量的A,B,C三种饱和溶液从 t2℃降至 t1℃时,析出晶体的质量最大的是 .
20.如图是A、B两种物质的溶解度曲线,根据图示回答下列问题:
(1)t1℃时,A,B两种物质的溶解度是A B(填“>”、“<”或“=”,下同)。
(2)将t3℃的A,B两种物质的饱和溶液各200g,降温至t1℃,析出晶体的质量关系是A B。
21.A、B、C三种物质的溶解度曲线如图所示.
(1)在t1℃时,A、B、C三种物质的溶解度由大到小的顺序是 .其中,可能是气态物质的是
(2)P点表示t2℃时,完全溶解a g A物质最少需 g水.
(3)若B是KCl,则B溶液中的溶质粒子是(填符号) .
四、实验探究题
22.化学是一门以实验为基础的学科
【实验一】常见气体的制取.如图1所示
(1)仪器a的名称 .
(2)实验室用A装置制取氧气,从燃烧条件分析,加热过程中试管内的棉花没有燃烧的原因是 .选择E装置收集氧气的理由是 .
(3)实验室常用锌与稀硫酸来制取氢气,反应的化学方程式为 ,氢气验纯时,最好选用 方法来收集氢气,再点燃试验.
(4)【实验二】对比归纳是学习化学的重要方法.如图2所示
实验A:②中反应更剧烈,可知影响硫燃烧剧烈程度的因素是 .
(5)实验B:④中固体消失,③中固体几乎不溶,可知影响物质溶解性的因素是
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】B
4.【答案】A
5.【答案】A
6.【答案】C
7.【答案】D
8.【答案】D
9.【答案】C
10.【答案】B
11.【答案】B
12.【答案】C
13.【答案】2;10
14.【答案】饱和溶液;加水使剩余的甲物质全部溶解。
15.【答案】(1)氯化钠
(2)20%
(3)加入硝酸钾
(4)降温结晶,再过滤
16.【答案】搅拌;将固体研碎(或加热)
17.【答案】甲;不能;增加溶质或蒸发溶剂;丙>乙>甲
18.【答案】36g;>;不饱和;21;Ⅱ、Ⅳ
19.【答案】(1)温度;溶解度
(2)t1
(3)A
20.【答案】(1)<
(2)>
21.【答案】(1)C>B>A;C
(2)100
(3)K+、Cl﹣
22.【答案】(1)集气瓶
(2)温度没有达到着火点;氧气不易溶于水
(3)Zn+H2SO4═ZnSO4+H2↑;排水
(4)氧气的浓度
(5)溶剂的性质
同课章节目录
