4.3 原子的核式结构模型(学案)——2022-2023学年高二物理人教版(2019)选择性必修第三册
文档属性
| 名称 | 4.3 原子的核式结构模型(学案)——2022-2023学年高二物理人教版(2019)选择性必修第三册 |

|
|
| 格式 | doc | ||
| 文件大小 | 680.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2023-03-13 00:00:00 | ||
图片预览


文档简介
4.3 原子的核式结构模型
学习目标
1、知道阴极射线是由电子组成的,电子是原子的组成部分,是比原子更基本的物质单元。
2、体会电子的发现过程体现的科学方法。
3、知道电荷是量子化的,即任何电荷只能是e的整数倍。
4、体会电子的发现对揭示原子结构的重大意义。
5、了解α粒子散射实验原理和实验现象。
6、知道原子的核式结构模型的主要内容。
7、知道原子和原子核的大小数量级,原子核的电荷数。
8、领会卢瑟福提出原子核式结构模型的实验和思维过程,培养学生抽象思维能力和想象力。
重点难点
1、了解α粒子散射实验原理和实验现象。(重点)
2、知道原子的核式结构模型的主要内容。(难点)
自主探究
一、电子的发现
1、阴极射线
荧光是由于玻璃受到阴极发出的某种射线的撞击而引起的,这种射线命名为阴极射线。
2、汤姆孙的探究方法及结论
(1)根据阴极射线在电场和磁场中的偏转情况断定,它的本质是带负电的粒子流,并求出了这种粒子的比荷。
(2)换用不同材料的阴极做实验,所得比荷的数值都相同,是氢离子比荷的近两千倍。
(3)结论:阴极射线粒子带负电,其电荷量的大小与氢离子大致相同,而质量比氢离子小得多,后来组成阴极射线的粒子被称为电子。
3、汤姆孙的进一步研究
汤姆孙又进一步研究了许多新现象,证明了电子是原子的组成部分。
4、电子的电荷量及电荷量子化
(1)电子电荷量:1910年前后由密立根通过著名的得出,电子电荷的现代值为e=1.602×10-19 C。
(2)电荷是量子化的,即任何带电体的电荷只能是e的整数倍。
(3)电子的质量:me=9.109 383 56×10-31 kg,质子质量与电子质量的比为1 836。
说明:阴极射线实质是带负电的电子流。
二、原子的核式结构模型
1.α粒子散射实验
(1)汤姆孙原子模型
汤姆孙于1898年提出了原子模型,他认为原子是一个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌在球中。
(2)α粒子散射实验
①实验装置:α粒子源、金箔、放大镜和荧光屏。
②实验现象:
a.绝大多数的α粒子穿过金箔后仍沿原来的方向前进。
b.少数α粒子发生了大角度的偏转。
c.极少数α粒子的偏转角大于90°,甚至有极个别α粒子被反弹回来。
③实验意义:卢瑟福通过α粒子散射实验,否定了汤姆孙的原子模型,建立了核式结构模型。
2.卢瑟福的核式结构模型
核式结构模型
1911年由卢瑟福提出,在原子中心有一个很小的核,叫原子核。它集中了原子全部的正电荷和几乎全部的质量,电子在核外空间运动。
三、原子核的电荷与尺度
1.原子内的电荷关系:各种元素的原子核的电荷数与含有的电子数相等,非常接近于它们的原子序数。
2.原子核的组成:原子核是由质子和中子组成的,原子核的电荷数就等于原子核中的质子数。
3.原子核的大小:实验确定的原子核半径R的数量级为10-15m,而原子的半径的数量级是10-10m,因而原子内部十分“空旷”。
探究思考
一、电子电荷量及比荷的测定
1、电子的电荷量
1909~1913年间美国物理学家密立根通过著名的“油滴实验”简练精确地测定了电子的电荷量。电子电荷量目前公认的值为e=1.602 176 634 x 10-19 C。
2、带电粒子比荷的测定
(1)电荷量的量子化
带电体所带电荷是量子化的,即任何带电体所带电荷量只能是电子电荷量的整数倍,即q=ne ( n为自然数)。
(2) 比荷的测定
根据电场、磁场对电子(带电粒子)的偏转测量比荷,分以下两步:
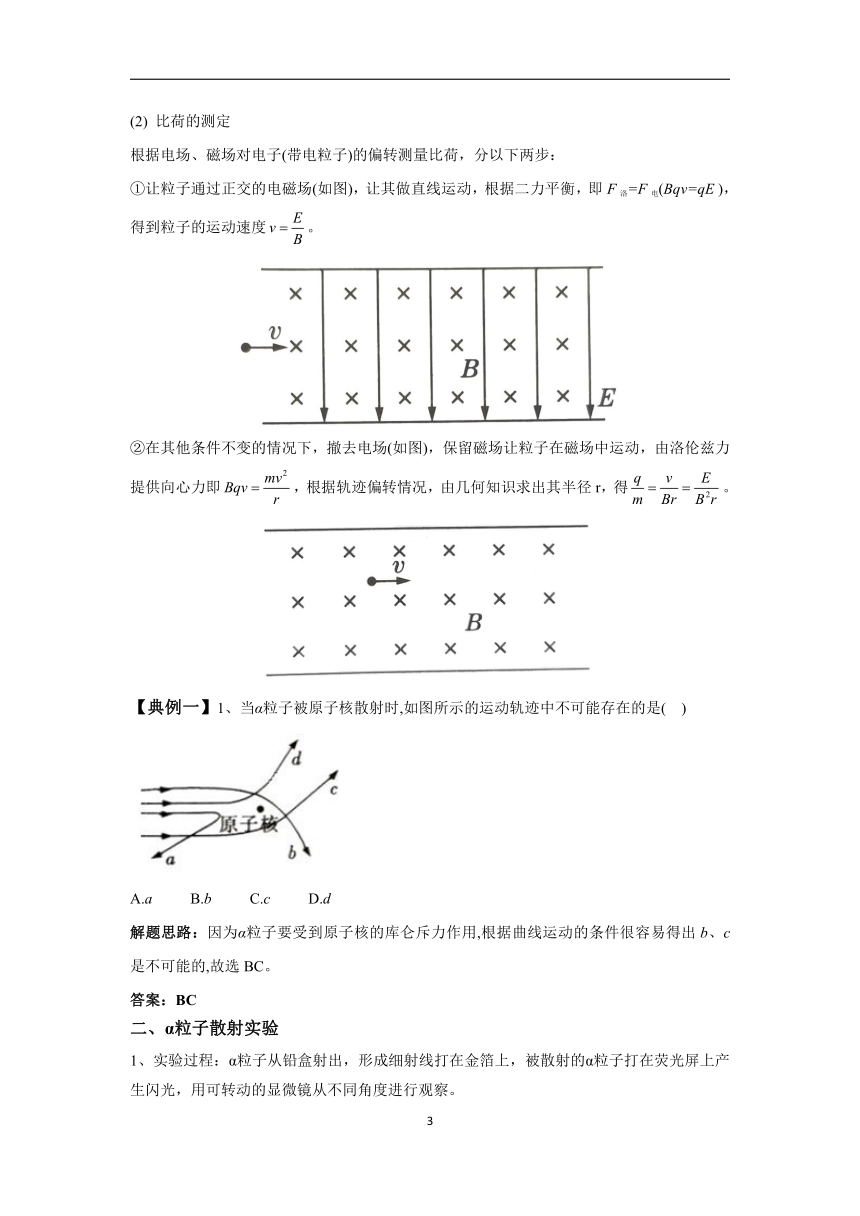
①让粒子通过正交的电磁场(如图),让其做直线运动,根据二力平衡,即F洛=F电(Bqv=qE ),得到粒子的运动速度。
②在其他条件不变的情况下,撤去电场(如图),保留磁场让粒子在磁场中运动,由洛伦兹力提供向心力即,根据轨迹偏转情况,由几何知识求出其半径r,得。
【典例一】1、当α粒子被原子核散射时,如图所示的运动轨迹中不可能存在的是( )
A.a B.b C.c D.d
解题思路:因为α粒子要受到原子核的库仑斥力作用,根据曲线运动的条件很容易得出b、c是不可能的,故选BC。
答案:BC
二、α粒子散射实验
1、实验过程:α粒子从铅盒射出,形成细射线打在金箔上,被散射的α粒子打在荧光屏上产生闪光,用可转动的显微镜从不同角度进行观察。
2、现象
(1)绝大多数的α粒子穿过金箔后仍沿原来的方向前进;
(2)少数α粒子发生较大的偏转;
(3)极少数α粒子偏转角度超过90°,有的几乎被“撞了回来”。如图所示。
3、α粒子散射实验与汤姆孙的原子模型的冲突分析
(1)由于电子质量远小于α粒子质量,所以电子不可能使α粒子发生大角度偏转。
(2)使α粒子发生大角度偏转的只能是原子中带正电的部分,按照汤姆孙原子模型,正电荷在原子内是均匀分布的,α粒子穿过原子时,它受到的两侧斥力大部分抵消,因而也不可能使α粒子发生大角度偏转,更不可能使α粒子反向弹回,这与α粒子的散射实验相矛盾。
(3)实验现象表明原子绝大部分是空的,除非原子的几乎全部质量和所有正电荷都集中在原子中心的一个很小的核上,否则,α粒子大角度散射是不可能的。
4、实验意义:否定了汤姆孙的原子结构模型,提出了原子核式结构模型,明确了原子核大小的数量级。
【典例二】2、粒子散射实验又称金箔实验、实验或卢瑟福粒子散射实验,实验装置如图所示。通过该实验,我们可以知道( )
A.该实验证实了汤姆孙的“西瓜模型”是正确的
B.大多数粒子穿过金箔后,其运动方向受到较大的影响
C.原子是一个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌在其中
D.占原子质量绝大部分的带正电的那部分物质集中在很小的空间范围内
解题思路: ACD、正电荷弥漫性地均匀分布在整个球体内,电子镶嵌其中是汤姆孙的认为,卢瑟福设计了粒子散射证明带正电的那部分物质占原子质量的绝大部分集中在很小的空间范围,从而证明汤姆孙的“西瓜模型”是错误的,故AC错误,D正确;
B、当粒子穿过原子时,电子对粒子影响很小,影响粒子运动的主要是原子核,离核远则粒子受到的库仑斥力很小,运动方向改变小。只有当粒子与核十分接近时,才会受到很大库仑斥力,而原子核很小,所以粒子接近它的机会就很少,所以只有极少数大角度的偏转,而绝大多数基本按直线方向前进,故B错误;
故选:D。
答案: D
三、原子的核式结构模型
1、原子的核式结构与原子的枣糕式结构的根本区别
核式结构 枣糕式结构
原子内部是非常空旷的,全部正电荷及几乎全部质量集中在一个很小的核里 原子是充满了正电荷的球体
电子绕核高速旋转 电子均匀嵌在原子球体内
2、原子核式结构模型
(1)在原子中心有一个很小的核,叫原子核。
(2)原子的全部正电荷和几乎全部质量都集中在这个核里。
(3)带负电的电子在核外空间绕核旋转。
随堂训练
1、卢瑟福提出原子的核式结构模型的依据是用α粒子轰击金箔,实验中发现α粒子( )
A.全部穿过或发生很小偏转
B.绝大多数发生很大偏转,甚至被弹回,只有少数穿过
C.全部发生很大偏转
D.绝大多数穿过,只有少数发生很大偏转,极少数甚至被弹回
答案:D
2、下列关于原子结构的说法正确的是( )
A.电子的发现说明了原子内部还有复杂结构
B.α粒子散射实验揭示了原子的核式结构
C.α粒子散射实验中绝大多数α粒子都发生了较大偏转
D.α粒子散射实验中有的α粒子发生较大偏转是α粒子与原子发生碰撞所致
答案:B
3、汤姆孙对阴极射线的探究,最终发现了电子,由此被称为“电子之父关于电子的说法正确的是( )
A.任何物质中均有电子
B.不同的物质中具有不同的电子
C.电子质量是质子质量的1836倍
D.电子是一种粒子,是构成物质的基本单元
答案:AD
4、关于原子的核式结构学说,下列说法正确的是( )
A.原子中绝大部分是“空”的,原子核很小
B.电子在核外绕核旋转的向心力是原子核对它的库仑力
C.原子的全部正电荷和质量都集中在原子核里
D.原子核的直径约是
答案:AB
2
学习目标
1、知道阴极射线是由电子组成的,电子是原子的组成部分,是比原子更基本的物质单元。
2、体会电子的发现过程体现的科学方法。
3、知道电荷是量子化的,即任何电荷只能是e的整数倍。
4、体会电子的发现对揭示原子结构的重大意义。
5、了解α粒子散射实验原理和实验现象。
6、知道原子的核式结构模型的主要内容。
7、知道原子和原子核的大小数量级,原子核的电荷数。
8、领会卢瑟福提出原子核式结构模型的实验和思维过程,培养学生抽象思维能力和想象力。
重点难点
1、了解α粒子散射实验原理和实验现象。(重点)
2、知道原子的核式结构模型的主要内容。(难点)
自主探究
一、电子的发现
1、阴极射线
荧光是由于玻璃受到阴极发出的某种射线的撞击而引起的,这种射线命名为阴极射线。
2、汤姆孙的探究方法及结论
(1)根据阴极射线在电场和磁场中的偏转情况断定,它的本质是带负电的粒子流,并求出了这种粒子的比荷。
(2)换用不同材料的阴极做实验,所得比荷的数值都相同,是氢离子比荷的近两千倍。
(3)结论:阴极射线粒子带负电,其电荷量的大小与氢离子大致相同,而质量比氢离子小得多,后来组成阴极射线的粒子被称为电子。
3、汤姆孙的进一步研究
汤姆孙又进一步研究了许多新现象,证明了电子是原子的组成部分。
4、电子的电荷量及电荷量子化
(1)电子电荷量:1910年前后由密立根通过著名的得出,电子电荷的现代值为e=1.602×10-19 C。
(2)电荷是量子化的,即任何带电体的电荷只能是e的整数倍。
(3)电子的质量:me=9.109 383 56×10-31 kg,质子质量与电子质量的比为1 836。
说明:阴极射线实质是带负电的电子流。
二、原子的核式结构模型
1.α粒子散射实验
(1)汤姆孙原子模型
汤姆孙于1898年提出了原子模型,他认为原子是一个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌在球中。
(2)α粒子散射实验
①实验装置:α粒子源、金箔、放大镜和荧光屏。
②实验现象:
a.绝大多数的α粒子穿过金箔后仍沿原来的方向前进。
b.少数α粒子发生了大角度的偏转。
c.极少数α粒子的偏转角大于90°,甚至有极个别α粒子被反弹回来。
③实验意义:卢瑟福通过α粒子散射实验,否定了汤姆孙的原子模型,建立了核式结构模型。
2.卢瑟福的核式结构模型
核式结构模型
1911年由卢瑟福提出,在原子中心有一个很小的核,叫原子核。它集中了原子全部的正电荷和几乎全部的质量,电子在核外空间运动。
三、原子核的电荷与尺度
1.原子内的电荷关系:各种元素的原子核的电荷数与含有的电子数相等,非常接近于它们的原子序数。
2.原子核的组成:原子核是由质子和中子组成的,原子核的电荷数就等于原子核中的质子数。
3.原子核的大小:实验确定的原子核半径R的数量级为10-15m,而原子的半径的数量级是10-10m,因而原子内部十分“空旷”。
探究思考
一、电子电荷量及比荷的测定
1、电子的电荷量
1909~1913年间美国物理学家密立根通过著名的“油滴实验”简练精确地测定了电子的电荷量。电子电荷量目前公认的值为e=1.602 176 634 x 10-19 C。
2、带电粒子比荷的测定
(1)电荷量的量子化
带电体所带电荷是量子化的,即任何带电体所带电荷量只能是电子电荷量的整数倍,即q=ne ( n为自然数)。
(2) 比荷的测定
根据电场、磁场对电子(带电粒子)的偏转测量比荷,分以下两步:
①让粒子通过正交的电磁场(如图),让其做直线运动,根据二力平衡,即F洛=F电(Bqv=qE ),得到粒子的运动速度。
②在其他条件不变的情况下,撤去电场(如图),保留磁场让粒子在磁场中运动,由洛伦兹力提供向心力即,根据轨迹偏转情况,由几何知识求出其半径r,得。
【典例一】1、当α粒子被原子核散射时,如图所示的运动轨迹中不可能存在的是( )
A.a B.b C.c D.d
解题思路:因为α粒子要受到原子核的库仑斥力作用,根据曲线运动的条件很容易得出b、c是不可能的,故选BC。
答案:BC
二、α粒子散射实验
1、实验过程:α粒子从铅盒射出,形成细射线打在金箔上,被散射的α粒子打在荧光屏上产生闪光,用可转动的显微镜从不同角度进行观察。
2、现象
(1)绝大多数的α粒子穿过金箔后仍沿原来的方向前进;
(2)少数α粒子发生较大的偏转;
(3)极少数α粒子偏转角度超过90°,有的几乎被“撞了回来”。如图所示。
3、α粒子散射实验与汤姆孙的原子模型的冲突分析
(1)由于电子质量远小于α粒子质量,所以电子不可能使α粒子发生大角度偏转。
(2)使α粒子发生大角度偏转的只能是原子中带正电的部分,按照汤姆孙原子模型,正电荷在原子内是均匀分布的,α粒子穿过原子时,它受到的两侧斥力大部分抵消,因而也不可能使α粒子发生大角度偏转,更不可能使α粒子反向弹回,这与α粒子的散射实验相矛盾。
(3)实验现象表明原子绝大部分是空的,除非原子的几乎全部质量和所有正电荷都集中在原子中心的一个很小的核上,否则,α粒子大角度散射是不可能的。
4、实验意义:否定了汤姆孙的原子结构模型,提出了原子核式结构模型,明确了原子核大小的数量级。
【典例二】2、粒子散射实验又称金箔实验、实验或卢瑟福粒子散射实验,实验装置如图所示。通过该实验,我们可以知道( )
A.该实验证实了汤姆孙的“西瓜模型”是正确的
B.大多数粒子穿过金箔后,其运动方向受到较大的影响
C.原子是一个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌在其中
D.占原子质量绝大部分的带正电的那部分物质集中在很小的空间范围内
解题思路: ACD、正电荷弥漫性地均匀分布在整个球体内,电子镶嵌其中是汤姆孙的认为,卢瑟福设计了粒子散射证明带正电的那部分物质占原子质量的绝大部分集中在很小的空间范围,从而证明汤姆孙的“西瓜模型”是错误的,故AC错误,D正确;
B、当粒子穿过原子时,电子对粒子影响很小,影响粒子运动的主要是原子核,离核远则粒子受到的库仑斥力很小,运动方向改变小。只有当粒子与核十分接近时,才会受到很大库仑斥力,而原子核很小,所以粒子接近它的机会就很少,所以只有极少数大角度的偏转,而绝大多数基本按直线方向前进,故B错误;
故选:D。
答案: D
三、原子的核式结构模型
1、原子的核式结构与原子的枣糕式结构的根本区别
核式结构 枣糕式结构
原子内部是非常空旷的,全部正电荷及几乎全部质量集中在一个很小的核里 原子是充满了正电荷的球体
电子绕核高速旋转 电子均匀嵌在原子球体内
2、原子核式结构模型
(1)在原子中心有一个很小的核,叫原子核。
(2)原子的全部正电荷和几乎全部质量都集中在这个核里。
(3)带负电的电子在核外空间绕核旋转。
随堂训练
1、卢瑟福提出原子的核式结构模型的依据是用α粒子轰击金箔,实验中发现α粒子( )
A.全部穿过或发生很小偏转
B.绝大多数发生很大偏转,甚至被弹回,只有少数穿过
C.全部发生很大偏转
D.绝大多数穿过,只有少数发生很大偏转,极少数甚至被弹回
答案:D
2、下列关于原子结构的说法正确的是( )
A.电子的发现说明了原子内部还有复杂结构
B.α粒子散射实验揭示了原子的核式结构
C.α粒子散射实验中绝大多数α粒子都发生了较大偏转
D.α粒子散射实验中有的α粒子发生较大偏转是α粒子与原子发生碰撞所致
答案:B
3、汤姆孙对阴极射线的探究,最终发现了电子,由此被称为“电子之父关于电子的说法正确的是( )
A.任何物质中均有电子
B.不同的物质中具有不同的电子
C.电子质量是质子质量的1836倍
D.电子是一种粒子,是构成物质的基本单元
答案:AD
4、关于原子的核式结构学说,下列说法正确的是( )
A.原子中绝大部分是“空”的,原子核很小
B.电子在核外绕核旋转的向心力是原子核对它的库仑力
C.原子的全部正电荷和质量都集中在原子核里
D.原子核的直径约是
答案:AB
2
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
