2022-2023学年高一化学人教版2019必修第二册第六章第一节第1课时化学反应与热能练习题(含解析)
文档属性
| 名称 | 2022-2023学年高一化学人教版2019必修第二册第六章第一节第1课时化学反应与热能练习题(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-14 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
2022-2023学年高一化学人教版2019必修第二册
第六章第一节第1课时化学反应与热能练习题
学校:___________姓名:___________班级:___________
一、单选题
1.下列变化一定是吸热反应的是( )
A.凡需加热后才能发生的反应
B.所有的分解反应
C.将化学能转变为热能的反应
D.生成物总能量大于反应物总能量的反应
2.下列反应属于氧化还原反应,并且 H>0的是( )
A.铝片与稀H2SO4反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2反应 D.甲烷在O2中的燃烧反应
3.下图为反应2H2(g)+O2(g)=2H2O(g)的能量变化示意图,下列说法正确的是( )
A.拆开2molH2 (g)和1 molO2(g)中的化学键成为H、O原子,共放出1368 kJ能量
B.由H、O原子形成2 molH2O(g),共吸收1852 kJ能量
C.2 molH2(g)和1 molO2 (g)反应生成2 mol H2O(1),共吸收484 kJ能量
D.2 molH2 (g)和1 molO2(g)反应生成2 molH2O(g),共放出484 kJ能量
4.下列过程中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧
C.液态水汽化 D.氧化钙与水反应
5.下列反应过程中的能量变化情况符合如图的是( )
A.酒精的燃烧 B.氢氧化钡晶体与氯化铵固体反应
C.镁和稀硫酸的反应 D.酸和碱的中和反应
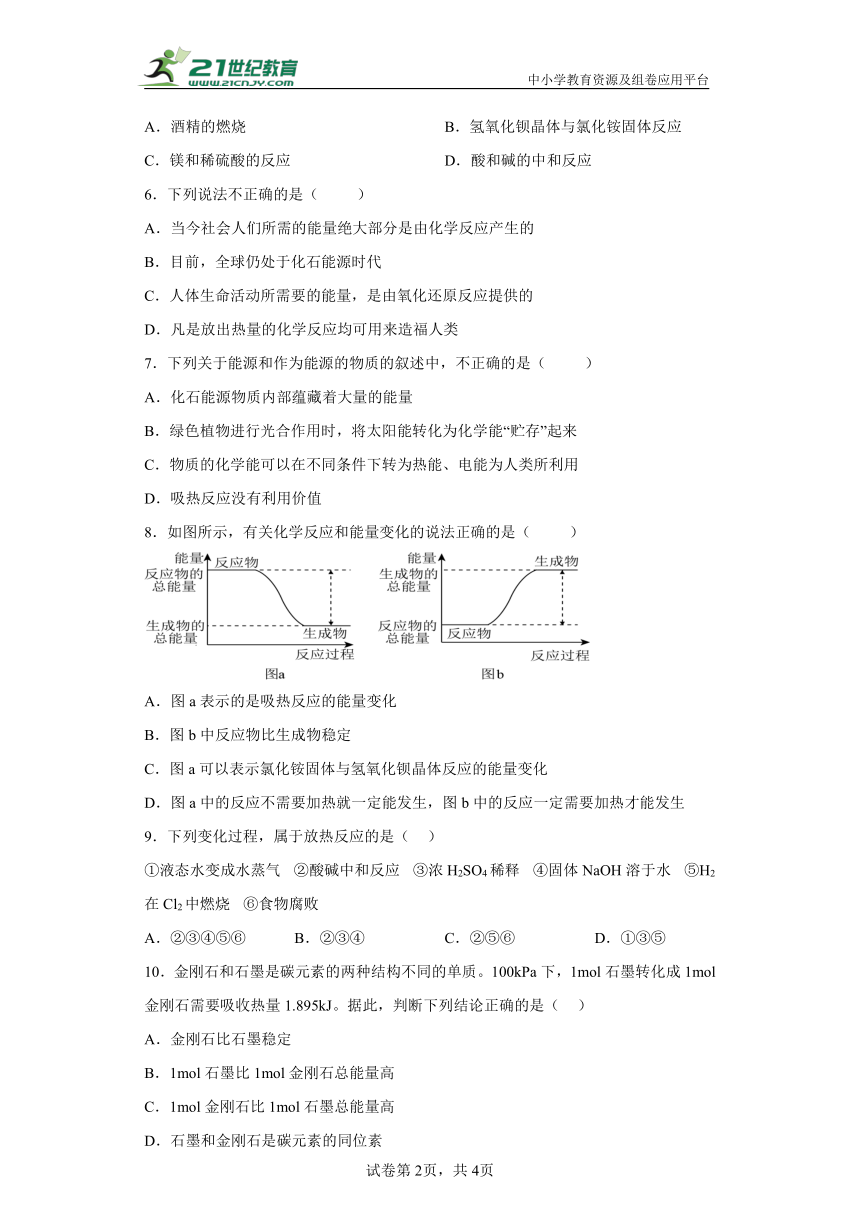
6.下列说法不正确的是( )
A.当今社会人们所需的能量绝大部分是由化学反应产生的
B.目前,全球仍处于化石能源时代
C.人体生命活动所需要的能量,是由氧化还原反应提供的
D.凡是放出热量的化学反应均可用来造福人类
7.下列关于能源和作为能源的物质的叙述中,不正确的是( )
A.化石能源物质内部蕴藏着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在不同条件下转为热能、电能为人类所利用
D.吸热反应没有利用价值
8.如图所示,有关化学反应和能量变化的说法正确的是( )
A.图a表示的是吸热反应的能量变化
B.图b中反应物比生成物稳定
C.图a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D.图a中的反应不需要加热就一定能发生,图b中的反应一定需要加热才能发生
9.下列变化过程,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释 ④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥食物腐败
A.②③④⑤⑥ B.②③④ C.②⑤⑥ D.①③⑤
10.金刚石和石墨是碳元素的两种结构不同的单质。100kPa下,1mol石墨转化成1mol金刚石需要吸收热量1.895kJ。据此,判断下列结论正确的是( )
A.金刚石比石墨稳定
B.1mol石墨比1mol金刚石总能量高
C.1mol金刚石比1mol石墨总能量高
D.石墨和金刚石是碳元素的同位素
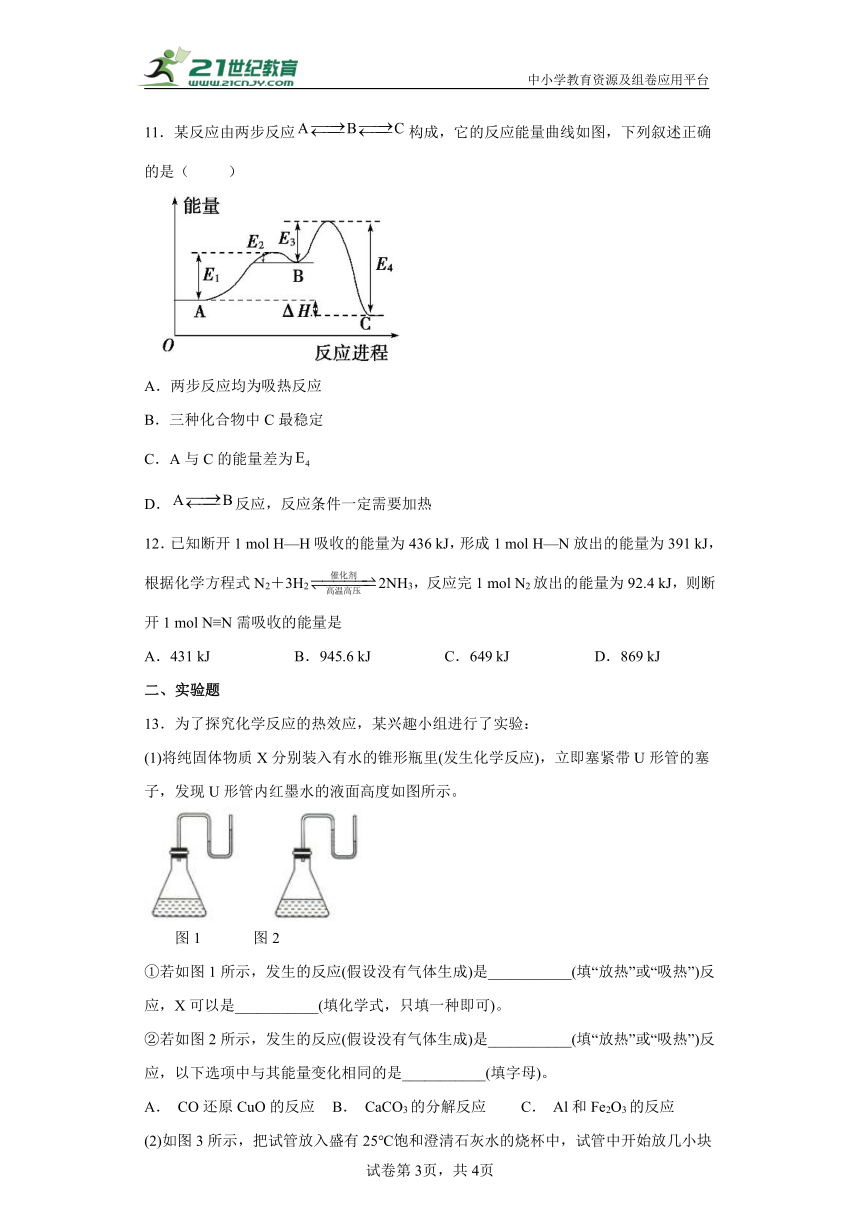
11.某反应由两步反应构成,它的反应能量曲线如图,下列叙述正确的是( )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为
D.反应,反应条件一定需要加热
12.已知断开1 mol H—H吸收的能量为436 kJ,形成1 mol H—N放出的能量为391 kJ,根据化学方程式N2+3H22NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N需吸收的能量是
A.431 kJ B.945.6 kJ C.649 kJ D.869 kJ
二、实验题
13.为了探究化学反应的热效应,某兴趣小组进行了实验:
(1)将纯固体物质X分别装入有水的锥形瓶里(发生化学反应),立即塞紧带U形管的塞子,发现U形管内红墨水的液面高度如图所示。
图1 图2
①若如图1所示,发生的反应(假设没有气体生成)是___________(填“放热”或“吸热”)反应,X可以是___________(填化学式,只填一种即可)。
②若如图2所示,发生的反应(假设没有气体生成)是___________(填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是___________(填字母)。
A. CO还原CuO的反应 B. CaCO3的分解反应 C. Al和Fe2O3的反应
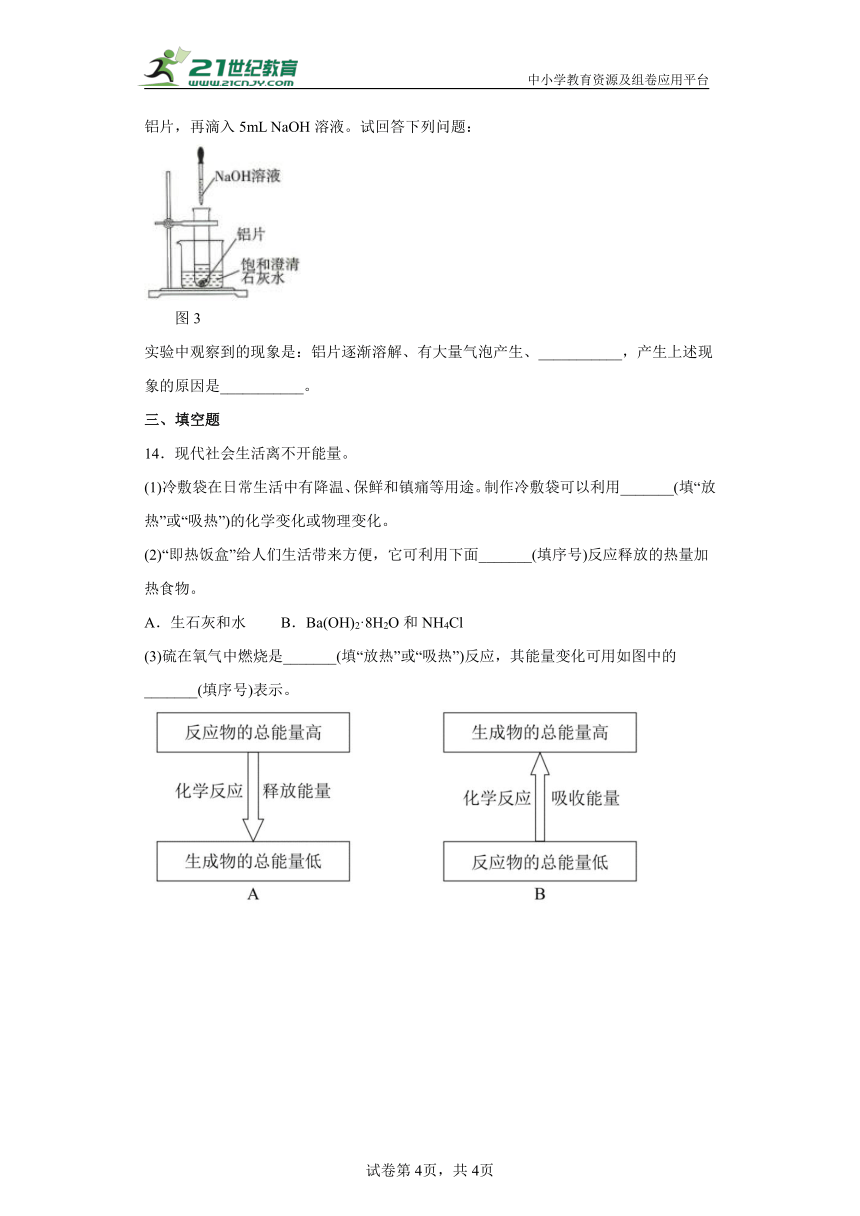
(2)如图3所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放几小块铝片,再滴入5mL NaOH溶液。试回答下列问题:
图3
实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、___________,产生上述现象的原因是___________。
三、填空题
14.现代社会生活离不开能量。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______(填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______(填序号)反应释放的热量加热食物。
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
(3)硫在氧气中燃烧是_______(填“放热”或“吸热”)反应,其能量变化可用如图中的_______(填序号)表示。
参考答案:
1.D
【详解】反应是放热反应,还是吸热反应,与反应条件无关系。只与反应物和生成物总能量的相对大小有关。如果反应物的总能量大于生成物的总能量,则反应是放热反应,反之是吸热反应,答案选D。
2.C
【详解】A.铝片与稀H2SO4的反应为放热反应,A错误;
B.Ba(OH)2 8H2O与NH4Cl的反应为吸热反应,但不属于氧化还原反应,B错误;
C.灼热的炭与CO2的反应中C元素化合价发生变化,属于氧化还原反应,且为吸热反应,C正确;
D.甲烷在O2中的燃烧反应是放热反应,D错误;
答案选C。
3.D
【详解】A.拆开化学键吸收能量,故A错误;
B.形成化学键放出能量,故B错误;
C.由题干方程式可知应生成气态水,而不是液态水时,放出484 kJ能量,故C错误;
D.依据图象数据分析计算,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量,故D正确;
故答案为C。
4.A
【详解】A.碳酸钙受热分解属于吸热反应,生成物的总能量高于反应物的总能量,A符合题意;
B.乙醇燃烧属于放热反应,生成物的总能量低于反应物的总能量,B不合题意;
C.液态水汽化是吸热过程,属于物理变化,C不合题意;
D.氧化钙与水反应是放热反应,生成物的总能量低于反应物的总能量,D不合题意;
故选A。
【点睛】对于常见的反应,燃烧反应、绝大部分化合反应、酸碱中和反应、活泼金属与酸或水的反应、铝热反应等,都是放热反应。
5.B
【分析】根据图中的能量变化,可知生成物的总能量高于反应物的总能量,其过程是个吸热反应过程,据此分析解答。
【详解】A.酒精的燃烧是放热反应,故A不符题意;
B.氢氧化钡晶体与氯化铵固体反应是吸热反应,故B符合题意;
C.镁和稀硫酸的反应是放热反应,给C不符合题意;
D.酸和碱的中和反应是放热反应,故D不符合题意;
本题答案B。
6.D
【详解】A.人类目前运用最多的能源是化石燃料,其释放的能量由化学反应产生,A正确;
B.煤、石油、天然气三大化石燃料,是当今世界最重要的能源,故目前,全球仍处于化石能源时代,B正确;
C.人体内有机物所含能量的释放是有机物被氧化成简单无机物的过程,属于氧化还原反应,所以人体运动所消耗的能量与氧化还原反应有关,C正确;
D.化学反应放出的能量,可以造福人类,也可以给人类带来灾难,比如火灾,D错误;
故选D。
7.D
【详解】A.化石能源物质内部蕴含的最初能量来源于太阳能,具有大量能量,A项正确;
B.植物光合作用通过一系列生理变化,将太阳能转化为化学能储存在植物体内,B项正确;
C.能量可以相互转化,因此物质的化学能在不同的条件下可以转化为热能,电能等,C项正确;
D.任何反应都有其存在价值,吸热反应可以降低周围的温度,如利用氯化铵和氢氧化钙来降温,D项错误;
故选D。
8.B
【分析】图a中反应物总能量高于生成物总能量,故为放热反应,图b反应中反应物的总能量低于生成物的总能量,反应是吸热反应,据此分析。
【详解】A.图a中反应物总能量高于生成物总能量,故为放热反应,故A错误;
B.能量越低物质越稳定,图b反应中反应物的总能量低于生成物的总能量,反应物比生成物稳定,故B正确;
C.图a为放热反应,氯化铵固体与氢氧化钡晶体的反应是吸热反应,图b中反应物总能量低于生成物总能量,可以表示吸热反应,应该用图b表示,故C错误;
D.图a表示的是放热反应,所有的燃烧均为放热反应,但是多数的燃烧需要加热,图b为吸热反应,吸热反应不一定需要加热才能发生,例如氯化铵和氢氧化钡的反应不需要加热,故D错误;
答案选B。
9.C
【详解】①液态水变成水蒸气是物理变化,①错误;
②酸碱中和反应是放热反应,②正确;
③浓H2SO4稀释是物理变化,③错误;
④固体NaOH溶于水是物理变化,④错误;
⑤H2在Cl2中燃烧是放热反应,⑤正确;
⑥食物腐败是缓慢氧化,是放热反应,⑥正确。
答案为C。
【点睛】常见的放热反应有:物质燃烧、金属与酸或与水反应、中和反应、绝大多数化合反应、铝热反应;常见的吸热反应有:绝大多数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气等)还原金属氧化物、某些复分解(如铵盐和强碱)等。
10.C
【详解】A.1mol石墨转化成1mol金刚石需要吸收热量,则表明石墨的能量比金刚石低,则石墨比金刚石稳定,A不正确;
B.由“1mol石墨转化成1mol金刚石需要吸热”可知,1mol石墨比1mol金刚石总能量低, B不正确;
C.由B选项的分析可知,1mol石墨比1mol金刚石总能量低,则1mol金刚石比1mol石墨总能量高,C正确;
D.同一元素的不同原子互称为同位素,而石墨和金刚石是碳元素构成的不同单质,D不正确;
故选C。
【点睛】对于一个化学反应,能量越低的物质,稳定性越强。
11.B
【详解】A.A→B的反应为吸热反应,B→C的反应为放热反应,故A错误;
B.物质的总能量越低,越稳定,三种化合物中的稳定性BC.A与C的能量差为E4-E3-E1+E2,故C错误;
D.A→B反应为吸热反应,但吸热反应不一定要加热,故D错误;
答案为B。
12.B
【详解】根据题意,H-H键能为436kJ/mol,H-N键能为391kJ/mol,设N≡N的键能为x,对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol,反应热△H =反应物的总键能-生成物的总键能,故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,解得:x=945.6 kJ/mol,则断开1mol N≡N键需吸收的能量是945.6kJ,故选B。
13. 放热 Na2O或CaO(答案合理即可) 吸热 B 饱和澄清石灰水变浑浊 铝和NaOH溶液反应生成H2的反应是放热反应,氢氧化钙的溶解度随温度的升高而降低
【详解】(1)①由图1可知,装置中的压强大于外界大气压,若反应没有气体生成时,说明该反应为放热反应,反应时放出热量使装置中压强增大,加入的物质X可能是Na2O、CaO等,故答案为:Na2O或CaO;
②由图2可知,装置中压强小于外界大气压,若反应没有气体生成时,说明该反应为吸热反应,反应时吸收热量使装置中压强减小;CO还原CuO的反应为放热反应,CaCO3受热分解的反应为吸热反应,Al和Fe2O3高温条件下的反应为放热反应,则B符合题意,故答案为:吸热;B;
(2)把试管放入盛有25℃饱和澄清石灰水的烧杯中,向试管中放入几小块铝片,再滴入5mL NaOH溶液,铝和NaOH溶液反应生成H2的反应是放热反应,放出的热量使澄清石灰水的温度升高,氢氧化钙的溶解度随温度的升高而降低,杯中析出氢氧化钙使饱和澄清石灰水变浑浊,故答案为:饱和澄清石灰水变浑浊;铝和NaOH溶液反应生成H2的反应是放热反应,氢氧化钙的溶解度随温度的升高而降低。
14.(1)吸热
(2)A
(3) 放热 A
【详解】(1)根据冷敷袋在日常生活中有降温、保鲜和镇痛等用途可判断,制作冷敷袋可以利用吸热的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,说明使用过程中需要放热,生石灰溶于水放热,Ba(OH)2·8H2O和NH4Cl混合反应吸热,答案选A。
(3)硫在氧气中燃烧生成二氧化硫是放热反应,反应物总能量高于生成物总能量,其能量变化可用如图中的A表示。答案选A。
试卷第1页,共3页
试卷第1页,共3页
2022-2023学年高一化学人教版2019必修第二册
第六章第一节第1课时化学反应与热能练习题
学校:___________姓名:___________班级:___________
一、单选题
1.下列变化一定是吸热反应的是( )
A.凡需加热后才能发生的反应
B.所有的分解反应
C.将化学能转变为热能的反应
D.生成物总能量大于反应物总能量的反应
2.下列反应属于氧化还原反应,并且 H>0的是( )
A.铝片与稀H2SO4反应 B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2反应 D.甲烷在O2中的燃烧反应
3.下图为反应2H2(g)+O2(g)=2H2O(g)的能量变化示意图,下列说法正确的是( )
A.拆开2molH2 (g)和1 molO2(g)中的化学键成为H、O原子,共放出1368 kJ能量
B.由H、O原子形成2 molH2O(g),共吸收1852 kJ能量
C.2 molH2(g)和1 molO2 (g)反应生成2 mol H2O(1),共吸收484 kJ能量
D.2 molH2 (g)和1 molO2(g)反应生成2 molH2O(g),共放出484 kJ能量
4.下列过程中生成物总能量高于反应物总能量的是( )
A.碳酸钙受热分解 B.乙醇燃烧
C.液态水汽化 D.氧化钙与水反应
5.下列反应过程中的能量变化情况符合如图的是( )
A.酒精的燃烧 B.氢氧化钡晶体与氯化铵固体反应
C.镁和稀硫酸的反应 D.酸和碱的中和反应
6.下列说法不正确的是( )
A.当今社会人们所需的能量绝大部分是由化学反应产生的
B.目前,全球仍处于化石能源时代
C.人体生命活动所需要的能量,是由氧化还原反应提供的
D.凡是放出热量的化学反应均可用来造福人类
7.下列关于能源和作为能源的物质的叙述中,不正确的是( )
A.化石能源物质内部蕴藏着大量的能量
B.绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来
C.物质的化学能可以在不同条件下转为热能、电能为人类所利用
D.吸热反应没有利用价值
8.如图所示,有关化学反应和能量变化的说法正确的是( )
A.图a表示的是吸热反应的能量变化
B.图b中反应物比生成物稳定
C.图a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D.图a中的反应不需要加热就一定能发生,图b中的反应一定需要加热才能发生
9.下列变化过程,属于放热反应的是( )
①液态水变成水蒸气 ②酸碱中和反应 ③浓H2SO4稀释 ④固体NaOH溶于水 ⑤H2在Cl2中燃烧 ⑥食物腐败
A.②③④⑤⑥ B.②③④ C.②⑤⑥ D.①③⑤
10.金刚石和石墨是碳元素的两种结构不同的单质。100kPa下,1mol石墨转化成1mol金刚石需要吸收热量1.895kJ。据此,判断下列结论正确的是( )
A.金刚石比石墨稳定
B.1mol石墨比1mol金刚石总能量高
C.1mol金刚石比1mol石墨总能量高
D.石墨和金刚石是碳元素的同位素
11.某反应由两步反应构成,它的反应能量曲线如图,下列叙述正确的是( )
A.两步反应均为吸热反应
B.三种化合物中C最稳定
C.A与C的能量差为
D.反应,反应条件一定需要加热
12.已知断开1 mol H—H吸收的能量为436 kJ,形成1 mol H—N放出的能量为391 kJ,根据化学方程式N2+3H22NH3,反应完1 mol N2放出的能量为92.4 kJ,则断开1 mol N≡N需吸收的能量是
A.431 kJ B.945.6 kJ C.649 kJ D.869 kJ
二、实验题
13.为了探究化学反应的热效应,某兴趣小组进行了实验:
(1)将纯固体物质X分别装入有水的锥形瓶里(发生化学反应),立即塞紧带U形管的塞子,发现U形管内红墨水的液面高度如图所示。
图1 图2
①若如图1所示,发生的反应(假设没有气体生成)是___________(填“放热”或“吸热”)反应,X可以是___________(填化学式,只填一种即可)。
②若如图2所示,发生的反应(假设没有气体生成)是___________(填“放热”或“吸热”)反应,以下选项中与其能量变化相同的是___________(填字母)。
A. CO还原CuO的反应 B. CaCO3的分解反应 C. Al和Fe2O3的反应
(2)如图3所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放几小块铝片,再滴入5mL NaOH溶液。试回答下列问题:
图3
实验中观察到的现象是:铝片逐渐溶解、有大量气泡产生、___________,产生上述现象的原因是___________。
三、填空题
14.现代社会生活离不开能量。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______(填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______(填序号)反应释放的热量加热食物。
A.生石灰和水 B.Ba(OH)2·8H2O和NH4Cl
(3)硫在氧气中燃烧是_______(填“放热”或“吸热”)反应,其能量变化可用如图中的_______(填序号)表示。
参考答案:
1.D
【详解】反应是放热反应,还是吸热反应,与反应条件无关系。只与反应物和生成物总能量的相对大小有关。如果反应物的总能量大于生成物的总能量,则反应是放热反应,反之是吸热反应,答案选D。
2.C
【详解】A.铝片与稀H2SO4的反应为放热反应,A错误;
B.Ba(OH)2 8H2O与NH4Cl的反应为吸热反应,但不属于氧化还原反应,B错误;
C.灼热的炭与CO2的反应中C元素化合价发生变化,属于氧化还原反应,且为吸热反应,C正确;
D.甲烷在O2中的燃烧反应是放热反应,D错误;
答案选C。
3.D
【详解】A.拆开化学键吸收能量,故A错误;
B.形成化学键放出能量,故B错误;
C.由题干方程式可知应生成气态水,而不是液态水时,放出484 kJ能量,故C错误;
D.依据图象数据分析计算,2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量,故D正确;
故答案为C。
4.A
【详解】A.碳酸钙受热分解属于吸热反应,生成物的总能量高于反应物的总能量,A符合题意;
B.乙醇燃烧属于放热反应,生成物的总能量低于反应物的总能量,B不合题意;
C.液态水汽化是吸热过程,属于物理变化,C不合题意;
D.氧化钙与水反应是放热反应,生成物的总能量低于反应物的总能量,D不合题意;
故选A。
【点睛】对于常见的反应,燃烧反应、绝大部分化合反应、酸碱中和反应、活泼金属与酸或水的反应、铝热反应等,都是放热反应。
5.B
【分析】根据图中的能量变化,可知生成物的总能量高于反应物的总能量,其过程是个吸热反应过程,据此分析解答。
【详解】A.酒精的燃烧是放热反应,故A不符题意;
B.氢氧化钡晶体与氯化铵固体反应是吸热反应,故B符合题意;
C.镁和稀硫酸的反应是放热反应,给C不符合题意;
D.酸和碱的中和反应是放热反应,故D不符合题意;
本题答案B。
6.D
【详解】A.人类目前运用最多的能源是化石燃料,其释放的能量由化学反应产生,A正确;
B.煤、石油、天然气三大化石燃料,是当今世界最重要的能源,故目前,全球仍处于化石能源时代,B正确;
C.人体内有机物所含能量的释放是有机物被氧化成简单无机物的过程,属于氧化还原反应,所以人体运动所消耗的能量与氧化还原反应有关,C正确;
D.化学反应放出的能量,可以造福人类,也可以给人类带来灾难,比如火灾,D错误;
故选D。
7.D
【详解】A.化石能源物质内部蕴含的最初能量来源于太阳能,具有大量能量,A项正确;
B.植物光合作用通过一系列生理变化,将太阳能转化为化学能储存在植物体内,B项正确;
C.能量可以相互转化,因此物质的化学能在不同的条件下可以转化为热能,电能等,C项正确;
D.任何反应都有其存在价值,吸热反应可以降低周围的温度,如利用氯化铵和氢氧化钙来降温,D项错误;
故选D。
8.B
【分析】图a中反应物总能量高于生成物总能量,故为放热反应,图b反应中反应物的总能量低于生成物的总能量,反应是吸热反应,据此分析。
【详解】A.图a中反应物总能量高于生成物总能量,故为放热反应,故A错误;
B.能量越低物质越稳定,图b反应中反应物的总能量低于生成物的总能量,反应物比生成物稳定,故B正确;
C.图a为放热反应,氯化铵固体与氢氧化钡晶体的反应是吸热反应,图b中反应物总能量低于生成物总能量,可以表示吸热反应,应该用图b表示,故C错误;
D.图a表示的是放热反应,所有的燃烧均为放热反应,但是多数的燃烧需要加热,图b为吸热反应,吸热反应不一定需要加热才能发生,例如氯化铵和氢氧化钡的反应不需要加热,故D错误;
答案选B。
9.C
【详解】①液态水变成水蒸气是物理变化,①错误;
②酸碱中和反应是放热反应,②正确;
③浓H2SO4稀释是物理变化,③错误;
④固体NaOH溶于水是物理变化,④错误;
⑤H2在Cl2中燃烧是放热反应,⑤正确;
⑥食物腐败是缓慢氧化,是放热反应,⑥正确。
答案为C。
【点睛】常见的放热反应有:物质燃烧、金属与酸或与水反应、中和反应、绝大多数化合反应、铝热反应;常见的吸热反应有:绝大多数分解反应、个别的化合反应(如C和CO2)、工业制水煤气、碳(一氧化碳、氢气等)还原金属氧化物、某些复分解(如铵盐和强碱)等。
10.C
【详解】A.1mol石墨转化成1mol金刚石需要吸收热量,则表明石墨的能量比金刚石低,则石墨比金刚石稳定,A不正确;
B.由“1mol石墨转化成1mol金刚石需要吸热”可知,1mol石墨比1mol金刚石总能量低, B不正确;
C.由B选项的分析可知,1mol石墨比1mol金刚石总能量低,则1mol金刚石比1mol石墨总能量高,C正确;
D.同一元素的不同原子互称为同位素,而石墨和金刚石是碳元素构成的不同单质,D不正确;
故选C。
【点睛】对于一个化学反应,能量越低的物质,稳定性越强。
11.B
【详解】A.A→B的反应为吸热反应,B→C的反应为放热反应,故A错误;
B.物质的总能量越低,越稳定,三种化合物中的稳定性B
D.A→B反应为吸热反应,但吸热反应不一定要加热,故D错误;
答案为B。
12.B
【详解】根据题意,H-H键能为436kJ/mol,H-N键能为391kJ/mol,设N≡N的键能为x,对于反应N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol,反应热△H =反应物的总键能-生成物的总键能,故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,解得:x=945.6 kJ/mol,则断开1mol N≡N键需吸收的能量是945.6kJ,故选B。
13. 放热 Na2O或CaO(答案合理即可) 吸热 B 饱和澄清石灰水变浑浊 铝和NaOH溶液反应生成H2的反应是放热反应,氢氧化钙的溶解度随温度的升高而降低
【详解】(1)①由图1可知,装置中的压强大于外界大气压,若反应没有气体生成时,说明该反应为放热反应,反应时放出热量使装置中压强增大,加入的物质X可能是Na2O、CaO等,故答案为:Na2O或CaO;
②由图2可知,装置中压强小于外界大气压,若反应没有气体生成时,说明该反应为吸热反应,反应时吸收热量使装置中压强减小;CO还原CuO的反应为放热反应,CaCO3受热分解的反应为吸热反应,Al和Fe2O3高温条件下的反应为放热反应,则B符合题意,故答案为:吸热;B;
(2)把试管放入盛有25℃饱和澄清石灰水的烧杯中,向试管中放入几小块铝片,再滴入5mL NaOH溶液,铝和NaOH溶液反应生成H2的反应是放热反应,放出的热量使澄清石灰水的温度升高,氢氧化钙的溶解度随温度的升高而降低,杯中析出氢氧化钙使饱和澄清石灰水变浑浊,故答案为:饱和澄清石灰水变浑浊;铝和NaOH溶液反应生成H2的反应是放热反应,氢氧化钙的溶解度随温度的升高而降低。
14.(1)吸热
(2)A
(3) 放热 A
【详解】(1)根据冷敷袋在日常生活中有降温、保鲜和镇痛等用途可判断,制作冷敷袋可以利用吸热的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,说明使用过程中需要放热,生石灰溶于水放热,Ba(OH)2·8H2O和NH4Cl混合反应吸热,答案选A。
(3)硫在氧气中燃烧生成二氧化硫是放热反应,反应物总能量高于生成物总能量,其能量变化可用如图中的A表示。答案选A。
试卷第1页,共3页
试卷第1页,共3页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
