实验活动1 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学
文档属性
| 名称 | 实验活动1 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 180.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-16 00:00:00 | ||
图片预览


文档简介
实验活动1 金属的物理性质和某些化学性质 同步练习
一、单选题
1.“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理方案的个数是( )
①比较硬度,硬度小的是“愚人金”
②灼烧,表面变色的是“愚人金”
③浸没在稀碗酸中,表面有气海产生的是“愚人金”
④浸没在硫酸镁溶液中,表面附着白色物质的是“愚人金”
A.1个 B.2个 C.3个 D.4个
2.教材中的图表、数据等能给我们的学习提供许多信息。下列说法中错误的是( )
A.根据某元素的原子结构示意图,可以判断该元素原子核内中子的数目
B.根据物质的溶解度曲线,可以确定某些混合物的分离方法
C.根据金属活动性顺序,可以判断某些置换反应能否发生
D.常见物质的溶解性表,是判断复分解反应能否发生的依据之一
3.下列所示的图像能反映相对应实验的是()
A.向pH=12的Ca(OH)2溶液中不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.将等质量的金属镁片和锌片分别和足量的相同质量分数的稀硫酸混合
4.为验证Zn、Cu、Ag三种金属的活动性强弱,某科学兴趣小组设计了下图所示的四个实验。其中不必进行的实验是( )
A. B.
C. D.
5.向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,充分反应后过滤,得到固体甲和溶液乙,下列说法错误的是( )
A.固体甲中一定含有银,溶液乙中一定含有硝酸锌
B.若溶液乙中呈现无色,则溶液乙中只含有一种溶质
C.向溶液乙中再加锌粉,若有红色固体析出,则固体甲的组成有两种可能
D.向溶液乙中滴加稀盐酸,若有白色沉淀生成,则溶液乙中含有两种溶质
6.下列物质的用途主要与其化学性质有关的是()
A.金刚石用于切割玻璃 B.高粱常用于酿制白酒
C.铜常用来做电线电缆 D.干冰可用作人工降雨
7.下列有关金属的说法错误的是( )
A.铜能导电 B.银能与稀盐酸反应
C.镁的活动性比铁强 D.铝具有良好的抗腐蚀性
8.如图所示的四个图象,能正确反映对应变化关系的是( )
A.镁在氧气中燃烧 B.向二氧化锰中加入过氧化氢溶液 C.向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
A.A B.B C.C D.D
9.下列关于物质用途的描述不正确的是( )
A.熟石灰用于改良酸性土壤 B.氧气可用做燃料
C.铜丝用做导线 D.二氧化碳可用做气体肥料
10.某金属放入稀硫酸中,不产生气泡,该金属可能是( )
A.Mg B.Al C.Zn D.Ag
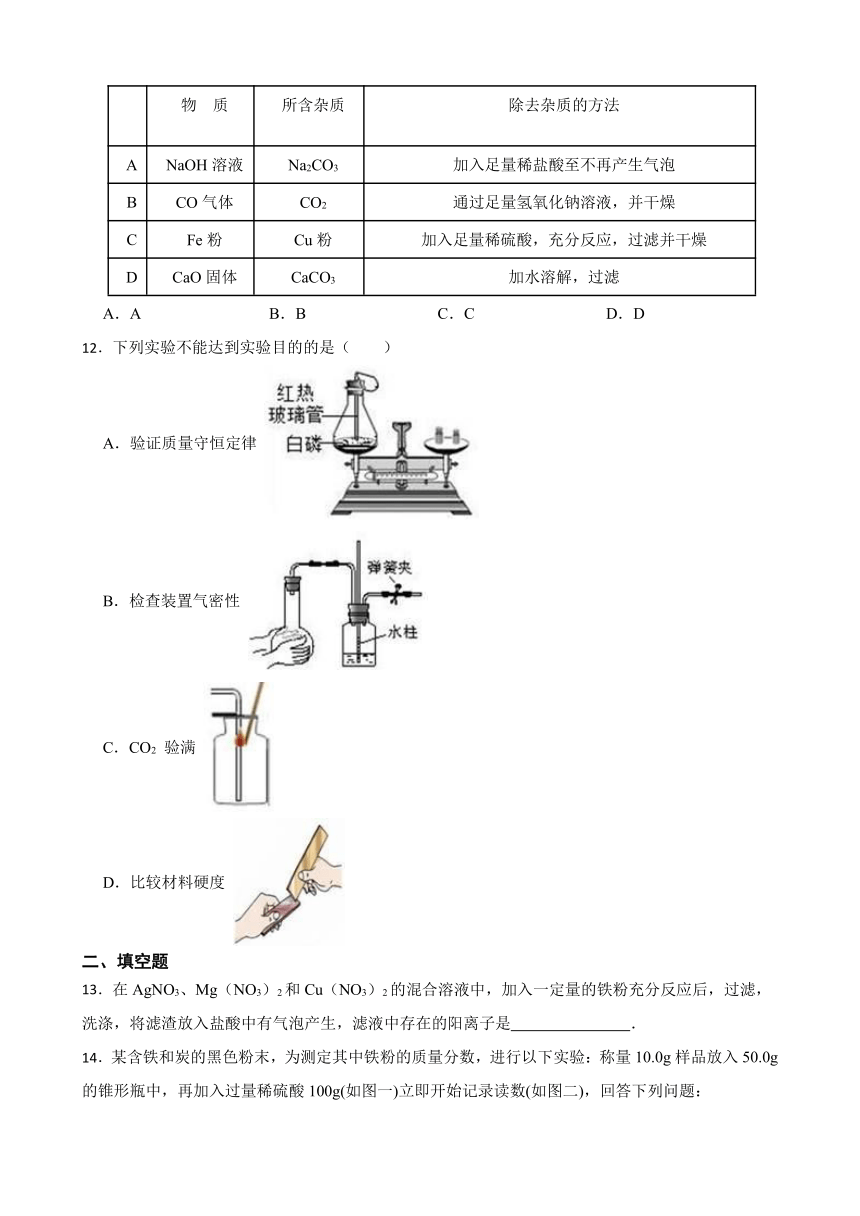
11.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
物 质 所含杂质 除去杂质的方法
A NaOH溶液 Na2CO3 加入足量稀盐酸至不再产生气泡
B CO气体 CO2 通过足量氢氧化钠溶液,并干燥
C Fe粉 Cu粉 加入足量稀硫酸,充分反应,过滤并干燥
D CaO固体 CaCO3 加水溶解,过滤
A.A B.B C.C D.D
12.下列实验不能达到实验目的的是( )
A.验证质量守恒定律
B.检查装置气密性
C.CO2 验满
D.比较材料硬度
二、填空题
13.在AgNO3、Mg(NO3)2和Cu(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子是 .
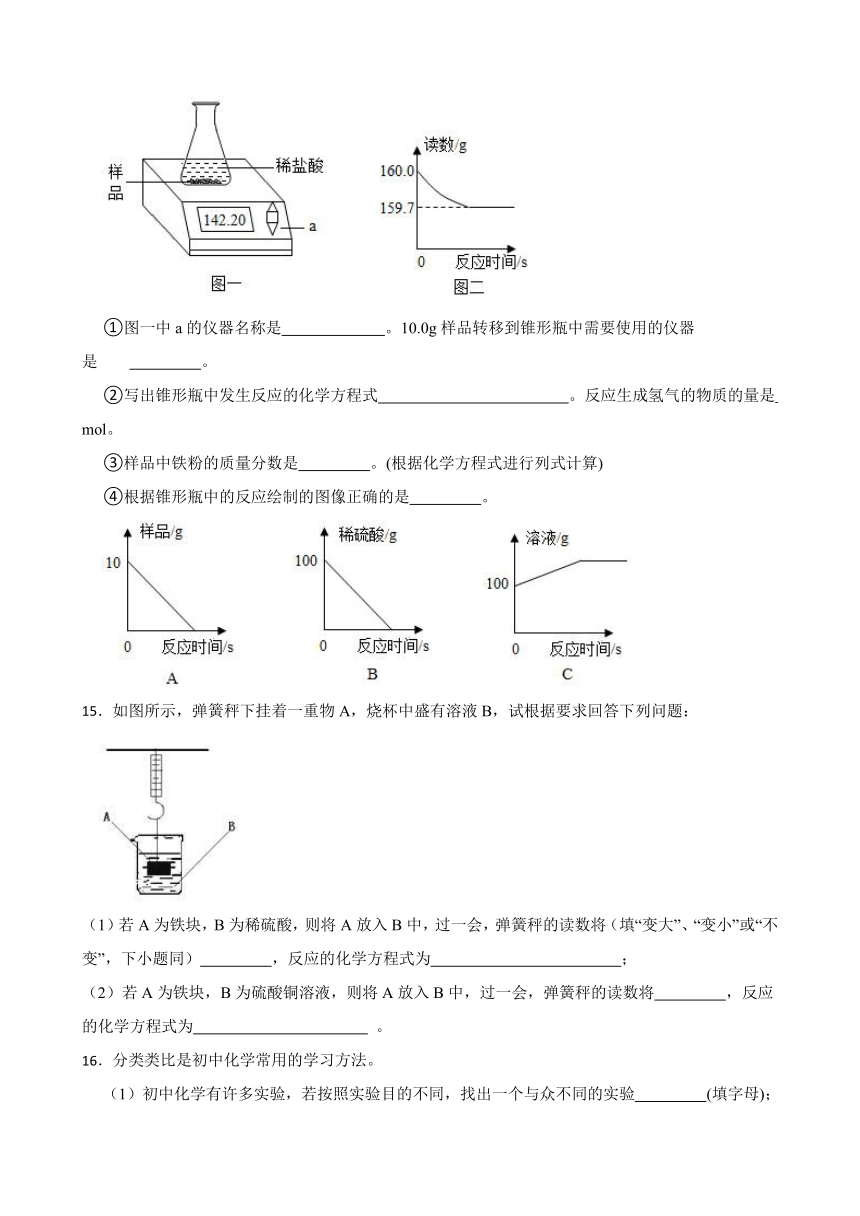
14.某含铁和炭的黑色粉末,为测定其中铁粉的质量分数,进行以下实验:称量10.0g样品放入50.0g的锥形瓶中,再加入过量稀硫酸100g(如图一)立即开始记录读数(如图二),回答下列问题:
①图一中a的仪器名称是 。10.0g样品转移到锥形瓶中需要使用的仪器是 。
②写出锥形瓶中发生反应的化学方程式 。反应生成氢气的物质的量是 mol。
③样品中铁粉的质量分数是 。(根据化学方程式进行列式计算)
④根据锥形瓶中的反应绘制的图像正确的是 。
15.如图所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:
(1)若A为铁块,B为稀硫酸,则将A放入B中,过一会,弹簧秤的读数将(填“变大”、“变小”或“不变”,下小题同) ,反应的化学方程式为 ;
(2)若A为铁块,B为硫酸铜溶液,则将A放入B中,过一会,弹簧秤的读数将 ,反应的化学方程式为 。
16.分类类比是初中化学常用的学习方法。
(1)初中化学有许多实验,若按照实验目的不同,找出一个与众不同的实验 (填字母);选择的依据是 。
A 将红热的木炭伸入盛有氧气的集气瓶中 B 将燃着的硫伸入盛有氧气的集气瓶中 C 将打磨过的铝丝浸入硫酸铜溶液中 D 在蓝色火焰上方罩一个冷而干的烧杯
(2)二氧化硫和二氧化碳的化学性质相似,能与水反应生成亚硫酸,请写出将二氧化硫气体通入到氨水中反应的化学方程式 ;亚硫酸和碳酸的化学性质相似,如常温下易分解,亚硫酸钠也能与硫酸发生反应,请写出此反应的化学方程式 。
17.如图台灯中,铜质插头是利用了金属铜的 性(填“导电”或“导热”);灯管后面的反光片为铝箔,铝制品耐腐蚀的原因是 ;制作铁螺丝钉需要利用高炉炼铁,其主要反应原理是一氧化碳与氧化铁的反应,该反应的化学方程式为 ;制作灯座的塑料属于 材料(填“天然”或“合成”)。
18.下列是与人类的生活与未来密切的物质:
A.氢气 B.干冰 C.酒精 D.甲烷 E.铁粉 F.钛合金,选择相应的编号填空
① 是实验室常用的燃料,
② 可以提供清洁、高效的能源,
③ 是天然气的主要成分,
④ 可用于人工降雨,
⑤ 可用来同时吸收氧气和水分,以防止食品腐败.
⑥ 与人体具有很好的“相容性”,因此可以用来制造人造骨.
三、综合题
19.金属材料用途广泛,回答下列问题:
(1)人们大量使用的是合金而不是纯金属,是因为合金具有更多优良性能.例如钢铁比纯铁硬度 (填“大”或“小”).
(2)钢铁表面刷油漆,目的是阻止铁与空气中的氧气、 接触而生锈,若要检测钢铁表面的油漆是否破损,可在油漆表面涂上Cu(NO3)2溶液,其原理是 (用化学方程式表示).
(3)锰钢是制造坦克装甲的原料.已知,镁能置换出MnSO4溶液中的Mn,而铁不能,则Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序为 .
(4)金属资源是有限的,我们要珍惜和保护它,有效途径是 (只写一点).
20.电动独轮车是新一代的节能、环保、便携的代步工具.它体形小巧、携带方便,最轻的一款只有10Kg,可以直接放进汽车后备箱,提到家里或是办公室.
(1)制造电动独轮车所用的主要材料最好是 ;(在A.B、C中选填)
A.韧性好、硬度大的锰钢
B.强度好、密度小的铝合金
C.抗腐蚀性好的不锈钢
(2)电动独轮车充电2个小时,可以行驶25Km,短途代步非常方便,可以代替公交和地铁.电动独轮车在行走时的全部能量转化是 .
(3)电动独轮车中许多电线为铜制的,铜能和浓硝酸反应,生成二氧化氮、硝酸铜和水,其反应方程式为 ,反应后氮元素的化合价为 .
(4)在环境污染日益严重的背景下,电动独轮车的大力普及,可缓解资源的消耗并减少 、 等空气污染物的排放.
21.
(1)归纳与比较,是学习化学的重要方法之一,对比CO和CO2,它们的组成元素 ,但它们的化学性质 ,工业上CO可用来冶炼金属,是利用它的 性.
(2)铝具有良好的抗腐蚀性,是由于铝在空气中与氧气反应,在其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化,铝与氧气反应的化学方程式为 .
(3)进入森林,注意防火,通常状况下燃烧需要三个条件:①可燃物 ②氧气(或空气) ③ ;当森林发生火灾时,将大火蔓延路线前的一片树木砍掉,形成隔离带,其灭火原理是 .
四、实验探究题
22.某实验小组拟利用相同条件下等质量的同种酸溶液与金属反应来探究“金属活动性与反应放出热量”之间的关系。实验装置如图1;实验完成后,根据传感器探头测量的从反应开始到反应停止时的数值绘制的曲线图如图2;实验所用酸与金属粉末的种类和质量如下表。请回答问题并进行相关计算。
实验编组 等质量稀硫酸 金属粉末质量/种类 对应曲线
① 含H2SO49.8g 6.5g/镁 a
② 含H2SO49.8g 6.5g/锌 b
③ 含H2SO49.8g 6.5g/铁 c(待绘制)
(1)根据实验探究目的,对比曲线a、b,可得出的结论是 。
(2)在图2画出曲线c的大致位置及趋势图。
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】B
4.【答案】B
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】B
10.【答案】D
11.【答案】B
12.【答案】C
13.【答案】Fe2+、Mg2+
14.【答案】电子天平;药匙;Fe+H2SO4=FeSO4+H2↑;0.15;84%;C
15.【答案】变小;Fe+H2SO4=FeSO4+H2↑;变大;Fe+CuSO4=FeSO4+Cu
16.【答案】(1)D;实验D是探究物质的组成
(2)SO2+2NH3 H2O=(NH4)2SO3+2H2O;Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
17.【答案】导电;铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;;合成
18.【答案】C;A;D;B;E;F
19.【答案】(1)大
(2)水蒸气;Fe+Cu(NO3)2=Fe(NO3)2+Cu
(3)Mg>Mn>Fe>Cu
(4)合理的开发金属资源
20.【答案】(1)B
(2)化学能转化为电能转化为机械能
(3)Cu+4HNO3=2NO2↑+Cu(NO3)2+2H2O;+4价、+5价
(4)CO、SO2、NO2;烟尘或粉尘
21.【答案】(1)相同;不同;还原
(2)4Al+3O2═2Al2O3
(3)温度达到可燃物的着火点;清除可燃物
22.【答案】(1)其它条件相同时,金属越活泼,反应放出热量越多
(2)
一、单选题
1.“愚人金”实为铜锌合金,外观与黄金极为相似,常被不法商贩冒充黄金牟取暴利,下列关于鉴别“愚人金”与黄金的实验方案,合理方案的个数是( )
①比较硬度,硬度小的是“愚人金”
②灼烧,表面变色的是“愚人金”
③浸没在稀碗酸中,表面有气海产生的是“愚人金”
④浸没在硫酸镁溶液中,表面附着白色物质的是“愚人金”
A.1个 B.2个 C.3个 D.4个
2.教材中的图表、数据等能给我们的学习提供许多信息。下列说法中错误的是( )
A.根据某元素的原子结构示意图,可以判断该元素原子核内中子的数目
B.根据物质的溶解度曲线,可以确定某些混合物的分离方法
C.根据金属活动性顺序,可以判断某些置换反应能否发生
D.常见物质的溶解性表,是判断复分解反应能否发生的依据之一
3.下列所示的图像能反映相对应实验的是()
A.向pH=12的Ca(OH)2溶液中不断加水稀释
B.向碳酸钙固体中逐滴加入稀盐酸至过量
C.在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D.将等质量的金属镁片和锌片分别和足量的相同质量分数的稀硫酸混合
4.为验证Zn、Cu、Ag三种金属的活动性强弱,某科学兴趣小组设计了下图所示的四个实验。其中不必进行的实验是( )
A. B.
C. D.
5.向硝酸银和硝酸铜的混合溶液中加入一定量的锌粉,充分反应后过滤,得到固体甲和溶液乙,下列说法错误的是( )
A.固体甲中一定含有银,溶液乙中一定含有硝酸锌
B.若溶液乙中呈现无色,则溶液乙中只含有一种溶质
C.向溶液乙中再加锌粉,若有红色固体析出,则固体甲的组成有两种可能
D.向溶液乙中滴加稀盐酸,若有白色沉淀生成,则溶液乙中含有两种溶质
6.下列物质的用途主要与其化学性质有关的是()
A.金刚石用于切割玻璃 B.高粱常用于酿制白酒
C.铜常用来做电线电缆 D.干冰可用作人工降雨
7.下列有关金属的说法错误的是( )
A.铜能导电 B.银能与稀盐酸反应
C.镁的活动性比铁强 D.铝具有良好的抗腐蚀性
8.如图所示的四个图象,能正确反映对应变化关系的是( )
A.镁在氧气中燃烧 B.向二氧化锰中加入过氧化氢溶液 C.向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 D.等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应
A.A B.B C.C D.D
9.下列关于物质用途的描述不正确的是( )
A.熟石灰用于改良酸性土壤 B.氧气可用做燃料
C.铜丝用做导线 D.二氧化碳可用做气体肥料
10.某金属放入稀硫酸中,不产生气泡,该金属可能是( )
A.Mg B.Al C.Zn D.Ag
11.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
物 质 所含杂质 除去杂质的方法
A NaOH溶液 Na2CO3 加入足量稀盐酸至不再产生气泡
B CO气体 CO2 通过足量氢氧化钠溶液,并干燥
C Fe粉 Cu粉 加入足量稀硫酸,充分反应,过滤并干燥
D CaO固体 CaCO3 加水溶解,过滤
A.A B.B C.C D.D
12.下列实验不能达到实验目的的是( )
A.验证质量守恒定律
B.检查装置气密性
C.CO2 验满
D.比较材料硬度
二、填空题
13.在AgNO3、Mg(NO3)2和Cu(NO3)2的混合溶液中,加入一定量的铁粉充分反应后,过滤,洗涤,将滤渣放入盐酸中有气泡产生,滤液中存在的阳离子是 .
14.某含铁和炭的黑色粉末,为测定其中铁粉的质量分数,进行以下实验:称量10.0g样品放入50.0g的锥形瓶中,再加入过量稀硫酸100g(如图一)立即开始记录读数(如图二),回答下列问题:
①图一中a的仪器名称是 。10.0g样品转移到锥形瓶中需要使用的仪器是 。
②写出锥形瓶中发生反应的化学方程式 。反应生成氢气的物质的量是 mol。
③样品中铁粉的质量分数是 。(根据化学方程式进行列式计算)
④根据锥形瓶中的反应绘制的图像正确的是 。
15.如图所示,弹簧秤下挂着一重物A,烧杯中盛有溶液B,试根据要求回答下列问题:
(1)若A为铁块,B为稀硫酸,则将A放入B中,过一会,弹簧秤的读数将(填“变大”、“变小”或“不变”,下小题同) ,反应的化学方程式为 ;
(2)若A为铁块,B为硫酸铜溶液,则将A放入B中,过一会,弹簧秤的读数将 ,反应的化学方程式为 。
16.分类类比是初中化学常用的学习方法。
(1)初中化学有许多实验,若按照实验目的不同,找出一个与众不同的实验 (填字母);选择的依据是 。
A 将红热的木炭伸入盛有氧气的集气瓶中 B 将燃着的硫伸入盛有氧气的集气瓶中 C 将打磨过的铝丝浸入硫酸铜溶液中 D 在蓝色火焰上方罩一个冷而干的烧杯
(2)二氧化硫和二氧化碳的化学性质相似,能与水反应生成亚硫酸,请写出将二氧化硫气体通入到氨水中反应的化学方程式 ;亚硫酸和碳酸的化学性质相似,如常温下易分解,亚硫酸钠也能与硫酸发生反应,请写出此反应的化学方程式 。
17.如图台灯中,铜质插头是利用了金属铜的 性(填“导电”或“导热”);灯管后面的反光片为铝箔,铝制品耐腐蚀的原因是 ;制作铁螺丝钉需要利用高炉炼铁,其主要反应原理是一氧化碳与氧化铁的反应,该反应的化学方程式为 ;制作灯座的塑料属于 材料(填“天然”或“合成”)。
18.下列是与人类的生活与未来密切的物质:
A.氢气 B.干冰 C.酒精 D.甲烷 E.铁粉 F.钛合金,选择相应的编号填空
① 是实验室常用的燃料,
② 可以提供清洁、高效的能源,
③ 是天然气的主要成分,
④ 可用于人工降雨,
⑤ 可用来同时吸收氧气和水分,以防止食品腐败.
⑥ 与人体具有很好的“相容性”,因此可以用来制造人造骨.
三、综合题
19.金属材料用途广泛,回答下列问题:
(1)人们大量使用的是合金而不是纯金属,是因为合金具有更多优良性能.例如钢铁比纯铁硬度 (填“大”或“小”).
(2)钢铁表面刷油漆,目的是阻止铁与空气中的氧气、 接触而生锈,若要检测钢铁表面的油漆是否破损,可在油漆表面涂上Cu(NO3)2溶液,其原理是 (用化学方程式表示).
(3)锰钢是制造坦克装甲的原料.已知,镁能置换出MnSO4溶液中的Mn,而铁不能,则Mn、Fe、Mg、Cu四种金属的活动性由强到弱的顺序为 .
(4)金属资源是有限的,我们要珍惜和保护它,有效途径是 (只写一点).
20.电动独轮车是新一代的节能、环保、便携的代步工具.它体形小巧、携带方便,最轻的一款只有10Kg,可以直接放进汽车后备箱,提到家里或是办公室.
(1)制造电动独轮车所用的主要材料最好是 ;(在A.B、C中选填)
A.韧性好、硬度大的锰钢
B.强度好、密度小的铝合金
C.抗腐蚀性好的不锈钢
(2)电动独轮车充电2个小时,可以行驶25Km,短途代步非常方便,可以代替公交和地铁.电动独轮车在行走时的全部能量转化是 .
(3)电动独轮车中许多电线为铜制的,铜能和浓硝酸反应,生成二氧化氮、硝酸铜和水,其反应方程式为 ,反应后氮元素的化合价为 .
(4)在环境污染日益严重的背景下,电动独轮车的大力普及,可缓解资源的消耗并减少 、 等空气污染物的排放.
21.
(1)归纳与比较,是学习化学的重要方法之一,对比CO和CO2,它们的组成元素 ,但它们的化学性质 ,工业上CO可用来冶炼金属,是利用它的 性.
(2)铝具有良好的抗腐蚀性,是由于铝在空气中与氧气反应,在其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化,铝与氧气反应的化学方程式为 .
(3)进入森林,注意防火,通常状况下燃烧需要三个条件:①可燃物 ②氧气(或空气) ③ ;当森林发生火灾时,将大火蔓延路线前的一片树木砍掉,形成隔离带,其灭火原理是 .
四、实验探究题
22.某实验小组拟利用相同条件下等质量的同种酸溶液与金属反应来探究“金属活动性与反应放出热量”之间的关系。实验装置如图1;实验完成后,根据传感器探头测量的从反应开始到反应停止时的数值绘制的曲线图如图2;实验所用酸与金属粉末的种类和质量如下表。请回答问题并进行相关计算。
实验编组 等质量稀硫酸 金属粉末质量/种类 对应曲线
① 含H2SO49.8g 6.5g/镁 a
② 含H2SO49.8g 6.5g/锌 b
③ 含H2SO49.8g 6.5g/铁 c(待绘制)
(1)根据实验探究目的,对比曲线a、b,可得出的结论是 。
(2)在图2画出曲线c的大致位置及趋势图。
答案解析部分
1.【答案】B
2.【答案】A
3.【答案】B
4.【答案】B
5.【答案】D
6.【答案】B
7.【答案】B
8.【答案】B
9.【答案】B
10.【答案】D
11.【答案】B
12.【答案】C
13.【答案】Fe2+、Mg2+
14.【答案】电子天平;药匙;Fe+H2SO4=FeSO4+H2↑;0.15;84%;C
15.【答案】变小;Fe+H2SO4=FeSO4+H2↑;变大;Fe+CuSO4=FeSO4+Cu
16.【答案】(1)D;实验D是探究物质的组成
(2)SO2+2NH3 H2O=(NH4)2SO3+2H2O;Na2SO3+H2SO4=Na2SO4+SO2↑+H2O
17.【答案】导电;铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;;合成
18.【答案】C;A;D;B;E;F
19.【答案】(1)大
(2)水蒸气;Fe+Cu(NO3)2=Fe(NO3)2+Cu
(3)Mg>Mn>Fe>Cu
(4)合理的开发金属资源
20.【答案】(1)B
(2)化学能转化为电能转化为机械能
(3)Cu+4HNO3=2NO2↑+Cu(NO3)2+2H2O;+4价、+5价
(4)CO、SO2、NO2;烟尘或粉尘
21.【答案】(1)相同;不同;还原
(2)4Al+3O2═2Al2O3
(3)温度达到可燃物的着火点;清除可燃物
22.【答案】(1)其它条件相同时,金属越活泼,反应放出热量越多
(2)
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
