3.2 酸和碱的中和反应 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学
文档属性
| 名称 | 3.2 酸和碱的中和反应 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 202.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-16 00:00:00 | ||
图片预览


文档简介
3.2 酸和碱的中和反应 同步练习
一、单选题
1.下列常见物质中,碱性最强的是( )
物质 橘子汁 西瓜汁 鸡蛋清 肥皂水
pH 3~4 6~7 7~8 9~10
A.橘子汁 B.西瓜汁 C.鸡蛋清 D.肥皂水
2.某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如右图所示。下列说法正确的是( )
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C.该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
3.下列说法中正确的是( )
A.通常把pH<7的降水称为酸雨
B.原子的质量几乎都集中在原子核中
C.氯化铵可以与草木灰(含碳酸钾)混合施用
D.生活中常接触到的“高钙牛奶”、“碘盐”中的“钙”、“碘”指的是离子
4.关于生活中的化学知识,下列说法正确的是( )
A.用厨房清洁剂除水垢
B.喝完汽水打嗝是因为压强增大气体溶解度减小
C.室内起火时立即打开所有门窗
D.人被蚊虫叮咬后可抹牙膏、肥皂水
5.已知生活中厕所清洁剂的pH=1,厨房的清洁剂的pH=12。下列关于两者的说法错误的是( )
A.厕所清洁剂加水稀释,溶液pH升高
B.厨房清洁剂可能含有NaOH
C.混合使用能提高两者的清洁效果
D.厕所清洁剂可能使铁制下水道腐蚀
6.下列有关量的描述正确的是( )
A.氧原子的相对原子质量是16g
B.用10mL量筒量取9.5mL蒸馏水
C.pH试纸测得某溶液的pH为7.8
D.空气中氧气的质量分数约为21%
7.下列实验操作正确的是( )
A. 点燃酒精灯 B. 闻气体气味
C. 稀释浓硫酸 D. 测溶液pH
8.如图中的“表示人体内的一些体液和排泄物的正常pH范围,据此判断其中酸性最强的是( )
A.血浆 B.唾液 C.胃液 D.尿液
9.以人为本,关注健康,是人类永恒的主题。下列叙述错误的是( )
A.人体的胃液pH<7。有助于消化
B.幼儿及青少年缺少钙元素,会得佝偻病和发育不良
C.铁、锌、硒、钾是人体所需的微量元素
D.“皮革奶”是将皮革加工成蛋白质加入奶粉中对健康有害,应禁止销售
10.目前,防治环境污染已成为保证人类健康生存、保障社会持续发展的全球性大事。下列有关说法错误的是( )
A.废旧电池随意丢弃,不会造成环境污染
B.废弃的聚乙烯塑料随意丢弃会造成“白色污染”
C.pH<5.6的降水称为酸雨,汽车尾气是导致酸雨的原因之一
D.水污染主要缘于工业废水、农业废水和生活污水的任意排放
11.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.将镁片和锌片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向硫酸和硫酸铜的混合溶液中加入过量的氢氧化钠溶液
12.等质量的氢氧化钠溶液和稀盐酸混合后,若所得溶液pH=7,则( )
A.混合溶液中钠离子与氯离子个数相等
B.所用氢氧化钠溶液和稀盐酸的溶质质量分数相等
C.混合前后阳离子总数不变
D.混合前后水分子总数不变
二、填空题
13.氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,应该用 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰粉与草木灰(主要成分:K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.在有露水的早晨,把“黑白粉”撒在植物茎叶上,可杀灭某些害虫.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
14.化学可以帮助人类认识改造周围的世界,促进社会发展.
糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
每100g含有 营养成分 糖类 油脂 蛋白质 维生素C 钙 镁 钠 锌
7.6g 7.8g 7.4g 18mg 201mg 18.2mg 30.8mg 8.1mg
①燕麦片的营养成分中能与水反应生成氨基酸的营养物质是 ;每克营养物质氧化时放出能量最多的是 ;人体必需的微量元素是 .
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意 ;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点 .
15.学习化学需要在宏观物质的性质与其微观结构之间建立联系.1个CO2分子由 构成.在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是 ,常温下,这三种物质的水溶液中pH<7的是 .
16.通过一年的化学学习,我们熟悉了许多物质,请从①红磷 ②氢氧化铝 ③火碱 ④二氧化锰 ⑤硫酸铜 ⑥酒精中选择相应物质的序号填空:
(1)碘酒中的溶剂是 ;
(2)实验室制氧气常用的催化剂是 ;
(3)常用于治疗胃酸过多的药物是 ;
(4)炉具清洁剂中含有的物质是 ;
(5)测定空气中氧气含量所用的固体单质是 ;
(6)用于配制农药波尔多液的是 .
17.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为 ;当加入熟石灰mg时,溶液中的溶质为 (填写化学式)
18.请回答下列与水有关的问题:
(1)生活中常用 的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为 不同,所以它们的化学性质不同;
(3)实验室中可通过Na2CO3和CaCO3在水中 的不同加以区别.
(4)可用 来测定水的酸碱度.
三、综合题
19.观察下列三幅微观结构示意图,并按要求填空:
(1)图1和图2分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图。请你结合已有的酸、碱知识,判断溴化氢的水溶液显 (填“酸性”“中性”或“碱性”,下同),乙醇的水溶液显 。
(2)图3代表氢氧化钠和盐酸反应的微观过程,由图中可知酸碱中和的实质是 和 (填离子符号)发生结合。类比写出溴化氢的水溶液和氢氧化钠反应的化学方程式 。
20.某氧化铜矿石主要成分是CuO、Cu(OH)2、CuCO3、Fe2O3及不溶于酸的杂质,用该矿石制备硫酸铜晶体和硫酸亚铁晶体的工艺流程如图。
(资料)Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.5 4.2
沉淀完全的pH 3.7 6.7
请回答问题:
(1)酸溶前粉碎氧化铜矿石的作用是 。
(2)写出往氧化铜矿粉中加入足量硫酸发生中和反应的化学方程式 。溶液1中溶质有CuSO4、 (写出一种的化学式)。
(3)调pH不高于 ,调pH选用的最佳化合物为 (填序号)。
A.Na2CO3 B.CuO C.NaCl D.H2SO4
(4)往溶液3中加入过量的铁粉,其中一个反应是铁与铁盐反应生成是硫酸亚铁,请写出反应方程式 。
(5)FeSO4 7H2O可部分脱水制备FeSO4 xH2O,x与加热温度和时间的关系如下表,则得到FeSO4 3H2O适宜的工艺条件为温度 ℃、时间 h。
序号 ① ② ③ ④ ⑤ ⑥
时间/h 2 3 3.5 4 4.2 4.3
温度℃ 50 80 100 130 150 230
x的数值 6 5 4 3 2 1
21.根据描述填空:
(1)根据下列图文回答问题:
①青铜剑属于 (填“纯金属”或“合金”).
②高钙豆奶粉的“钙”指的是 (填“元素”、“原子”、或“分子”).
③C60分子是由 构成的.
④干冰可用于 (填一例).
(2)根据图2中自制汽水的配料回答问题.
①柠檬酸的pH 7(填“<”、“=”或“>”),能使紫色石蕊溶液变为 色.
②配料中富含维生素的是 ,小苏打的化学式是 .
四、实验探究题
22.华雪在做氢氧化钠溶液和稀盐酸发生中和反应的实验时使用了无色酚酞试液.
(1)使用无色酚酞试液的作用是 .
(2)实验过程中,华雪同学发现溶液由红色变成了无色,于是她判断该溶液呈中性.你认为正确吗? ,理由是 .
(3)下面我们就这个问题一起来进行实验探究:
【猜想假设】
猜想①:该溶液呈中性,是氯化钠溶液.
猜想②:该溶液显碱性,是氯化钠溶液和氢氧化钠溶液的混合溶液.
猜想③:该溶液显酸性,是 和 混合溶液.
吴丽认为猜想 肯定是错误的,理由是 .
【探究实验】取样,向溶液中加入 物质,看到 现象.
【结论与反思】通过以上实验现象得出:猜想 正确.使酚酞溶液显无色的不一定是中性溶液.
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】B
4.【答案】D
5.【答案】C
6.【答案】B
7.【答案】B
8.【答案】C
9.【答案】C
10.【答案】A
11.【答案】B
12.【答案】A
13.【答案】CaO+H2O═Ca(OH)2;用玻璃棒蘸取少量待测液滴在干燥的pH试纸上;CO2+Ca(OH)2═CaCO3↓+H2O;Ca(OH)2+K2CO3=CaCO3↓+2KOH;K
14.【答案】蛋白质;油脂;锌;不要高温加热;食醋
15.【答案】一个碳原子和两个氧原子;氢氧化钠、氯化钠;硫酸
16.【答案】(1)⑥
(2)④
(3)②
(4)③
(5)①
(6)⑤
17.【答案】Ca(OH)2+2HCl=CaCl2+2H2O;CaCl2和HCl
18.【答案】煮沸;分子结构;溶解性;pH试纸
19.【答案】(1)酸性;中性
(2)H+;OH-;HBr + NaOH = NaBr + H2O
20.【答案】(1)增大反应物接触面积,加快反应速率
(2)Cu(OH)2+H2SO4═CuSO4+2H2O;H2SO4或Fe2(SO4)3
(3)3.7;B
(4)Fe2(SO4)3+Fe=3FeSO4
(5)130;4
21.【答案】(1)合金;元素;碳原子;人工降雨
(2)<;红;果汁;NaHCO3
22.【答案】(1)实验时便于观察现象
(2)不正确;酸和中性的物质均使无色酚酞不变色
(3)盐酸溶液;氯化钠溶液;②;溶液呈碱性酚酞溶液呈红色;锌粒(合理即可);有气泡产生;③(现象与结论要一致才算对)
一、单选题
1.下列常见物质中,碱性最强的是( )
物质 橘子汁 西瓜汁 鸡蛋清 肥皂水
pH 3~4 6~7 7~8 9~10
A.橘子汁 B.西瓜汁 C.鸡蛋清 D.肥皂水
2.某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如右图所示。下列说法正确的是( )
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是Na2SO4和H2SO4
C.该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
3.下列说法中正确的是( )
A.通常把pH<7的降水称为酸雨
B.原子的质量几乎都集中在原子核中
C.氯化铵可以与草木灰(含碳酸钾)混合施用
D.生活中常接触到的“高钙牛奶”、“碘盐”中的“钙”、“碘”指的是离子
4.关于生活中的化学知识,下列说法正确的是( )
A.用厨房清洁剂除水垢
B.喝完汽水打嗝是因为压强增大气体溶解度减小
C.室内起火时立即打开所有门窗
D.人被蚊虫叮咬后可抹牙膏、肥皂水
5.已知生活中厕所清洁剂的pH=1,厨房的清洁剂的pH=12。下列关于两者的说法错误的是( )
A.厕所清洁剂加水稀释,溶液pH升高
B.厨房清洁剂可能含有NaOH
C.混合使用能提高两者的清洁效果
D.厕所清洁剂可能使铁制下水道腐蚀
6.下列有关量的描述正确的是( )
A.氧原子的相对原子质量是16g
B.用10mL量筒量取9.5mL蒸馏水
C.pH试纸测得某溶液的pH为7.8
D.空气中氧气的质量分数约为21%
7.下列实验操作正确的是( )
A. 点燃酒精灯 B. 闻气体气味
C. 稀释浓硫酸 D. 测溶液pH
8.如图中的“表示人体内的一些体液和排泄物的正常pH范围,据此判断其中酸性最强的是( )
A.血浆 B.唾液 C.胃液 D.尿液
9.以人为本,关注健康,是人类永恒的主题。下列叙述错误的是( )
A.人体的胃液pH<7。有助于消化
B.幼儿及青少年缺少钙元素,会得佝偻病和发育不良
C.铁、锌、硒、钾是人体所需的微量元素
D.“皮革奶”是将皮革加工成蛋白质加入奶粉中对健康有害,应禁止销售
10.目前,防治环境污染已成为保证人类健康生存、保障社会持续发展的全球性大事。下列有关说法错误的是( )
A.废旧电池随意丢弃,不会造成环境污染
B.废弃的聚乙烯塑料随意丢弃会造成“白色污染”
C.pH<5.6的降水称为酸雨,汽车尾气是导致酸雨的原因之一
D.水污染主要缘于工业废水、农业废水和生活污水的任意排放
11.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.将镁片和锌片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合
C.向pH=10的氢氧化钙溶液中不断加水稀释
D.向硫酸和硫酸铜的混合溶液中加入过量的氢氧化钠溶液
12.等质量的氢氧化钠溶液和稀盐酸混合后,若所得溶液pH=7,则( )
A.混合溶液中钠离子与氯离子个数相等
B.所用氢氧化钠溶液和稀盐酸的溶质质量分数相等
C.混合前后阳离子总数不变
D.混合前后水分子总数不变
二、填空题
13.氢氧化钙俗称熟石灰,在生产和生活中有广泛的用途.
(1)熟石灰可由生石灰溶于水制得,反应的化学方程式是: .测量其溶液的pH时,应该用 ,再用标准比色卡比较试纸显示的颜色,读取该溶液的pH.
(2)用石灰浆粉刷墙壁,干燥后墙面变硬,反应的化学方程式是: .
(3)用熟石灰粉与草木灰(主要成分:K2CO3)按一定比例混合可制得高效环保农药“黑白粉”.在有露水的早晨,把“黑白粉”撒在植物茎叶上,可杀灭某些害虫.
①“黑白粉”比熟石灰更高效,是由于生成了碱性更强的KOH,反应的化学方程式是 .
②“黑白粉”还可提供植物必需的营养素是 (填元素符号).
14.化学可以帮助人类认识改造周围的世界,促进社会发展.
糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
每100g含有 营养成分 糖类 油脂 蛋白质 维生素C 钙 镁 钠 锌
7.6g 7.8g 7.4g 18mg 201mg 18.2mg 30.8mg 8.1mg
①燕麦片的营养成分中能与水反应生成氨基酸的营养物质是 ;每克营养物质氧化时放出能量最多的是 ;人体必需的微量元素是 .
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意 ;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点 .
15.学习化学需要在宏观物质的性质与其微观结构之间建立联系.1个CO2分子由 构成.在氢氧化钠、氯化钠、硫酸三种物质中,由阴阳离子构成的是 ,常温下,这三种物质的水溶液中pH<7的是 .
16.通过一年的化学学习,我们熟悉了许多物质,请从①红磷 ②氢氧化铝 ③火碱 ④二氧化锰 ⑤硫酸铜 ⑥酒精中选择相应物质的序号填空:
(1)碘酒中的溶剂是 ;
(2)实验室制氧气常用的催化剂是 ;
(3)常用于治疗胃酸过多的药物是 ;
(4)炉具清洁剂中含有的物质是 ;
(5)测定空气中氧气含量所用的固体单质是 ;
(6)用于配制农药波尔多液的是 .
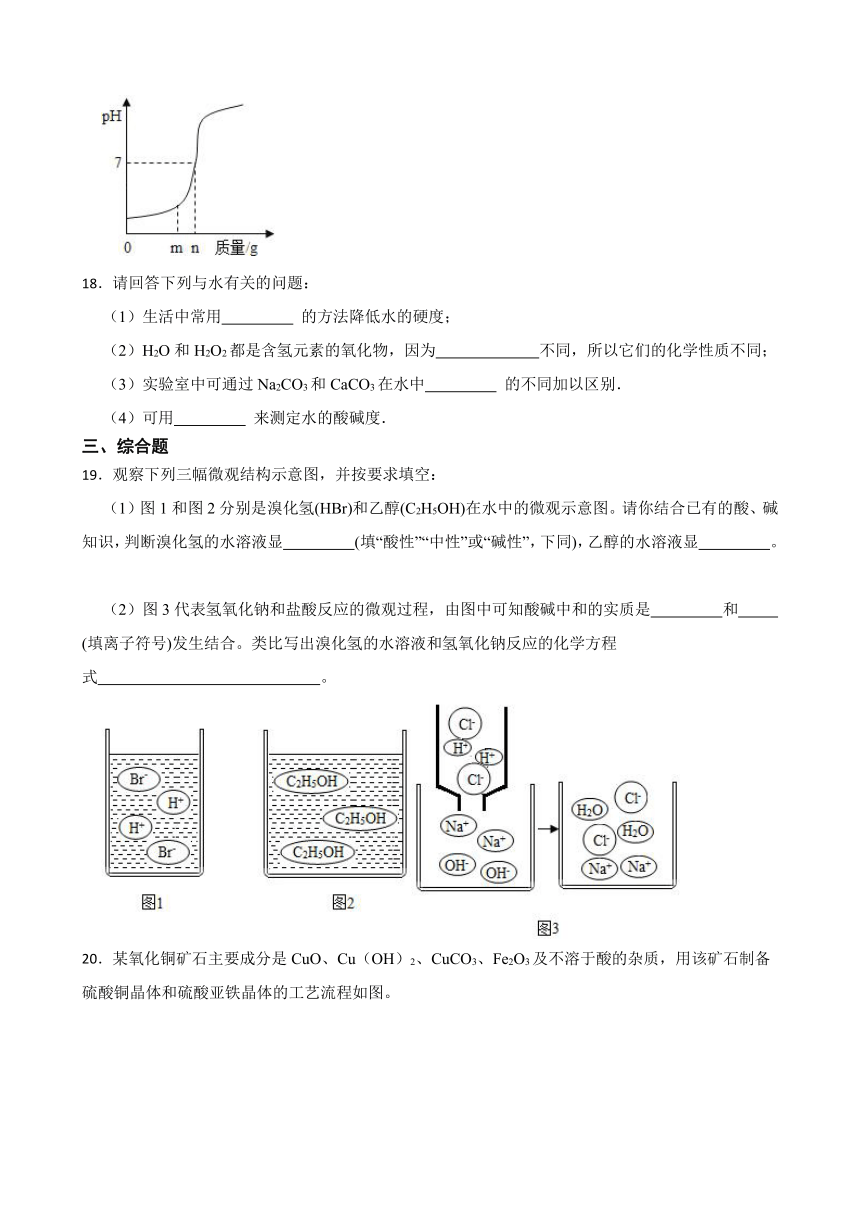
17.用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为 ;当加入熟石灰mg时,溶液中的溶质为 (填写化学式)
18.请回答下列与水有关的问题:
(1)生活中常用 的方法降低水的硬度;
(2)H2O和H2O2都是含氢元素的氧化物,因为 不同,所以它们的化学性质不同;
(3)实验室中可通过Na2CO3和CaCO3在水中 的不同加以区别.
(4)可用 来测定水的酸碱度.
三、综合题
19.观察下列三幅微观结构示意图,并按要求填空:
(1)图1和图2分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图。请你结合已有的酸、碱知识,判断溴化氢的水溶液显 (填“酸性”“中性”或“碱性”,下同),乙醇的水溶液显 。
(2)图3代表氢氧化钠和盐酸反应的微观过程,由图中可知酸碱中和的实质是 和 (填离子符号)发生结合。类比写出溴化氢的水溶液和氢氧化钠反应的化学方程式 。
20.某氧化铜矿石主要成分是CuO、Cu(OH)2、CuCO3、Fe2O3及不溶于酸的杂质,用该矿石制备硫酸铜晶体和硫酸亚铁晶体的工艺流程如图。
(资料)Cu2+、Fe3+以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 Fe(OH)3 Cu(OH)2
开始沉淀的pH 1.5 4.2
沉淀完全的pH 3.7 6.7
请回答问题:
(1)酸溶前粉碎氧化铜矿石的作用是 。
(2)写出往氧化铜矿粉中加入足量硫酸发生中和反应的化学方程式 。溶液1中溶质有CuSO4、 (写出一种的化学式)。
(3)调pH不高于 ,调pH选用的最佳化合物为 (填序号)。
A.Na2CO3 B.CuO C.NaCl D.H2SO4
(4)往溶液3中加入过量的铁粉,其中一个反应是铁与铁盐反应生成是硫酸亚铁,请写出反应方程式 。
(5)FeSO4 7H2O可部分脱水制备FeSO4 xH2O,x与加热温度和时间的关系如下表,则得到FeSO4 3H2O适宜的工艺条件为温度 ℃、时间 h。
序号 ① ② ③ ④ ⑤ ⑥
时间/h 2 3 3.5 4 4.2 4.3
温度℃ 50 80 100 130 150 230
x的数值 6 5 4 3 2 1
21.根据描述填空:
(1)根据下列图文回答问题:
①青铜剑属于 (填“纯金属”或“合金”).
②高钙豆奶粉的“钙”指的是 (填“元素”、“原子”、或“分子”).
③C60分子是由 构成的.
④干冰可用于 (填一例).
(2)根据图2中自制汽水的配料回答问题.
①柠檬酸的pH 7(填“<”、“=”或“>”),能使紫色石蕊溶液变为 色.
②配料中富含维生素的是 ,小苏打的化学式是 .
四、实验探究题
22.华雪在做氢氧化钠溶液和稀盐酸发生中和反应的实验时使用了无色酚酞试液.
(1)使用无色酚酞试液的作用是 .
(2)实验过程中,华雪同学发现溶液由红色变成了无色,于是她判断该溶液呈中性.你认为正确吗? ,理由是 .
(3)下面我们就这个问题一起来进行实验探究:
【猜想假设】
猜想①:该溶液呈中性,是氯化钠溶液.
猜想②:该溶液显碱性,是氯化钠溶液和氢氧化钠溶液的混合溶液.
猜想③:该溶液显酸性,是 和 混合溶液.
吴丽认为猜想 肯定是错误的,理由是 .
【探究实验】取样,向溶液中加入 物质,看到 现象.
【结论与反思】通过以上实验现象得出:猜想 正确.使酚酞溶液显无色的不一定是中性溶液.
答案解析部分
1.【答案】D
2.【答案】D
3.【答案】B
4.【答案】D
5.【答案】C
6.【答案】B
7.【答案】B
8.【答案】C
9.【答案】C
10.【答案】A
11.【答案】B
12.【答案】A
13.【答案】CaO+H2O═Ca(OH)2;用玻璃棒蘸取少量待测液滴在干燥的pH试纸上;CO2+Ca(OH)2═CaCO3↓+H2O;Ca(OH)2+K2CO3=CaCO3↓+2KOH;K
14.【答案】蛋白质;油脂;锌;不要高温加热;食醋
15.【答案】一个碳原子和两个氧原子;氢氧化钠、氯化钠;硫酸
16.【答案】(1)⑥
(2)④
(3)②
(4)③
(5)①
(6)⑤
17.【答案】Ca(OH)2+2HCl=CaCl2+2H2O;CaCl2和HCl
18.【答案】煮沸;分子结构;溶解性;pH试纸
19.【答案】(1)酸性;中性
(2)H+;OH-;HBr + NaOH = NaBr + H2O
20.【答案】(1)增大反应物接触面积,加快反应速率
(2)Cu(OH)2+H2SO4═CuSO4+2H2O;H2SO4或Fe2(SO4)3
(3)3.7;B
(4)Fe2(SO4)3+Fe=3FeSO4
(5)130;4
21.【答案】(1)合金;元素;碳原子;人工降雨
(2)<;红;果汁;NaHCO3
22.【答案】(1)实验时便于观察现象
(2)不正确;酸和中性的物质均使无色酚酞不变色
(3)盐酸溶液;氯化钠溶液;②;溶液呈碱性酚酞溶液呈红色;锌粒(合理即可);有气泡产生;③(现象与结论要一致才算对)
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
