实验活动2 一定溶质质量分数的氯化钠溶液的配制 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学
文档属性
| 名称 | 实验活动2 一定溶质质量分数的氯化钠溶液的配制 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级下册化学 |

|
|
| 格式 | zip | ||
| 文件大小 | 217.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-16 00:00:00 | ||
图片预览



文档简介
实验活动2 一定溶质质量分数的氯化钠溶液的配制
一、单选题
1.某同学欲配制50g 5%的氯化钠溶液,下列说法中正确的是( )
A.用蒸馏水洗涤试剂瓶后立即盛装配好的氯化钠溶液
B.用500mL的烧杯量取所需要的水
C.用托盘天平准确称取氯化钠固体2.5g
D.氯化钠固体溶解时用玻璃棒搅拌的目的是增大其在水中的溶解度
2.氯化钠在生活、生产中有广泛应用.下列做法或说法中错误的是( )
A.配制一定溶质质量分数的氯化钠溶液时,使用玻璃棒搅拌,加快氯化钠的溶解
B.“粗盐中难溶性杂质的去除”的实验中,当蒸发皿中的滤液全部蒸干后才能停止加热
C.氯化钠的水溶液能导电是因为它在水中解离出自由移动的和
D.氯化钠的溶解度受温度变化的影响不大
3.配制一定溶质质量分数的氯化钠溶液,操作步骤如下图所示。则正确的操作顺序是( )
A.④⑤①②③ B.①②③④⑤ C.③④①②⑤ D.②①④③⑤
4.泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%.在配制4%的食盐水时,会导致溶液浓度偏小的是
( )
①称量好的食盐倒入烧杯时,有少许洒出 ②量水的体积时,俯视量筒 ③溶解食盐的烧杯内壁是潮湿的
④用4g食盐和100g水配制溶液.
A.②③ B.①③④ C.①②③ D.①②③④
5.用氯化钠固体配制 10%的氯化钠溶液,下列说法正确的是()
A.实验操作依次是:计算、溶解、称量、装瓶并贴标签
B.实验中必须用到的仪器有:玻璃棒、量筒、烧杯、蒸发皿
C.把 10g 氯化钠固体放入盛有 90mL 水的量筒中混合均匀
D.转移配置好的溶液时有少量液体溅出,溶质质量分数不变
6.将含泥沙的粗盐提纯,并用制得的精盐配制80g10%的食盐溶液.下列说法错误的是( )
A.过滤操作时,搅拌漏斗中的液体,可以加快过滤的速度
B.配制时需用的主要仪器有:天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
C.配制溶液的步骤是:计算、称量、溶解、转移装瓶、贴标签
D.蒸发滤液时,不断用玻璃棒搅拌,防止液体溅出
7.现有烧杯、试管、量筒、带铁圈的铁架台、酒精灯、集气瓶、玻璃片、水槽、带导管橡皮塞、天平、玻璃棒,仅有这些仪器(所需化学药品可任选)不能完成实验是()
A.制取氧气
B.粗盐提纯
C.制取二氧化碳
D.用氯化钠晶体配制100g5%的氯化钠溶液
8.小明同学要用6%的氯化钠溶液配制100g 3%的氯化钠溶液,下列说法不正确是( )
A.小明同学需要量取水的体积为50mL
B.实验的步骤为计算、称量、量取、溶解、装瓶贴签
C.实验中所需玻璃仪器为玻璃棒、胶头滴管、烧杯、量筒、细口瓶
D.在其他操作均正确情况下,若在量取6%的氯化钠溶液过程中,仰视刻度量取该溶液了,则所配制溶液的溶质质量分数大于3%
9.现配制溶质质量分数为5%的NaCl溶液,下列说法正确的是( )
A.将氯化钠固体直接放在天平的托盘上称量
B.配制溶液的烧杯留有水
C.为加快固体溶解,用温度计搅拌
D.将配好的溶液倒入细口瓶中,塞紧瓶塞并贴上标签
10.农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该浓度溶液的过程如下图所示。下列说法错误的是( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16g
C.选用100mL量筒量取所需水
D.①中有部分固体洒落所配溶液的浓度偏大
11.下列是“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
A.取用氯化钠固体
B.称量氯化钠固体
C.量取水的体积
D.溶解
12.实验室中配制100mL10%的稀硫酸,不需要使用的仪器是( )
A.烧杯 B.托盘天平 C.量筒 D.玻璃棒
二、填空题
13.在实验室配制溶质的质量分数为10%的氯化钠溶液100g,经计算,在 上称量 g氯化钠并倒入干燥洁净的烧杯里,然后用 量取 mL蒸馏水倒入装有氯化钠的烧杯里,并用 不断搅拌,使氯化钠完全溶解,即得所需的溶液.
14.配制100g溶质的质量分数为16%的氯化钠溶液,实验操作如下:
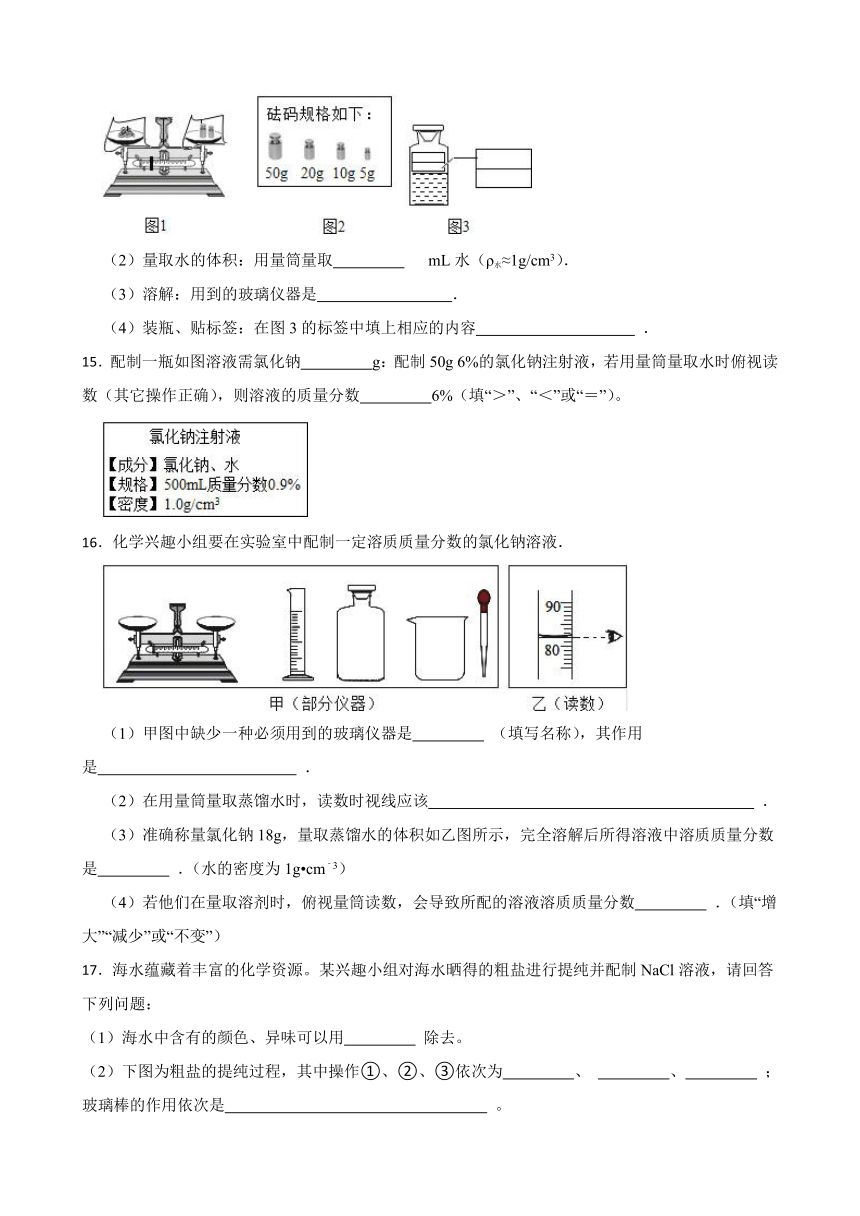
(1)称量氯化钠固体的质量:所选砝码为 、游码的示数为 .
(2)量取水的体积:用量筒量取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在图3的标签中填上相应的内容 .
15.配制一瓶如图溶液需氯化钠 g:配制50g 6%的氯化钠注射液,若用量筒量取水时俯视读数(其它操作正确),则溶液的质量分数 6%(填“>”、“<”或“=”)。
16.化学兴趣小组要在实验室中配制一定溶质质量分数的氯化钠溶液.
(1)甲图中缺少一种必须用到的玻璃仪器是 (填写名称),其作用是 .
(2)在用量筒量取蒸馏水时,读数时视线应该 .
(3)准确称量氯化钠18g,量取蒸馏水的体积如乙图所示,完全溶解后所得溶液中溶质质量分数是 .(水的密度为1g cm﹣3)
(4)若他们在量取溶剂时,俯视量筒读数,会导致所配的溶液溶质质量分数 .(填“增大”“减少”或“不变”)
17.海水蕴藏着丰富的化学资源。某兴趣小组对海水晒得的粗盐进行提纯并配制NaCl溶液,请回答下列问题:
(1)海水中含有的颜色、异味可以用 除去。
(2)下图为粗盐的提纯过程,其中操作①、②、③依次为 、 、 ;玻璃棒的作用依次是 。
(3)若NaCl的产率偏低(),则可能的原因是(填字母)
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含泥沙的粗食盐时,加入的水量不足
(4)用上述实验所得NaCl晶体配制50g溶质质量分数为5%NaCl溶液,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、
18.某同学用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你参与完成:
(1)计算:氯化钠的质量为 g;
(2)称量:用托盘天平称量,氯化钠应放在 (填“左盘”或“右盘”);
(3)溶解:溶解时要用到玻璃棒,其作用是 .
三、综合题
19.学习了酸、碱、盐有关知识后,小明在实验室称量氢氧化钠固体,配制了溶质质量分数为10%的氢氧化钠溶液,进行以下探究:
(1)若图Ⅰ中游码标尺读数为1.8,则他称取的氢氧化钠质量是 g.
(2)图Ⅱ中反应的化学方程式是 .
(3)图Ⅲ中玻璃棒的作用是 ,当出现较多固体时,应 .
20.配制溶质质量分数一定的氯化钠溶液,常按以下操作顺序进行。请回答下列问题:
(1)计算:配制100g溶质质量分数为5%的氯化钠溶液所需:氯化钠5g。
称量:用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应____;
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节平衡螺母 D.向右盘加砝码
(2)量取:用量筒来量取所需的水,若仰视读数,则配制后溶液的质量分数会 ;
(3)溶解:将氯化钠和水倒入烧杯中,溶解时玻璃棒搅拌的目的是 ;
转移到试剂瓶中贴好标签。
21.水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。
(1)生活中常用 的方法降低水的硬度;
(2)在电解水的实验中,电源的正、负极产生的气体体积比约为 。
(3)某同学配制50g质量分数为10%的Na2CO3溶液,操作过程如图所示:
配制溶液的正确操作顺序为 (填序号);步骤④中玻璃棒的作用 。
四、实验探究题
22.以下是实验室配制一定溶质质量分数的氯化钠溶液的流程示意图。请根据示意图回答:
(1)托盘天平左盘中固体氯化钠的质量为 g,量筒中水的体积为 mL;
(2)上述溶液取10g加40g水进行稀释,所得氯化钠溶液的溶质质量分数是 。
(3)上述操作中玻璃棒的作用是 。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】A
4.【答案】B
5.【答案】D
6.【答案】A
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】B
13.【答案】托盘天平;10;100mL量筒;90;玻璃棒
14.【答案】10g和5g;1g;84;烧杯、玻璃棒;16% 氯化钠溶液
15.【答案】4.5;>
16.【答案】玻璃棒;加快氯化钠的溶解速度;与量筒内液体的凹液面的最低处保持水平;18%;偏大
17.【答案】活性炭;溶解;过滤;蒸发;加速溶解、引流、防止液滴飞溅;BC;量筒
18.【答案】11.7;左盘;搅拌以加速溶解
19.【答案】(1)8.8
(2)HCl+NaOH=NaCl+H2O
(3)搅拌,防止局部温度过高而使液体飞溅;停止加热
20.【答案】(1)B
(2)偏小
(3)搅拌,加速氯化钠溶解
21.【答案】(1)加热煮沸
(2)1:2
(3)②①⑤③④;搅拌,加速溶解
22.【答案】(1)12;68
(2)3%
(3)搅拌,加快溶解
一、单选题
1.某同学欲配制50g 5%的氯化钠溶液,下列说法中正确的是( )
A.用蒸馏水洗涤试剂瓶后立即盛装配好的氯化钠溶液
B.用500mL的烧杯量取所需要的水
C.用托盘天平准确称取氯化钠固体2.5g
D.氯化钠固体溶解时用玻璃棒搅拌的目的是增大其在水中的溶解度
2.氯化钠在生活、生产中有广泛应用.下列做法或说法中错误的是( )
A.配制一定溶质质量分数的氯化钠溶液时,使用玻璃棒搅拌,加快氯化钠的溶解
B.“粗盐中难溶性杂质的去除”的实验中,当蒸发皿中的滤液全部蒸干后才能停止加热
C.氯化钠的水溶液能导电是因为它在水中解离出自由移动的和
D.氯化钠的溶解度受温度变化的影响不大
3.配制一定溶质质量分数的氯化钠溶液,操作步骤如下图所示。则正确的操作顺序是( )
A.④⑤①②③ B.①②③④⑤ C.③④①②⑤ D.②①④③⑤
4.泡菜具有独特的风味,适合制作泡菜的食盐水浓度是4%.在配制4%的食盐水时,会导致溶液浓度偏小的是
( )
①称量好的食盐倒入烧杯时,有少许洒出 ②量水的体积时,俯视量筒 ③溶解食盐的烧杯内壁是潮湿的
④用4g食盐和100g水配制溶液.
A.②③ B.①③④ C.①②③ D.①②③④
5.用氯化钠固体配制 10%的氯化钠溶液,下列说法正确的是()
A.实验操作依次是:计算、溶解、称量、装瓶并贴标签
B.实验中必须用到的仪器有:玻璃棒、量筒、烧杯、蒸发皿
C.把 10g 氯化钠固体放入盛有 90mL 水的量筒中混合均匀
D.转移配置好的溶液时有少量液体溅出,溶质质量分数不变
6.将含泥沙的粗盐提纯,并用制得的精盐配制80g10%的食盐溶液.下列说法错误的是( )
A.过滤操作时,搅拌漏斗中的液体,可以加快过滤的速度
B.配制时需用的主要仪器有:天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
C.配制溶液的步骤是:计算、称量、溶解、转移装瓶、贴标签
D.蒸发滤液时,不断用玻璃棒搅拌,防止液体溅出
7.现有烧杯、试管、量筒、带铁圈的铁架台、酒精灯、集气瓶、玻璃片、水槽、带导管橡皮塞、天平、玻璃棒,仅有这些仪器(所需化学药品可任选)不能完成实验是()
A.制取氧气
B.粗盐提纯
C.制取二氧化碳
D.用氯化钠晶体配制100g5%的氯化钠溶液
8.小明同学要用6%的氯化钠溶液配制100g 3%的氯化钠溶液,下列说法不正确是( )
A.小明同学需要量取水的体积为50mL
B.实验的步骤为计算、称量、量取、溶解、装瓶贴签
C.实验中所需玻璃仪器为玻璃棒、胶头滴管、烧杯、量筒、细口瓶
D.在其他操作均正确情况下,若在量取6%的氯化钠溶液过程中,仰视刻度量取该溶液了,则所配制溶液的溶质质量分数大于3%
9.现配制溶质质量分数为5%的NaCl溶液,下列说法正确的是( )
A.将氯化钠固体直接放在天平的托盘上称量
B.配制溶液的烧杯留有水
C.为加快固体溶解,用温度计搅拌
D.将配好的溶液倒入细口瓶中,塞紧瓶塞并贴上标签
10.农业上常用质量分数为16%的NaCl溶液选种。实验室配制100g该浓度溶液的过程如下图所示。下列说法错误的是( )
A.实验操作顺序为④②①⑤③
B.②中需称量NaCl的质量为16g
C.选用100mL量筒量取所需水
D.①中有部分固体洒落所配溶液的浓度偏大
11.下列是“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
A.取用氯化钠固体
B.称量氯化钠固体
C.量取水的体积
D.溶解
12.实验室中配制100mL10%的稀硫酸,不需要使用的仪器是( )
A.烧杯 B.托盘天平 C.量筒 D.玻璃棒
二、填空题
13.在实验室配制溶质的质量分数为10%的氯化钠溶液100g,经计算,在 上称量 g氯化钠并倒入干燥洁净的烧杯里,然后用 量取 mL蒸馏水倒入装有氯化钠的烧杯里,并用 不断搅拌,使氯化钠完全溶解,即得所需的溶液.
14.配制100g溶质的质量分数为16%的氯化钠溶液,实验操作如下:
(1)称量氯化钠固体的质量:所选砝码为 、游码的示数为 .
(2)量取水的体积:用量筒量取 mL水(ρ水≈1g/cm3).
(3)溶解:用到的玻璃仪器是 .
(4)装瓶、贴标签:在图3的标签中填上相应的内容 .
15.配制一瓶如图溶液需氯化钠 g:配制50g 6%的氯化钠注射液,若用量筒量取水时俯视读数(其它操作正确),则溶液的质量分数 6%(填“>”、“<”或“=”)。
16.化学兴趣小组要在实验室中配制一定溶质质量分数的氯化钠溶液.
(1)甲图中缺少一种必须用到的玻璃仪器是 (填写名称),其作用是 .
(2)在用量筒量取蒸馏水时,读数时视线应该 .
(3)准确称量氯化钠18g,量取蒸馏水的体积如乙图所示,完全溶解后所得溶液中溶质质量分数是 .(水的密度为1g cm﹣3)
(4)若他们在量取溶剂时,俯视量筒读数,会导致所配的溶液溶质质量分数 .(填“增大”“减少”或“不变”)
17.海水蕴藏着丰富的化学资源。某兴趣小组对海水晒得的粗盐进行提纯并配制NaCl溶液,请回答下列问题:
(1)海水中含有的颜色、异味可以用 除去。
(2)下图为粗盐的提纯过程,其中操作①、②、③依次为 、 、 ;玻璃棒的作用依次是 。
(3)若NaCl的产率偏低(),则可能的原因是(填字母)
A.过滤时滤纸有破损
B.蒸发时有固体溅出
C.溶解含泥沙的粗食盐时,加入的水量不足
(4)用上述实验所得NaCl晶体配制50g溶质质量分数为5%NaCl溶液,配制时需要的玻璃仪器有烧杯、玻璃棒、滴管、
18.某同学用提取的精盐配制100g质量分数为11.7%的氯化钠溶液,请你参与完成:
(1)计算:氯化钠的质量为 g;
(2)称量:用托盘天平称量,氯化钠应放在 (填“左盘”或“右盘”);
(3)溶解:溶解时要用到玻璃棒,其作用是 .
三、综合题
19.学习了酸、碱、盐有关知识后,小明在实验室称量氢氧化钠固体,配制了溶质质量分数为10%的氢氧化钠溶液,进行以下探究:
(1)若图Ⅰ中游码标尺读数为1.8,则他称取的氢氧化钠质量是 g.
(2)图Ⅱ中反应的化学方程式是 .
(3)图Ⅲ中玻璃棒的作用是 ,当出现较多固体时,应 .
20.配制溶质质量分数一定的氯化钠溶液,常按以下操作顺序进行。请回答下列问题:
(1)计算:配制100g溶质质量分数为5%的氯化钠溶液所需:氯化钠5g。
称量:用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应____;
A.增加适量氯化钠固体 B.减少适量氯化钠固体
C.调节平衡螺母 D.向右盘加砝码
(2)量取:用量筒来量取所需的水,若仰视读数,则配制后溶液的质量分数会 ;
(3)溶解:将氯化钠和水倒入烧杯中,溶解时玻璃棒搅拌的目的是 ;
转移到试剂瓶中贴好标签。
21.水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。
(1)生活中常用 的方法降低水的硬度;
(2)在电解水的实验中,电源的正、负极产生的气体体积比约为 。
(3)某同学配制50g质量分数为10%的Na2CO3溶液,操作过程如图所示:
配制溶液的正确操作顺序为 (填序号);步骤④中玻璃棒的作用 。
四、实验探究题
22.以下是实验室配制一定溶质质量分数的氯化钠溶液的流程示意图。请根据示意图回答:
(1)托盘天平左盘中固体氯化钠的质量为 g,量筒中水的体积为 mL;
(2)上述溶液取10g加40g水进行稀释,所得氯化钠溶液的溶质质量分数是 。
(3)上述操作中玻璃棒的作用是 。
答案解析部分
1.【答案】C
2.【答案】B
3.【答案】A
4.【答案】B
5.【答案】D
6.【答案】A
7.【答案】B
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】C
12.【答案】B
13.【答案】托盘天平;10;100mL量筒;90;玻璃棒
14.【答案】10g和5g;1g;84;烧杯、玻璃棒;16% 氯化钠溶液
15.【答案】4.5;>
16.【答案】玻璃棒;加快氯化钠的溶解速度;与量筒内液体的凹液面的最低处保持水平;18%;偏大
17.【答案】活性炭;溶解;过滤;蒸发;加速溶解、引流、防止液滴飞溅;BC;量筒
18.【答案】11.7;左盘;搅拌以加速溶解
19.【答案】(1)8.8
(2)HCl+NaOH=NaCl+H2O
(3)搅拌,防止局部温度过高而使液体飞溅;停止加热
20.【答案】(1)B
(2)偏小
(3)搅拌,加速氯化钠溶解
21.【答案】(1)加热煮沸
(2)1:2
(3)②①⑤③④;搅拌,加速溶解
22.【答案】(1)12;68
(2)3%
(3)搅拌,加快溶解
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
