实验活动4 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版九年级下册化学
文档属性
| 名称 | 实验活动4 金属的物理性质和某些化学性质 同步练习(含答案) 2022-2023学年人教版九年级下册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 159.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-16 10:15:16 | ||
图片预览




文档简介
实验活动4 金属的物理性质和某些化学性质 同步练习
一、单选题
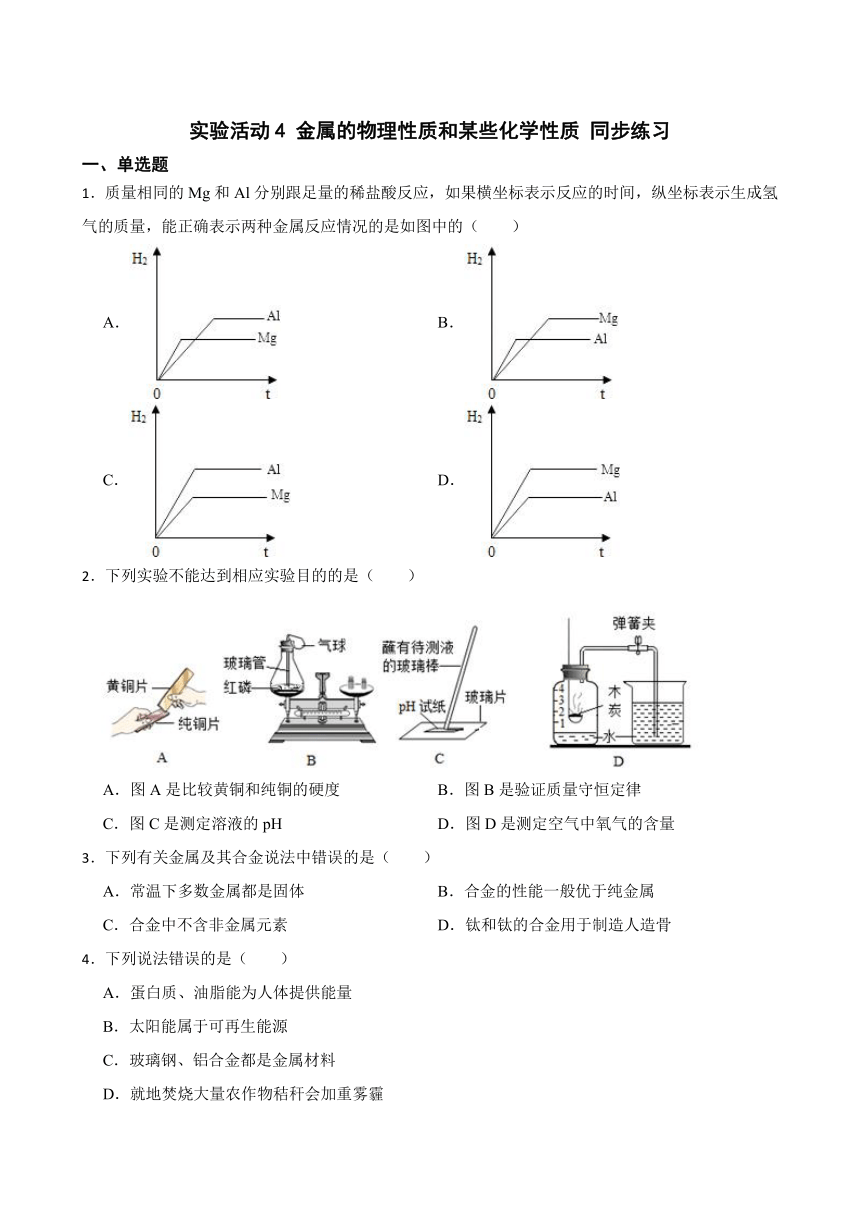
1.质量相同的Mg和Al分别跟足量的稀盐酸反应,如果横坐标表示反应的时间,纵坐标表示生成氢气的质量,能正确表示两种金属反应情况的是如图中的( )
A. B.
C. D.
2.下列实验不能达到相应实验目的的是( )
A.图A是比较黄铜和纯铜的硬度 B.图B是验证质量守恒定律
C.图C是测定溶液的pH D.图D是测定空气中氧气的含量
3.下列有关金属及其合金说法中错误的是( )
A.常温下多数金属都是固体 B.合金的性能一般优于纯金属
C.合金中不含非金属元素 D.钛和钛的合金用于制造人造骨
4.下列说法错误的是( )
A.蛋白质、油脂能为人体提供能量
B.太阳能属于可再生能源
C.玻璃钢、铝合金都是金属材料
D.就地焚烧大量农作物秸秆会加重雾霾
5.下面是利用化学知识对有关事实的解释,其中错误的是( )
A.金刚石和石墨物理性质差异很大,与它们碳原子的排列方式有关
B.生铁和钢的性能不同,与它们的组成中含碳量不同有关
C.当喝了冰镇汽水后常常会打嗝,这种现象说明气体的溶解度与压强有关
D.物质在溶解过程中常伴随热量变化,如硝酸铵溶解时会出现吸热现象
6.根据下图实验流程,下列分析正确的是( )
A.滤液中一定有硝酸镁,可能有硝酸锌和硝酸亚铁
B.滤渣中一定有银和铜,可能有锌
C.滤渣中一定有银和铜,可能有镁
D.滤液中一定有硝酸镁和硝酸锌,可能有硝酸铜
7.北斗系统的全面建成彰显了中国航天的力量。在航天科技中会用到大量金属材料,下列有关金属材料的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
8.下列质可以由金属跟酸反应直接得到的是( )
A.CuCl2 B.FeCl3 C.AgCl D.MgCl2
9.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,乙、丙表面出现红色物质,甲没有明显现象;再将大小相同的乙、丙分别放到相同的盐酸中,乙、丙均产生气泡,但乙产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.乙>甲>丙 D.乙>丙>甲
10.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片
C.向 pH=10 的氢氧化钙溶液中不断加水稀释
D.向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液
11.对比实验是科学探究中常用的一种实验方法。下列实验不属于对比实验的是( )
A.图中甲比较铁,铜的金属性活动性强弱
B.图中研究分子运动
C.图中丙研究燃烧的条件
D.图中丁研究二氧化碳与水的反应
12.欲除去不纯物质中的杂质(括号内为杂质),除去杂质所用方法不正确的是( )
选项 待提纯物质 除杂方法
A O2(CO2) 将混合气通入足量氢氧化钙溶液
B CO2(CO) 通过足量O2点燃
C Cu粉(Fe粉) 加足量稀硫酸,充分反应后过滤
D N2(O2) 通过灼热的铜网
A.A B.B C.C D.D
二、填空题
13.下列分别利用了金属的什么物理性质?
①用铜制导线 ;②铝能制成铝箔 。
14.科学家研发出一种铝镓(Ga)合金,从物质分类的角度看,铝镓合金属于 (填“纯净物”或“混合物”);用该合金与铝片相互刻画,发现铝片上有划痕,说明 .
15.我国化学家傅鹰教授有一句名言“科学只给我们知识,而历史却给我们智慧”在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质。
①我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为 (用化学方程式表示)。
②十八世纪,化学家们研究发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程。该气体在空气中燃烧制造水的化学方程式是 。
③现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用。2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有 (填序号)。
a.硬度大 b.密度小 c.易导电 d.耐腐蚀
④单层石墨烯(Graphene):指由一层以苯环结构(即六角形蜂巢结构)周期性紧密堆积的碳原子构成的一种二维碳材料。厚度是头发丝的20万分之一,强度是钢的200倍,是世界上已知的最轻最薄、最强的材料,用途极广,形成的石墨烯铝电池快速充电可以1.1秒充满电,中国石墨烯的专利总数占全世界的56%,排名第一,是中国复兴的有力支撑。从物质分类来看,单层石墨烯是 (填“单质、化合物或混合物”)
16.回答下列与铁有关的问题。
(1)细铁丝在氧气中燃烧生成黑色固体,该反应的化学方程式为 。
(2)工业炼铁反应:3CO+Fe2O3 Fe+3CO2,其中发生了还原反应 。
(3)将一定量的Mg、Fe放入CuSO4溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤液中所含溶质的所有可能情况是 。
17.生活中处处有化学.请根据所学知识填写以下空白:
(1)食品包装袋中充氮气以防腐,说明氮气的化学性质 (填“活泼”或“不活泼”);
(2)燃着的香烟产生的烟气中含有一种能与血液中血红蛋白结合的有毒气体是 ;
(3)打开汽水瓶盖时,汽水会自动喷出来,说明压强越小气体在水中的溶解度越 ;
(4)铝制品很耐腐蚀,其原因是铝在常温下就能够与氧气反应,生成致密的氧化铝薄膜,请写出该反应的化学方程式 .
18.要除去FeSO4中含有的CuSO4杂质。可以在其溶液中加入 ,充分反应后,再用 方法除去杂质;该反应的化学方程式是: 。
三、综合题
19.请根据有关化学实验操作回答下列问题:
(1)实验室用CO还原氧化铁时,先通一会CO的作用是 ;
(2)金属铝在常温下具有良好的耐腐蚀性的原因是 ;
(3)在红磷测定空气中氧气含量的实验中,结果偏低的原因是 .
20.某厂的工业废水中含有大量的硫酸亚铁,少量的硫酸铜以及污泥。某同学设计了一个既经济又合理的方法回收铜和硫酸亚铁晶体。方案流程如图所示:
回答下列问题:
(1)步骤①②③涉及到的基本操作是 。
(2)步骤③中发生反应的化学方程式是 。
(3)步骤③的实验目的是 ,为达到该实验目的,还可以采用的物理方法是 。
21.化学与生活、生产息息相关,请运用化学知识回答以下问题.
(1)铝制品耐腐蚀的原因是 (用化学方程式表示).
(2)金刚石和石墨都可以氧化成二氧化碳的原因是 .
(3)军事上照明弹的反应原理是 (用化学方程式表示).
(4)铁制容器不能盛装波尔多液的原因是 (用化学方程式表示).
(5)用汽油洗去油污的原理是 .
(6)实验室石灰水的表面常有一层白膜,原因是 (用化学方程式表示).
四、实验探究题
22.化学兴趣小组的同学设计并完成了如下图所示实验:
(1)实验一:仪器a的名称是 。实验室采用该装置制取氧气的反应方程式为: 。
(2)实验二:过程2的操作时机是 。按图示操作,可能引发的后果是 。
(3)实验三:使热水中的白磷燃烧应进行的操作是 ,该实验利用了铜片的物理性质是 。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】C
4.【答案】C
5.【答案】C
6.【答案】B
7.【答案】D
8.【答案】D
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】导电性;延展性
14.【答案】混合物;合金的硬度大于组成它的纯金属的硬度
15.【答案】Fe+CuSO4═FeSO4+Cu;2H2+O2 2H2O;abd;单质
16.【答案】(1)3Fe+2O2 Fe3O4
(2)Fe2O3
(3)MgSO4或MgSO4和FeSO4
17.【答案】不活泼;CO;小;4Al+3O2=2Al2O3
18.【答案】铁;过滤;Fe+CuSO4= FeSO4+Cu
19.【答案】(1)排除玻璃管内的空气,防止加热时爆炸
(2)铝与氧气反应生成的一层致密的氧化铝薄膜
(3)装置漏气、红磷量不足、未冷却至室温就打开止水夹等
20.【答案】(1)过滤
(2) 或
(3)除去剩余的铁;用磁铁吸引
21.【答案】(1)4Al+3O2=2Al2O3
(2)因为这两种物质都是由碳元素组成的
(3)2Mg+O2 2MgO
(4)Fe+CuSO4═FeSO4+Cu
(5)油污能溶于汽油
(6)Ca(OH)2+CO2═CaCO3↓+H2O
22.【答案】(1)锥形瓶;
(2)待引燃的火柴快燃尽时;瓶底炸裂
(3)向热水中通入氧气并与白磷接触;导热性
一、单选题
1.质量相同的Mg和Al分别跟足量的稀盐酸反应,如果横坐标表示反应的时间,纵坐标表示生成氢气的质量,能正确表示两种金属反应情况的是如图中的( )
A. B.
C. D.
2.下列实验不能达到相应实验目的的是( )
A.图A是比较黄铜和纯铜的硬度 B.图B是验证质量守恒定律
C.图C是测定溶液的pH D.图D是测定空气中氧气的含量
3.下列有关金属及其合金说法中错误的是( )
A.常温下多数金属都是固体 B.合金的性能一般优于纯金属
C.合金中不含非金属元素 D.钛和钛的合金用于制造人造骨
4.下列说法错误的是( )
A.蛋白质、油脂能为人体提供能量
B.太阳能属于可再生能源
C.玻璃钢、铝合金都是金属材料
D.就地焚烧大量农作物秸秆会加重雾霾
5.下面是利用化学知识对有关事实的解释,其中错误的是( )
A.金刚石和石墨物理性质差异很大,与它们碳原子的排列方式有关
B.生铁和钢的性能不同,与它们的组成中含碳量不同有关
C.当喝了冰镇汽水后常常会打嗝,这种现象说明气体的溶解度与压强有关
D.物质在溶解过程中常伴随热量变化,如硝酸铵溶解时会出现吸热现象
6.根据下图实验流程,下列分析正确的是( )
A.滤液中一定有硝酸镁,可能有硝酸锌和硝酸亚铁
B.滤渣中一定有银和铜,可能有锌
C.滤渣中一定有银和铜,可能有镁
D.滤液中一定有硝酸镁和硝酸锌,可能有硝酸铜
7.北斗系统的全面建成彰显了中国航天的力量。在航天科技中会用到大量金属材料,下列有关金属材料的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
8.下列质可以由金属跟酸反应直接得到的是( )
A.CuCl2 B.FeCl3 C.AgCl D.MgCl2
9.有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后,乙、丙表面出现红色物质,甲没有明显现象;再将大小相同的乙、丙分别放到相同的盐酸中,乙、丙均产生气泡,但乙产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是( )
A.甲>丙>乙 B.丙>乙>甲 C.乙>甲>丙 D.乙>丙>甲
10.如图分别与相应的操作过程相对应,其中正确的是( )
A.向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)
B.向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片
C.向 pH=10 的氢氧化钙溶液中不断加水稀释
D.向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液
11.对比实验是科学探究中常用的一种实验方法。下列实验不属于对比实验的是( )
A.图中甲比较铁,铜的金属性活动性强弱
B.图中研究分子运动
C.图中丙研究燃烧的条件
D.图中丁研究二氧化碳与水的反应
12.欲除去不纯物质中的杂质(括号内为杂质),除去杂质所用方法不正确的是( )
选项 待提纯物质 除杂方法
A O2(CO2) 将混合气通入足量氢氧化钙溶液
B CO2(CO) 通过足量O2点燃
C Cu粉(Fe粉) 加足量稀硫酸,充分反应后过滤
D N2(O2) 通过灼热的铜网
A.A B.B C.C D.D
二、填空题
13.下列分别利用了金属的什么物理性质?
①用铜制导线 ;②铝能制成铝箔 。
14.科学家研发出一种铝镓(Ga)合金,从物质分类的角度看,铝镓合金属于 (填“纯净物”或“混合物”);用该合金与铝片相互刻画,发现铝片上有划痕,说明 .
15.我国化学家傅鹰教授有一句名言“科学只给我们知识,而历史却给我们智慧”在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质。
①我国西汉时期就有“曾青得铁则化为铜”的记载,其中蕴涵的湿法冶铜原理为 (用化学方程式表示)。
②十八世纪,化学家们研究发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程。该气体在空气中燃烧制造水的化学方程式是 。
③现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用。2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的优点有 (填序号)。
a.硬度大 b.密度小 c.易导电 d.耐腐蚀
④单层石墨烯(Graphene):指由一层以苯环结构(即六角形蜂巢结构)周期性紧密堆积的碳原子构成的一种二维碳材料。厚度是头发丝的20万分之一,强度是钢的200倍,是世界上已知的最轻最薄、最强的材料,用途极广,形成的石墨烯铝电池快速充电可以1.1秒充满电,中国石墨烯的专利总数占全世界的56%,排名第一,是中国复兴的有力支撑。从物质分类来看,单层石墨烯是 (填“单质、化合物或混合物”)
16.回答下列与铁有关的问题。
(1)细铁丝在氧气中燃烧生成黑色固体,该反应的化学方程式为 。
(2)工业炼铁反应:3CO+Fe2O3 Fe+3CO2,其中发生了还原反应 。
(3)将一定量的Mg、Fe放入CuSO4溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气泡产生。则滤液中所含溶质的所有可能情况是 。
17.生活中处处有化学.请根据所学知识填写以下空白:
(1)食品包装袋中充氮气以防腐,说明氮气的化学性质 (填“活泼”或“不活泼”);
(2)燃着的香烟产生的烟气中含有一种能与血液中血红蛋白结合的有毒气体是 ;
(3)打开汽水瓶盖时,汽水会自动喷出来,说明压强越小气体在水中的溶解度越 ;
(4)铝制品很耐腐蚀,其原因是铝在常温下就能够与氧气反应,生成致密的氧化铝薄膜,请写出该反应的化学方程式 .
18.要除去FeSO4中含有的CuSO4杂质。可以在其溶液中加入 ,充分反应后,再用 方法除去杂质;该反应的化学方程式是: 。
三、综合题
19.请根据有关化学实验操作回答下列问题:
(1)实验室用CO还原氧化铁时,先通一会CO的作用是 ;
(2)金属铝在常温下具有良好的耐腐蚀性的原因是 ;
(3)在红磷测定空气中氧气含量的实验中,结果偏低的原因是 .
20.某厂的工业废水中含有大量的硫酸亚铁,少量的硫酸铜以及污泥。某同学设计了一个既经济又合理的方法回收铜和硫酸亚铁晶体。方案流程如图所示:
回答下列问题:
(1)步骤①②③涉及到的基本操作是 。
(2)步骤③中发生反应的化学方程式是 。
(3)步骤③的实验目的是 ,为达到该实验目的,还可以采用的物理方法是 。
21.化学与生活、生产息息相关,请运用化学知识回答以下问题.
(1)铝制品耐腐蚀的原因是 (用化学方程式表示).
(2)金刚石和石墨都可以氧化成二氧化碳的原因是 .
(3)军事上照明弹的反应原理是 (用化学方程式表示).
(4)铁制容器不能盛装波尔多液的原因是 (用化学方程式表示).
(5)用汽油洗去油污的原理是 .
(6)实验室石灰水的表面常有一层白膜,原因是 (用化学方程式表示).
四、实验探究题
22.化学兴趣小组的同学设计并完成了如下图所示实验:
(1)实验一:仪器a的名称是 。实验室采用该装置制取氧气的反应方程式为: 。
(2)实验二:过程2的操作时机是 。按图示操作,可能引发的后果是 。
(3)实验三:使热水中的白磷燃烧应进行的操作是 ,该实验利用了铜片的物理性质是 。
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】C
4.【答案】C
5.【答案】C
6.【答案】B
7.【答案】D
8.【答案】D
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】B
13.【答案】导电性;延展性
14.【答案】混合物;合金的硬度大于组成它的纯金属的硬度
15.【答案】Fe+CuSO4═FeSO4+Cu;2H2+O2 2H2O;abd;单质
16.【答案】(1)3Fe+2O2 Fe3O4
(2)Fe2O3
(3)MgSO4或MgSO4和FeSO4
17.【答案】不活泼;CO;小;4Al+3O2=2Al2O3
18.【答案】铁;过滤;Fe+CuSO4= FeSO4+Cu
19.【答案】(1)排除玻璃管内的空气,防止加热时爆炸
(2)铝与氧气反应生成的一层致密的氧化铝薄膜
(3)装置漏气、红磷量不足、未冷却至室温就打开止水夹等
20.【答案】(1)过滤
(2) 或
(3)除去剩余的铁;用磁铁吸引
21.【答案】(1)4Al+3O2=2Al2O3
(2)因为这两种物质都是由碳元素组成的
(3)2Mg+O2 2MgO
(4)Fe+CuSO4═FeSO4+Cu
(5)油污能溶于汽油
(6)Ca(OH)2+CO2═CaCO3↓+H2O
22.【答案】(1)锥形瓶;
(2)待引燃的火柴快燃尽时;瓶底炸裂
(3)向热水中通入氧气并与白磷接触;导热性
同课章节目录
