人教版(2019)高中化学选修三 1.1.2 有机化合物中的共价键 课件(19张PPT)
文档属性
| 名称 | 人教版(2019)高中化学选修三 1.1.2 有机化合物中的共价键 课件(19张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-16 15:31:21 | ||
图片预览



文档简介
(共21张PPT)
第一节 有机化合物的结构特点
课时2 有机化合物中的共价键
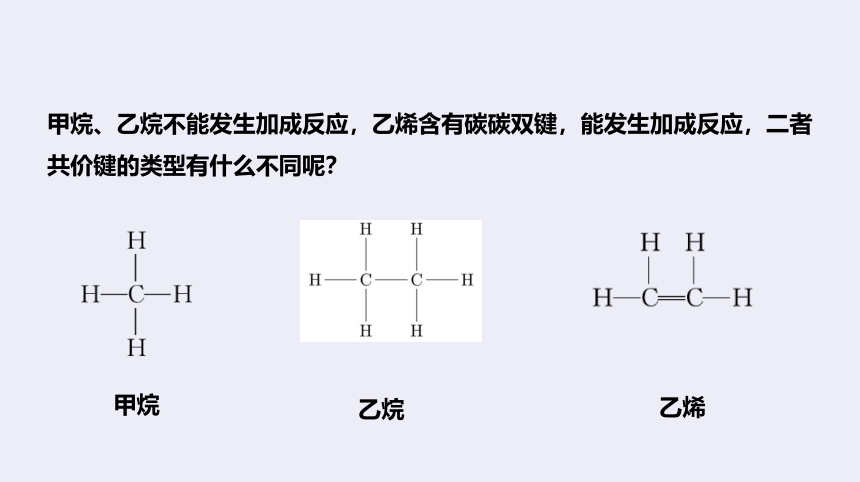
甲烷、乙烷不能发生加成反应,乙烯含有碳碳双键,能发生加成反应,二者共价键的类型有什么不同呢?
甲烷
乙烯
乙烷
共价键的类型
1.有机化合物中共价键的类型
原子轨道的重叠方式
σ键和π键
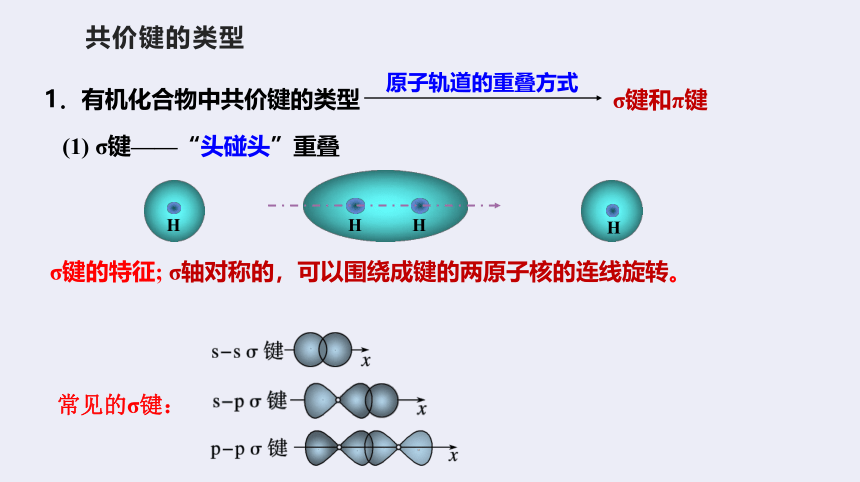
(1) σ键——“头碰头”重叠
σ键的特征; σ轴对称的,可以围绕成键的两原子核的连线旋转。
常见的σ键:
H
H
H
H
甲烷分子的成键分析
109°28′
四个氢原子的1s轨道和碳原子的四个sp3杂化轨道形成四个σ键
4 + →
H C CH4
共价键的类型
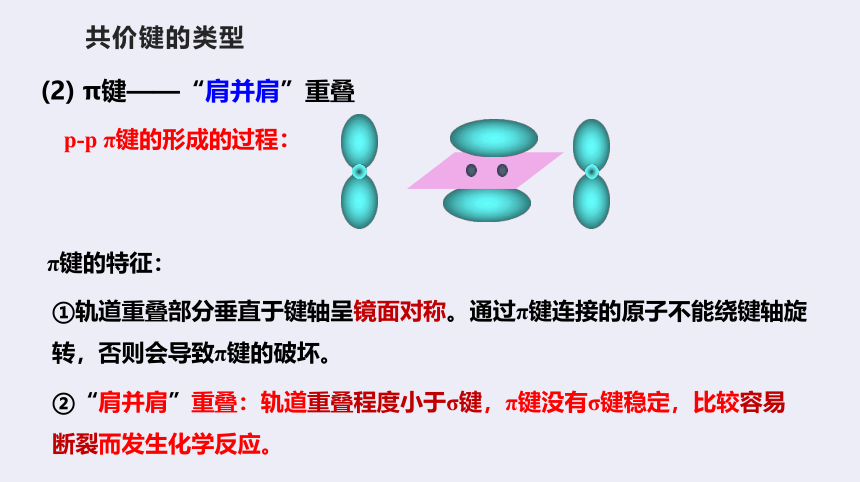
p-p π键的形成的过程:
(2) π键——“肩并肩”重叠
②“肩并肩”重叠:轨道重叠程度小于σ键,π键没有σ键稳定,比较容易断裂而发生化学反应。
π键的特征:
①轨道重叠部分垂直于键轴呈镜面对称。通过π键连接的原子不能绕键轴旋转,否则会导致π键的破坏。
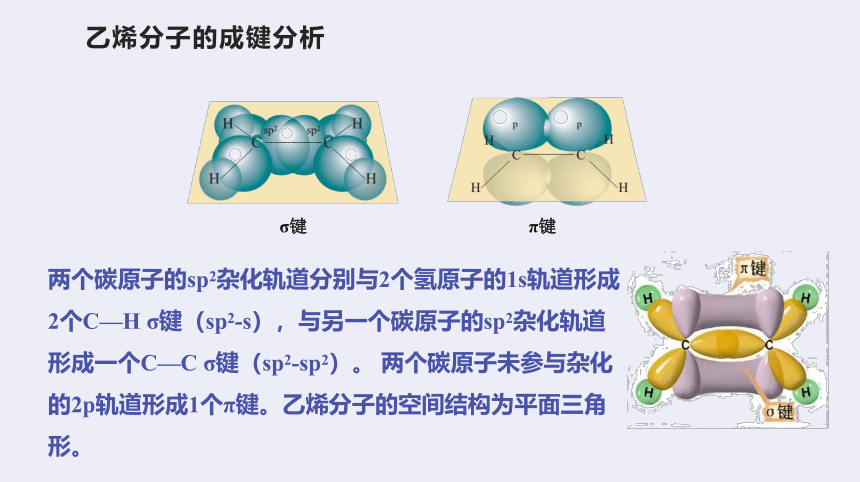
乙烯分子的成键分析
两个碳原子的sp2杂化轨道分别与2个氢原子的1s轨道形成2个C—H σ键(sp2-s),与另一个碳原子的sp2杂化轨道形成一个C—C σ键(sp2-sp2)。 两个碳原子未参与杂化的2p轨道形成1个π键。乙烯分子的空间结构为平面三角形。
σ键
π键
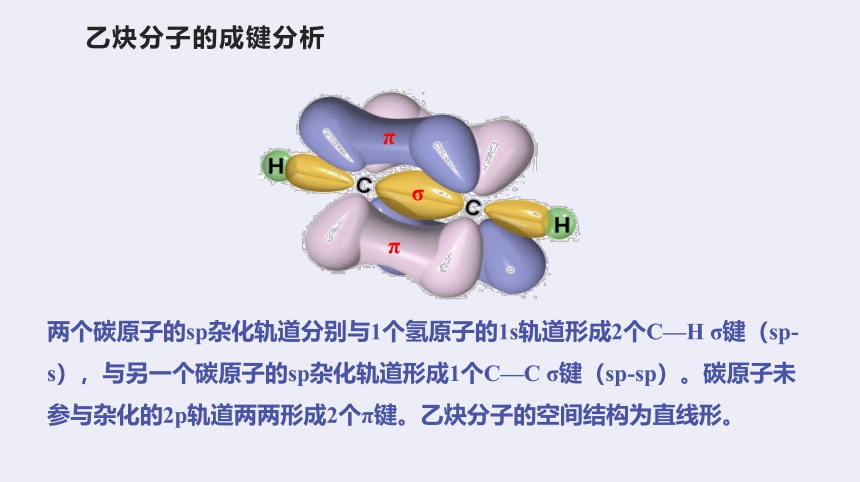
乙炔分子的成键分析
两个碳原子的sp杂化轨道分别与1个氢原子的1s轨道形成2个C—H σ键(sp-s),与另一个碳原子的sp杂化轨道形成1个C—C σ键(sp-sp)。碳原子未参与杂化的2p轨道两两形成2个π键。乙炔分子的空间结构为直线形。
σ
π
π
共价键的类型
(3)根据成键原子形成共用电子对的数目可分为单键、双键、三键。
(4)共价键类型与有机反应类型的关系
①甲烷含有C—H σ键,能发生取代反应。
②π键的轨道重叠程度比σ键的小,比较容易断裂,π键更活泼,如乙烯和乙炔含有π键,能发生加成反应。
有机化合物中的共价键
单键只含σ键
双键中含有一个σ键和一个π键
三键中含有一个σ键和两个π键
σ键 π键
原子轨道 重叠方式
能否绕轴旋转
原子轨道 重叠程度
键强度及 稳定性
平行于键轴方向,
“肩并肩”重叠
沿键轴方向,
“头碰头”重叠
可旋转
不可旋转
重叠程度较大
重叠程度较小
键强度较大,较稳定
键强度较小,较不稳定
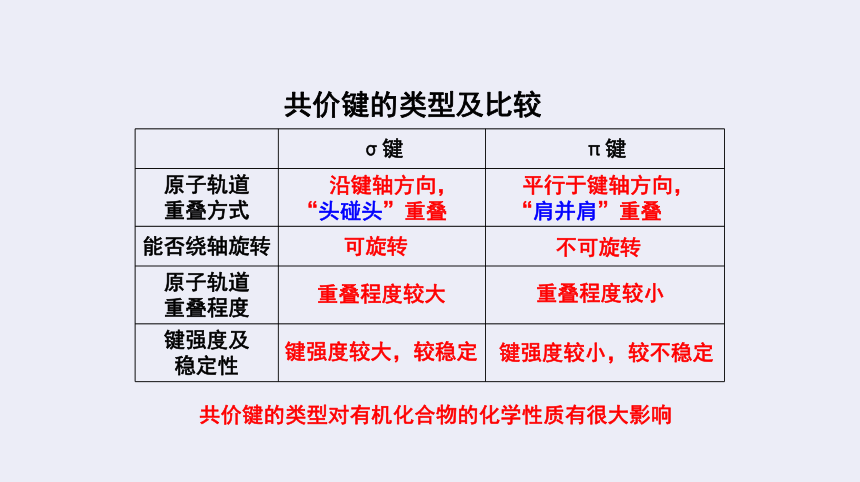
共价键的类型对有机化合物的化学性质有很大影响
共价键的类型及比较
共价键的极性与有机反应
H2
HCl
非极性共价键:同种元素的原子之间形成的共价键
极性共价键: 不同元素的原子之间形成的共价键
共价键
共价键的极性与有机反应
(1) 电负性与共价键极性的关系
原子间电负性的差异越大→共用电子对偏移的程度 →共价键极性 ,在反应中越 发生断裂→ 及其邻近的化学键往往是发生化学反应的活性部位。
越大
越强
容易
官能团
共价键的极性与有机反应
邻近基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
有机化合物分子中共价键断裂的位置存在多种可能。因此相对无机反应,有机反应的副反应较多,产物比较复杂,速率也比较慢。
(2) 基团之间的相互影响
实验——钠与乙醇、水反应的对比
实验操作
现象 都有 ,乙醇与钠的反应的剧烈程度 水与钠的反应 气泡产生
小于
【问题1】乙醇为什么能和金属钠反应?
乙醇分子中的氢氧键极性较强,能够发生断裂。
实验——钠与乙醇、水反应的对比
实验操作
现象 都有 ,乙醇与钠的反应的剧烈程度 水与钠的反应 【问题2】为什么乙醇与钠反应不如水与钠反应剧烈?
氢氧键的极性:水 > 乙醇
气泡产生
小于
实验——钠与乙醇、水反应的对比
羟基中氧原子的电负性 ,乙醇分子中的碳氧键极性也较 , 反应中 , 键发生了断裂。
【问题3】在这个反应中乙醇的断键位置在哪里?
+ H-Br + H2O
较大
强
碳氧
同样条件下,乙酸、无水乙醇、水分别与钠的反应剧烈程度比较?
乙酸 > 水 >乙醇
结论:乙酸分子中的H-O的极性 > 水中的H-O的极性 >乙醇中的H-O的极性
【解释】由于乙酸中羰基的吸电子效应,使其分子中H-O的极性比水中H-O的强,故乙酸具有弱酸性。
试从键的极性强弱角度比较甲酸、乙酸、丙酸的酸性强弱?
烃基为推电子基团,烃基越长推电子效应越大,使羧基中的羟基极性越小,羧酸的酸性越弱。
甲酸>乙酸>丙酸
1.正误判断
(1)σ键比π键牢固,所以不会断裂( )
(2)甲烷分子中只有C—H σ键,只能发生取代反应( )
(3)乙烯分子中含有π键,所以化学性质比甲烷活泼( )
(4)乙酸与钠反应比水与钠反应更剧烈,是因为乙酸分子中氢氧键的极性更强
( )
×
×
√
√
2.下列关于有机化合物中化学键的说法不正确的是
A.烷烃中的化学键均为σ键
B.CH3NH2中C—H的极性比N—H的极性弱
C.乙烯分子中含有极性键和非极性键
D.1个丙炔分子中含有5个σ键和3个π键
√
电负性:N > C
HC≡C—CH3
6个σ键、2个π键
②CH2 CH2 + Br2 CH2Br-CH2Br
3. 分析下列反应中有机化合物的断键情况,并归纳其反应类型。
断C-H,σ键。
①CH4 + Cl2 CH3Cl + HCl
光
断碳碳双键中的π键。
取代反应
加成反应
4. 某有机物分子的结构简式为 ,该分子
中有 个σ键, 个π键, (填“有”或“没有”)非极性键。
根据共价键的类型和极性可推测该物质可发生 反应和
_______反应,与钠反应的剧烈程度比水与钠反应的 。原因是______________________________________________________
_______________________________________________________。
8
2
有
加成
取代
大
CH2==CHCOOH中 —COOH 中的氢氧键受酮羰基影响,
极性更强,更易断裂
第一节 有机化合物的结构特点
课时2 有机化合物中的共价键
甲烷、乙烷不能发生加成反应,乙烯含有碳碳双键,能发生加成反应,二者共价键的类型有什么不同呢?
甲烷
乙烯
乙烷
共价键的类型
1.有机化合物中共价键的类型
原子轨道的重叠方式
σ键和π键
(1) σ键——“头碰头”重叠
σ键的特征; σ轴对称的,可以围绕成键的两原子核的连线旋转。
常见的σ键:
H
H
H
H
甲烷分子的成键分析
109°28′
四个氢原子的1s轨道和碳原子的四个sp3杂化轨道形成四个σ键
4 + →
H C CH4
共价键的类型
p-p π键的形成的过程:
(2) π键——“肩并肩”重叠
②“肩并肩”重叠:轨道重叠程度小于σ键,π键没有σ键稳定,比较容易断裂而发生化学反应。
π键的特征:
①轨道重叠部分垂直于键轴呈镜面对称。通过π键连接的原子不能绕键轴旋转,否则会导致π键的破坏。
乙烯分子的成键分析
两个碳原子的sp2杂化轨道分别与2个氢原子的1s轨道形成2个C—H σ键(sp2-s),与另一个碳原子的sp2杂化轨道形成一个C—C σ键(sp2-sp2)。 两个碳原子未参与杂化的2p轨道形成1个π键。乙烯分子的空间结构为平面三角形。
σ键
π键
乙炔分子的成键分析
两个碳原子的sp杂化轨道分别与1个氢原子的1s轨道形成2个C—H σ键(sp-s),与另一个碳原子的sp杂化轨道形成1个C—C σ键(sp-sp)。碳原子未参与杂化的2p轨道两两形成2个π键。乙炔分子的空间结构为直线形。
σ
π
π
共价键的类型
(3)根据成键原子形成共用电子对的数目可分为单键、双键、三键。
(4)共价键类型与有机反应类型的关系
①甲烷含有C—H σ键,能发生取代反应。
②π键的轨道重叠程度比σ键的小,比较容易断裂,π键更活泼,如乙烯和乙炔含有π键,能发生加成反应。
有机化合物中的共价键
单键只含σ键
双键中含有一个σ键和一个π键
三键中含有一个σ键和两个π键
σ键 π键
原子轨道 重叠方式
能否绕轴旋转
原子轨道 重叠程度
键强度及 稳定性
平行于键轴方向,
“肩并肩”重叠
沿键轴方向,
“头碰头”重叠
可旋转
不可旋转
重叠程度较大
重叠程度较小
键强度较大,较稳定
键强度较小,较不稳定
共价键的类型对有机化合物的化学性质有很大影响
共价键的类型及比较
共价键的极性与有机反应
H2
HCl
非极性共价键:同种元素的原子之间形成的共价键
极性共价键: 不同元素的原子之间形成的共价键
共价键
共价键的极性与有机反应
(1) 电负性与共价键极性的关系
原子间电负性的差异越大→共用电子对偏移的程度 →共价键极性 ,在反应中越 发生断裂→ 及其邻近的化学键往往是发生化学反应的活性部位。
越大
越强
容易
官能团
共价键的极性与有机反应
邻近基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
有机化合物分子中共价键断裂的位置存在多种可能。因此相对无机反应,有机反应的副反应较多,产物比较复杂,速率也比较慢。
(2) 基团之间的相互影响
实验——钠与乙醇、水反应的对比
实验操作
现象 都有 ,乙醇与钠的反应的剧烈程度 水与钠的反应 气泡产生
小于
【问题1】乙醇为什么能和金属钠反应?
乙醇分子中的氢氧键极性较强,能够发生断裂。
实验——钠与乙醇、水反应的对比
实验操作
现象 都有 ,乙醇与钠的反应的剧烈程度 水与钠的反应 【问题2】为什么乙醇与钠反应不如水与钠反应剧烈?
氢氧键的极性:水 > 乙醇
气泡产生
小于
实验——钠与乙醇、水反应的对比
羟基中氧原子的电负性 ,乙醇分子中的碳氧键极性也较 , 反应中 , 键发生了断裂。
【问题3】在这个反应中乙醇的断键位置在哪里?
+ H-Br + H2O
较大
强
碳氧
同样条件下,乙酸、无水乙醇、水分别与钠的反应剧烈程度比较?
乙酸 > 水 >乙醇
结论:乙酸分子中的H-O的极性 > 水中的H-O的极性 >乙醇中的H-O的极性
【解释】由于乙酸中羰基的吸电子效应,使其分子中H-O的极性比水中H-O的强,故乙酸具有弱酸性。
试从键的极性强弱角度比较甲酸、乙酸、丙酸的酸性强弱?
烃基为推电子基团,烃基越长推电子效应越大,使羧基中的羟基极性越小,羧酸的酸性越弱。
甲酸>乙酸>丙酸
1.正误判断
(1)σ键比π键牢固,所以不会断裂( )
(2)甲烷分子中只有C—H σ键,只能发生取代反应( )
(3)乙烯分子中含有π键,所以化学性质比甲烷活泼( )
(4)乙酸与钠反应比水与钠反应更剧烈,是因为乙酸分子中氢氧键的极性更强
( )
×
×
√
√
2.下列关于有机化合物中化学键的说法不正确的是
A.烷烃中的化学键均为σ键
B.CH3NH2中C—H的极性比N—H的极性弱
C.乙烯分子中含有极性键和非极性键
D.1个丙炔分子中含有5个σ键和3个π键
√
电负性:N > C
HC≡C—CH3
6个σ键、2个π键
②CH2 CH2 + Br2 CH2Br-CH2Br
3. 分析下列反应中有机化合物的断键情况,并归纳其反应类型。
断C-H,σ键。
①CH4 + Cl2 CH3Cl + HCl
光
断碳碳双键中的π键。
取代反应
加成反应
4. 某有机物分子的结构简式为 ,该分子
中有 个σ键, 个π键, (填“有”或“没有”)非极性键。
根据共价键的类型和极性可推测该物质可发生 反应和
_______反应,与钠反应的剧烈程度比水与钠反应的 。原因是______________________________________________________
_______________________________________________________。
8
2
有
加成
取代
大
CH2==CHCOOH中 —COOH 中的氢氧键受酮羰基影响,
极性更强,更易断裂
