第一单元 溶液 综合素质评价 (含答案)
文档属性
| 名称 | 第一单元 溶液 综合素质评价 (含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 240.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-18 00:00:00 | ||
图片预览



文档简介
第一单元 溶液 综合素质评价
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(本题包括12小题,每题3分,共36分)
1.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.食盐 B.面粉 C.泥沙 D.花生油
2.下列有关碘酒的说法错误的是( )
A.碘酒是混合物 B.碘酒是溶液 C.碘是溶质 D.酒精是溶质
3.下列除垢或除污过程中利用乳化作用的是( )
A.自来水洗手 B.食醋除水垢 C.汽油除油污 D.洗洁精除油污
4.某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )
A.变大 不变 B.变大 变小 C.不变 变大 D.不变 不变
5.【2022·衡阳】下列关于溶液的说法正确的是( )
A.溶液是具有均一性、稳定性的混合物
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.打开汽水瓶盖后有气泡冒出,主要是因为温度升高,气体溶解度减小
D.溶液都是无色透明的液体
6.向100 g溶质质量分数为20%的NaCl溶液中加入3 g NaCl固体和12 g水,使其完全溶解,所得溶液中NaCl的质量分数是( )
A.20% B.22.5% C.25% D.30%
7.某温度时,将20 g KNO3溶解在100 g水中恰好饱和,关于该饱和溶液的叙述正确的是( )
A.m(溶质)∶m(溶剂)=20∶120 B.溶质的质量分数为20%
C.升温后,溶质的质量分数增大 D.降温后,有固体析出
8.【2023·青岛模拟】向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,符合题意的是(提示:氧化钙与水反应放出大量热)( )
A.X是水,Y是氧化钙 B.X是水,Y是氢氧化钠
C.X是水,Y是硝酸铵 D.X是水,Y是氯化钠
9.在20 ℃时,将40 g氯化钠固体加入100 g水中,充分搅拌后,有4 g固体未溶解。下列说法正确的是( )
A.20 ℃时,氯化钠的溶解度为36 g
B.该溶液不能继续溶解硝酸钾固体
C.所得氯化钠溶液的质量为140 g
D.将该溶液倒出一半,则溶液的浓度改变
10.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是( )
A.P点表示t2 ℃时,甲和乙的溶解度相等
B.t3 ℃时Q点表示甲的不饱和溶液
C.t3 ℃时,将25 g乙放入50 g水中,所得溶液中溶质和溶剂的质量比为2∶5
D.将t3 ℃时甲、乙、丙的饱和溶液降温至t1 ℃,溶质的质量分数由大到小的顺序为丙>甲>乙
11.如果所配制的6%的氯化钠溶液的溶质质量分数偏小,其原因可能是( )
A.称取的氯化钠固体质量偏大
B.转移称量好的氯化钠固体时,有少量撒落在桌面上
C.量取水的体积偏小
D.转移配制好的溶液时,有少量液体溅出
12.【2022·云南】为探究硝酸钾的溶解性,进行了如图所示实验。
INCLUDEPICTURE "../WJ53.EPS" \* MERGEFORMAT INCLUDEPICTURE "../WJ53.EPS" \* MERGEFORMAT \d
结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO3溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
C.②③④中溶液的溶质质量分数:③>②>④
D.④中析出晶体的质量是0.9 g
二、填空题(本题包括4小题,共34分)
13.(5分)小刚分别试用以下方法清洗餐具:①只用冷水;②只用热水;③在冷水中加入几滴洗涤剂;④在热水中加入几滴洗涤剂,然后清洗,并用清水把餐具上的洗涤剂漂洗干净。
(1)上述方法中清洗餐具最干净的是________(填序号)。
(2)以上对比实验说明了温度越________(填“高”或“低”),洗涤剂洗涤效果越好。你的理由是__________________________________________。
(3)用下列选项填空:A.反应 B.溶解 C.乳化 D.过滤
①洗涤剂对油污有________(填字母,下同)作用;
②小刚认为:汽油也能除去油污,但去污原理不同。其中汽油可以______油污。
14.(8分)【2022·滨州】如图为A、B两种固体物质的溶解度曲线,请根据图示信息回答:
(1)t1 ℃时,A物质的溶解度是________g。
(2)A、B两种物质中,________的溶解度受温度的影响较小。
(3)t2 ℃时,将35 g A物质加入到50 g水中,充分溶解后,得到该温度下A物质的________(填“饱和”或“不饱和”)溶液。此时溶液的溶质质量分数为________。
15.(6分)在一定温度下,向100 g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是________(填“饱和”或“不饱和”)溶液。
(2)该温度下,KCl的溶解度为________。
(3)实验③所得溶液中溶质的质量分数是________(填字母)。
A.40% B.37.5% C.28.6%
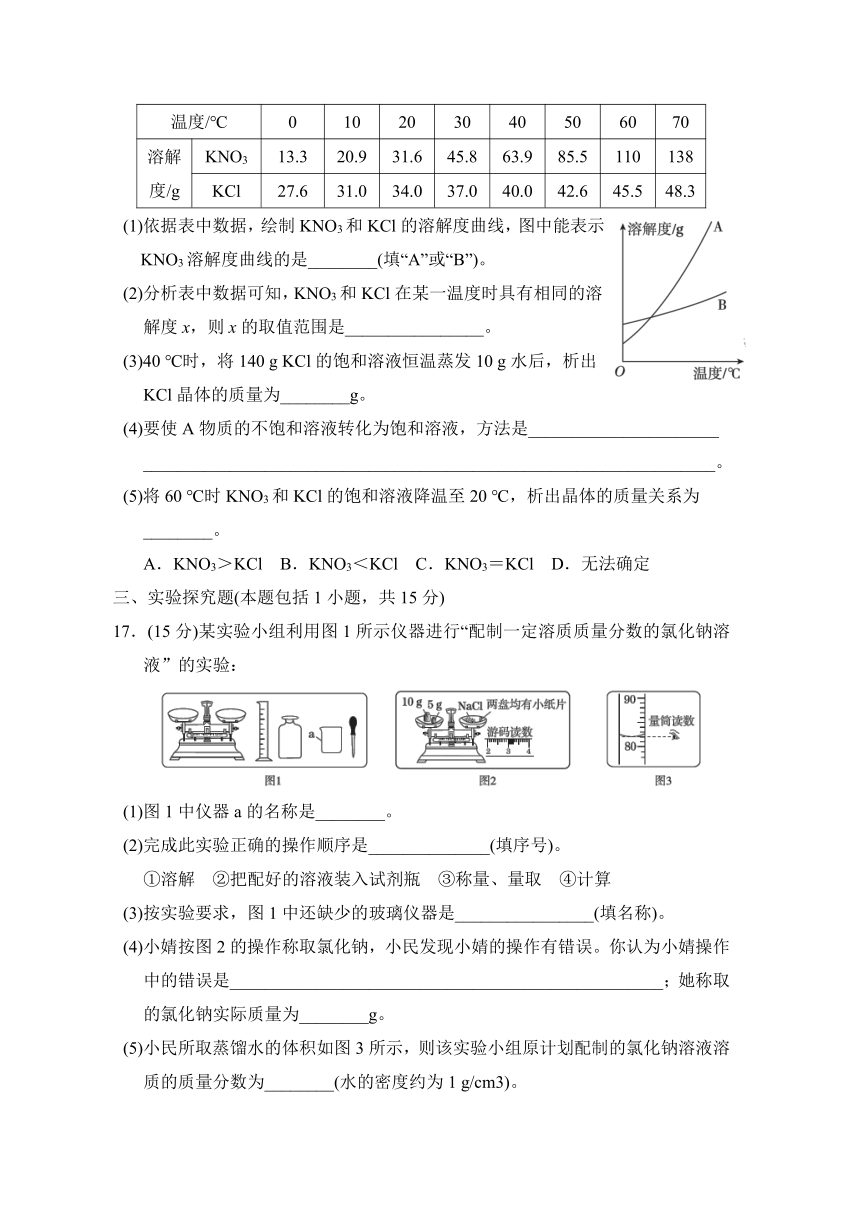
16.(15分)【2023·成都模拟】数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如表所示,请回答下列问题:
温度/℃ 0 10 20 30 40 50 60 70
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138
KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3
(1)依据表中数据,绘制KNO3和KCl的溶解度曲线,图中能表示KNO3溶解度曲线的是________(填“A”或“B”)。
(2)分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是________________。
(3)40 ℃时,将140 g KCl的饱和溶液恒温蒸发10 g水后,析出KCl晶体的质量为________g。
(4)要使A物质的不饱和溶液转化为饱和溶液,方法是______________________
__________________________________________________________________。
(5)将60 ℃时KNO3和KCl的饱和溶液降温至20 ℃,析出晶体的质量关系为________。
A.KNO3>KCl B.KNO3<KCl C.KNO3=KCl D.无法确定
三、实验探究题(本题包括1小题,共15分)
17.(15分)某实验小组利用图1所示仪器进行“配制一定溶质质量分数的氯化钠溶液”的实验:
INCLUDEPICTURE "../T15.EPS" \* MERGEFORMAT INCLUDEPICTURE "../T15.EPS" \* MERGEFORMAT \d
(1)图1中仪器a的名称是________。
(2)完成此实验正确的操作顺序是______________(填序号)。
①溶解 ②把配好的溶液装入试剂瓶 ③称量、量取 ④计算
(3)按实验要求,图1中还缺少的玻璃仪器是________________(填名称)。
(4)小婧按图2的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__________________________________________________;她称取的氯化钠实际质量为________g。
(5)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液溶质的质量分数为________(水的密度约为1 g/cm3)。
四、计算题(本题包括2小题,共15分)
18.(7分)50 ℃时,将12 g硝酸钾完全溶解到48 g水中,所得溶液溶质质量分数为______。将此溶液分成两等份。
(1)取第一份溶液,使其溶质质量分数变为原来的2倍,需加入硝酸钾晶体______g(假设所加固体完全溶解),或者蒸发掉水______ g(假设蒸发过程中无溶质析出)。
(2)取第二份溶液,使其溶质质量分数变为原来的一半,需加水多少克?(写出解题过程)
19.(8分)【2022·黔东南】石灰石是生产水泥、玻璃等建筑材料的重要原料。某课外兴趣小组的同学为了测定某地石灰石中碳酸钙的质量分数,称取石灰石样品4.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不溶于水,也不与稀盐酸反应),测得剩余固体的质量记录如下。
加入稀盐酸的质量/g 10 10 10 10 10
剩余固体的质量/g x 2.0 1.0 0.4 0.4
请回答下列问题:
(1)表中x的值为________。
(2)该石灰石样品中碳酸钙的质量分数是______。
(3)所用稀盐酸中溶质的质量分数。
答案
一、1.A 2.D 3.D 4.D
5.A 【点拨】溶液是具有均一性、稳定性的混合物,A正确;饱和溶液不一定是浓溶液,如饱和氢氧化钙溶液是稀溶液,不饱和溶液不一定是稀溶液,如未饱和的浓硝酸钾溶液,B错误;打开汽水瓶盖,压强减小,气体的溶解度减小,气体逸出,C错误;溶液不一定是无色的,如硫酸铜溶液显蓝色,D错误。
6.A 【点拨】所得氯化钠溶液中溶质的质量分数为×100%=20%。
7.D 【点拨】20 g KNO3溶解在100 g水中,则溶质与溶剂的质量比为20?100,故A错;所得溶液溶质质量分数为×100%≈16.7%,故B错;升温后,KNO3的饱和溶液将变成较高温度时的不饱和溶液,溶质质量分数不变,故C错;降温后,由于KNO3的溶解度减小,故有晶体析出,D正确。
8.C 【点拨】氧化钙和水反应放出大量的热,使瓶内气体温度升高,U形管内红墨水左侧液面下降,A错误;氢氧化钠溶于水放热,使瓶内气体温度升高,受热膨胀,U形管内红墨水左侧液面下降,B错误;硝酸铵溶于水吸热,使瓶内气体温度降低,压强减小,U形管内红墨水左侧液面上升,C正确;氯化钠溶于水温度几乎无变化,U形管内红墨水液面无明显变化,D错误。
9.A
10.D 【点拨】P点表示t2 ℃时,甲和乙的溶解度相等,A正确;t3 ℃时Q点表示甲的不饱和溶液,B正确;t3 ℃时乙的溶解度是40 g,将25 g乙放入50 g水中,最多只能溶解20 g,所得溶液中溶质和溶剂的质量比为20 g∶50 g=2∶5,C正确;将t3 ℃时甲、乙、丙的饱和溶液降温至t1 ℃,丙变成不饱和溶液,溶质质量分数不变,大于t1 ℃时乙、甲的饱和溶液的溶质质量分数,t1 ℃时,乙的溶解度大于甲,因此乙的溶液的质量分数大于甲的,溶质的质量分数由大到小的顺序为丙>乙>甲,D不正确。
11.B 【点拨】称取的氯化钠固体质量偏大、量取水的体积偏小,都会导致溶质质量分数偏大;转移称量好的氯化钠固体时,有少量撒落在桌面上,会导致所配溶液溶质质量分数偏小;转移配制好的溶液时,有少量液体溅出,溶质质量分数不变。
12.D 【点拨】20 ℃时,硝酸钾的溶解度为31.6 g,60 ℃时,硝酸钾的溶解度为110.0 g,则20 ℃时,50 g水中最多溶解硝酸钾15.8 g,60 ℃时,50 g水中最多溶解硝酸钾55 g;则①③中的溶液均为不饱和溶液,故A说法正确;②③中溶剂的质量相等,③中溶解的溶质的质量最多,则②③中溶液的质量:③>②,故B说法正确;②③④分别是20 ℃时的饱和溶液、60 ℃时的不饱和溶液、10 ℃时的饱和溶液;②③④中溶剂的质量相等,③中溶解的溶质的质量最多,④中溶解的溶质质量最少,则溶液的溶质质量分数:③>②>④,故C说法正确;10 ℃时硝酸钾的溶解度为20.9 g,则10 ℃时,50 g水中最多溶解硝酸钾10.45 g,④中析出晶体的质量是10 g+10 g-10.45 g=9.55 g,故D说法错误。
二、13.(1)④ (2)高;温度越高,乳化效果越好
(3)①C ②B
14.(1)20 (2)B (3)饱和;37.5%
【点拨】(1)根据图示溶解度曲线图可知,t1 ℃时,A物质的溶解度是20 g。(2)两物质的溶解度曲线图中A的溶解度曲线较陡,B的溶解度曲线较平缓,则B的溶解度受温度影响较小。(3)t2 ℃时,A的溶解度为60 g,则此温度下100 g水中最多溶解A 60 g,所以50 g水中最多能溶解A 30 g,故将35 g A物质加入到50 g水中,充分溶解后,得到A的饱和溶液,且溶液中只能溶解A 30 g,则A的溶质质量分数=×100%=37.5%。
15.(1)不饱和 (2)40 g (3)C
【点拨】(1)饱和溶液是指一定温度下不能继续溶解某种溶质的溶液,①能继续溶解20 g KCl,所以是KCl的不饱和溶液。(2)根据题中的实验可知,该温度下100 g水中加入40 g氯化钾恰好饱和,故该温度下氯化钾的溶解度是40 g。(3)实验③溶液中溶质的质量分数为×100%≈28.6%。
16.(1)A (2)34.0 g【点拨】(1)通过分析溶解度表中的数据可知,硝酸钾的溶解度受温度变化影响较大,所以图中能表示KNO3溶解度曲线的是A。(2)通过分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是
34.0 g三、17. (1)烧杯 (2)④③①② (3)玻璃棒
(4)称量时砝码和氯化钠的位置放反了;12 (5)18%
四、18. 20% (1)10;15
(2)【解】设需加水的质量为x,则根据稀释前后溶质的质量不变,可列方程如下:
×20%=(+x)×10% x=30 g
答:要使溶质质量分数变为原来的一半,需加水30 g。
19.【解】(1)3.0 (2)90%
(3)设10 g盐酸中HCl的质量为y。
CaCO3 + 2HCl===CaCl2+H2O+CO2↑
100 73
1 g y
= y=0.73 g
所用稀盐酸的溶质质量分数为×100%=7.3%
答:所用稀盐酸的溶质质量分数为7.3%。
可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40
一、选择题(本题包括12小题,每题3分,共36分)
1.把少量下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
A.食盐 B.面粉 C.泥沙 D.花生油
2.下列有关碘酒的说法错误的是( )
A.碘酒是混合物 B.碘酒是溶液 C.碘是溶质 D.酒精是溶质
3.下列除垢或除污过程中利用乳化作用的是( )
A.自来水洗手 B.食醋除水垢 C.汽油除油污 D.洗洁精除油污
4.某兴趣小组分别用加溶质和恒温蒸发溶剂的方法,将一定质量的硝酸钾不饱和溶液转化为饱和溶液。实验过程中,硝酸钾溶解度的变化情况分别是( )
A.变大 不变 B.变大 变小 C.不变 变大 D.不变 不变
5.【2022·衡阳】下列关于溶液的说法正确的是( )
A.溶液是具有均一性、稳定性的混合物
B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液
C.打开汽水瓶盖后有气泡冒出,主要是因为温度升高,气体溶解度减小
D.溶液都是无色透明的液体
6.向100 g溶质质量分数为20%的NaCl溶液中加入3 g NaCl固体和12 g水,使其完全溶解,所得溶液中NaCl的质量分数是( )
A.20% B.22.5% C.25% D.30%
7.某温度时,将20 g KNO3溶解在100 g水中恰好饱和,关于该饱和溶液的叙述正确的是( )
A.m(溶质)∶m(溶剂)=20∶120 B.溶质的质量分数为20%
C.升温后,溶质的质量分数增大 D.降温后,有固体析出
8.【2023·青岛模拟】向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,符合题意的是(提示:氧化钙与水反应放出大量热)( )
A.X是水,Y是氧化钙 B.X是水,Y是氢氧化钠
C.X是水,Y是硝酸铵 D.X是水,Y是氯化钠
9.在20 ℃时,将40 g氯化钠固体加入100 g水中,充分搅拌后,有4 g固体未溶解。下列说法正确的是( )
A.20 ℃时,氯化钠的溶解度为36 g
B.该溶液不能继续溶解硝酸钾固体
C.所得氯化钠溶液的质量为140 g
D.将该溶液倒出一半,则溶液的浓度改变
10.甲、乙、丙三种固体物质的溶解度曲线如图所示。下列说法不正确的是( )
A.P点表示t2 ℃时,甲和乙的溶解度相等
B.t3 ℃时Q点表示甲的不饱和溶液
C.t3 ℃时,将25 g乙放入50 g水中,所得溶液中溶质和溶剂的质量比为2∶5
D.将t3 ℃时甲、乙、丙的饱和溶液降温至t1 ℃,溶质的质量分数由大到小的顺序为丙>甲>乙
11.如果所配制的6%的氯化钠溶液的溶质质量分数偏小,其原因可能是( )
A.称取的氯化钠固体质量偏大
B.转移称量好的氯化钠固体时,有少量撒落在桌面上
C.量取水的体积偏小
D.转移配制好的溶液时,有少量液体溅出
12.【2022·云南】为探究硝酸钾的溶解性,进行了如图所示实验。
INCLUDEPICTURE "../WJ53.EPS" \* MERGEFORMAT INCLUDEPICTURE "../WJ53.EPS" \* MERGEFORMAT \d
结合硝酸钾在不同温度下的溶解度,判断下列说法不正确的是( )
温度/℃ 10 20 30 40 50 60
KNO3溶解度/g 20.9 31.6 45.8 63.9 85.5 110.0
A.①③中的溶液均为不饱和溶液
B.②③中溶液的质量:③>②
C.②③④中溶液的溶质质量分数:③>②>④
D.④中析出晶体的质量是0.9 g
二、填空题(本题包括4小题,共34分)
13.(5分)小刚分别试用以下方法清洗餐具:①只用冷水;②只用热水;③在冷水中加入几滴洗涤剂;④在热水中加入几滴洗涤剂,然后清洗,并用清水把餐具上的洗涤剂漂洗干净。
(1)上述方法中清洗餐具最干净的是________(填序号)。
(2)以上对比实验说明了温度越________(填“高”或“低”),洗涤剂洗涤效果越好。你的理由是__________________________________________。
(3)用下列选项填空:A.反应 B.溶解 C.乳化 D.过滤
①洗涤剂对油污有________(填字母,下同)作用;
②小刚认为:汽油也能除去油污,但去污原理不同。其中汽油可以______油污。
14.(8分)【2022·滨州】如图为A、B两种固体物质的溶解度曲线,请根据图示信息回答:
(1)t1 ℃时,A物质的溶解度是________g。
(2)A、B两种物质中,________的溶解度受温度的影响较小。
(3)t2 ℃时,将35 g A物质加入到50 g水中,充分溶解后,得到该温度下A物质的________(填“饱和”或“不饱和”)溶液。此时溶液的溶质质量分数为________。
15.(6分)在一定温度下,向100 g水中依次加入一定质量的KCl固体,充分溶解,加入KCl固体的质量与所得溶液质量的关系如图所示:
(1)该温度下,实验①所得溶液是________(填“饱和”或“不饱和”)溶液。
(2)该温度下,KCl的溶解度为________。
(3)实验③所得溶液中溶质的质量分数是________(填字母)。
A.40% B.37.5% C.28.6%
16.(15分)【2023·成都模拟】数据处理是对数据进行加工的过程,列表法和作图法是常用的数据处理方法。已知KNO3和KCl在不同温度时的溶解度如表所示,请回答下列问题:
温度/℃ 0 10 20 30 40 50 60 70
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138
KCl 27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3
(1)依据表中数据,绘制KNO3和KCl的溶解度曲线,图中能表示KNO3溶解度曲线的是________(填“A”或“B”)。
(2)分析表中数据可知,KNO3和KCl在某一温度时具有相同的溶解度x,则x的取值范围是________________。
(3)40 ℃时,将140 g KCl的饱和溶液恒温蒸发10 g水后,析出KCl晶体的质量为________g。
(4)要使A物质的不饱和溶液转化为饱和溶液,方法是______________________
__________________________________________________________________。
(5)将60 ℃时KNO3和KCl的饱和溶液降温至20 ℃,析出晶体的质量关系为________。
A.KNO3>KCl B.KNO3<KCl C.KNO3=KCl D.无法确定
三、实验探究题(本题包括1小题,共15分)
17.(15分)某实验小组利用图1所示仪器进行“配制一定溶质质量分数的氯化钠溶液”的实验:
INCLUDEPICTURE "../T15.EPS" \* MERGEFORMAT INCLUDEPICTURE "../T15.EPS" \* MERGEFORMAT \d
(1)图1中仪器a的名称是________。
(2)完成此实验正确的操作顺序是______________(填序号)。
①溶解 ②把配好的溶液装入试剂瓶 ③称量、量取 ④计算
(3)按实验要求,图1中还缺少的玻璃仪器是________________(填名称)。
(4)小婧按图2的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__________________________________________________;她称取的氯化钠实际质量为________g。
(5)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液溶质的质量分数为________(水的密度约为1 g/cm3)。
四、计算题(本题包括2小题,共15分)
18.(7分)50 ℃时,将12 g硝酸钾完全溶解到48 g水中,所得溶液溶质质量分数为______。将此溶液分成两等份。
(1)取第一份溶液,使其溶质质量分数变为原来的2倍,需加入硝酸钾晶体______g(假设所加固体完全溶解),或者蒸发掉水______ g(假设蒸发过程中无溶质析出)。
(2)取第二份溶液,使其溶质质量分数变为原来的一半,需加水多少克?(写出解题过程)
19.(8分)【2022·黔东南】石灰石是生产水泥、玻璃等建筑材料的重要原料。某课外兴趣小组的同学为了测定某地石灰石中碳酸钙的质量分数,称取石灰石样品4.0 g于烧杯中,将50 g稀盐酸分5次加入烧杯中,充分反应后(杂质不溶于水,也不与稀盐酸反应),测得剩余固体的质量记录如下。
加入稀盐酸的质量/g 10 10 10 10 10
剩余固体的质量/g x 2.0 1.0 0.4 0.4
请回答下列问题:
(1)表中x的值为________。
(2)该石灰石样品中碳酸钙的质量分数是______。
(3)所用稀盐酸中溶质的质量分数。
答案
一、1.A 2.D 3.D 4.D
5.A 【点拨】溶液是具有均一性、稳定性的混合物,A正确;饱和溶液不一定是浓溶液,如饱和氢氧化钙溶液是稀溶液,不饱和溶液不一定是稀溶液,如未饱和的浓硝酸钾溶液,B错误;打开汽水瓶盖,压强减小,气体的溶解度减小,气体逸出,C错误;溶液不一定是无色的,如硫酸铜溶液显蓝色,D错误。
6.A 【点拨】所得氯化钠溶液中溶质的质量分数为×100%=20%。
7.D 【点拨】20 g KNO3溶解在100 g水中,则溶质与溶剂的质量比为20?100,故A错;所得溶液溶质质量分数为×100%≈16.7%,故B错;升温后,KNO3的饱和溶液将变成较高温度时的不饱和溶液,溶质质量分数不变,故C错;降温后,由于KNO3的溶解度减小,故有晶体析出,D正确。
8.C 【点拨】氧化钙和水反应放出大量的热,使瓶内气体温度升高,U形管内红墨水左侧液面下降,A错误;氢氧化钠溶于水放热,使瓶内气体温度升高,受热膨胀,U形管内红墨水左侧液面下降,B错误;硝酸铵溶于水吸热,使瓶内气体温度降低,压强减小,U形管内红墨水左侧液面上升,C正确;氯化钠溶于水温度几乎无变化,U形管内红墨水液面无明显变化,D错误。
9.A
10.D 【点拨】P点表示t2 ℃时,甲和乙的溶解度相等,A正确;t3 ℃时Q点表示甲的不饱和溶液,B正确;t3 ℃时乙的溶解度是40 g,将25 g乙放入50 g水中,最多只能溶解20 g,所得溶液中溶质和溶剂的质量比为20 g∶50 g=2∶5,C正确;将t3 ℃时甲、乙、丙的饱和溶液降温至t1 ℃,丙变成不饱和溶液,溶质质量分数不变,大于t1 ℃时乙、甲的饱和溶液的溶质质量分数,t1 ℃时,乙的溶解度大于甲,因此乙的溶液的质量分数大于甲的,溶质的质量分数由大到小的顺序为丙>乙>甲,D不正确。
11.B 【点拨】称取的氯化钠固体质量偏大、量取水的体积偏小,都会导致溶质质量分数偏大;转移称量好的氯化钠固体时,有少量撒落在桌面上,会导致所配溶液溶质质量分数偏小;转移配制好的溶液时,有少量液体溅出,溶质质量分数不变。
12.D 【点拨】20 ℃时,硝酸钾的溶解度为31.6 g,60 ℃时,硝酸钾的溶解度为110.0 g,则20 ℃时,50 g水中最多溶解硝酸钾15.8 g,60 ℃时,50 g水中最多溶解硝酸钾55 g;则①③中的溶液均为不饱和溶液,故A说法正确;②③中溶剂的质量相等,③中溶解的溶质的质量最多,则②③中溶液的质量:③>②,故B说法正确;②③④分别是20 ℃时的饱和溶液、60 ℃时的不饱和溶液、10 ℃时的饱和溶液;②③④中溶剂的质量相等,③中溶解的溶质的质量最多,④中溶解的溶质质量最少,则溶液的溶质质量分数:③>②>④,故C说法正确;10 ℃时硝酸钾的溶解度为20.9 g,则10 ℃时,50 g水中最多溶解硝酸钾10.45 g,④中析出晶体的质量是10 g+10 g-10.45 g=9.55 g,故D说法错误。
二、13.(1)④ (2)高;温度越高,乳化效果越好
(3)①C ②B
14.(1)20 (2)B (3)饱和;37.5%
【点拨】(1)根据图示溶解度曲线图可知,t1 ℃时,A物质的溶解度是20 g。(2)两物质的溶解度曲线图中A的溶解度曲线较陡,B的溶解度曲线较平缓,则B的溶解度受温度影响较小。(3)t2 ℃时,A的溶解度为60 g,则此温度下100 g水中最多溶解A 60 g,所以50 g水中最多能溶解A 30 g,故将35 g A物质加入到50 g水中,充分溶解后,得到A的饱和溶液,且溶液中只能溶解A 30 g,则A的溶质质量分数=×100%=37.5%。
15.(1)不饱和 (2)40 g (3)C
【点拨】(1)饱和溶液是指一定温度下不能继续溶解某种溶质的溶液,①能继续溶解20 g KCl,所以是KCl的不饱和溶液。(2)根据题中的实验可知,该温度下100 g水中加入40 g氯化钾恰好饱和,故该温度下氯化钾的溶解度是40 g。(3)实验③溶液中溶质的质量分数为×100%≈28.6%。
16.(1)A (2)34.0 g
34.0 g
(4)称量时砝码和氯化钠的位置放反了;12 (5)18%
四、18. 20% (1)10;15
(2)【解】设需加水的质量为x,则根据稀释前后溶质的质量不变,可列方程如下:
×20%=(+x)×10% x=30 g
答:要使溶质质量分数变为原来的一半,需加水30 g。
19.【解】(1)3.0 (2)90%
(3)设10 g盐酸中HCl的质量为y。
CaCO3 + 2HCl===CaCl2+H2O+CO2↑
100 73
1 g y
= y=0.73 g
所用稀盐酸的溶质质量分数为×100%=7.3%
答:所用稀盐酸的溶质质量分数为7.3%。
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
