第五单元_定量研究化学反应(复习) 23张幻灯片
文档属性
| 名称 | 第五单元_定量研究化学反应(复习) 23张幻灯片 |

|
|
| 格式 | zip | ||
| 文件大小 | 135.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-04-25 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
第五单元 定量研究化学反应
复习课
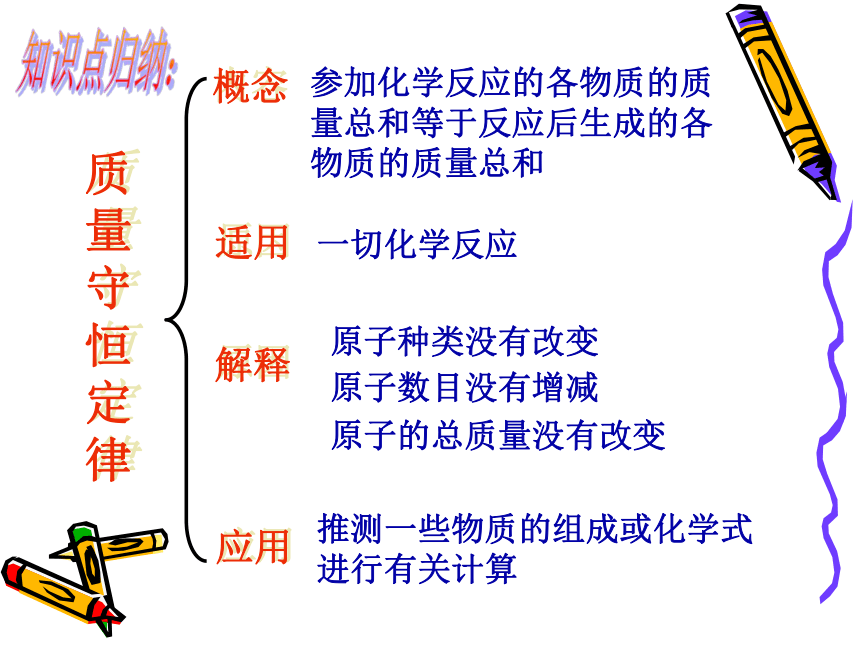
质量守恒定律
质量守恒定律
原因
解释
原子种类没有改变
原子数目没有增减
原子的总质量没有改变
应用
应用
推测一些物质的组成或化学式进行有关计算
内容
概念
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
原因
适用
一切化学反应
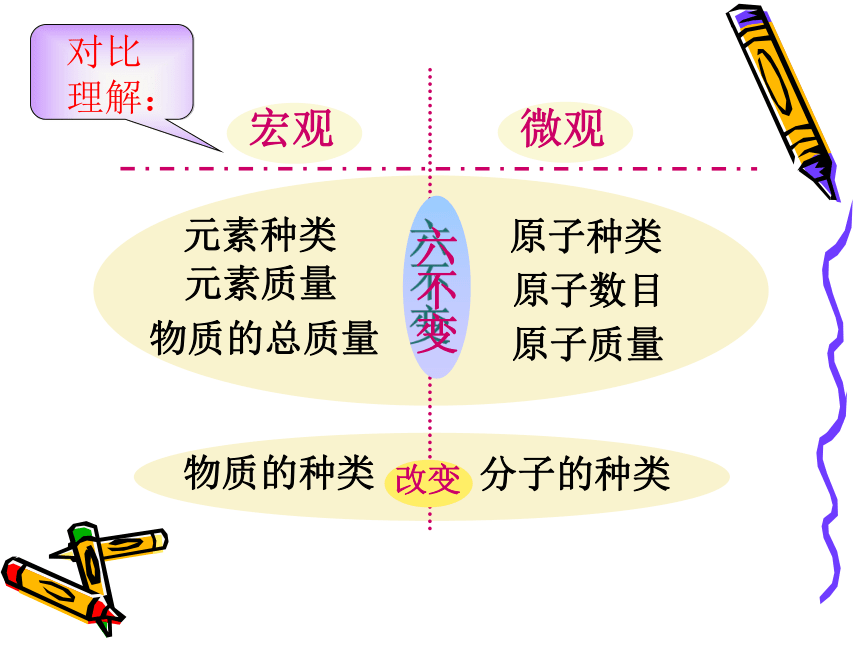
宏观
微观
物质的总质量
元素质量
元素种类
原子数目
原子质量
原子种类
六不变
物质的种类
分子的种类
改变
对比
理解:
考点 1
如何用实验来探究化学反应中的质量守恒
例题1:小明用按右图所示先测定蜡烛燃烧前的质量,然后点燃蜡烛,燃烧一段时间后,他发现天平的指针偏向右边。由此小明得出“蜡烛燃烧后质量减少,不符合质量守恒定律”的错误结论。
(1)你认为实验失败的原因是?
(2)你的改正方案是?
蜡烛未放在密闭容器中燃烧
将蜡烛放在密闭容器中燃烧
考点 2
质量守恒定律的概念
例题2:在化学反应A+B→C中,8gA和足量的B完全反应后,得到11gC,那么,参加反应的B的质量是( )
A.8g B. 5g C.3g D. 2g
C
考点 3
质量守恒定律的应用
例题3:化学反应中可能改变的是( )
A.物质的种类 B. 分子的种类 C.分子数目 D.原子种类
C
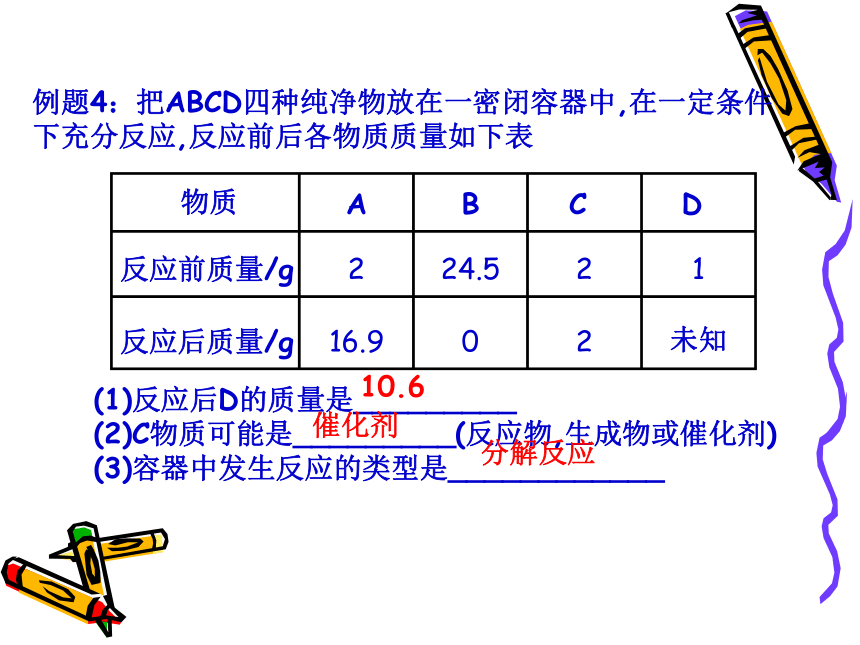
例题4:把ABCD四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质质量如下表
物质
反应前质量/g
反应后质量/g
A
B
C
D
2
2
2
1
0
24.5
16.9
未知
(1)反应后D的质量是_________
(2)C物质可能是_________(反应物,生成物或催化剂)
(3)容器中发生反应的类型是____________
10.6
催化剂
分解反应
化学方程式
应用
计算
计算的思路和步骤:审题;设未知数,找出已知量和未知量的关系,列比例,求解,写出简明的答案
内容
概念
用化学式来表示化学反应的式子
原因
涵义
表明反应物、生成物、反应条件
表明反应物和生成物之间的微观粒子数之比
表明反应物和生成物之间的质量关系
原因
书写原则
以客观事实为依据
遵守质量守恒定律
原因
书写
1.写:正确书写化学式
2.配:依据:质量守恒定律
3.标:标注反应条件,生成物状态
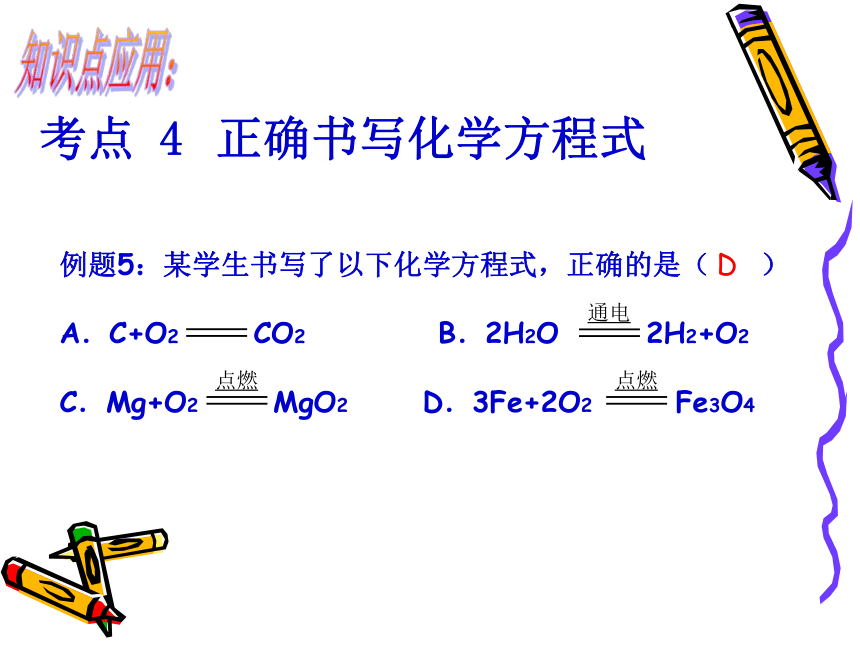
考点 4
正确书写化学方程式
例题5:某学生书写了以下化学方程式,正确的是( )
A.C+O2 CO2 B.2H2O 2H2+O2
C.Mg+O2 MgO2 D.3Fe+2O2 Fe3O4
点燃
通电
点燃
D
考点 5
根据题意信息,按要求书写化学方程式
例题6:
用纳米级某种氧化物做催化剂,使汽车尾气中的CO和NO反应,转化成两种气体,其中一种可参与植物的光合作用,另一种是空气中含量最多的气体。请根据所给信息,写出相应的化学方程式。
2CO+ 2NO====N2+2CO2
催化剂
1.质量与相对质量的关系
例题7. 在反应2A+B=2C中,1.6g的A完全反应生成2gC,又已知B的相对分子质量为32,则C的相对分子质量是( )
A、28 B、64 C、80 D、44
C
解析:
2A + B = 2C
设C的相对分子质量为M
32 2M
0.4g 2g
根据质量守恒可知mB=2g-1.6g=0.4g
2M×0.4g=32×2g
M=80
考点 6
常见计算题型
例题8
某可燃气体A与7.2gO2恰好完全反应,生成3.6g H2O和8.8g CO2,则A气体中( )
A.一定含C、H元素,不含O元素
B.可能含C、H、O三种元素
C.一定含C、H、O三种元素 D.不能确定
2.由反应前后元素的种类和质量守恒,推断物质的组成
解析:
首先根据元素守恒可知A中一定含有C、H元素,可能含有O元素。
若A中不含O元素,氧气质量=反应后氧元素质量
若A 中含有O,则氧气质量<反应后氧元素质量
反应后氧元素质量=二氧化碳中氧元素质量+
水中氧元素质量
=6.4g+3.2g=9.6g
二氧化碳中氧元素质量=8.8g × =6.4g
44
32
水中氧元素质量=3.6g × =3.2g
36
32
9.6g > 7.2g
所以,A中一定含有O元素
3.根据化学方程式的计算
例题9:发射火箭用联氨(N2H4)做燃料,用四氧化氮(N2O4)助燃,生成物不会对大气污染。
(1)反应的化学方程式为:2N2H4+N2O4 3 +4H2O,请在横线上填写化学式以完成该化学方程式。
(2)请计算9.6N2H4完全燃烧需要N2O4的质量。
课堂达标测试
1、下列叙述完全符合质量守恒定律的是 ( )
A.水结成冰前后,质量保持不变
B.50 mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2 g碳与3.2 g氧气恰好完全反应,可生成4.4 g二氧化碳
2、(2011.桂林市)某纯净物M微热就能分解生成NH3、H2O和CO2,由此还不能得出的结论是 ( )
A.M不稳定 B.M是化合物 C.M中含有水 D.M由四种元素组成
3、(2012.青岛市)以下是某化学反应的微观示意图( 、 分别表示不同
元素的原子),下列对图示反应的理解中,
正确的是( )
A.反应物和生成物中共含有三种元素
B.参加反应的物质分子个数之比为1:1
C.反应物和生成物中只有一种单质
D.该反应属于化合反应
+
4、(2013泰安)关于化学方程式CH4+2O2点燃CO2+2H2O的描述正确的是 ( )
A.甲烷加氧气在点燃条件下,反应生成二氧化碳和水
B.1个甲烷和2个氧气在点燃条件下,生成1个二氧化碳和 2个水
C.1个CH4分子和2个O2分子在点燃条件下,生成1个CO2分子和2个H2O分子
D.1 g CH4和2 g O2在点燃条件下,生成1 g CO2和2 g H2O
5、(2011.淄博市)在化学反应A+B=C+D中,若12 g A与一定量的B恰好完全反应,生成28 g C和2 g D,则参加反应的B的质量为 ( )
A.8 g B.18 g C.28 g D.30 g
6、(2012.鸡西市)氯气是一种有毒的气体,实验室制取氯气时,可以用氢氧化钠溶液来吸收尾气,其反应原理为Cl2 + 2NaOH = X + NaClO + H2O, 则X 的化学式为 ( )
A. NaCl B. H2 C. HCl D. HClO
7、(2012.宜宾市)一定条件下,下列物质在密闭容器内反应一段时间,测得反应产前后各物质的质量如下:
物质
反应前质量/g
反应后质量/g
X
Y
Z
W
10
16.2
8.1
0.9
4.4
2.2
a
1.8
根据上表信息判断,下列说法中不正确的是 ( )
A.X、Z是反应物,Y、W是生成物 B.a=15
C.反应中Y、W两种物质变化的质量比为22︰9 D.Z为化合物
8.(2013 长沙)实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有100g过氧化氢溶液的锥形瓶中,反应完全结束后,共收集到1.6g气体.请完成下列问题:
(1)反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为 g.
(2)计算原过氧化氢溶液中溶质的质量分数.
第五单元 定量研究化学反应
复习课
质量守恒定律
质量守恒定律
原因
解释
原子种类没有改变
原子数目没有增减
原子的总质量没有改变
应用
应用
推测一些物质的组成或化学式进行有关计算
内容
概念
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
原因
适用
一切化学反应
宏观
微观
物质的总质量
元素质量
元素种类
原子数目
原子质量
原子种类
六不变
物质的种类
分子的种类
改变
对比
理解:
考点 1
如何用实验来探究化学反应中的质量守恒
例题1:小明用按右图所示先测定蜡烛燃烧前的质量,然后点燃蜡烛,燃烧一段时间后,他发现天平的指针偏向右边。由此小明得出“蜡烛燃烧后质量减少,不符合质量守恒定律”的错误结论。
(1)你认为实验失败的原因是?
(2)你的改正方案是?
蜡烛未放在密闭容器中燃烧
将蜡烛放在密闭容器中燃烧
考点 2
质量守恒定律的概念
例题2:在化学反应A+B→C中,8gA和足量的B完全反应后,得到11gC,那么,参加反应的B的质量是( )
A.8g B. 5g C.3g D. 2g
C
考点 3
质量守恒定律的应用
例题3:化学反应中可能改变的是( )
A.物质的种类 B. 分子的种类 C.分子数目 D.原子种类
C
例题4:把ABCD四种纯净物放在一密闭容器中,在一定条件下充分反应,反应前后各物质质量如下表
物质
反应前质量/g
反应后质量/g
A
B
C
D
2
2
2
1
0
24.5
16.9
未知
(1)反应后D的质量是_________
(2)C物质可能是_________(反应物,生成物或催化剂)
(3)容器中发生反应的类型是____________
10.6
催化剂
分解反应
化学方程式
应用
计算
计算的思路和步骤:审题;设未知数,找出已知量和未知量的关系,列比例,求解,写出简明的答案
内容
概念
用化学式来表示化学反应的式子
原因
涵义
表明反应物、生成物、反应条件
表明反应物和生成物之间的微观粒子数之比
表明反应物和生成物之间的质量关系
原因
书写原则
以客观事实为依据
遵守质量守恒定律
原因
书写
1.写:正确书写化学式
2.配:依据:质量守恒定律
3.标:标注反应条件,生成物状态
考点 4
正确书写化学方程式
例题5:某学生书写了以下化学方程式,正确的是( )
A.C+O2 CO2 B.2H2O 2H2+O2
C.Mg+O2 MgO2 D.3Fe+2O2 Fe3O4
点燃
通电
点燃
D
考点 5
根据题意信息,按要求书写化学方程式
例题6:
用纳米级某种氧化物做催化剂,使汽车尾气中的CO和NO反应,转化成两种气体,其中一种可参与植物的光合作用,另一种是空气中含量最多的气体。请根据所给信息,写出相应的化学方程式。
2CO+ 2NO====N2+2CO2
催化剂
1.质量与相对质量的关系
例题7. 在反应2A+B=2C中,1.6g的A完全反应生成2gC,又已知B的相对分子质量为32,则C的相对分子质量是( )
A、28 B、64 C、80 D、44
C
解析:
2A + B = 2C
设C的相对分子质量为M
32 2M
0.4g 2g
根据质量守恒可知mB=2g-1.6g=0.4g
2M×0.4g=32×2g
M=80
考点 6
常见计算题型
例题8
某可燃气体A与7.2gO2恰好完全反应,生成3.6g H2O和8.8g CO2,则A气体中( )
A.一定含C、H元素,不含O元素
B.可能含C、H、O三种元素
C.一定含C、H、O三种元素 D.不能确定
2.由反应前后元素的种类和质量守恒,推断物质的组成
解析:
首先根据元素守恒可知A中一定含有C、H元素,可能含有O元素。
若A中不含O元素,氧气质量=反应后氧元素质量
若A 中含有O,则氧气质量<反应后氧元素质量
反应后氧元素质量=二氧化碳中氧元素质量+
水中氧元素质量
=6.4g+3.2g=9.6g
二氧化碳中氧元素质量=8.8g × =6.4g
44
32
水中氧元素质量=3.6g × =3.2g
36
32
9.6g > 7.2g
所以,A中一定含有O元素
3.根据化学方程式的计算
例题9:发射火箭用联氨(N2H4)做燃料,用四氧化氮(N2O4)助燃,生成物不会对大气污染。
(1)反应的化学方程式为:2N2H4+N2O4 3 +4H2O,请在横线上填写化学式以完成该化学方程式。
(2)请计算9.6N2H4完全燃烧需要N2O4的质量。
课堂达标测试
1、下列叙述完全符合质量守恒定律的是 ( )
A.水结成冰前后,质量保持不变
B.50 mL水和50 mL乙醇混合后总体积小于100 mL
C.在100 g过氧化氢溶液中,含有30 g过氧化氢和70 g水
D.1.2 g碳与3.2 g氧气恰好完全反应,可生成4.4 g二氧化碳
2、(2011.桂林市)某纯净物M微热就能分解生成NH3、H2O和CO2,由此还不能得出的结论是 ( )
A.M不稳定 B.M是化合物 C.M中含有水 D.M由四种元素组成
3、(2012.青岛市)以下是某化学反应的微观示意图( 、 分别表示不同
元素的原子),下列对图示反应的理解中,
正确的是( )
A.反应物和生成物中共含有三种元素
B.参加反应的物质分子个数之比为1:1
C.反应物和生成物中只有一种单质
D.该反应属于化合反应
+
4、(2013泰安)关于化学方程式CH4+2O2点燃CO2+2H2O的描述正确的是 ( )
A.甲烷加氧气在点燃条件下,反应生成二氧化碳和水
B.1个甲烷和2个氧气在点燃条件下,生成1个二氧化碳和 2个水
C.1个CH4分子和2个O2分子在点燃条件下,生成1个CO2分子和2个H2O分子
D.1 g CH4和2 g O2在点燃条件下,生成1 g CO2和2 g H2O
5、(2011.淄博市)在化学反应A+B=C+D中,若12 g A与一定量的B恰好完全反应,生成28 g C和2 g D,则参加反应的B的质量为 ( )
A.8 g B.18 g C.28 g D.30 g
6、(2012.鸡西市)氯气是一种有毒的气体,实验室制取氯气时,可以用氢氧化钠溶液来吸收尾气,其反应原理为Cl2 + 2NaOH = X + NaClO + H2O, 则X 的化学式为 ( )
A. NaCl B. H2 C. HCl D. HClO
7、(2012.宜宾市)一定条件下,下列物质在密闭容器内反应一段时间,测得反应产前后各物质的质量如下:
物质
反应前质量/g
反应后质量/g
X
Y
Z
W
10
16.2
8.1
0.9
4.4
2.2
a
1.8
根据上表信息判断,下列说法中不正确的是 ( )
A.X、Z是反应物,Y、W是生成物 B.a=15
C.反应中Y、W两种物质变化的质量比为22︰9 D.Z为化合物
8.(2013 长沙)实验室常用过氧化氢溶液与二氧化锰混合制取氧气.现将2.5g二氧化锰放入盛有100g过氧化氢溶液的锥形瓶中,反应完全结束后,共收集到1.6g气体.请完成下列问题:
(1)反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为 g.
(2)计算原过氧化氢溶液中溶质的质量分数.
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
