实验活动5 粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级全册化学
文档属性
| 名称 | 实验活动5 粗盐中难溶性杂质的去除 同步练习(含答案) 2022-2023学年人教版(五四学制)九年级全册化学 |
|
|
| 格式 | zip | ||
| 文件大小 | 248.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-18 00:00:00 | ||
图片预览

文档简介
实验活动5 粗盐中难溶性杂质的去除 同步练习
一、单选题
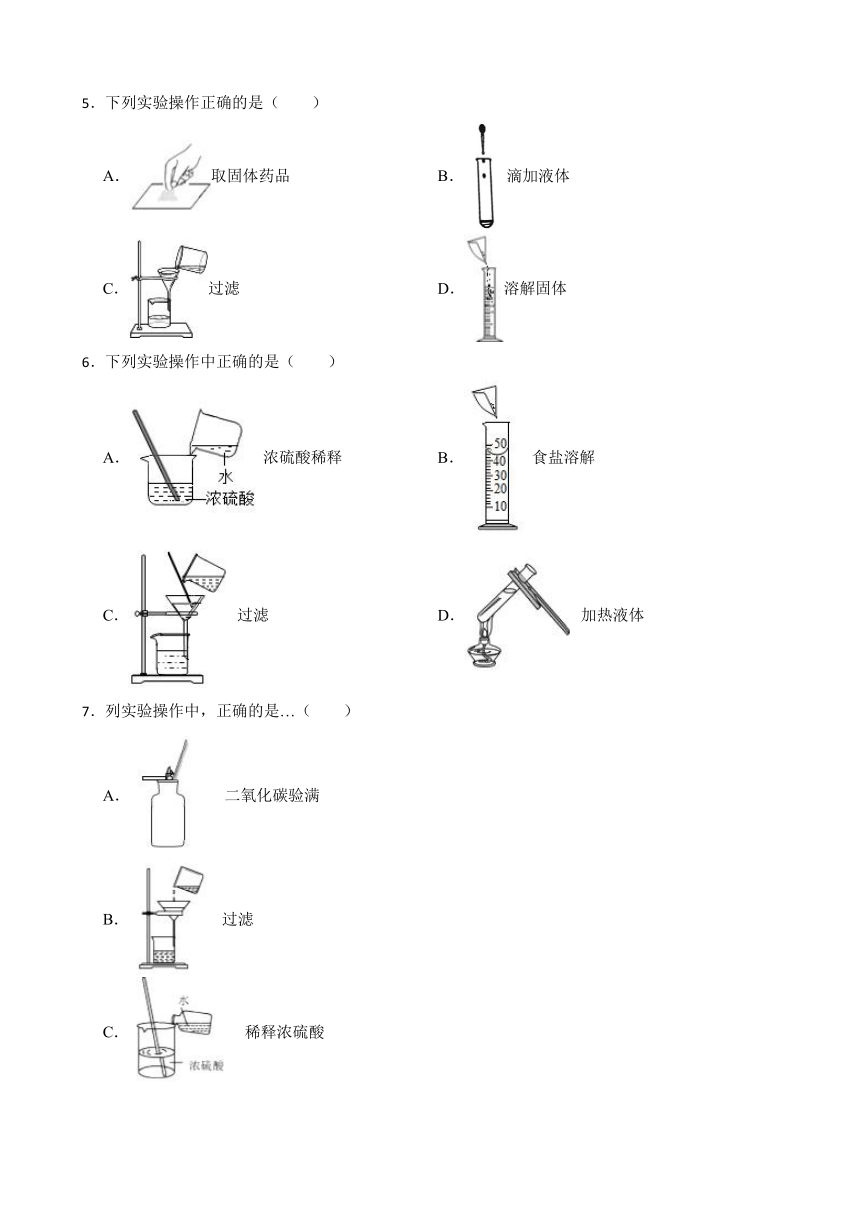
1.如图所示的实验操作正确的是( )
A.检查气密性 B.稀释浓硫酸
C.过滤粗盐水 D.量取液体
2.下列图示实验操作中正确的是( )
A. 滴加液体 B. 过滤
C. 检查气密性 D. 加热液体
3.下列有关水的说法正确的是( )
A.可以用肥皂水区分硬水和软水 B.过滤可以除去水中所有杂质
C.无色无味的水都能饮用 D.水蒸发时水分子种类改变
4.下列实验能达到目的的是()
A.①分离溶液中的FeCl2和CuCl2 B.②检验蜡烛燃烧生成的水
C.③检验碳酸盐的存在 D.④用水吸收CO
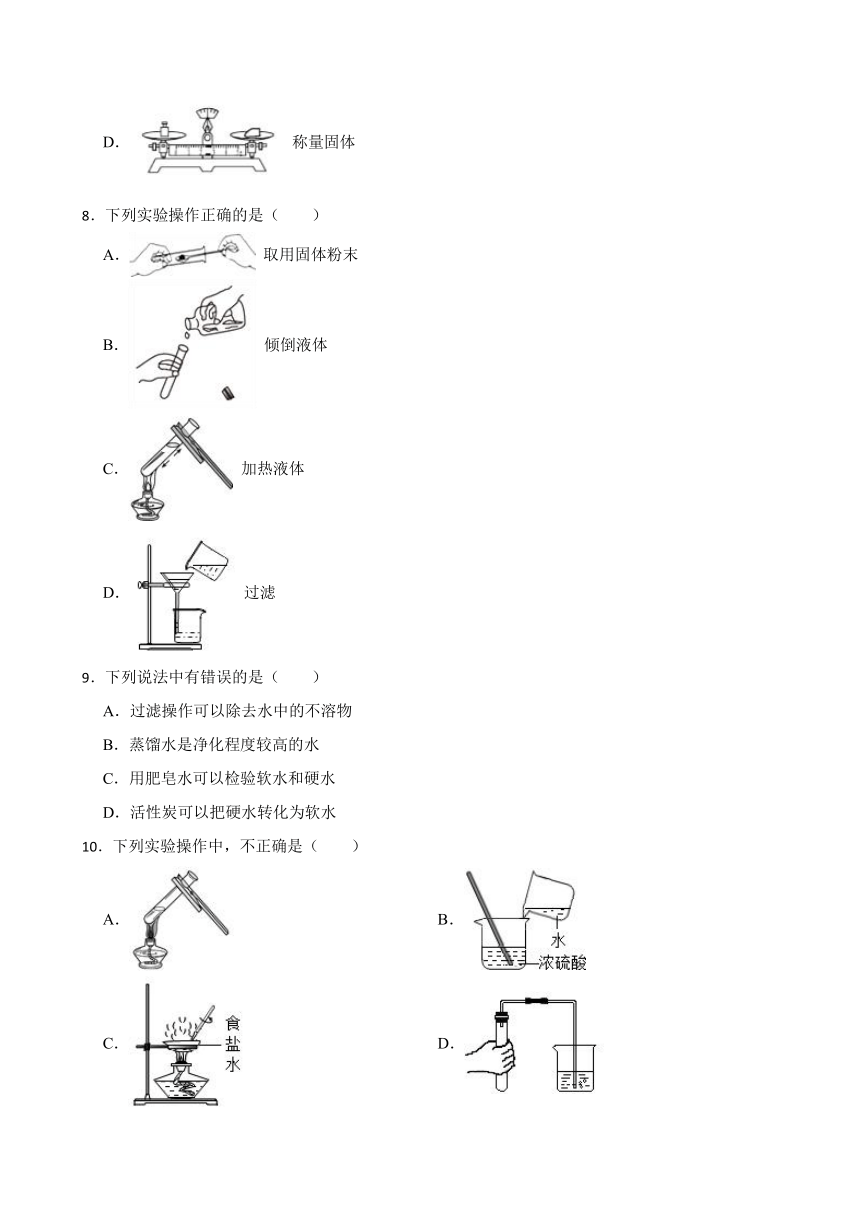
5.下列实验操作正确的是( )
A.取固体药品 B.滴加液体
C.过滤 D.溶解固体
6.下列实验操作中正确的是( )
A. 浓硫酸稀释 B. 食盐溶解
C. 过滤 D. 加热液体
7.列实验操作中,正确的是…( )
A. 二氧化碳验满
B. 过滤
C. 稀释浓硫酸
D. 称量固体
8.下列实验操作正确的是( )
A. 取用固体粉末
B. 倾倒液体
C. 加热液体
D. 过滤
9.下列说法中有错误的是( )
A.过滤操作可以除去水中的不溶物
B.蒸馏水是净化程度较高的水
C.用肥皂水可以检验软水和硬水
D.活性炭可以把硬水转化为软水
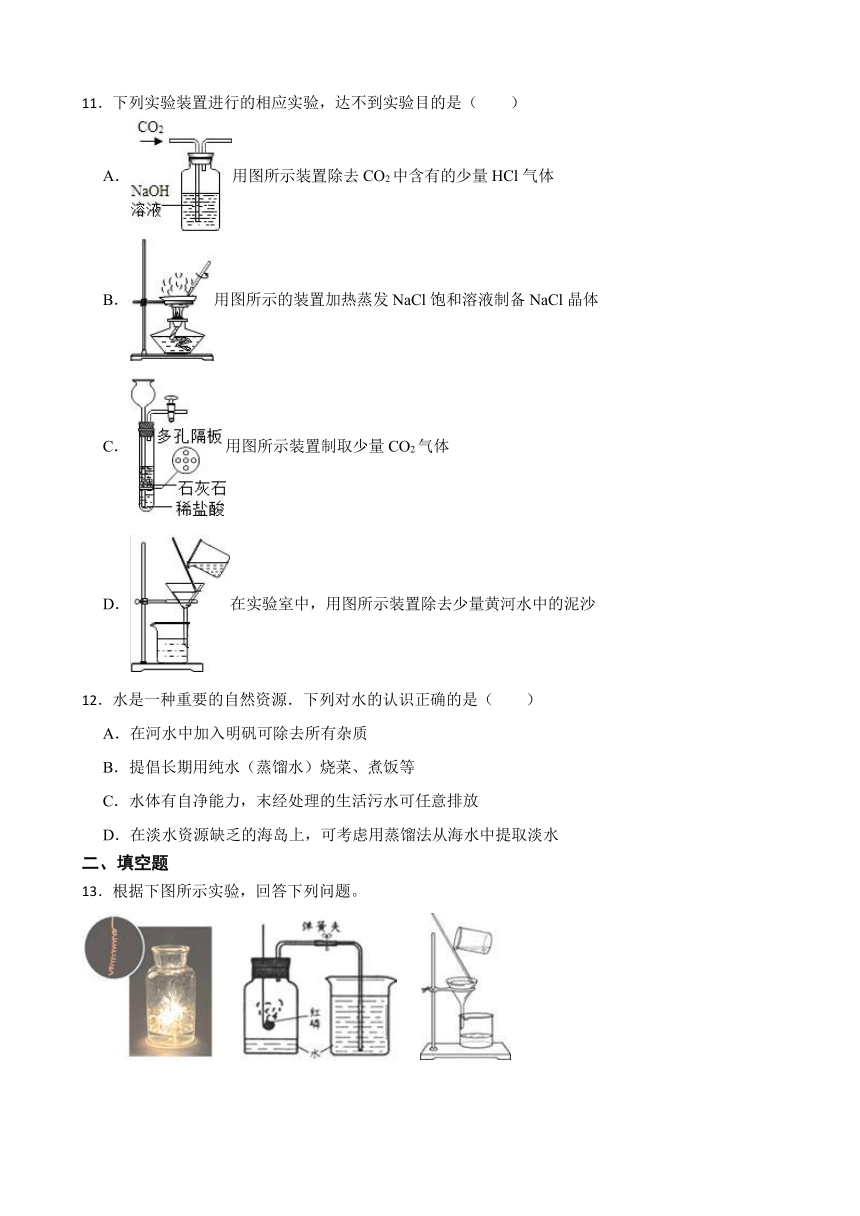
10.下列实验操作中,不正确是( )
A. B.
C. D.
11.下列实验装置进行的相应实验,达不到实验目的是( )
A.用图所示装置除去CO2中含有的少量HCl气体
B.用图所示的装置加热蒸发NaCl饱和溶液制备NaCl晶体
C.用图所示装置制取少量CO2气体
D.在实验室中,用图所示装置除去少量黄河水中的泥沙
12.水是一种重要的自然资源.下列对水的认识正确的是( )
A.在河水中加入明矾可除去所有杂质
B.提倡长期用纯水(蒸馏水)烧菜、煮饭等
C.水体有自净能力,末经处理的生活污水可任意排放
D.在淡水资源缺乏的海岛上,可考虑用蒸馏法从海水中提取淡水
二、填空题
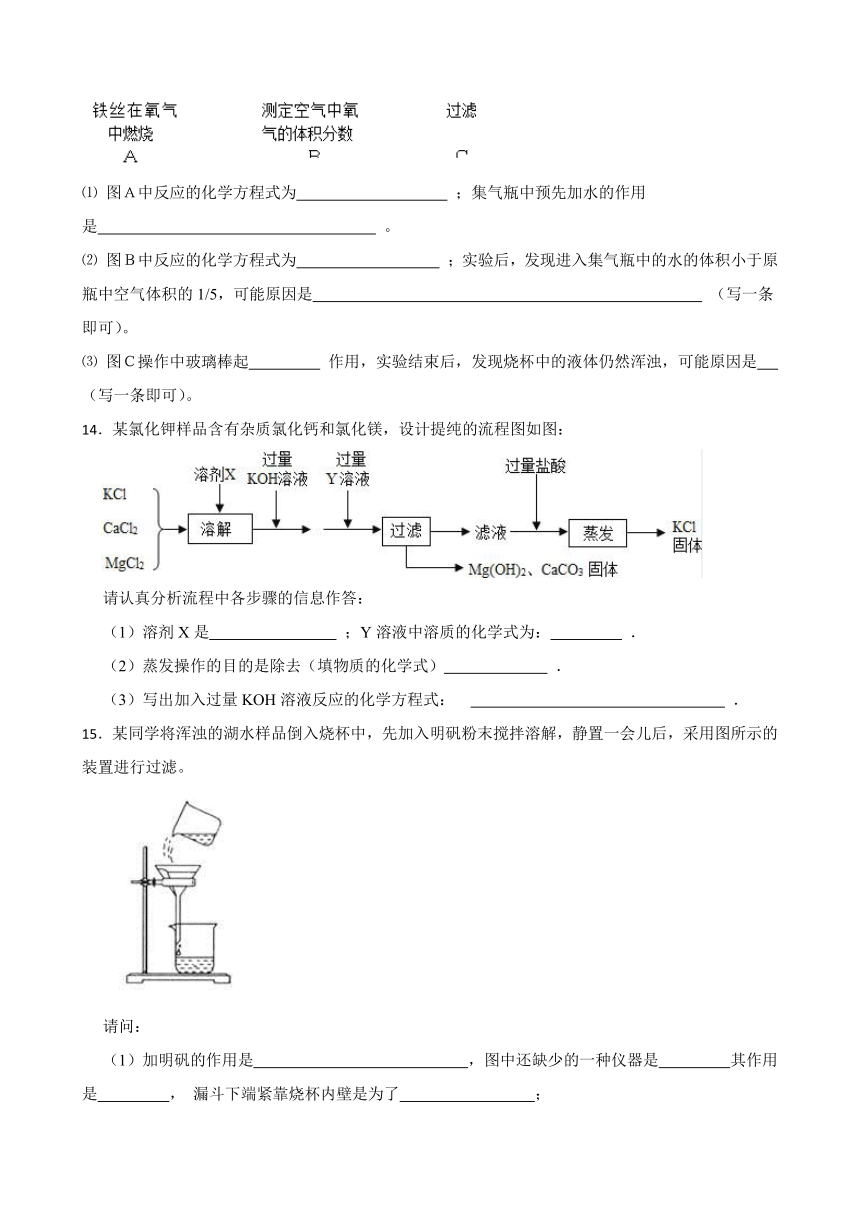
13.根据下图所示实验,回答下列问题。
⑴ 图A中反应的化学方程式为 ;集气瓶中预先加水的作用是 。
⑵ 图B中反应的化学方程式为 ;实验后,发现进入集气瓶中的水的体积小于原瓶中空气体积的1/5,可能原因是 (写一条即可)。
⑶ 图C操作中玻璃棒起 作用,实验结束后,发现烧杯中的液体仍然浑浊,可能原因是 (写一条即可)。
14.某氯化钾样品含有杂质氯化钙和氯化镁,设计提纯的流程图如图:
请认真分析流程中各步骤的信息作答:
(1)溶剂X是 ;Y溶液中溶质的化学式为: .
(2)蒸发操作的目的是除去(填物质的化学式) .
(3)写出加入过量KOH溶液反应的化学方程式: .
15.某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用图所示的装置进行过滤。
请问:
(1)加明矾的作用是 ,图中还缺少的一种仪器是 其作用是 , 漏斗下端紧靠烧杯内壁是为了 ;
(2)操作过程中,他发现过滤速度太慢,原因可能是 ;
(3)过滤后发现,滤液仍浑浊,可能的原因是 ;
(4)改进后得到澄清、透明的水,他兴奋地宣布,我终于制得了纯水,对此你有无不同的看法?理由是 , 若要制取纯水,还需采用的净水方法是 。
16.过滤是一种净水的方法,利用过滤的方法,可将不溶于水的固体杂质与水分离开来.如图是过滤操作示意图,请指出错误,并加以改正.
错误之处: .
改正方法: .
17.水是弥足珍贵的资源.
①在自来水生产过程中要进行消毒杀菌,常加入的消毒剂是 ,在该过程中发生的变化属于 (填“化学变化”或“物理变化”);
②图1中甲是淡化海水的模拟装置,乙是电解水的装置.
I.图1甲中水的状态变化为:液态→气态→液态,这个过程中水分子的 发生了改变.冷凝器中用水作冷却剂是利用其 (填字母)
a.水分子的缔合性b.比热容大c.分散性
II.图1乙中试管“2”内气体的检验方法是 ,水分解过程中不能分解的微粒是图2中的 (填字母)( 可表示一个水分子)用硬水洗衣服既浪费肥皂也洗不净
III.“嫦娥三号”探月使用的液氢即为电解水所得.制取3molH2需电解水的物质的量为 (根据方程式列式计算)
18.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是 ;
(2)操作①②③都要用到的一种玻璃仪器是 ,在操作③中,使用这种玻璃仪器的目的是 .
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是 (只写一种原因).
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号).
a、称量氯化钠所用天平砝码沾有杂质;b、用量筒取水时俯视读数;c、用量筒取水时仰视读数;d、配制溶液的烧杯用蒸馏水润洗过
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液 mL(结果保留小数点后一位).
三、综合题
19.现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末.欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置.
(2)这三种金属中,与盐酸反应最剧烈的是 ;取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是 .
(3)待不再产生气泡时,再进行 (填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 .
(4)写出金属R与稀硫酸反应的化学方程式 .该反应的基本类型属于 (选填“化合”、“分解”、“置换”或“复分解”)反应.
20.如图是实验室常见的实验仪器,请按要求填空。
(1)分别写出相关仪器的名称:④ ;⑥ 。
(2)取用 的蒸馏水,可选用的仪器是 (填序号,下同),读数时视线要与 保持水平,再读出液体的体积。
(3)在实验室要进行过滤操作,现有带铁圈的铁架台、玻璃棒两种仪器,还需要上述仪器中的 。
(4)欲用①和②两种仪器给少量液体加热,还需要的仪器是 。
21.自来水厂净水过程的主要操作流程如图所示。
回答下列问题:
(1)操作 的名称是 ,试剂A的名称是 。
(2)明矾作絮凝剂是因为与水反应生成氢氧化铝胶状物。该过程为 (填“物理”或“化学”)变化。
(3)生活中将硬水软化的方法是 。
四、实验探究题
22.海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。下图是某厂生产纯碱的工艺流程图:
(1)流程I中加入药品的顺序还可以是 。
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液。请分析加入过量的碳酸钠溶液的作用是 ;过滤后得到的沉淀含 种物质。
(3)若在上述制取纯碱的过程中CO2和NH3都是可以循环使用的物质,试写出一种再获得NH3的一个最佳的反应方程式: 。
(4)我国化学家侯德榜创立的联合制碱法的优点有______。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】A
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】3Fe + 2O2Fe3O4;防止高温熔化物溅落,炸裂集气瓶;4P + 5O22P2O5;装置漏气(或红磷不足量或未冷却就打开弹簧夹);引流;滤纸破损(或漏斗内液面超过滤纸边缘或仪器不干净)
14.【答案】水(或H2O);K2CO3;HCl、H2O;MgCl2+2KOH=Mg(OH)2↓+2KCl
15.【答案】(1)吸附杂质,使悬浮物沉降;玻璃棒;引流;防止液体溅出
(2)滤纸没有紧贴漏斗内壁,中间残留气泡
(3)滤纸破损,液面高于滤纸边缘
(4)不是纯水,还含有可溶性的杂质;蒸馏
16.【答案】①未用玻璃棒引流;②滤纸比漏斗边高;③漏斗远离烧杯壁;①液体沿玻璃棒流入过滤器;②滤纸比漏斗边应稍低;③漏斗尖端紧靠烧杯内壁
17.【答案】液氯;化学变化;间隔;b;将带火星的木条伸入试管内,若木条复燃证明是氧气;bd;3mol.
18.【答案】过滤;玻璃棒;防止液体外溅;蒸发溶液时液体外溅了一部分;ab;7.7
19.【答案】(1)
(2)镁(或Mg);银(或Ag)
(3)过滤;铁(或Fe)
(4)Fe+H2SO4=FeSO4+H2↑;置换
20.【答案】(1)烧杯;集气瓶
(2)⑤;量筒内液体凹液面的最低处
(3)③和④
(4)试管夹
21.【答案】(1)过滤;明矾
(2)化学
(3)煮沸
22.【答案】(1)氢氧化钠溶液、氯化钡溶液、碳酸钠溶液(或氯化钡溶液、碳酸钠溶液、氢氧化钠溶液)
(2)除去氯化钙和过量的氯化钡;4或四
(3)Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O
(4)A;B
一、单选题
1.如图所示的实验操作正确的是( )
A.检查气密性 B.稀释浓硫酸
C.过滤粗盐水 D.量取液体
2.下列图示实验操作中正确的是( )
A. 滴加液体 B. 过滤
C. 检查气密性 D. 加热液体
3.下列有关水的说法正确的是( )
A.可以用肥皂水区分硬水和软水 B.过滤可以除去水中所有杂质
C.无色无味的水都能饮用 D.水蒸发时水分子种类改变
4.下列实验能达到目的的是()
A.①分离溶液中的FeCl2和CuCl2 B.②检验蜡烛燃烧生成的水
C.③检验碳酸盐的存在 D.④用水吸收CO
5.下列实验操作正确的是( )
A.取固体药品 B.滴加液体
C.过滤 D.溶解固体
6.下列实验操作中正确的是( )
A. 浓硫酸稀释 B. 食盐溶解
C. 过滤 D. 加热液体
7.列实验操作中,正确的是…( )
A. 二氧化碳验满
B. 过滤
C. 稀释浓硫酸
D. 称量固体
8.下列实验操作正确的是( )
A. 取用固体粉末
B. 倾倒液体
C. 加热液体
D. 过滤
9.下列说法中有错误的是( )
A.过滤操作可以除去水中的不溶物
B.蒸馏水是净化程度较高的水
C.用肥皂水可以检验软水和硬水
D.活性炭可以把硬水转化为软水
10.下列实验操作中,不正确是( )
A. B.
C. D.
11.下列实验装置进行的相应实验,达不到实验目的是( )
A.用图所示装置除去CO2中含有的少量HCl气体
B.用图所示的装置加热蒸发NaCl饱和溶液制备NaCl晶体
C.用图所示装置制取少量CO2气体
D.在实验室中,用图所示装置除去少量黄河水中的泥沙
12.水是一种重要的自然资源.下列对水的认识正确的是( )
A.在河水中加入明矾可除去所有杂质
B.提倡长期用纯水(蒸馏水)烧菜、煮饭等
C.水体有自净能力,末经处理的生活污水可任意排放
D.在淡水资源缺乏的海岛上,可考虑用蒸馏法从海水中提取淡水
二、填空题
13.根据下图所示实验,回答下列问题。
⑴ 图A中反应的化学方程式为 ;集气瓶中预先加水的作用是 。
⑵ 图B中反应的化学方程式为 ;实验后,发现进入集气瓶中的水的体积小于原瓶中空气体积的1/5,可能原因是 (写一条即可)。
⑶ 图C操作中玻璃棒起 作用,实验结束后,发现烧杯中的液体仍然浑浊,可能原因是 (写一条即可)。
14.某氯化钾样品含有杂质氯化钙和氯化镁,设计提纯的流程图如图:
请认真分析流程中各步骤的信息作答:
(1)溶剂X是 ;Y溶液中溶质的化学式为: .
(2)蒸发操作的目的是除去(填物质的化学式) .
(3)写出加入过量KOH溶液反应的化学方程式: .
15.某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉末搅拌溶解,静置一会儿后,采用图所示的装置进行过滤。
请问:
(1)加明矾的作用是 ,图中还缺少的一种仪器是 其作用是 , 漏斗下端紧靠烧杯内壁是为了 ;
(2)操作过程中,他发现过滤速度太慢,原因可能是 ;
(3)过滤后发现,滤液仍浑浊,可能的原因是 ;
(4)改进后得到澄清、透明的水,他兴奋地宣布,我终于制得了纯水,对此你有无不同的看法?理由是 , 若要制取纯水,还需采用的净水方法是 。
16.过滤是一种净水的方法,利用过滤的方法,可将不溶于水的固体杂质与水分离开来.如图是过滤操作示意图,请指出错误,并加以改正.
错误之处: .
改正方法: .
17.水是弥足珍贵的资源.
①在自来水生产过程中要进行消毒杀菌,常加入的消毒剂是 ,在该过程中发生的变化属于 (填“化学变化”或“物理变化”);
②图1中甲是淡化海水的模拟装置,乙是电解水的装置.
I.图1甲中水的状态变化为:液态→气态→液态,这个过程中水分子的 发生了改变.冷凝器中用水作冷却剂是利用其 (填字母)
a.水分子的缔合性b.比热容大c.分散性
II.图1乙中试管“2”内气体的检验方法是 ,水分解过程中不能分解的微粒是图2中的 (填字母)( 可表示一个水分子)用硬水洗衣服既浪费肥皂也洗不净
III.“嫦娥三号”探月使用的液氢即为电解水所得.制取3molH2需电解水的物质的量为 (根据方程式列式计算)
18.同学们在实验室对含有泥沙的粗盐进行提纯,实验的基本流程如下:
(1)操作②的名称是 ;
(2)操作①②③都要用到的一种玻璃仪器是 ,在操作③中,使用这种玻璃仪器的目的是 .
(3)计算所获得的氯化钠产率,发现产率偏低,由实验不当导致的可能原因是 (只写一种原因).
(4)用提纯所得的氯化钠溶液配制100g6%的氯化钠溶液,若实际所配溶液溶质质量分数大于6%,可能的原因是 (填字母编号).
a、称量氯化钠所用天平砝码沾有杂质;b、用量筒取水时俯视读数;c、用量筒取水时仰视读数;d、配制溶液的烧杯用蒸馏水润洗过
(5)若用6%的氯化钠溶液(密度为1.04g/cm3),配制16g质量分数为3%的氯化钠溶液,需要6%的氯化钠溶液 mL(结果保留小数点后一位).
三、综合题
19.现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末.欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置.
(2)这三种金属中,与盐酸反应最剧烈的是 ;取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是 .
(3)待不再产生气泡时,再进行 (填写一种实验操作方法),得到溶液和铜.然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是 .
(4)写出金属R与稀硫酸反应的化学方程式 .该反应的基本类型属于 (选填“化合”、“分解”、“置换”或“复分解”)反应.
20.如图是实验室常见的实验仪器,请按要求填空。
(1)分别写出相关仪器的名称:④ ;⑥ 。
(2)取用 的蒸馏水,可选用的仪器是 (填序号,下同),读数时视线要与 保持水平,再读出液体的体积。
(3)在实验室要进行过滤操作,现有带铁圈的铁架台、玻璃棒两种仪器,还需要上述仪器中的 。
(4)欲用①和②两种仪器给少量液体加热,还需要的仪器是 。
21.自来水厂净水过程的主要操作流程如图所示。
回答下列问题:
(1)操作 的名称是 ,试剂A的名称是 。
(2)明矾作絮凝剂是因为与水反应生成氢氧化铝胶状物。该过程为 (填“物理”或“化学”)变化。
(3)生活中将硬水软化的方法是 。
四、实验探究题
22.海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧。下图是某厂生产纯碱的工艺流程图:
(1)流程I中加入药品的顺序还可以是 。
(2)流程I中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液。请分析加入过量的碳酸钠溶液的作用是 ;过滤后得到的沉淀含 种物质。
(3)若在上述制取纯碱的过程中CO2和NH3都是可以循环使用的物质,试写出一种再获得NH3的一个最佳的反应方程式: 。
(4)我国化学家侯德榜创立的联合制碱法的优点有______。
A.无“索尔维氨碱法”中的废弃物CaCl2生成,有利于保护环境
B.大大提高了食盐的利用率,节约了成本
C.将“制碱”与制氨生产联合起来,同时析出的NH4Cl晶体可用作复合肥
答案解析部分
1.【答案】A
2.【答案】C
3.【答案】A
4.【答案】B
5.【答案】B
6.【答案】C
7.【答案】A
8.【答案】A
9.【答案】D
10.【答案】B
11.【答案】A
12.【答案】D
13.【答案】3Fe + 2O2Fe3O4;防止高温熔化物溅落,炸裂集气瓶;4P + 5O22P2O5;装置漏气(或红磷不足量或未冷却就打开弹簧夹);引流;滤纸破损(或漏斗内液面超过滤纸边缘或仪器不干净)
14.【答案】水(或H2O);K2CO3;HCl、H2O;MgCl2+2KOH=Mg(OH)2↓+2KCl
15.【答案】(1)吸附杂质,使悬浮物沉降;玻璃棒;引流;防止液体溅出
(2)滤纸没有紧贴漏斗内壁,中间残留气泡
(3)滤纸破损,液面高于滤纸边缘
(4)不是纯水,还含有可溶性的杂质;蒸馏
16.【答案】①未用玻璃棒引流;②滤纸比漏斗边高;③漏斗远离烧杯壁;①液体沿玻璃棒流入过滤器;②滤纸比漏斗边应稍低;③漏斗尖端紧靠烧杯内壁
17.【答案】液氯;化学变化;间隔;b;将带火星的木条伸入试管内,若木条复燃证明是氧气;bd;3mol.
18.【答案】过滤;玻璃棒;防止液体外溅;蒸发溶液时液体外溅了一部分;ab;7.7
19.【答案】(1)
(2)镁(或Mg);银(或Ag)
(3)过滤;铁(或Fe)
(4)Fe+H2SO4=FeSO4+H2↑;置换
20.【答案】(1)烧杯;集气瓶
(2)⑤;量筒内液体凹液面的最低处
(3)③和④
(4)试管夹
21.【答案】(1)过滤;明矾
(2)化学
(3)煮沸
22.【答案】(1)氢氧化钠溶液、氯化钡溶液、碳酸钠溶液(或氯化钡溶液、碳酸钠溶液、氢氧化钠溶液)
(2)除去氯化钙和过量的氯化钡;4或四
(3)Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O
(4)A;B
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
