第七章有机化合物随堂练习(含答案)2022-2023学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 第七章有机化合物随堂练习(含答案)2022-2023学年下学期高一化学人教版(2019)必修第二册 |  | |
| 格式 | docx | ||
| 文件大小 | 249.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-19 11:07:00 | ||
图片预览




文档简介
第七章有机化合物 随堂练习
一、单选题
1.地球在流浪,学习不能忘”,学好化学让生活更美好。下列说法错误的是
A.港珠澳大桥采用的超高分子量聚乙烯纤维吊绳,是有机高分子化合物
B.“玉兔二号”月球车首次在月球背面着陆,其帆板太阳能电池的材料是SiO2
C.《天工开物》中“凡石灰经火焚炼为用”,其中“石灰”指的是CaCO3
D.宋·王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜
2.下列说法不正确的是
A.油脂是油和脂肪的统称,都是高级脂肪酸与甘油形成的酯
B.棉花、羊毛、蚕丝和麻等是天然纤维
C.高聚物中的官能团是酯基
D.可以用溴水鉴别乙醛和乙烯
3.下列物质中,属于烷烃的是
A.C8H16 B.CH3CH2OH C. D.CH2=CH2
4.NA为阿伏加德罗常数的值,下列说法不正确的是
A.1 mol 羟基所含的质子数和电子数均为9NA
B.2.3 g Na与O2完全反应,反应中转移的电子数介于0.1NA和0.2NA之间
C.一定条件下,合成氨反应中有0.5 mol N2发生反应,则反应中转移电子数为3NA
D.1 mol C5H12(戊烷)中含有的C-C数为4NA
5.下列各组物质中,互为同位素的是
A.CH4和C3H8 B.H2O和D2O C.金刚石和石墨 D.氕和氚
6.要除去下列物质中的杂质,下列除杂方法不能达到目的是
气体(杂质) 除杂方法
A 依次通过饱和溶液、浓硫酸
B 加足量蒸馏
C 固体 将固体高温加热至质量恒定后冷却
D 溶液 通入氯化氢气体至不再有气体产生
A.A B.B C.C D.D
7.下列说法中错误的是
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的熔、沸点都比C2H6、C2H4的高
C.乙醇能发生氧化反应
D.乙醇和乙酸都可发生酯化反应,酯化反应是不可逆的
8.现有五种有机物,其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是
①
②
③
④
⑤
A.③⑤ B.①②⑤ C.②④ D.③④
9.广州亚运会的“潮流”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
A.分子中碳原子不在一条直线上 B.光照下能够发生取代反应
C.比丁烷更易液化 D.是石油分馏的一种产品
10.下列物质属于烃的衍生物的是
A.C6H6 B.C2H6 C.C2H4 D.C2H5OH
11.化学在疫情防控中发挥着重要作用。下列说法不正确的是
A.医用消毒酒精是75%的乙醇溶液
B.氯仿可有效灭活病毒,其化学名称是三氯甲烷
C.乙酸可用于家用除垢剂,它的酸性比苯酚弱
D.84消毒液和酒精混合消毒作用减弱,可能发生了氧化反应
二、填空题
12.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_______。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______。
(3)下列关于乙醇的说法不正确的是_______(选填字母)。
A.乙醇与乙烷相比,乙醇熔沸点较高,易溶解于水,主要是氢键所致
B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
D.医用酒精含乙醇体积分数95%
E.用工业酒精与生石灰通过蒸馏的方法制无水酒精
(4)乙醇能够发生氧化反应:
①46g乙醇完全燃烧消耗氧气的物质的量_______。
②在试管里加入2 mL乙醇。把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄层黑色的氧化铜,立即把它插入盛有乙醇的试管里,取出铜丝,可以观察到铜丝表面_______。写出灼热的铜丝插入乙醇中发生反应的化学方程式:_______。
13.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇和乙酸是比较常见的有机物。
(1)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______________(不用写反应条件)。
(2)乙醇能够发生氧化反应:乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_______。
(3)下列关于乙醇的说法正确的是______(选填字母)。
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.乙醇只能被氧化成乙醛
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
(4)当乙酸分子中的O都是18O时,乙醇分子中的O都是16O时,二者在一定条件下反应,生成物中水的相对分子质量为________。
14.有机化学中的反应类型较多,将下列反应归类,用序号回答问题:
①由乙炔制氯乙烯②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色⑤由乙烯制聚乙烯⑥甲烷与氯气在光照的条件下反应⑦甲苯与浓硝酸在加热条件下反应⑧由氯乙烯制备聚氯乙烯(PVC)
(1)其中属于取代反应的是_______;属于加聚反应的是_______;
(2)其中⑦对应的化学反应方程式_______;⑧对应的化学反应方程式为_______;
15.下面列出了几组物质,请用物质的组号填写下表。
类型 同位素 同素异形体 同分异构体 同系物
组号 _____ _____ _____ _____
①CH(CH3)3和CH3CH2CH(CH3)2
②C(CH3)4和CH3CH2CH(CH3)2
③CH4和CH3CH2CH3
④金刚石和石墨
⑤H、D、T
⑥12C、13C、14C
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3)
⑧臭氧(18O3)和氧气(16O18O )
⑨ 和
⑩ H216O和H218O
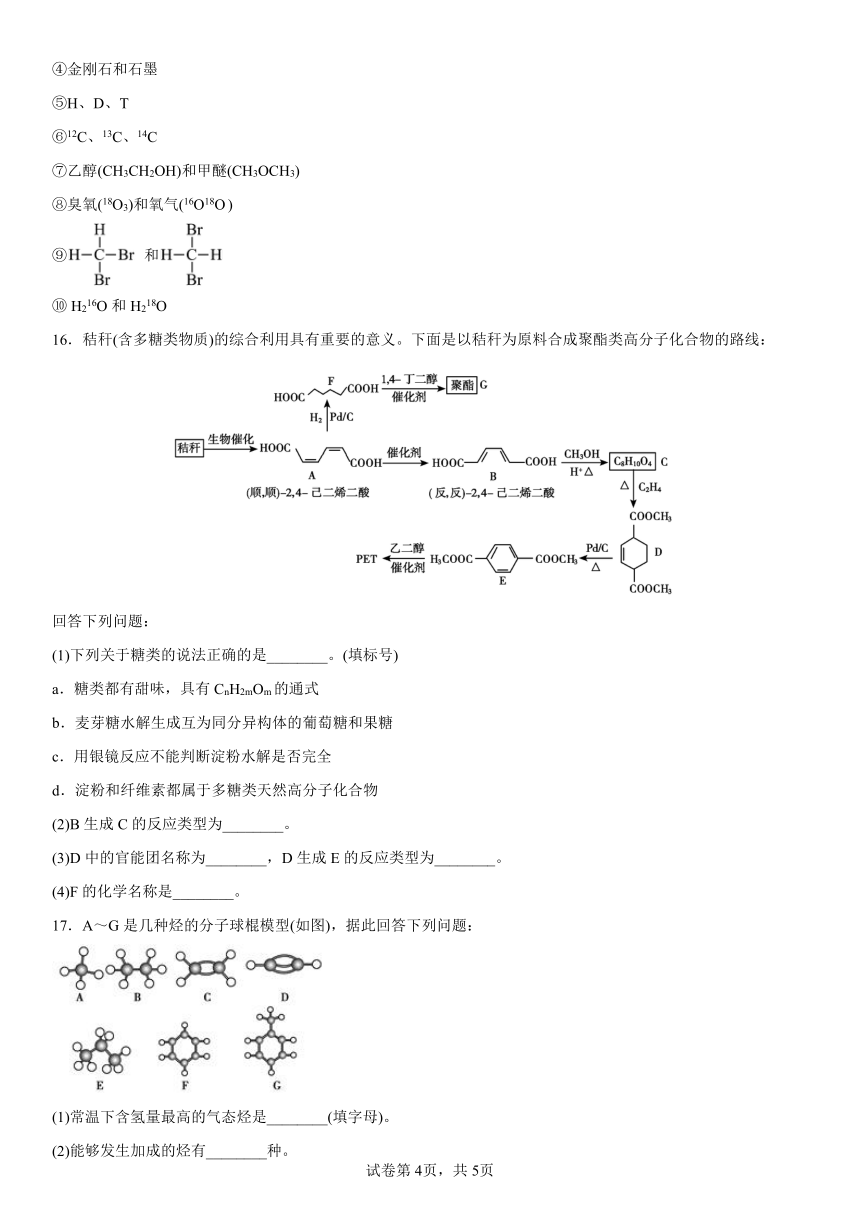
16.秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
回答下列问题:
(1)下列关于糖类的说法正确的是________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为________。
(3)D中的官能团名称为________,D生成E的反应类型为________。
(4)F的化学名称是________。
17.A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
(1)常温下含氢量最高的气态烃是________(填字母)。
(2)能够发生加成的烃有________种。
(3)一卤代物种类最多的是________(填写字母)。
(4)写出实验室制D的化学方程式:__________________________________________。
(5)写出G发生硝化反应的化学方程式:______________________________________。
18.请用三种不同的方法区分厨房中的淀粉和食盐_______。
19.丙烯酸乙酯是一种食用香料,用乙烯、丙烯等石油化工产品为原料合成丙烯酸乙酯的路线如图所示。
回答下列问题:
(1)CH2=CH2是重要的化工原料,CH2=CH2的电子式为___________,CH2=CH2能使溴的四氯化碳溶液褪色,该反应的化学方程式为_____________________。
(2)化合物B中所含官能团的名称为____________ 、 ____________。
(3)CH2=CH2→A,A+B→丙烯酸乙酯的反应类型分别为__________、___________。
(4)丁醇与CH3CH2OH互为同系物,丁醇的醇类同分异构体有_______种。
(5)丙烯酸乙酯一定条件下会发生聚合反应,该聚合物有较好的弹性,可用于生产织物。该聚合反应的化学方程式为__________________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A、聚乙烯纤维,由小分子乙烯加聚得到,是有机高分子化合物,A不符合题意;
B、太阳能电池的材料是Si,而不是SiO2,B符合题意;
C、石灰石的主要成分为CaCO3,受热分解得到CaO,C不符合题意;
D、铜绿的主要成分为碱式碳酸铜,Cu2(OH)2CO3;D不符合题意;
答案选B。
2.D
【详解】A、油脂分为油和脂肪,无论油还是脂肪都是高级脂肪酸与甘油形成的酯,故A不符合题意;
B、棉花、羊毛、蚕丝和麻等是天然纤维,故B不符合题意;
C、是由羟基乙酸发生缩聚反应生成的酯,含有的官能团为酯基,故C不符合题意;
D、溴水是一种强氧化剂,能把乙醛氧化成乙酸,发生氧化反应使其褪色,乙烯与溴水发生加成反应使其褪色,故不能利用溴水鉴别乙醛和乙烯,故D符合题意;
故选D。
【点睛】自然界存在的天然纤维主要有:棉花,麻类,蚕丝和动物毛,其中棉花和麻类的分子成份主要是天然纤维素,而蚕丝和毛类的分子成份主要是蛋白质(呈聚酰胺高分子形式存在);天然界除棉花、麻类外,树木、草类也大量生长着纤维素高分子,然而树木、草类生长的纤维素,不是呈长纤维状态存在,不能直接当作纤维来应用,将这些天然纤维素高分子经过化学处理,不改变它的化学结构,仅仅改变天然纤维素的物理结构,从而制造出来可以作为纤维应用的而且性能更好的纤维素纤维。
3.C
【详解】烷烃属于饱和烃,分子中只含有C、H元素,烷烃分子中只存在单键,烷烃的通式可用CnH2n+2表示,满足该通式的有机物一定属于烷烃;
A.C8H16属于烯烃或环烷烃,故A不选;
B.CH3CH2OH属于醇类,故B不选;
C.属于烷烃,故C选;
D.CH2=CH2属于烯烃,故D不选;
故选C。
4.B
【详解】A. 1 mol 羟基所含的质子数和电子数均为(1+8)NA=9NA,故A正确;
B. 2.3 g Na与O2完全反应,反应中转移的电子数0.1NA,故B错误;
C. 一定条件下,合成氨反应中氮由0价降为-3价,有0.5 mol N2发生反应,则反应中转移电子数为3NA,故C正确;
D. 1 mol C5H12(戊烷)中含有的C-C数为(5-1)NA=4NA,故D正确;
主选B。
5.D
【详解】A.CH4和C3H8均为烷烃,相差2个CH2,属于同系物,A错误;
B.H2O和D2O是同一物质,B错误;
C.金刚石和石墨都是由C原子构成的单质,互为同素异形体,C错误;
D.氕和氚为1H和3H,是质子数相同而中子数不同的同种元素的不同原子,互为同位素,D正确;
故选D。
6.D
【详解】A.亚硫酸的酸性比碳酸强,SO2通过饱和溶液可除去杂质二氧化硫、通过浓硫酸可干燥二氧化碳,A正确;
B.乙酸和CaO反应形成高沸点物质,蒸馏收集乙醇,B正确;
C.CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,C正确;
D.NaOH溶液通入氯化氢反应生成氯化钠和水,不符合除杂原则,D错误;
故选:D。
7.D
【详解】A、乙醇和乙酸是生活中的调味品,酒精调制的酒可以饮用,食醋的主要成分为乙酸,说法正确,故A不符合题意;
B、乙醇和乙酸中含有羟基,能够形成分子间氢键,增大了熔沸点,C2H6、C2H4中不能形成氢键,说法正确,故B不符合题意;
C、乙醇可被酸性高锰酸钾氧化,也可发生催化氧化,乙酸发生氧化反应生成过氧乙酸,说法正确,故C不符合题意;
D、乙醇和乙酸在浓硫酸催化作用下发生酯化反应生成乙酸乙酯,酯化反应是可逆反应,说法错误,故D符合题意。
8.A
【详解】①中含醛基,能发生加成反应和氧化反应;含醇羟基,能发生酯化反应和氧化反应,不能发生加聚反应,不符合题意;②中含醇羟基,能发生酯化反应和氧化反应,不能发生加成反应和加聚反应不符合题意;③中含碳碳双键,能发生加成反应、加聚反应和氧化反应;含醇羟基,能发生酯化反应和氧化反应,符合题意;④中含碳碳双键,能发生加成反应、加聚反应和氧化反应,含酯基能发生水解反应(或取代反应),不能发生酯化反应,不符合题意;⑤中含碳碳双键,能发生加成反应、加聚反应和氧化反应;含羧基,能发生酯化反应,符合题意;由分析可知符合题意的有③⑤,A项正确;
故选A
9.C
【详解】A.丙烷有3个碳原子,中间的碳原子连接了两个碳原子和两个氢原子,这两个碳原子和两个氢原子构成了一个四面体结构,中间的碳原子在四面体的中心。在四面体结构中,键角接近109°28ˊ,所以这三个碳原子构成了一个角形结构,夹角大约109°,所以三个碳原子不在一条直线上。故A不选;
B. 丙烷属于烷烃,烷烃都可以在光照下和卤素单质发生取代反应,故B不选;
C.丙烷的沸点比丁烷低,所以比丁烷难液化,故C选;
D.丙烷和丁烷都是通过石油分馏获得的石油气中的成分,故D不选。
故选C。
10.D
【分析】烃分子中的氢原子被其他原子或者原子团所取代而生成的一系列化合物称为烃的衍生物,据此分析判断。
【详解】A.C6H6中只含有C和H两种元素,属于烃,故A不选;
B.C2H6中只含有C和H两种元素,属于烃,故B不选;
C.C2H4中只含有C和H两种元素,属于烃,故C不选;
D.C2H5OH是乙烷中的一个H原子被羟基代替得到的化合物,属于烃的衍生物,故D选;
故选D。
11.C
【详解】A.医用消毒酒精是体积份数为75%的乙醇溶液,故A说法正确;
B.氯仿是指三氯甲烷,可以有效灭活病毒,故B说法正确;
C.乙酸的酸性比苯酚的酸性强,可用于家用除垢剂,故C说法错误;
D.84消毒液的成分是次氯酸钠,具有强氧化性,乙醇中的羟基具有还原性能被氧化,故D说法正确;
本题答案C。
12. 小 CH2=CH2+H2OCH3CH2OH D 3mol 恢复光亮的红色 2C2H5OH+O22CH3CHO+2H2O
【详解】(1)乙醇是无色有特殊香味的液体,密度比水小,故答案为:小;
(2)乙烯中含碳碳双键可和水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2OCH3CH2OH,故答案为:CH2=CH2+H2OCH3CH2OH;
(3)A.乙醇能和水生成氢键,则与乙烷相比,乙醇熔沸点较高,易溶解于水,主要是氢键所致,A正确;
B.乙醇含有羟基,能被酸性重铬酸钾溶液氧化,因此交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车,B正确;
C.黄酒中某些微生物将乙醇氧化为乙酸,乙酸具有酸性,于是酒就变酸了,C正确;
D.医用酒精含乙醇体积分数为75%,D错误;
E.生石灰和水反应生成氢氧化钙,用工业酒精与生石灰通过蒸馏的方法制无水酒精,E正确;
答案选D。
(4)①46g乙醇的物质的量是1mol,根据方程式可知C2H5OH+3O22CO2+3H2O完全燃烧消耗氧气的物质的量3mol。
②在试管里加入2 mL乙醇,把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄层黑色的氧化铜,立即把它插入盛有乙醇的试管里,氧化铜被乙醇还原生成铜、乙醛和水,则取出铜丝,可以观察到铜丝表面又恢复光亮的红色。乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O22CH3CHO+2H2O。
13. CH2=CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O C 20
【详解】(1)乙烯与水反应可制得乙醇,该反应的化学方程式为CH2=CH2+H2OCH3CH2OH;(2)乙醇能够发生氧化反应:乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,同时生成水,反应的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;(3)A、—CH2OH原子团可被酸性KMnO4溶液氧化,选项A错误;B、乙醇也可直接氧化成CH3COOH,选项B错误;C、黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了,选项C正确。答案选C;(4)乙酸与乙醇反应的化学方程式为: ,生成的水为HO,故水的相对分子质量为20。
14.(1) ⑥⑦ ⑤⑧
(2)
【分析】①由乙炔制氯乙烯为加成反应;②乙烷在空气中燃烧为氧化反应;③乙烯使溴的四氯化碳溶液褪色为加成反应;④乙烯使酸性高锰酸钾溶液褪色为氧化反应;⑤由乙烯制聚乙烯为加聚反应;⑥甲烷与氯气在光照的条件下反应为取代反应;⑦甲苯与浓硝酸在加热条件下反应为取代反应;⑧由氯乙烯制备聚氯乙烯为加聚反应。
(1)
属于取代反应的为⑥⑦,属于加聚反应的是⑤⑧
(2)
⑦甲苯和浓硝酸在加热条件下发生取代反应,化学方程式为;
⑧为氯乙烯发生加聚生成聚氯乙烯,反应方程式为。
15. ⑤⑥ ④⑧ ②⑦ ①③
【分析】质子数相同而中子数不同的核素,互称为同位素;由同种元素形成的单质,是同素异形体;若为分子式相同、结构不同的化合物,则为同分异构体;若是结构相似、分子组成相差若干个“CH2”原子团的有机化合物,则为同系物。
【详解】质子数相同而中子数不同的核素,互称为同位素,满足的为⑤⑥;由同种元素形成的单质,是同素异形体,满足的为④⑧;若为分子式相同、结构不同的化合物,则为同分异构体,满足的为②⑦;若是结构相似、分子组成相差若干个“CH2”原子团的有机化合物,则为同系物,满足的为①③,故答案为:⑤⑥;④⑧;②⑦;①③。
16. cd 取代反应(酯化反应) 酯基、碳碳双键 消去反应 己二酸
【详解】(1)a选项,不是所有的糖都有甜味,如纤维素等多糖没有甜味,也不是所有的糖都具有CnH2mOm的通式,如脱氧核糖的分子式为C5H10O4,所以说法错误;
b选项,麦芽糖水解只生成葡萄糖,所以说法错误;
c选项,如果淀粉部分水解生成葡萄糖,也可以发生银镜反应,即银镜反应不能判断溶液中是否还含有淀粉,因此只用银镜反应不能判断淀粉水解是否完全,所以说法正确;
d选项,淀粉和纤维素都属于多糖类天然高分子化合物,所以说法正确。
故答案为cd;
(2)B生成C的反应是酸和醇生成酯的反应,属于取代(或酯化)反应,
故答案为取代反应(酯化反应);
(3)通过观察D分子的结构简式,可判断D分子中含有酯基和碳碳双键;由D生成E的反应为消去反应,
故答案为酯基、碳碳双键;消去反应;
(4)F为分子中含6个碳原子的二元酸,名称为己二酸,
故答案为己二酸。
【点睛】本题考查有机物的结构、性质、转化、反应类型的判断,掌握常见的有机代表物的性质、各类官能团的性质、化学反应类型,充分利用题目提供的信息进行分析、判断是解题关键。
17. A 4 G CaC2+2H2O→Ca(OH)2+C2H2↑ +3HNO3(浓)+3H2O。
【分析】根据图示球棍模型可以看出,A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,则
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的;
(2)含有碳碳双键或三键或苯环的烃能发生加成反应;
(3)根据烃的球棍模型结合等效氢思想确定同分异构体种类;
(4)实验室用碳化钙和水反应制取乙炔;
(5)甲苯和硝酸在浓硫酸作催化剂、加热条件下制取三硝基甲苯。
【详解】(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最小即为含氢量最高的,所以含氢量最大的是甲烷,即A,
故答案为:A;
(2)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、苯和甲苯都能发生加成反应,所以是4种,
故答案为:4;
(3)甲烷、乙烷、乙烯、乙炔、苯的一卤代物都只有1种,丙烷的一卤代物有2种,甲苯的有一卤代物有4种,
故答案为:G;
(4)实验室用碳化钙和水反应制取乙炔,反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(5)在浓硫酸作催化剂、加热条件下甲苯和浓硝酸反应生成三硝基甲苯,反应方程式为:+3HNO3(浓)+3H2O。
18.a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐(或通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉)
【分析】淀粉和食盐的外观不同,食盐的主要成分为氯化钠,氯化钠在水溶液中可以电离出钠离子和氯离子,淀粉不能电离,据此分析解答。
【详解】食盐为白色颗粒状固体,淀粉是白色粉末状固体;淀粉没有味道,食盐有咸味;食盐的主要成分为氯化钠,氯化钠在水溶液中可以电离出钠离子和氯离子,可以用硝酸银检验氯离子确定是氯化钠溶液,淀粉不能电离;还可以通过检验钠离子的存在来确定氯化钠,因此区分厨房中的食盐和淀粉的方法有:a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐;d.通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉;故答案为:a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐(或通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉)。
19. CH2=CH2+Br2→CH2BrCH2Br 碳碳双键 羧基 加成反应 取代反应(酯化反应) 4 nCH2=CH-COOC2H5
【详解】(1)CH2=CH2是共价化合物,CH2=CH2的电子式为,CH2=CH2能和溴水发生加成反应,使溴的四氯化碳溶液褪色,该反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br。故答案为:;CH2=CH2+Br2→CH2BrCH2Br;
(2)化合物B的结构简式为CH2=CHCOOH,其中所含官能团的名称为碳碳双键、羧基。故答案为:碳碳双键;羧基;
(3)CH2=CH2和水发生加成反应生成乙醇,乙醇和丙烯酸发生酯化反应生成丙烯酸乙酯。故答案为:加成反应;取代反应(酯化反应);
(4)丁醇是C4H10O,也可以写成C4H9OH,可以看出丁烷(C4H10)的一元取代物,即用羟基取代丁烷上的氢,丁烷的结构简式为CH3CH2CH2CH3,(CH3)2CHCH3,所以丁烷的氢原子共有4种,所以丁醇属于醇类的同分异构体共有4种;故答案为:4;
(5)丙烯酸乙酯含有碳碳双键,一定条件下会发生聚合反应,该聚合反应的化学方程式为nCH2=CH-COOC2H5。故答案为:nCH2=CH-COOC2H5。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.地球在流浪,学习不能忘”,学好化学让生活更美好。下列说法错误的是
A.港珠澳大桥采用的超高分子量聚乙烯纤维吊绳,是有机高分子化合物
B.“玉兔二号”月球车首次在月球背面着陆,其帆板太阳能电池的材料是SiO2
C.《天工开物》中“凡石灰经火焚炼为用”,其中“石灰”指的是CaCO3
D.宋·王希孟《千里江山图》卷中的绿色颜料铜绿的主要成分是碱式碳酸铜
2.下列说法不正确的是
A.油脂是油和脂肪的统称,都是高级脂肪酸与甘油形成的酯
B.棉花、羊毛、蚕丝和麻等是天然纤维
C.高聚物中的官能团是酯基
D.可以用溴水鉴别乙醛和乙烯
3.下列物质中,属于烷烃的是
A.C8H16 B.CH3CH2OH C. D.CH2=CH2
4.NA为阿伏加德罗常数的值,下列说法不正确的是
A.1 mol 羟基所含的质子数和电子数均为9NA
B.2.3 g Na与O2完全反应,反应中转移的电子数介于0.1NA和0.2NA之间
C.一定条件下,合成氨反应中有0.5 mol N2发生反应,则反应中转移电子数为3NA
D.1 mol C5H12(戊烷)中含有的C-C数为4NA
5.下列各组物质中,互为同位素的是
A.CH4和C3H8 B.H2O和D2O C.金刚石和石墨 D.氕和氚
6.要除去下列物质中的杂质,下列除杂方法不能达到目的是
气体(杂质) 除杂方法
A 依次通过饱和溶液、浓硫酸
B 加足量蒸馏
C 固体 将固体高温加热至质量恒定后冷却
D 溶液 通入氯化氢气体至不再有气体产生
A.A B.B C.C D.D
7.下列说法中错误的是
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的熔、沸点都比C2H6、C2H4的高
C.乙醇能发生氧化反应
D.乙醇和乙酸都可发生酯化反应,酯化反应是不可逆的
8.现有五种有机物,其中既能发生加成反应、加聚反应、酯化反应,又能发生氧化反应的是
①
②
③
④
⑤
A.③⑤ B.①②⑤ C.②④ D.③④
9.广州亚运会的“潮流”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
A.分子中碳原子不在一条直线上 B.光照下能够发生取代反应
C.比丁烷更易液化 D.是石油分馏的一种产品
10.下列物质属于烃的衍生物的是
A.C6H6 B.C2H6 C.C2H4 D.C2H5OH
11.化学在疫情防控中发挥着重要作用。下列说法不正确的是
A.医用消毒酒精是75%的乙醇溶液
B.氯仿可有效灭活病毒,其化学名称是三氯甲烷
C.乙酸可用于家用除垢剂,它的酸性比苯酚弱
D.84消毒液和酒精混合消毒作用减弱,可能发生了氧化反应
二、填空题
12.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇是比较常见的有机物。
(1)乙醇是无色有特殊香味的液体,密度比水_______。
(2)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______。
(3)下列关于乙醇的说法不正确的是_______(选填字母)。
A.乙醇与乙烷相比,乙醇熔沸点较高,易溶解于水,主要是氢键所致
B.交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
D.医用酒精含乙醇体积分数95%
E.用工业酒精与生石灰通过蒸馏的方法制无水酒精
(4)乙醇能够发生氧化反应:
①46g乙醇完全燃烧消耗氧气的物质的量_______。
②在试管里加入2 mL乙醇。把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄层黑色的氧化铜,立即把它插入盛有乙醇的试管里,取出铜丝,可以观察到铜丝表面_______。写出灼热的铜丝插入乙醇中发生反应的化学方程式:_______。
13.生活中的有机物种类丰富,在衣食住行等多方面应用广泛,其中乙醇和乙酸是比较常见的有机物。
(1)工业上用乙烯与水反应可制得乙醇,该反应的化学方程式为_______________(不用写反应条件)。
(2)乙醇能够发生氧化反应:乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为_______。
(3)下列关于乙醇的说法正确的是______(选填字母)。
A.乙醇不能和酸性高锰酸钾溶液发生氧化还原反应
B.乙醇只能被氧化成乙醛
C.黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了
(4)当乙酸分子中的O都是18O时,乙醇分子中的O都是16O时,二者在一定条件下反应,生成物中水的相对分子质量为________。
14.有机化学中的反应类型较多,将下列反应归类,用序号回答问题:
①由乙炔制氯乙烯②乙烷在空气中燃烧③乙烯使溴的四氯化碳溶液褪色④乙烯使酸性高锰酸钾溶液褪色⑤由乙烯制聚乙烯⑥甲烷与氯气在光照的条件下反应⑦甲苯与浓硝酸在加热条件下反应⑧由氯乙烯制备聚氯乙烯(PVC)
(1)其中属于取代反应的是_______;属于加聚反应的是_______;
(2)其中⑦对应的化学反应方程式_______;⑧对应的化学反应方程式为_______;
15.下面列出了几组物质,请用物质的组号填写下表。
类型 同位素 同素异形体 同分异构体 同系物
组号 _____ _____ _____ _____
①CH(CH3)3和CH3CH2CH(CH3)2
②C(CH3)4和CH3CH2CH(CH3)2
③CH4和CH3CH2CH3
④金刚石和石墨
⑤H、D、T
⑥12C、13C、14C
⑦乙醇(CH3CH2OH)和甲醚(CH3OCH3)
⑧臭氧(18O3)和氧气(16O18O )
⑨ 和
⑩ H216O和H218O
16.秸秆(含多糖类物质)的综合利用具有重要的意义。下面是以秸秆为原料合成聚酯类高分子化合物的路线:
回答下列问题:
(1)下列关于糖类的说法正确的是________。(填标号)
a.糖类都有甜味,具有CnH2mOm的通式
b.麦芽糖水解生成互为同分异构体的葡萄糖和果糖
c.用银镜反应不能判断淀粉水解是否完全
d.淀粉和纤维素都属于多糖类天然高分子化合物
(2)B生成C的反应类型为________。
(3)D中的官能团名称为________,D生成E的反应类型为________。
(4)F的化学名称是________。
17.A~G是几种烃的分子球棍模型(如图),据此回答下列问题:
(1)常温下含氢量最高的气态烃是________(填字母)。
(2)能够发生加成的烃有________种。
(3)一卤代物种类最多的是________(填写字母)。
(4)写出实验室制D的化学方程式:__________________________________________。
(5)写出G发生硝化反应的化学方程式:______________________________________。
18.请用三种不同的方法区分厨房中的淀粉和食盐_______。
19.丙烯酸乙酯是一种食用香料,用乙烯、丙烯等石油化工产品为原料合成丙烯酸乙酯的路线如图所示。
回答下列问题:
(1)CH2=CH2是重要的化工原料,CH2=CH2的电子式为___________,CH2=CH2能使溴的四氯化碳溶液褪色,该反应的化学方程式为_____________________。
(2)化合物B中所含官能团的名称为____________ 、 ____________。
(3)CH2=CH2→A,A+B→丙烯酸乙酯的反应类型分别为__________、___________。
(4)丁醇与CH3CH2OH互为同系物,丁醇的醇类同分异构体有_______种。
(5)丙烯酸乙酯一定条件下会发生聚合反应,该聚合物有较好的弹性,可用于生产织物。该聚合反应的化学方程式为__________________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A、聚乙烯纤维,由小分子乙烯加聚得到,是有机高分子化合物,A不符合题意;
B、太阳能电池的材料是Si,而不是SiO2,B符合题意;
C、石灰石的主要成分为CaCO3,受热分解得到CaO,C不符合题意;
D、铜绿的主要成分为碱式碳酸铜,Cu2(OH)2CO3;D不符合题意;
答案选B。
2.D
【详解】A、油脂分为油和脂肪,无论油还是脂肪都是高级脂肪酸与甘油形成的酯,故A不符合题意;
B、棉花、羊毛、蚕丝和麻等是天然纤维,故B不符合题意;
C、是由羟基乙酸发生缩聚反应生成的酯,含有的官能团为酯基,故C不符合题意;
D、溴水是一种强氧化剂,能把乙醛氧化成乙酸,发生氧化反应使其褪色,乙烯与溴水发生加成反应使其褪色,故不能利用溴水鉴别乙醛和乙烯,故D符合题意;
故选D。
【点睛】自然界存在的天然纤维主要有:棉花,麻类,蚕丝和动物毛,其中棉花和麻类的分子成份主要是天然纤维素,而蚕丝和毛类的分子成份主要是蛋白质(呈聚酰胺高分子形式存在);天然界除棉花、麻类外,树木、草类也大量生长着纤维素高分子,然而树木、草类生长的纤维素,不是呈长纤维状态存在,不能直接当作纤维来应用,将这些天然纤维素高分子经过化学处理,不改变它的化学结构,仅仅改变天然纤维素的物理结构,从而制造出来可以作为纤维应用的而且性能更好的纤维素纤维。
3.C
【详解】烷烃属于饱和烃,分子中只含有C、H元素,烷烃分子中只存在单键,烷烃的通式可用CnH2n+2表示,满足该通式的有机物一定属于烷烃;
A.C8H16属于烯烃或环烷烃,故A不选;
B.CH3CH2OH属于醇类,故B不选;
C.属于烷烃,故C选;
D.CH2=CH2属于烯烃,故D不选;
故选C。
4.B
【详解】A. 1 mol 羟基所含的质子数和电子数均为(1+8)NA=9NA,故A正确;
B. 2.3 g Na与O2完全反应,反应中转移的电子数0.1NA,故B错误;
C. 一定条件下,合成氨反应中氮由0价降为-3价,有0.5 mol N2发生反应,则反应中转移电子数为3NA,故C正确;
D. 1 mol C5H12(戊烷)中含有的C-C数为(5-1)NA=4NA,故D正确;
主选B。
5.D
【详解】A.CH4和C3H8均为烷烃,相差2个CH2,属于同系物,A错误;
B.H2O和D2O是同一物质,B错误;
C.金刚石和石墨都是由C原子构成的单质,互为同素异形体,C错误;
D.氕和氚为1H和3H,是质子数相同而中子数不同的同种元素的不同原子,互为同位素,D正确;
故选D。
6.D
【详解】A.亚硫酸的酸性比碳酸强,SO2通过饱和溶液可除去杂质二氧化硫、通过浓硫酸可干燥二氧化碳,A正确;
B.乙酸和CaO反应形成高沸点物质,蒸馏收集乙醇,B正确;
C.CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,C正确;
D.NaOH溶液通入氯化氢反应生成氯化钠和水,不符合除杂原则,D错误;
故选:D。
7.D
【详解】A、乙醇和乙酸是生活中的调味品,酒精调制的酒可以饮用,食醋的主要成分为乙酸,说法正确,故A不符合题意;
B、乙醇和乙酸中含有羟基,能够形成分子间氢键,增大了熔沸点,C2H6、C2H4中不能形成氢键,说法正确,故B不符合题意;
C、乙醇可被酸性高锰酸钾氧化,也可发生催化氧化,乙酸发生氧化反应生成过氧乙酸,说法正确,故C不符合题意;
D、乙醇和乙酸在浓硫酸催化作用下发生酯化反应生成乙酸乙酯,酯化反应是可逆反应,说法错误,故D符合题意。
8.A
【详解】①中含醛基,能发生加成反应和氧化反应;含醇羟基,能发生酯化反应和氧化反应,不能发生加聚反应,不符合题意;②中含醇羟基,能发生酯化反应和氧化反应,不能发生加成反应和加聚反应不符合题意;③中含碳碳双键,能发生加成反应、加聚反应和氧化反应;含醇羟基,能发生酯化反应和氧化反应,符合题意;④中含碳碳双键,能发生加成反应、加聚反应和氧化反应,含酯基能发生水解反应(或取代反应),不能发生酯化反应,不符合题意;⑤中含碳碳双键,能发生加成反应、加聚反应和氧化反应;含羧基,能发生酯化反应,符合题意;由分析可知符合题意的有③⑤,A项正确;
故选A
9.C
【详解】A.丙烷有3个碳原子,中间的碳原子连接了两个碳原子和两个氢原子,这两个碳原子和两个氢原子构成了一个四面体结构,中间的碳原子在四面体的中心。在四面体结构中,键角接近109°28ˊ,所以这三个碳原子构成了一个角形结构,夹角大约109°,所以三个碳原子不在一条直线上。故A不选;
B. 丙烷属于烷烃,烷烃都可以在光照下和卤素单质发生取代反应,故B不选;
C.丙烷的沸点比丁烷低,所以比丁烷难液化,故C选;
D.丙烷和丁烷都是通过石油分馏获得的石油气中的成分,故D不选。
故选C。
10.D
【分析】烃分子中的氢原子被其他原子或者原子团所取代而生成的一系列化合物称为烃的衍生物,据此分析判断。
【详解】A.C6H6中只含有C和H两种元素,属于烃,故A不选;
B.C2H6中只含有C和H两种元素,属于烃,故B不选;
C.C2H4中只含有C和H两种元素,属于烃,故C不选;
D.C2H5OH是乙烷中的一个H原子被羟基代替得到的化合物,属于烃的衍生物,故D选;
故选D。
11.C
【详解】A.医用消毒酒精是体积份数为75%的乙醇溶液,故A说法正确;
B.氯仿是指三氯甲烷,可以有效灭活病毒,故B说法正确;
C.乙酸的酸性比苯酚的酸性强,可用于家用除垢剂,故C说法错误;
D.84消毒液的成分是次氯酸钠,具有强氧化性,乙醇中的羟基具有还原性能被氧化,故D说法正确;
本题答案C。
12. 小 CH2=CH2+H2OCH3CH2OH D 3mol 恢复光亮的红色 2C2H5OH+O22CH3CHO+2H2O
【详解】(1)乙醇是无色有特殊香味的液体,密度比水小,故答案为:小;
(2)乙烯中含碳碳双键可和水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2OCH3CH2OH,故答案为:CH2=CH2+H2OCH3CH2OH;
(3)A.乙醇能和水生成氢键,则与乙烷相比,乙醇熔沸点较高,易溶解于水,主要是氢键所致,A正确;
B.乙醇含有羟基,能被酸性重铬酸钾溶液氧化,因此交警用橙色的酸性重铬酸钾溶液检查司机是否酒后驾车,B正确;
C.黄酒中某些微生物将乙醇氧化为乙酸,乙酸具有酸性,于是酒就变酸了,C正确;
D.医用酒精含乙醇体积分数为75%,D错误;
E.生石灰和水反应生成氢氧化钙,用工业酒精与生石灰通过蒸馏的方法制无水酒精,E正确;
答案选D。
(4)①46g乙醇的物质的量是1mol,根据方程式可知C2H5OH+3O22CO2+3H2O完全燃烧消耗氧气的物质的量3mol。
②在试管里加入2 mL乙醇,把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄层黑色的氧化铜,立即把它插入盛有乙醇的试管里,氧化铜被乙醇还原生成铜、乙醛和水,则取出铜丝,可以观察到铜丝表面又恢复光亮的红色。乙醇在铜做催化剂的条件下可被氧气氧化为乙醛,反应的化学方程式为2C2H5OH+O22CH3CHO+2H2O。
13. CH2=CH2+H2OCH3CH2OH 2CH3CH2OH+O22CH3CHO+2H2O C 20
【详解】(1)乙烯与水反应可制得乙醇,该反应的化学方程式为CH2=CH2+H2OCH3CH2OH;(2)乙醇能够发生氧化反应:乙醇在铜作催化剂的条件下可被氧气氧化为乙醛,同时生成水,反应的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;(3)A、—CH2OH原子团可被酸性KMnO4溶液氧化,选项A错误;B、乙醇也可直接氧化成CH3COOH,选项B错误;C、黄酒中某些微生物使乙醇氧化为乙酸,于是酒就变酸了,选项C正确。答案选C;(4)乙酸与乙醇反应的化学方程式为: ,生成的水为HO,故水的相对分子质量为20。
14.(1) ⑥⑦ ⑤⑧
(2)
【分析】①由乙炔制氯乙烯为加成反应;②乙烷在空气中燃烧为氧化反应;③乙烯使溴的四氯化碳溶液褪色为加成反应;④乙烯使酸性高锰酸钾溶液褪色为氧化反应;⑤由乙烯制聚乙烯为加聚反应;⑥甲烷与氯气在光照的条件下反应为取代反应;⑦甲苯与浓硝酸在加热条件下反应为取代反应;⑧由氯乙烯制备聚氯乙烯为加聚反应。
(1)
属于取代反应的为⑥⑦,属于加聚反应的是⑤⑧
(2)
⑦甲苯和浓硝酸在加热条件下发生取代反应,化学方程式为;
⑧为氯乙烯发生加聚生成聚氯乙烯,反应方程式为。
15. ⑤⑥ ④⑧ ②⑦ ①③
【分析】质子数相同而中子数不同的核素,互称为同位素;由同种元素形成的单质,是同素异形体;若为分子式相同、结构不同的化合物,则为同分异构体;若是结构相似、分子组成相差若干个“CH2”原子团的有机化合物,则为同系物。
【详解】质子数相同而中子数不同的核素,互称为同位素,满足的为⑤⑥;由同种元素形成的单质,是同素异形体,满足的为④⑧;若为分子式相同、结构不同的化合物,则为同分异构体,满足的为②⑦;若是结构相似、分子组成相差若干个“CH2”原子团的有机化合物,则为同系物,满足的为①③,故答案为:⑤⑥;④⑧;②⑦;①③。
16. cd 取代反应(酯化反应) 酯基、碳碳双键 消去反应 己二酸
【详解】(1)a选项,不是所有的糖都有甜味,如纤维素等多糖没有甜味,也不是所有的糖都具有CnH2mOm的通式,如脱氧核糖的分子式为C5H10O4,所以说法错误;
b选项,麦芽糖水解只生成葡萄糖,所以说法错误;
c选项,如果淀粉部分水解生成葡萄糖,也可以发生银镜反应,即银镜反应不能判断溶液中是否还含有淀粉,因此只用银镜反应不能判断淀粉水解是否完全,所以说法正确;
d选项,淀粉和纤维素都属于多糖类天然高分子化合物,所以说法正确。
故答案为cd;
(2)B生成C的反应是酸和醇生成酯的反应,属于取代(或酯化)反应,
故答案为取代反应(酯化反应);
(3)通过观察D分子的结构简式,可判断D分子中含有酯基和碳碳双键;由D生成E的反应为消去反应,
故答案为酯基、碳碳双键;消去反应;
(4)F为分子中含6个碳原子的二元酸,名称为己二酸,
故答案为己二酸。
【点睛】本题考查有机物的结构、性质、转化、反应类型的判断,掌握常见的有机代表物的性质、各类官能团的性质、化学反应类型,充分利用题目提供的信息进行分析、判断是解题关键。
17. A 4 G CaC2+2H2O→Ca(OH)2+C2H2↑ +3HNO3(浓)+3H2O。
【分析】根据图示球棍模型可以看出,A为甲烷,B为乙烷,C为乙烯,D为乙炔,E为丙烷,F为苯,G为甲苯,则
(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最大即为含碳量最高的;
(2)含有碳碳双键或三键或苯环的烃能发生加成反应;
(3)根据烃的球棍模型结合等效氢思想确定同分异构体种类;
(4)实验室用碳化钙和水反应制取乙炔;
(5)甲苯和硝酸在浓硫酸作催化剂、加热条件下制取三硝基甲苯。
【详解】(1)常温下,分子中含有碳原子个数不大于4的烃为气态烃,根据其球棍模型判断,分子中含有碳氢原子个数比最小即为含氢量最高的,所以含氢量最大的是甲烷,即A,
故答案为:A;
(2)含有碳碳双键或三键或苯环的烃能发生加成反应,所以乙烯、乙炔、苯和甲苯都能发生加成反应,所以是4种,
故答案为:4;
(3)甲烷、乙烷、乙烯、乙炔、苯的一卤代物都只有1种,丙烷的一卤代物有2种,甲苯的有一卤代物有4种,
故答案为:G;
(4)实验室用碳化钙和水反应制取乙炔,反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O→Ca(OH)2+C2H2↑;
(5)在浓硫酸作催化剂、加热条件下甲苯和浓硝酸反应生成三硝基甲苯,反应方程式为:+3HNO3(浓)+3H2O。
18.a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐(或通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉)
【分析】淀粉和食盐的外观不同,食盐的主要成分为氯化钠,氯化钠在水溶液中可以电离出钠离子和氯离子,淀粉不能电离,据此分析解答。
【详解】食盐为白色颗粒状固体,淀粉是白色粉末状固体;淀粉没有味道,食盐有咸味;食盐的主要成分为氯化钠,氯化钠在水溶液中可以电离出钠离子和氯离子,可以用硝酸银检验氯离子确定是氯化钠溶液,淀粉不能电离;还可以通过检验钠离子的存在来确定氯化钠,因此区分厨房中的食盐和淀粉的方法有:a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐;d.通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉;故答案为:a.取样分别尝味道,咸的是食盐;b.分别取样配制成溶液,加硝酸银溶液,产生白色沉淀的是食盐;c.分别做焰色反应,焰色反应呈黄色的是食盐(或通过观察外观区分,颗粒状的是食盐,粉末状的是淀粉)。
19. CH2=CH2+Br2→CH2BrCH2Br 碳碳双键 羧基 加成反应 取代反应(酯化反应) 4 nCH2=CH-COOC2H5
【详解】(1)CH2=CH2是共价化合物,CH2=CH2的电子式为,CH2=CH2能和溴水发生加成反应,使溴的四氯化碳溶液褪色,该反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br。故答案为:;CH2=CH2+Br2→CH2BrCH2Br;
(2)化合物B的结构简式为CH2=CHCOOH,其中所含官能团的名称为碳碳双键、羧基。故答案为:碳碳双键;羧基;
(3)CH2=CH2和水发生加成反应生成乙醇,乙醇和丙烯酸发生酯化反应生成丙烯酸乙酯。故答案为:加成反应;取代反应(酯化反应);
(4)丁醇是C4H10O,也可以写成C4H9OH,可以看出丁烷(C4H10)的一元取代物,即用羟基取代丁烷上的氢,丁烷的结构简式为CH3CH2CH2CH3,(CH3)2CHCH3,所以丁烷的氢原子共有4种,所以丁醇属于醇类的同分异构体共有4种;故答案为:4;
(5)丙烯酸乙酯含有碳碳双键,一定条件下会发生聚合反应,该聚合反应的化学方程式为nCH2=CH-COOC2H5。故答案为:nCH2=CH-COOC2H5。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
