5.3 无机非金属材料课件(共26张PPT)2022-2023学年下学期高一化学人教版(2019)必修第二册
文档属性
| 名称 | 5.3 无机非金属材料课件(共26张PPT)2022-2023学年下学期高一化学人教版(2019)必修第二册 |  | |
| 格式 | pptx | ||
| 文件大小 | 12.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-20 14:59:28 | ||
图片预览







文档简介
(共26张PPT)
第五章 第三节 无机非金属材料
无机非金属材料
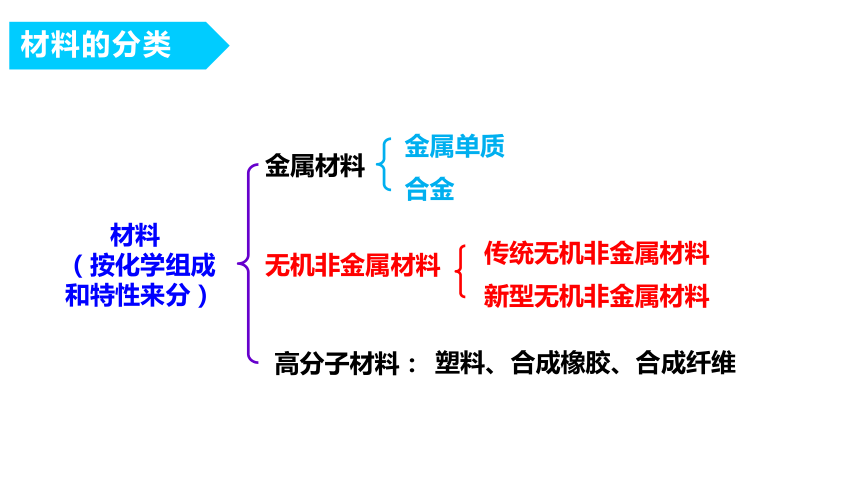
材料
(按化学组成和特性来分)
无机非金属材料
金属材料
高分子材料:
传统无机非金属材料
新型无机非金属材料
塑料、合成橡胶、合成纤维
金属单质
合金
材料的分类
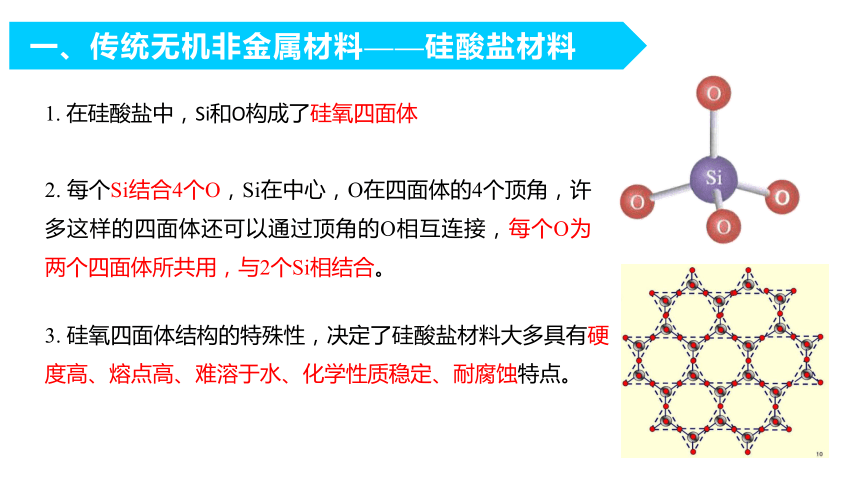
1. 在硅酸盐中,Si和O构成了硅氧四面体
2. 每个Si结合4个O,Si在中心,O在四面体的4个顶角,许多这样的四面体还可以通过顶角的O相互连接,每个O为两个四面体所共用,与2个Si相结合。
3. 硅氧四面体结构的特殊性,决定了硅酸盐材料大多具有硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀特点。
一、传统无机非金属材料——硅酸盐材料
传统无机非金属材料--硅酸盐材料
陶瓷
玻璃
水泥
陶瓷
水泥
玻璃
一、传统无机非金属材料
黏土 (主要成分为含水的铝硅酸盐)
高温烧结而成
抗氧化、抗酸碱腐蚀、耐高温、绝缘
生产建筑材料、绝缘材料、日用器皿、卫生洁具等
(人类最早使用的硅酸盐产品)
主要原料
反应原理
特 点
应 用
1. 陶 瓷
石英砂 (主要成分SiO2)、纯碱、石灰石
主要原料
反应原理
主要成分
高温下发生复杂的物理和化学变化制得
Na2SiO3
CaSiO3
SiO2
2. 玻璃
玻璃无固定的熔沸点。
SiO2+Na2CO3 Na2SiO3+CO2↑
SiO2+CaCO3 CaSiO3+CO2↑
应 用
生产建筑材料、光学仪器和各种器皿、还可制造玻璃纤维用于高强度符合材料等。
加入一些金属氧化物或盐可以得到彩色玻璃,常用于建筑和装饰
2. 玻璃
用含铅的原料制造的光学玻璃
黏土 、石灰石
主要原料
反应原理
特 点
应 用
水泥回转窑中煅烧,发生复杂的物理和化学变化
加适量石膏可调节水泥硬化速率
具有水硬性(与水掺和搅拌并静置后,很容易凝固变硬)
水泥、沙子和碎石等与水混合可以得到混凝土,大量用于建筑和水利工程
3. 水泥
新型无机非金属材料
高纯度的含硅元素的材料:
单晶硅、二氧化硅等,具有特殊的光学和电学性能。
含碳、氮等其他元素:
在航天、能源和医疗等领域广泛应用。
二、新型无机非金属材料
+14
2
8
4
Si
第三周期、第IV A族,处于金属和非金属的过渡位置
在地壳中含量居第二位
1. 硅
岩石
沙子(SiO2)
土壤
硅在自然界中只有化合态,主要以二氧化硅和硅酸盐的形式存在。
玛瑙( SiO2 )
水晶、石英( SiO2 )
硅酸盐矿石
颜色 状态 硬度 熔沸点 导电性
灰黑色、
有金属光泽
固体
大
高
介于导体和
绝缘体之间
硅的正四面体结构
物理性质
① 常温下能与氟气、氢氟酸、强碱等反应
Si+4HF===SiF4↑+2H2↑
② 加热时能与氧气、氯气、碳等反应
化学性质
应 用
①良好的半导体材料 ②计算机芯片
③太阳能电池
高纯Si
SiHCl3
粗硅
廉价的沙子
石英砂
主要成分:SiO2
1800-2000℃
98%纯度
H2
HCl
焦炭
1100℃
300℃
99.999%纯度
三氯硅烷
SiO2+2C ======= Si+2CO↑
1800~2000 ℃
Si+3HCl ==== SiHCl3+H2↑
300 ℃
SiHCl3+H2 ==== Si+3HCl
1100 ℃
工业制取
从沙滩到用户
沙子
石英砂
玛瑙
水晶
SiO2
2. 二氧化硅
硅藻土
石英、水晶、玛瑙、沙子
结晶形:
无定形:
统称硅石
硬度大、熔沸点高、常温下为固体、难溶于水、不导电、立体网状结构
物理性质
空间构型
硅氧四面体(空间网状)
① 具有酸性氧化物的通性(类比CO2)
a. 不溶于水,不与水反应(特殊)
SiO2 + CaO CaSiO3
高温
b. 与强碱反应
c. 与碱性氧化物反应
SiO2 + 2NaOH Na2SiO3 + H2O
化学性质
Si SiO2 H2SiO3 Na2SiO3
Na2SiO3可溶于水,其水溶液俗名水玻璃,有粘性
应用:①制硅酸;②黏合剂(矿物胶);③耐火阻燃剂;④防腐剂
③ 特性:与氢氟酸(HF)反应
SiO2 + 4HF SiF4↑ + 2H2O
SiO2+2C ==== Si+2CO↑
高温
② 氧化性
实验室用塑料瓶盛装氢氟酸,不用玻璃瓶
化学性质
(雕刻玻璃)
二氧化硅可用来生产光导纤维。
光导纤维
石英坩埚
玻璃仪器
精美瓷器
(通信)
用 途
光导纤维的通信容量大,抗干扰性能好,传输的信号不易衰减,能有效提高通讯效率高纯硅广泛应用于信息技术和新能源技术领域。
2. 二氧化硅
1. 实验室盛NaOH溶液的试剂瓶为什么用橡胶塞不用玻璃塞?
NaOH溶液能与玻璃中的SiO2反应生成 Na2SiO3,硅酸钠水溶液有粘性,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞而要用橡胶塞。
SiO2+2NaOH == Na2SiO3 + H2O
2.某同学根据SiO2既可与碱反应,也能与氢氟酸反应,推
断 SiO2为两性氧化物是否正确?
不正确。二氧化硅不属于两性氧化物,但属于酸性氧化物。
思考与讨论
硅 酸
聚合
硅酸凝胶
干燥脱水
硅酸干凝胶
“硅胶”
硅胶的用途:
食品、药品的干燥剂
催化剂的载体
高中化学唯一难溶性酸,酸性比碳酸还弱
硅酸H2SiO3
碳原子和硅原子通过共价键连接
结构
性能
砂纸和砂轮的磨料
SiC(金刚砂)陶瓷
高温抗氧化
硬度大
耐高温结构材料
耐高温半导体材料
3.新型陶瓷
碳纳米材料是近年来人们十分关注的一类新型无机非金属材料,主要包括富勒烯、碳纳米管、石墨烯等,在能源、信息、医药等领域有着广阔的应用前景。
4.碳纳米材料
由碳原子构成的一系列笼形分子的总称,其代表物为C60。
富勒烯
由石墨片层卷成的管状物,具有纳米尺度的直径。
具有相当高的强度和优良的电学性能,可用于生产复合材料、电池和传感器等。
碳纳米管
只有一个碳原子直径厚度的单层石墨
电阻率低、热导率高,具有很高的强度;应用于光电器件、超级电容器、电池和复合材料等方面。
石墨烯
第五章 第三节 无机非金属材料
无机非金属材料
材料
(按化学组成和特性来分)
无机非金属材料
金属材料
高分子材料:
传统无机非金属材料
新型无机非金属材料
塑料、合成橡胶、合成纤维
金属单质
合金
材料的分类
1. 在硅酸盐中,Si和O构成了硅氧四面体
2. 每个Si结合4个O,Si在中心,O在四面体的4个顶角,许多这样的四面体还可以通过顶角的O相互连接,每个O为两个四面体所共用,与2个Si相结合。
3. 硅氧四面体结构的特殊性,决定了硅酸盐材料大多具有硬度高、熔点高、难溶于水、化学性质稳定、耐腐蚀特点。
一、传统无机非金属材料——硅酸盐材料
传统无机非金属材料--硅酸盐材料
陶瓷
玻璃
水泥
陶瓷
水泥
玻璃
一、传统无机非金属材料
黏土 (主要成分为含水的铝硅酸盐)
高温烧结而成
抗氧化、抗酸碱腐蚀、耐高温、绝缘
生产建筑材料、绝缘材料、日用器皿、卫生洁具等
(人类最早使用的硅酸盐产品)
主要原料
反应原理
特 点
应 用
1. 陶 瓷
石英砂 (主要成分SiO2)、纯碱、石灰石
主要原料
反应原理
主要成分
高温下发生复杂的物理和化学变化制得
Na2SiO3
CaSiO3
SiO2
2. 玻璃
玻璃无固定的熔沸点。
SiO2+Na2CO3 Na2SiO3+CO2↑
SiO2+CaCO3 CaSiO3+CO2↑
应 用
生产建筑材料、光学仪器和各种器皿、还可制造玻璃纤维用于高强度符合材料等。
加入一些金属氧化物或盐可以得到彩色玻璃,常用于建筑和装饰
2. 玻璃
用含铅的原料制造的光学玻璃
黏土 、石灰石
主要原料
反应原理
特 点
应 用
水泥回转窑中煅烧,发生复杂的物理和化学变化
加适量石膏可调节水泥硬化速率
具有水硬性(与水掺和搅拌并静置后,很容易凝固变硬)
水泥、沙子和碎石等与水混合可以得到混凝土,大量用于建筑和水利工程
3. 水泥
新型无机非金属材料
高纯度的含硅元素的材料:
单晶硅、二氧化硅等,具有特殊的光学和电学性能。
含碳、氮等其他元素:
在航天、能源和医疗等领域广泛应用。
二、新型无机非金属材料
+14
2
8
4
Si
第三周期、第IV A族,处于金属和非金属的过渡位置
在地壳中含量居第二位
1. 硅
岩石
沙子(SiO2)
土壤
硅在自然界中只有化合态,主要以二氧化硅和硅酸盐的形式存在。
玛瑙( SiO2 )
水晶、石英( SiO2 )
硅酸盐矿石
颜色 状态 硬度 熔沸点 导电性
灰黑色、
有金属光泽
固体
大
高
介于导体和
绝缘体之间
硅的正四面体结构
物理性质
① 常温下能与氟气、氢氟酸、强碱等反应
Si+4HF===SiF4↑+2H2↑
② 加热时能与氧气、氯气、碳等反应
化学性质
应 用
①良好的半导体材料 ②计算机芯片
③太阳能电池
高纯Si
SiHCl3
粗硅
廉价的沙子
石英砂
主要成分:SiO2
1800-2000℃
98%纯度
H2
HCl
焦炭
1100℃
300℃
99.999%纯度
三氯硅烷
SiO2+2C ======= Si+2CO↑
1800~2000 ℃
Si+3HCl ==== SiHCl3+H2↑
300 ℃
SiHCl3+H2 ==== Si+3HCl
1100 ℃
工业制取
从沙滩到用户
沙子
石英砂
玛瑙
水晶
SiO2
2. 二氧化硅
硅藻土
石英、水晶、玛瑙、沙子
结晶形:
无定形:
统称硅石
硬度大、熔沸点高、常温下为固体、难溶于水、不导电、立体网状结构
物理性质
空间构型
硅氧四面体(空间网状)
① 具有酸性氧化物的通性(类比CO2)
a. 不溶于水,不与水反应(特殊)
SiO2 + CaO CaSiO3
高温
b. 与强碱反应
c. 与碱性氧化物反应
SiO2 + 2NaOH Na2SiO3 + H2O
化学性质
Si SiO2 H2SiO3 Na2SiO3
Na2SiO3可溶于水,其水溶液俗名水玻璃,有粘性
应用:①制硅酸;②黏合剂(矿物胶);③耐火阻燃剂;④防腐剂
③ 特性:与氢氟酸(HF)反应
SiO2 + 4HF SiF4↑ + 2H2O
SiO2+2C ==== Si+2CO↑
高温
② 氧化性
实验室用塑料瓶盛装氢氟酸,不用玻璃瓶
化学性质
(雕刻玻璃)
二氧化硅可用来生产光导纤维。
光导纤维
石英坩埚
玻璃仪器
精美瓷器
(通信)
用 途
光导纤维的通信容量大,抗干扰性能好,传输的信号不易衰减,能有效提高通讯效率高纯硅广泛应用于信息技术和新能源技术领域。
2. 二氧化硅
1. 实验室盛NaOH溶液的试剂瓶为什么用橡胶塞不用玻璃塞?
NaOH溶液能与玻璃中的SiO2反应生成 Na2SiO3,硅酸钠水溶液有粘性,使瓶塞部分粘结而无法打开。因此盛装NaOH溶液的试剂瓶不能用玻璃塞而要用橡胶塞。
SiO2+2NaOH == Na2SiO3 + H2O
2.某同学根据SiO2既可与碱反应,也能与氢氟酸反应,推
断 SiO2为两性氧化物是否正确?
不正确。二氧化硅不属于两性氧化物,但属于酸性氧化物。
思考与讨论
硅 酸
聚合
硅酸凝胶
干燥脱水
硅酸干凝胶
“硅胶”
硅胶的用途:
食品、药品的干燥剂
催化剂的载体
高中化学唯一难溶性酸,酸性比碳酸还弱
硅酸H2SiO3
碳原子和硅原子通过共价键连接
结构
性能
砂纸和砂轮的磨料
SiC(金刚砂)陶瓷
高温抗氧化
硬度大
耐高温结构材料
耐高温半导体材料
3.新型陶瓷
碳纳米材料是近年来人们十分关注的一类新型无机非金属材料,主要包括富勒烯、碳纳米管、石墨烯等,在能源、信息、医药等领域有着广阔的应用前景。
4.碳纳米材料
由碳原子构成的一系列笼形分子的总称,其代表物为C60。
富勒烯
由石墨片层卷成的管状物,具有纳米尺度的直径。
具有相当高的强度和优良的电学性能,可用于生产复合材料、电池和传感器等。
碳纳米管
只有一个碳原子直径厚度的单层石墨
电阻率低、热导率高,具有很高的强度;应用于光电器件、超级电容器、电池和复合材料等方面。
石墨烯
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
