鲁教版(五四制)九年级教学课件:2.3 溶液的酸碱性(共20张PPT)
文档属性
| 名称 | 鲁教版(五四制)九年级教学课件:2.3 溶液的酸碱性(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-21 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第三节 溶液的酸碱性
第二单元 常见的酸和碱
一、导入新课
在日常生活中,我们品尝到食醋、酸奶和某些水果都有酸味,这些溶液是显酸性的。那有没有显碱性的溶液呢?对于不能品尝的溶液,我们又该如何来确定它们是呈酸性还是碱性呢?
二、如何检验溶液的酸碱性
将二氧化碳通入紫色石蕊溶液中,溶液的颜色有什么变化?是什么物质使溶液改变了颜色?
观察下面的实验,可以看到什么现象?这说明酚酞溶液有什么性质?
【定义】能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。
【常见的酸碱指示剂】石蕊溶液、酚酞溶液。
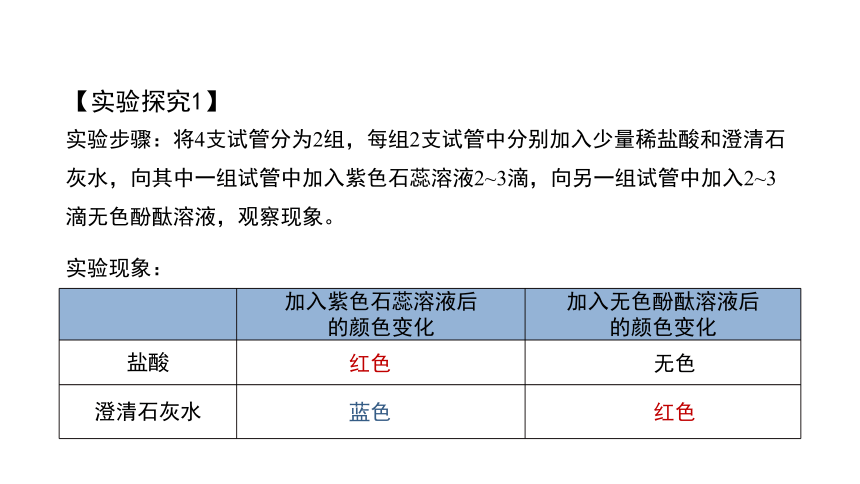
【实验探究1】
实验步骤:将4支试管分为2组,每组2支试管中分别加入少量稀盐酸和澄清石灰水,向其中一组试管中加入紫色石蕊溶液2~3滴,向另一组试管中加入2~3滴无色酚酞溶液,观察现象。
加入紫色石蕊溶液后 的颜色变化 加入无色酚酞溶液后
的颜色变化
盐酸
澄清石灰水
实验现象:
红色
红色
蓝色
无色
【结论】
酸能使紫色石蕊溶液变成红色,不能使无色酚酞溶液变色。
碱能使紫色石蕊溶液变成蓝色,使无色酚酞溶液变成红色。
【总结】
1.酸碱指示剂(指示剂):能跟酸或碱的溶液起作用而显示不同颜色的物质。
2.常见的酸碱指示剂:石蕊溶液、酚酞溶液。
3.变色规律:
指示剂溶液 酸性溶液中 碱性溶液中
石蕊溶液 红色 蓝色
酚酞溶液 无色 红色
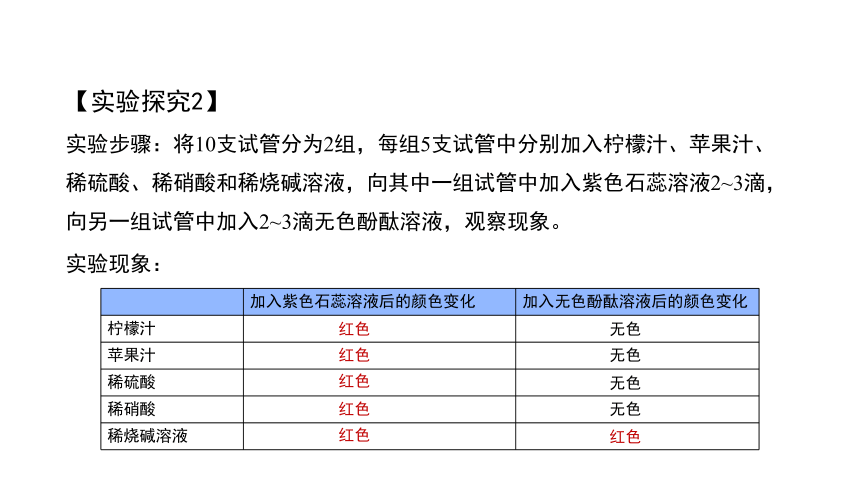
【实验探究2】
实验步骤:将10支试管分为2组,每组5支试管中分别加入柠檬汁、苹果汁、稀硫酸、稀硝酸和稀烧碱溶液,向其中一组试管中加入紫色石蕊溶液2~3滴,向另一组试管中加入2~3滴无色酚酞溶液,观察现象。
实验现象:
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
柠檬汁
苹果汁
稀硫酸
稀硝酸
稀烧碱溶液
红色
红色
红色
红色
红色
无色
无色
无色
无色
红色
【结论】
1.柠檬汁、苹果汁、稀硫酸、稀硝酸是酸性溶液,稀烧碱溶液是碱性溶液。
2.检验溶液为酸性的方法:取少量该溶液,滴入几滴紫色石蕊溶液,若溶液呈现红色,说明该溶液为酸性溶液。
3.检验溶液为碱性的方法:取少量该溶液,滴入几滴紫色石蕊溶液,若溶液呈现蓝色;或者滴入几滴无色酚酞溶液,若溶液呈现红色,说明该溶液为碱性溶液。
寻找科学家的足迹 (发现酸碱指示剂)
著名化学家罗伯特·波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,他惊奇地发现,紫色的花瓣上出现了红点点。波义耳对这一意外的发现,作出了各种假设,经过多次实验验证,探究普遍规律,终于获得了成功。
三、怎样判断溶液酸碱性的强弱
【总结】溶液的酸碱度用pH表示,范围为0~14。
①酸性溶液pH<7,pH越小,酸性越强。
②中性溶液pH=7。
③碱性溶液pH>7,pH越大,碱性越强。
【实验探究3】
实验步骤:用pH试纸测定稀盐酸、稀硫酸、食醋、石灰水、洗涤剂、橙汁、氢氧化钠溶液、氯化钠溶液的pH。按pH由小到大的顺序将被检验试样排序:
试样 稀盐酸 稀硫酸 食醋 石灰水 洗涤剂 橙汁 氢氧化钠溶液 氯化钠溶液
pH
实验结果:
1
1
3
11
7
4
11
7
【思考】各小组之间的数据一致吗?如果有一下情况会造成什么结果。
(1)测溶液酸碱度时,pH试纸要预先湿润会造成什么结果?
(2)测溶液酸碱度时,pH试纸能直接伸入待测液吗?
(3)玻璃棒不干净会怎么样?
(4)根据试纸所显示的颜色应立即对比,为什么?
易造成溶液浓度变稀。
不能,会污染药品。
会污染药品,且不准确。
时间长了易变色,导致数值不准确。
三、怎样判断溶液酸碱性的强弱
【提问】
(1)以上生活中样品哪些是酸性的,哪些是碱性的?酸碱性强弱程度如何?
(2)肥皂、洗衣粉可以直接用手使用,厕所清洁剂能否也能用手直接使用,为什么?
【总结】溶液的酸碱性的意义主要表现在以下方面:
(1)化工生产中许多反应必须控制在一定pH范围内。
(2)农作物适宜在pH为7或接近7的土壤中生长。
(3)测定雨水的pH,可以了解空气的污染情况。
(4)测定人体内或排出的液体的pH,可以了解人体的健康状况。
四、课堂练习
1.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )
A. 食盐 B. 味精 C. 食醋 D. 香油
C
2.能使石蕊溶液变红的溶液,如果滴入酚酞溶液,酚酞显( )
A. 紫色 B. 无色 C. 红色 D. 蓝色
B
五、课堂小结
1.酸碱指示剂(指示剂):能跟酸或碱的溶液起作用而显示不同颜色的物质。
2.常见的酸碱指示剂:石蕊溶液、酚酞溶液。
3.变色规律:
指示剂溶液 酸性溶液中 碱性溶液中
石蕊溶液 红色 蓝色
酚酞溶液 无色 红色
(一)如何检验溶液的酸碱性
(二)怎样判断溶液酸碱性的强弱
(三)物质的酸碱性对生命活动的意义
溶液的酸碱度用pH表示,范围为0~14。
①酸性溶液pH<7,pH越小,酸性越强。
②中性溶液pH=7。
③碱性溶液pH>7,pH越大,碱性越强。
再 见
第三节 溶液的酸碱性
第二单元 常见的酸和碱
一、导入新课
在日常生活中,我们品尝到食醋、酸奶和某些水果都有酸味,这些溶液是显酸性的。那有没有显碱性的溶液呢?对于不能品尝的溶液,我们又该如何来确定它们是呈酸性还是碱性呢?
二、如何检验溶液的酸碱性
将二氧化碳通入紫色石蕊溶液中,溶液的颜色有什么变化?是什么物质使溶液改变了颜色?
观察下面的实验,可以看到什么现象?这说明酚酞溶液有什么性质?
【定义】能跟酸或碱的溶液起作用而显示不同的颜色的物质叫做酸碱指示剂。
【常见的酸碱指示剂】石蕊溶液、酚酞溶液。
【实验探究1】
实验步骤:将4支试管分为2组,每组2支试管中分别加入少量稀盐酸和澄清石灰水,向其中一组试管中加入紫色石蕊溶液2~3滴,向另一组试管中加入2~3滴无色酚酞溶液,观察现象。
加入紫色石蕊溶液后 的颜色变化 加入无色酚酞溶液后
的颜色变化
盐酸
澄清石灰水
实验现象:
红色
红色
蓝色
无色
【结论】
酸能使紫色石蕊溶液变成红色,不能使无色酚酞溶液变色。
碱能使紫色石蕊溶液变成蓝色,使无色酚酞溶液变成红色。
【总结】
1.酸碱指示剂(指示剂):能跟酸或碱的溶液起作用而显示不同颜色的物质。
2.常见的酸碱指示剂:石蕊溶液、酚酞溶液。
3.变色规律:
指示剂溶液 酸性溶液中 碱性溶液中
石蕊溶液 红色 蓝色
酚酞溶液 无色 红色
【实验探究2】
实验步骤:将10支试管分为2组,每组5支试管中分别加入柠檬汁、苹果汁、稀硫酸、稀硝酸和稀烧碱溶液,向其中一组试管中加入紫色石蕊溶液2~3滴,向另一组试管中加入2~3滴无色酚酞溶液,观察现象。
实验现象:
加入紫色石蕊溶液后的颜色变化 加入无色酚酞溶液后的颜色变化
柠檬汁
苹果汁
稀硫酸
稀硝酸
稀烧碱溶液
红色
红色
红色
红色
红色
无色
无色
无色
无色
红色
【结论】
1.柠檬汁、苹果汁、稀硫酸、稀硝酸是酸性溶液,稀烧碱溶液是碱性溶液。
2.检验溶液为酸性的方法:取少量该溶液,滴入几滴紫色石蕊溶液,若溶液呈现红色,说明该溶液为酸性溶液。
3.检验溶液为碱性的方法:取少量该溶液,滴入几滴紫色石蕊溶液,若溶液呈现蓝色;或者滴入几滴无色酚酞溶液,若溶液呈现红色,说明该溶液为碱性溶液。
寻找科学家的足迹 (发现酸碱指示剂)
著名化学家罗伯特·波义耳在一次实验中,不小心将盐酸溅到紫罗兰花瓣上,过一会儿,他惊奇地发现,紫色的花瓣上出现了红点点。波义耳对这一意外的发现,作出了各种假设,经过多次实验验证,探究普遍规律,终于获得了成功。
三、怎样判断溶液酸碱性的强弱
【总结】溶液的酸碱度用pH表示,范围为0~14。
①酸性溶液pH<7,pH越小,酸性越强。
②中性溶液pH=7。
③碱性溶液pH>7,pH越大,碱性越强。
【实验探究3】
实验步骤:用pH试纸测定稀盐酸、稀硫酸、食醋、石灰水、洗涤剂、橙汁、氢氧化钠溶液、氯化钠溶液的pH。按pH由小到大的顺序将被检验试样排序:
试样 稀盐酸 稀硫酸 食醋 石灰水 洗涤剂 橙汁 氢氧化钠溶液 氯化钠溶液
pH
实验结果:
1
1
3
11
7
4
11
7
【思考】各小组之间的数据一致吗?如果有一下情况会造成什么结果。
(1)测溶液酸碱度时,pH试纸要预先湿润会造成什么结果?
(2)测溶液酸碱度时,pH试纸能直接伸入待测液吗?
(3)玻璃棒不干净会怎么样?
(4)根据试纸所显示的颜色应立即对比,为什么?
易造成溶液浓度变稀。
不能,会污染药品。
会污染药品,且不准确。
时间长了易变色,导致数值不准确。
三、怎样判断溶液酸碱性的强弱
【提问】
(1)以上生活中样品哪些是酸性的,哪些是碱性的?酸碱性强弱程度如何?
(2)肥皂、洗衣粉可以直接用手使用,厕所清洁剂能否也能用手直接使用,为什么?
【总结】溶液的酸碱性的意义主要表现在以下方面:
(1)化工生产中许多反应必须控制在一定pH范围内。
(2)农作物适宜在pH为7或接近7的土壤中生长。
(3)测定雨水的pH,可以了解空气的污染情况。
(4)测定人体内或排出的液体的pH,可以了解人体的健康状况。
四、课堂练习
1.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液变红色,遇碱性溶液变蓝色,在凉拌紫甘蓝丝时,观察到菜丝变成红色,可能是加入了下列哪种调味品( )
A. 食盐 B. 味精 C. 食醋 D. 香油
C
2.能使石蕊溶液变红的溶液,如果滴入酚酞溶液,酚酞显( )
A. 紫色 B. 无色 C. 红色 D. 蓝色
B
五、课堂小结
1.酸碱指示剂(指示剂):能跟酸或碱的溶液起作用而显示不同颜色的物质。
2.常见的酸碱指示剂:石蕊溶液、酚酞溶液。
3.变色规律:
指示剂溶液 酸性溶液中 碱性溶液中
石蕊溶液 红色 蓝色
酚酞溶液 无色 红色
(一)如何检验溶液的酸碱性
(二)怎样判断溶液酸碱性的强弱
(三)物质的酸碱性对生命活动的意义
溶液的酸碱度用pH表示,范围为0~14。
①酸性溶液pH<7,pH越小,酸性越强。
②中性溶液pH=7。
③碱性溶液pH>7,pH越大,碱性越强。
再 见
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
