鲁教版(五四制)九年级教学课件:2.4 酸碱中和反应(共14张PPT)
文档属性
| 名称 | 鲁教版(五四制)九年级教学课件:2.4 酸碱中和反应(共14张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-21 00:00:00 | ||
图片预览






文档简介
(共14张PPT)
第四节 酸碱中和反应
第二单元 常见的酸和碱
一、导入新课
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
二、中和反应
【提出问题】
用滴管向盛有5%的氢氧化钠溶液试管中滴加5%的稀盐酸,观察现象。你认为稀盐酸和氢氧化钠溶液发生反应了吗?如何去验证反应的发生呢?
【猜想假设】
盐酸和氢氧化钠________________________________。
【设计方案、进行实验】
利用桌面上提供的实验仪器及以下药品:①稀盐酸 ②氢氧化钠 ③酚酞
设计实验方案,选择的试剂及加入的顺序是:_________________________。
② ③ ①
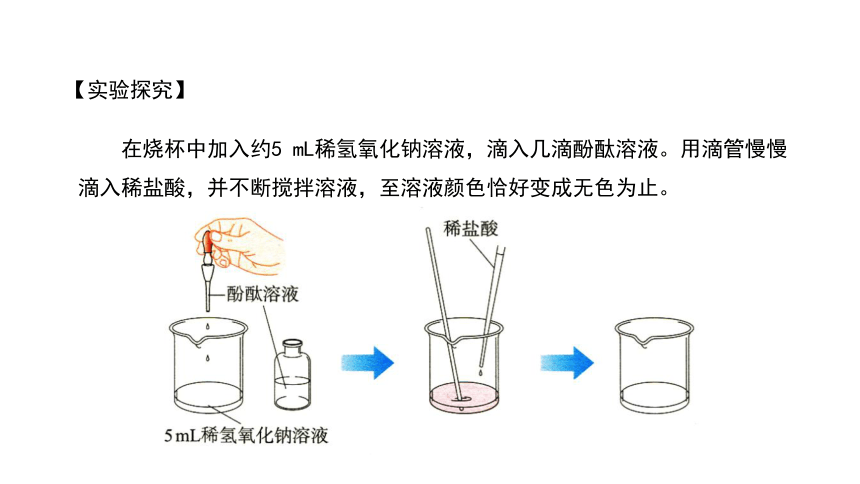
【实验探究】
在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
【提问】为什么酚酞溶液红色消失,就能说明氢氧化钠溶液与稀盐酸发生了反应呢?
酚酞溶液红色消失,说明试管中的物质已经没有氢氧化钠,因此氢氧化钠和稀盐酸一定发生了反应。
【提问】酚酞在实验中起什么作用?
防止稀盐酸滴加过量。
起指示作用。因为NaOH与HCl反应无明显的现象发生,根据酚酞溶液由红色变为无色来判断NaOH和HCl是否反应完全。
【提问】为什么在操作中必须逐滴滴入稀盐酸?
【总结】
(1)氢氧化钠溶液和稀盐酸反应生成氯化钠和水。
(2)化学方程式:
(3)酸和碱反应的实质:
NaOH + HCl NaCl + H2O
H+和OH-结合生成H2O。
【讨论】你可以写出其他酸和碱发生类似反应的化学方程式吗?
盐酸与氢氧化钾反应
盐酸与氢氧化钡反应
硫酸与氢氧化钠反应
硫酸与氢氧化钡反应
Ba(OH)2 + 2HCl BaCl2 + H2O
2NaOH + H2SO4 Na2SO4 + 2H2O
Ba(OH)2 + H2SO4 BaSO4 +2H2O
KOH + HCl KCl + H2O
【总结】
(1)反应特点:双交换
(2)生成物书写:价不变
(3)配平技巧:
OH- + H+ H2O (1:1:1)
【提问】阅读[活动天地7-5],思考在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH是怎样变化的?你能说出曲线上坐标为(18,7)的点所表示的意义吗?
(18,7)点代表恰好完全中和
当滴入盐酸量较少时,溶液中氢氧化钠有剩余,溶液呈碱性,pH>7;
当滴入盐酸恰好与溶液中氢氧化钠完全反应时,溶液呈中性,pH=7;
当滴入盐酸过量时,溶液中盐酸有剩余,溶液呈酸性,pH<7。
三、中和反应的应用
应用于医药卫生 改变土壤的酸碱性 处理工业废水 调节溶液的pH
三、中和反应的应用
【提问】
(1)为什么常用熟石灰改良酸性土壤,而不用氢氧化钠溶液?
(2)试书写硫酸厂处理废水的反应方程式?
(3)试书写胃药中和胃酸反应的化学方程式?
(4)你还能举出一些常见的酸碱中和反应的实例吗?
氢氧化钠的腐蚀性太强。
Ca(OH)2 + H2SO4 CaSO4 +2H2O
Al(OH)3 + 3HCl AlCl3 + 3H2O
被虫蚁蛰咬后涂抹碱性药品缓解疼痛。
四、课堂练习
1. 厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是( )
A. 氢气 B. 二氧化硫 C. 氧气 D. 二氧化碳
2. 下列有关物质用途的叙述中,正确的是( )
A. 用氢氧化钠溶液中和胃中过多盐酸
B. 用稀硫酸清除钢铁表面的铁锈
C. 室内放一大盆水就可以防止煤气中毒
D. 用甲醛的水溶液浸泡豆制品和海产品以保鲜
B
D
3. 中和反应在工农业生产和日常生活中有广泛的用途。下列应用一定与中和反应原理无关的是( )
A. 石灰浆抹的墙壁变得坚硬
B. 服用含Al(OH)3的药物治疗胃酸过多
C. 施用熟石灰改良酸性土壤
D. 用NaOH溶液洗涤石油产品中残余硫酸
A
五、课堂小结
(一)中和反应
1.中和反应的定义:酸和碱作用生成盐和水的反应。
2.中和反应的实质:H+和OH-能结合生成H2O。
(二)中和反应在实际中的应用
1.用于医药卫生
2.改变土壤的酸碱性
3.处理工业废水
4.调节溶液的酸碱性
再 见
第四节 酸碱中和反应
第二单元 常见的酸和碱
一、导入新课
腌制过程中生成了碱
吃起来有涩味
蘸少量的食醋
涩味消失
二、中和反应
【提出问题】
用滴管向盛有5%的氢氧化钠溶液试管中滴加5%的稀盐酸,观察现象。你认为稀盐酸和氢氧化钠溶液发生反应了吗?如何去验证反应的发生呢?
【猜想假设】
盐酸和氢氧化钠________________________________。
【设计方案、进行实验】
利用桌面上提供的实验仪器及以下药品:①稀盐酸 ②氢氧化钠 ③酚酞
设计实验方案,选择的试剂及加入的顺序是:_________________________。
② ③ ①
【实验探究】
在烧杯中加入约5 mL稀氢氧化钠溶液,滴入几滴酚酞溶液。用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
【提问】为什么酚酞溶液红色消失,就能说明氢氧化钠溶液与稀盐酸发生了反应呢?
酚酞溶液红色消失,说明试管中的物质已经没有氢氧化钠,因此氢氧化钠和稀盐酸一定发生了反应。
【提问】酚酞在实验中起什么作用?
防止稀盐酸滴加过量。
起指示作用。因为NaOH与HCl反应无明显的现象发生,根据酚酞溶液由红色变为无色来判断NaOH和HCl是否反应完全。
【提问】为什么在操作中必须逐滴滴入稀盐酸?
【总结】
(1)氢氧化钠溶液和稀盐酸反应生成氯化钠和水。
(2)化学方程式:
(3)酸和碱反应的实质:
NaOH + HCl NaCl + H2O
H+和OH-结合生成H2O。
【讨论】你可以写出其他酸和碱发生类似反应的化学方程式吗?
盐酸与氢氧化钾反应
盐酸与氢氧化钡反应
硫酸与氢氧化钠反应
硫酸与氢氧化钡反应
Ba(OH)2 + 2HCl BaCl2 + H2O
2NaOH + H2SO4 Na2SO4 + 2H2O
Ba(OH)2 + H2SO4 BaSO4 +2H2O
KOH + HCl KCl + H2O
【总结】
(1)反应特点:双交换
(2)生成物书写:价不变
(3)配平技巧:
OH- + H+ H2O (1:1:1)
【提问】阅读[活动天地7-5],思考在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH是怎样变化的?你能说出曲线上坐标为(18,7)的点所表示的意义吗?
(18,7)点代表恰好完全中和
当滴入盐酸量较少时,溶液中氢氧化钠有剩余,溶液呈碱性,pH>7;
当滴入盐酸恰好与溶液中氢氧化钠完全反应时,溶液呈中性,pH=7;
当滴入盐酸过量时,溶液中盐酸有剩余,溶液呈酸性,pH<7。
三、中和反应的应用
应用于医药卫生 改变土壤的酸碱性 处理工业废水 调节溶液的pH
三、中和反应的应用
【提问】
(1)为什么常用熟石灰改良酸性土壤,而不用氢氧化钠溶液?
(2)试书写硫酸厂处理废水的反应方程式?
(3)试书写胃药中和胃酸反应的化学方程式?
(4)你还能举出一些常见的酸碱中和反应的实例吗?
氢氧化钠的腐蚀性太强。
Ca(OH)2 + H2SO4 CaSO4 +2H2O
Al(OH)3 + 3HCl AlCl3 + 3H2O
被虫蚁蛰咬后涂抹碱性药品缓解疼痛。
四、课堂练习
1. 厕所用清洁剂中含有盐酸,如果不慎洒到大理石地面上,会发出嘶嘶声,并有气体产生。这种气体是( )
A. 氢气 B. 二氧化硫 C. 氧气 D. 二氧化碳
2. 下列有关物质用途的叙述中,正确的是( )
A. 用氢氧化钠溶液中和胃中过多盐酸
B. 用稀硫酸清除钢铁表面的铁锈
C. 室内放一大盆水就可以防止煤气中毒
D. 用甲醛的水溶液浸泡豆制品和海产品以保鲜
B
D
3. 中和反应在工农业生产和日常生活中有广泛的用途。下列应用一定与中和反应原理无关的是( )
A. 石灰浆抹的墙壁变得坚硬
B. 服用含Al(OH)3的药物治疗胃酸过多
C. 施用熟石灰改良酸性土壤
D. 用NaOH溶液洗涤石油产品中残余硫酸
A
五、课堂小结
(一)中和反应
1.中和反应的定义:酸和碱作用生成盐和水的反应。
2.中和反应的实质:H+和OH-能结合生成H2O。
(二)中和反应在实际中的应用
1.用于医药卫生
2.改变土壤的酸碱性
3.处理工业废水
4.调节溶液的酸碱性
再 见
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
