鲁教版化学九下导学案:7.1 酸及其性质 第二课时
文档属性
| 名称 | 鲁教版化学九下导学案:7.1 酸及其性质 第二课时 |
|
|
| 格式 | doc | ||
| 文件大小 | 61.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-21 00:00:00 | ||
图片预览


文档简介
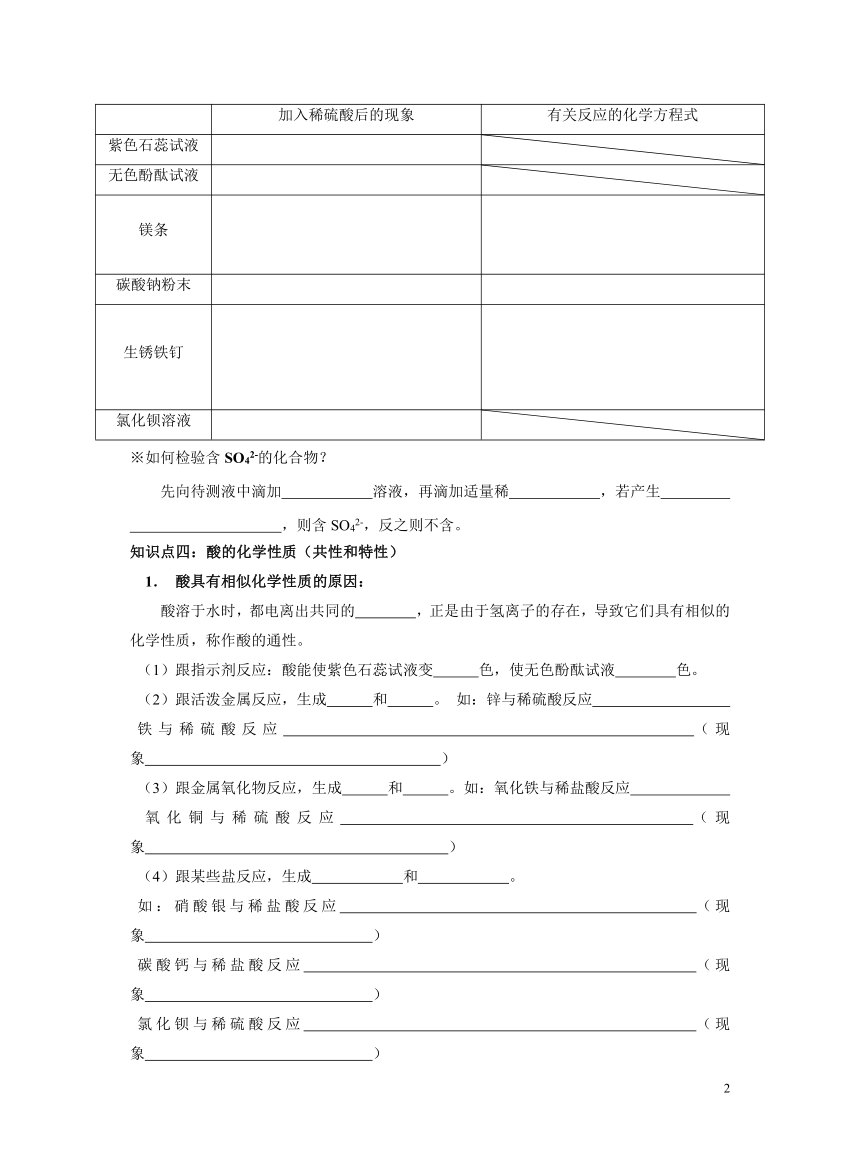
7.1 酸及其性质 第二课时
【学习目标】
1.掌握酸的化学性质。
2.会描述酸与其它物质反应的实验现象,会书写反应的化学方程式。
3.知道酸具有相似的化学性质的原因。
【学习过程】
知识点一:盐酸的化学性质
加入稀盐酸后的现象 有关反应的化学方程式
紫色石蕊试液
无色酚酞试液
镁条
碳酸钠粉末
生锈铁钉
硝酸银溶液
氯化钡溶液 无现象
※如何检验含Cl-的化合物?
先向待测液中滴加 溶液,再滴加适量 ,若产生
,则含有Cl-,反之则不含。
说明:像MgCl2、NaCl、FeCl3、FeCl2等均是由 和 构成的化合物,化学上把这类化合物称为盐。
知识点二:复分解反应
1. 定义: 。
2.字母表示: 。
知识点三:硫酸的化学性质
加入稀硫酸后的现象 有关反应的化学方程式
紫色石蕊试液
无色酚酞试液
镁条
碳酸钠粉末
生锈铁钉
氯化钡溶液
※如何检验含SO42-的化合物?
先向待测液中滴加 溶液,再滴加适量稀 ,若产生
,则含SO42-,反之则不含。
知识点四:酸的化学性质(共性和特性)
1. 酸具有相似化学性质的原因:
酸溶于水时,都电离出共同的 ,正是由于氢离子的存在,导致它们具有相似的化学性质,称作酸的通性。
(1)跟指示剂反应:酸能使紫色石蕊试液变 色,使无色酚酞试液 色。
(2)跟活泼金属反应,生成 和 。 如:锌与稀硫酸反应
铁与稀硫酸反应 (现象 )
(3)跟金属氧化物反应,生成 和 。如:氧化铁与稀盐酸反应
氧化铜与稀硫酸反应 (现象 )
(4)跟某些盐反应,生成 和 。
如:硝酸银与稀盐酸反应 (现象 )
碳酸钙与稀盐酸反应 (现象 )
氯化钡与稀硫酸反应 (现象 )
(5)跟碱反应,生成 和 。如:氢氧化钠与稀盐酸反应
氢氧化钙与稀盐酸反应
2. 性质存在差异的原因:
由于不同的酸溶于水时电离出的 不同,其性质也存在差异。
例如:硫酸能与氯化钡反应,生成白色的硫酸钡沉淀,而盐酸则不能。
知识点五:酸的用途 (了解)
【随堂练习】
1.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.在水溶液中都能解离出酸根离子 B.在水溶液中都能解离出氢离子
C.组成中都含有氢元素 D.都能与指示剂作用
2.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质,下列有关叙述正确的是( )
A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加无色酚酞溶液,都变红
3.物质X可发生下列所示的两个反应,则X可能是( )
①X+金属→盐+H2 ②X+金属氧化物→盐+H2O
A.HCl B.CaO C.CO D.Na2CO3
4.自来水生产中常通适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。为辨别真伪,可用下列一种化学试剂来鉴别,该试剂是( )
A.酚酞试液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
5.柠檬酸(C6H8O7)是一种较强的有机酸,主要用于香料或作为饮料的酸化剂,化学性质与稀盐酸相似,下列物质不能与柠檬酸反应的是( )
A.Mg B.CO2 C.Fe2O3 D.Na2CO3
6.化学无处不在,如图是物质间发生反应时的颜色变化,其中X是( )
A.稀盐酸 B.稀硫酸
C.硫酸钠溶液 D.氯化钠溶液
7.稀盐酸、稀硫酸都有一些重要的化学性质,下列有关叙述正确的是( )
A.稀盐酸能使紫色石蕊试液变红,稀硫酸不能
B.稀盐酸和稀硫酸都可用于除铁锈
C.稀盐酸与铁反应的化学方程式为2Fe+6HCl=2FeCl3+3H2↑
D.在稀盐酸中滴加氯化钡溶液,会有白色沉淀生成
8.下列区分稀硫酸与稀盐酸的方法中,正确的是( )
A. 分别加入碳酸钠 B.分别加入锌粒 C.分别加入氯化钡溶液 D.分别加入酚酞试液
9.下列化学方程式中属于复分解反应的是( )
A.C+O2CO2 B.2H2O2H2↑+O2↑
C.3CO+Fe2O32Fe+3CO2 D.HCl+AgNO3===AgCl↓+HNO3
10.铁锈的主要成分是 ,为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的盐酸中,他首先看到锈迹溶解,溶液呈 色。这是因为(用化学方程式表示) ;不一会儿,又看到溶液中有 的现象,这是因为(用化学方程式表示) 。
11.硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应: ;②与碳酸钠溶液反应: ;
③与氯化钡溶液反应: ;
上述反应中,属于酸的共同性质的是 (填编号)。
(3)盐酸的下列用途中,不能用硫酸代替的是 (填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
12.化学使世界变得绚丽多彩,如图是物质之间发生化学反应的颜色变化。
(1)请你在编号②、③处各填入一种物质,②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质。请你写出编号①稀硫酸的化学性质 。
(3)若编号④的物质是盐。请你写出符合编号④的一个化学方程式: ,反应类型是 。
答案
1.B 2.B 3.A 4.D 5.B 6.B 7.B 8.C 9.D
10. Fe2O3,黄,Fe2O3+6HCl═2FeCl3+3H2O,气泡冒出, Fe+2HCl═FeCl2+H2↑
11.(1)吸水性;(2)①Fe+H2SO4=FeSO4+H2↑;②Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
③H2SO4+BaCl2═BaSO4↓+2HCl;①②;(3)②③
12.(1)铁(或Fe);氧化铜(或CuO);(2)硫酸可使紫色石蕊试液变红;
(3)BaCl2+H2SO4=BaSO4↓+2HCl(合理均可);复分解反应
1
【学习目标】
1.掌握酸的化学性质。
2.会描述酸与其它物质反应的实验现象,会书写反应的化学方程式。
3.知道酸具有相似的化学性质的原因。
【学习过程】
知识点一:盐酸的化学性质
加入稀盐酸后的现象 有关反应的化学方程式
紫色石蕊试液
无色酚酞试液
镁条
碳酸钠粉末
生锈铁钉
硝酸银溶液
氯化钡溶液 无现象
※如何检验含Cl-的化合物?
先向待测液中滴加 溶液,再滴加适量 ,若产生
,则含有Cl-,反之则不含。
说明:像MgCl2、NaCl、FeCl3、FeCl2等均是由 和 构成的化合物,化学上把这类化合物称为盐。
知识点二:复分解反应
1. 定义: 。
2.字母表示: 。
知识点三:硫酸的化学性质
加入稀硫酸后的现象 有关反应的化学方程式
紫色石蕊试液
无色酚酞试液
镁条
碳酸钠粉末
生锈铁钉
氯化钡溶液
※如何检验含SO42-的化合物?
先向待测液中滴加 溶液,再滴加适量稀 ,若产生
,则含SO42-,反之则不含。
知识点四:酸的化学性质(共性和特性)
1. 酸具有相似化学性质的原因:
酸溶于水时,都电离出共同的 ,正是由于氢离子的存在,导致它们具有相似的化学性质,称作酸的通性。
(1)跟指示剂反应:酸能使紫色石蕊试液变 色,使无色酚酞试液 色。
(2)跟活泼金属反应,生成 和 。 如:锌与稀硫酸反应
铁与稀硫酸反应 (现象 )
(3)跟金属氧化物反应,生成 和 。如:氧化铁与稀盐酸反应
氧化铜与稀硫酸反应 (现象 )
(4)跟某些盐反应,生成 和 。
如:硝酸银与稀盐酸反应 (现象 )
碳酸钙与稀盐酸反应 (现象 )
氯化钡与稀硫酸反应 (现象 )
(5)跟碱反应,生成 和 。如:氢氧化钠与稀盐酸反应
氢氧化钙与稀盐酸反应
2. 性质存在差异的原因:
由于不同的酸溶于水时电离出的 不同,其性质也存在差异。
例如:硫酸能与氯化钡反应,生成白色的硫酸钡沉淀,而盐酸则不能。
知识点五:酸的用途 (了解)
【随堂练习】
1.稀盐酸和稀硫酸具有相似的化学性质,其本质原因是( )
A.在水溶液中都能解离出酸根离子 B.在水溶液中都能解离出氢离子
C.组成中都含有氢元素 D.都能与指示剂作用
2.盐酸、稀硫酸在水溶液中都能产生H+,故有许多共同的性质,下列有关叙述正确的是( )
A.打开盛有浓盐酸和浓硫酸的试剂瓶瓶塞,在瓶口都有白雾
B.稀盐酸和稀硫酸都可用于除铁锈
C.浓盐酸、浓硫酸都可用来干燥氧气
D.在稀盐酸、稀硫酸中滴加无色酚酞溶液,都变红
3.物质X可发生下列所示的两个反应,则X可能是( )
①X+金属→盐+H2 ②X+金属氧化物→盐+H2O
A.HCl B.CaO C.CO D.Na2CO3
4.自来水生产中常通适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售。为辨别真伪,可用下列一种化学试剂来鉴别,该试剂是( )
A.酚酞试液 B.氯化钡溶液 C.氢氧化钠溶液 D.硝酸银溶液
5.柠檬酸(C6H8O7)是一种较强的有机酸,主要用于香料或作为饮料的酸化剂,化学性质与稀盐酸相似,下列物质不能与柠檬酸反应的是( )
A.Mg B.CO2 C.Fe2O3 D.Na2CO3
6.化学无处不在,如图是物质间发生反应时的颜色变化,其中X是( )
A.稀盐酸 B.稀硫酸
C.硫酸钠溶液 D.氯化钠溶液
7.稀盐酸、稀硫酸都有一些重要的化学性质,下列有关叙述正确的是( )
A.稀盐酸能使紫色石蕊试液变红,稀硫酸不能
B.稀盐酸和稀硫酸都可用于除铁锈
C.稀盐酸与铁反应的化学方程式为2Fe+6HCl=2FeCl3+3H2↑
D.在稀盐酸中滴加氯化钡溶液,会有白色沉淀生成
8.下列区分稀硫酸与稀盐酸的方法中,正确的是( )
A. 分别加入碳酸钠 B.分别加入锌粒 C.分别加入氯化钡溶液 D.分别加入酚酞试液
9.下列化学方程式中属于复分解反应的是( )
A.C+O2CO2 B.2H2O2H2↑+O2↑
C.3CO+Fe2O32Fe+3CO2 D.HCl+AgNO3===AgCl↓+HNO3
10.铁锈的主要成分是 ,为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的盐酸中,他首先看到锈迹溶解,溶液呈 色。这是因为(用化学方程式表示) ;不一会儿,又看到溶液中有 的现象,这是因为(用化学方程式表示) 。
11.硫酸、盐酸是重要的化工原料。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)写出稀硫酸与下列物质反应的化学方程式:
①与铁粉反应: ;②与碳酸钠溶液反应: ;
③与氯化钡溶液反应: ;
上述反应中,属于酸的共同性质的是 (填编号)。
(3)盐酸的下列用途中,不能用硫酸代替的是 (填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
12.化学使世界变得绚丽多彩,如图是物质之间发生化学反应的颜色变化。
(1)请你在编号②、③处各填入一种物质,②是 ;③是 ;
(2)根据上图可以总结出稀硫酸的五个化学性质。请你写出编号①稀硫酸的化学性质 。
(3)若编号④的物质是盐。请你写出符合编号④的一个化学方程式: ,反应类型是 。
答案
1.B 2.B 3.A 4.D 5.B 6.B 7.B 8.C 9.D
10. Fe2O3,黄,Fe2O3+6HCl═2FeCl3+3H2O,气泡冒出, Fe+2HCl═FeCl2+H2↑
11.(1)吸水性;(2)①Fe+H2SO4=FeSO4+H2↑;②Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
③H2SO4+BaCl2═BaSO4↓+2HCl;①②;(3)②③
12.(1)铁(或Fe);氧化铜(或CuO);(2)硫酸可使紫色石蕊试液变红;
(3)BaCl2+H2SO4=BaSO4↓+2HCl(合理均可);复分解反应
1
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
