2-2-1电解质的电离(共18张PPT)2022-2023学年高一上学期鲁科版(2019)必修第一册
文档属性
| 名称 | 2-2-1电解质的电离(共18张PPT)2022-2023学年高一上学期鲁科版(2019)必修第一册 |
|
|
| 格式 | pptx | ||
| 文件大小 | 9.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-22 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
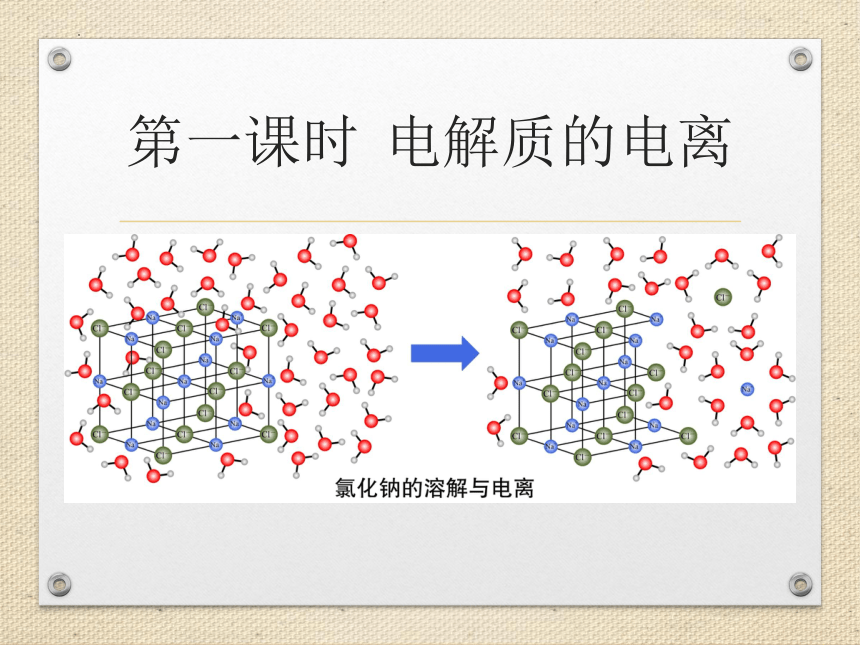
第一课时 电解质的电离
联想 质疑
为什么固体泡腾片不产生气体,放入水中就会立刻放出二氧化碳气体?
泡腾片放入水中发生了什么变化?
干燥的泡腾片和水中的泡腾片
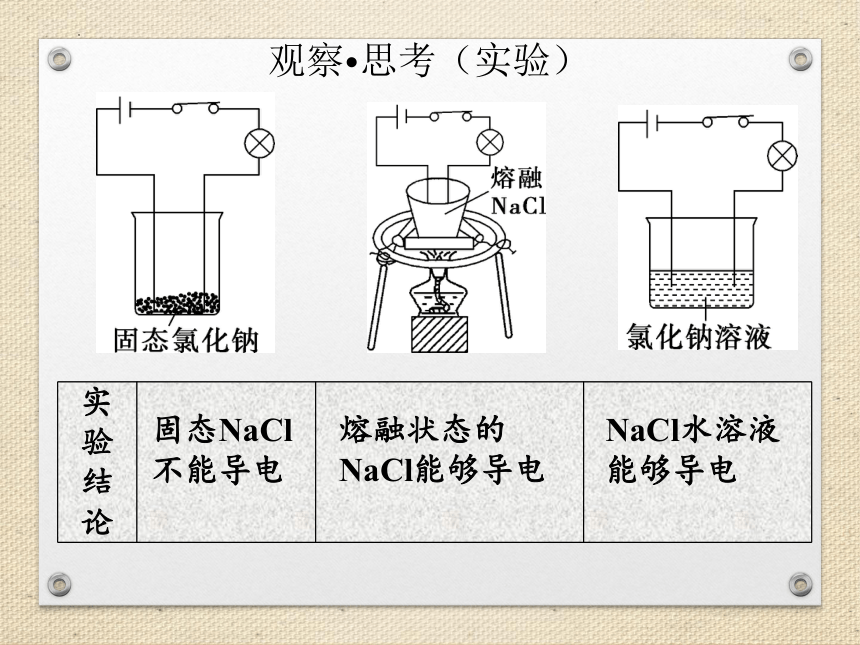
观察 思考(实验)
实验 结论
固态NaCl
不能导电
熔融状态的
NaCl能够导电
NaCl水溶液
能够导电
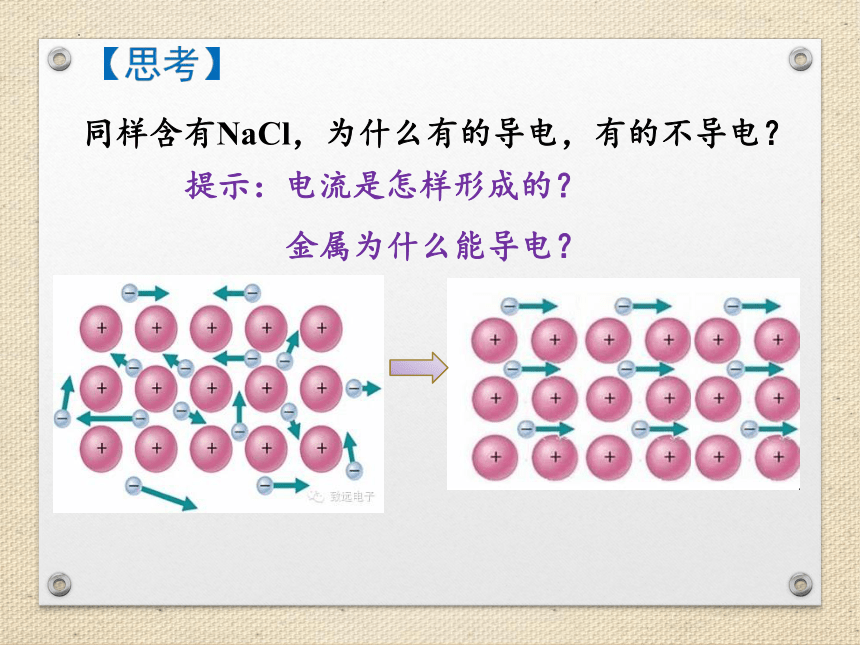
同样含有NaCl,为什么有的导电,有的不导电?
【思考】
提示:电流是怎样形成的?
金属为什么能导电?
推测:熔融状态的NaCl和NaCl水溶液中含有能自由移动的带电粒子。这些自由移动的能够导电的微粒是什么?如何产生的?
结论1:这些粒子是Na+和Cl-。
结论2:氯化钠溶于水或受热熔化时解离成能够自由移动的离子的过程称为电离。
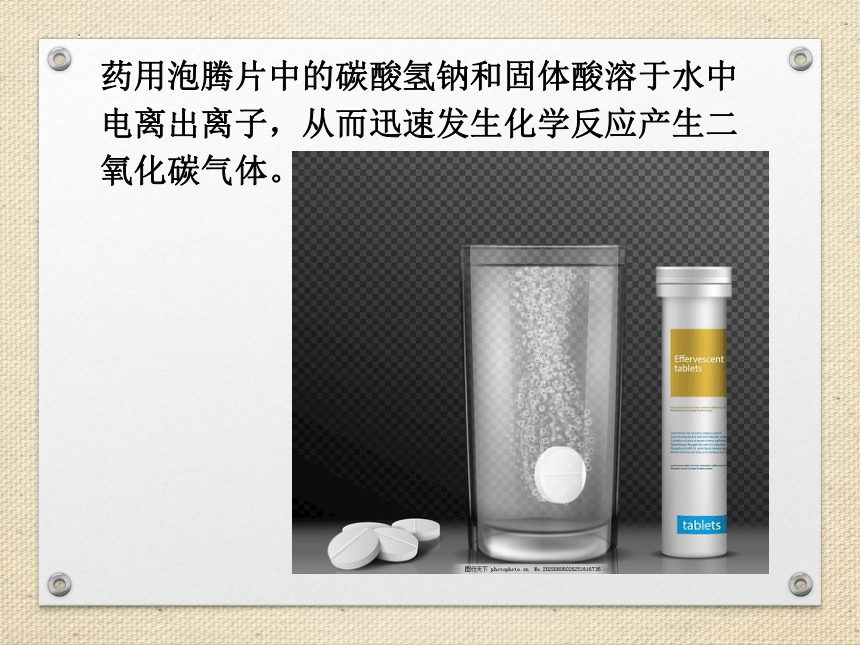
药用泡腾片中的碳酸氢钠和固体酸溶于水中电离出离子,从而迅速发生化学反应产生二氧化碳气体。
不同溶液的导电能力比较(实验视频)
Cl-
H+
HCl的电离微观示意图
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COO-
液 面
CH3COO-
CH3COO-
CH3COO-
H+
H+
H+
H+
H+
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COO-
醋酸的电离微观示意图
一、电解质和非电解质
化
合
物
电
解
质
非电解质:非金属氧化物、NH3、大部分
有机化合物
强电
解质
弱电
解质
活泼金属氧化物
强酸
强碱
大部分盐
弱酸
弱碱
少部分盐:(CH3COO)2Pb、HgCl2
H2O
1、以下属于强电解质的是___________________
属于弱电解质的是__________________________
属于非电解质的是__________________________
既不是电解质,也不是非电解质的____________
液氨 NH3 氨水 NH3·H2O 盐酸 HI 醋酸
SO2 Na2O 澄清石灰水 Ca(OH)2 CH4
Fe 液氯 NaHCO3 蔗糖 BaSO4
既不是电解质,也不是非电解质的(混合物和单质)
氨水、盐酸 、澄清石灰水、 Fe 、液氯
属于电解质的是
NH3·H2O、 HI、醋酸、
Na2O、 Ca(OH)2 、
NaHCO3 、 BaSO4
HI、 Ca(OH)2 、NaHCO3 、 BaSO4 、 Na2O
NH3·H2O、 醋酸
强
弱
属于非电解质的是
液氨、NH3 、 SO2 、 CH4、蔗糖
2、以下可以导电的是:
3、下列物质中,导电性能最差的是( )
A. 1mol/L盐酸
B. 1mol/L醋酸
C. 熔融氢氧化钠
D. 固体氯化钾
固体NaCl 熔融Al2O3 NaOH溶液 石墨
Cu 液态HCl 盐酸 酒精 熔融KNO3
D
(1)电解质不一定导电,非电解质一定不导电。
(2)导电的物质不一定是电解质,不导电的物质
不一定是非电解质。
4、判断题
(3)某单质固体能导电,其单质一定是金属。
(4)某化合物的水溶液能导电,该化合物一定是电
解质。
(5)某化合物的熔融状态能导电,该化合物中一定
是电解质。
(6)强电解质溶液一定比弱电解质溶液的导电能力
强。
电解质溶液中离子浓度的测定方法
所测离子类别 测定方法
H+或OH- 酸碱指示剂或pH计
有色离子 比色计
5、已知:CO2+Ca(OH)2===CaCO3↓+H2O,
CaCO3+CO2+H2O===Ca(HCO3)2,且Ca(HCO3)2
易溶于水。
(1)通入CO2前,灯泡_______(填“亮”或“不亮”)。
(2)开始通入CO2时,灯泡的亮度______________。
(3)继续通入过量的CO2,灯泡的亮度___________。
亮
先变暗后熄灭
又逐渐变亮
(4)下列四个图中,能准确反映出溶液的导电能力和通入CO2气体量的关系的是________(x轴表示CO2通入的量,y轴表示导电能力)。
D
第一课时 电解质的电离
联想 质疑
为什么固体泡腾片不产生气体,放入水中就会立刻放出二氧化碳气体?
泡腾片放入水中发生了什么变化?
干燥的泡腾片和水中的泡腾片
观察 思考(实验)
实验 结论
固态NaCl
不能导电
熔融状态的
NaCl能够导电
NaCl水溶液
能够导电
同样含有NaCl,为什么有的导电,有的不导电?
【思考】
提示:电流是怎样形成的?
金属为什么能导电?
推测:熔融状态的NaCl和NaCl水溶液中含有能自由移动的带电粒子。这些自由移动的能够导电的微粒是什么?如何产生的?
结论1:这些粒子是Na+和Cl-。
结论2:氯化钠溶于水或受热熔化时解离成能够自由移动的离子的过程称为电离。
药用泡腾片中的碳酸氢钠和固体酸溶于水中电离出离子,从而迅速发生化学反应产生二氧化碳气体。
不同溶液的导电能力比较(实验视频)
Cl-
H+
HCl的电离微观示意图
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
Cl-
H+
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COO-
液 面
CH3COO-
CH3COO-
CH3COO-
H+
H+
H+
H+
H+
CH3COOH
CH3COOH
CH3COOH
CH3COOH
CH3COO-
醋酸的电离微观示意图
一、电解质和非电解质
化
合
物
电
解
质
非电解质:非金属氧化物、NH3、大部分
有机化合物
强电
解质
弱电
解质
活泼金属氧化物
强酸
强碱
大部分盐
弱酸
弱碱
少部分盐:(CH3COO)2Pb、HgCl2
H2O
1、以下属于强电解质的是___________________
属于弱电解质的是__________________________
属于非电解质的是__________________________
既不是电解质,也不是非电解质的____________
液氨 NH3 氨水 NH3·H2O 盐酸 HI 醋酸
SO2 Na2O 澄清石灰水 Ca(OH)2 CH4
Fe 液氯 NaHCO3 蔗糖 BaSO4
既不是电解质,也不是非电解质的(混合物和单质)
氨水、盐酸 、澄清石灰水、 Fe 、液氯
属于电解质的是
NH3·H2O、 HI、醋酸、
Na2O、 Ca(OH)2 、
NaHCO3 、 BaSO4
HI、 Ca(OH)2 、NaHCO3 、 BaSO4 、 Na2O
NH3·H2O、 醋酸
强
弱
属于非电解质的是
液氨、NH3 、 SO2 、 CH4、蔗糖
2、以下可以导电的是:
3、下列物质中,导电性能最差的是( )
A. 1mol/L盐酸
B. 1mol/L醋酸
C. 熔融氢氧化钠
D. 固体氯化钾
固体NaCl 熔融Al2O3 NaOH溶液 石墨
Cu 液态HCl 盐酸 酒精 熔融KNO3
D
(1)电解质不一定导电,非电解质一定不导电。
(2)导电的物质不一定是电解质,不导电的物质
不一定是非电解质。
4、判断题
(3)某单质固体能导电,其单质一定是金属。
(4)某化合物的水溶液能导电,该化合物一定是电
解质。
(5)某化合物的熔融状态能导电,该化合物中一定
是电解质。
(6)强电解质溶液一定比弱电解质溶液的导电能力
强。
电解质溶液中离子浓度的测定方法
所测离子类别 测定方法
H+或OH- 酸碱指示剂或pH计
有色离子 比色计
5、已知:CO2+Ca(OH)2===CaCO3↓+H2O,
CaCO3+CO2+H2O===Ca(HCO3)2,且Ca(HCO3)2
易溶于水。
(1)通入CO2前,灯泡_______(填“亮”或“不亮”)。
(2)开始通入CO2时,灯泡的亮度______________。
(3)继续通入过量的CO2,灯泡的亮度___________。
亮
先变暗后熄灭
又逐渐变亮
(4)下列四个图中,能准确反映出溶液的导电能力和通入CO2气体量的关系的是________(x轴表示CO2通入的量,y轴表示导电能力)。
D
