第三章第三节 醛 酮(第一课时)课件(共26张PPT)-2022-2023学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第三章第三节 醛 酮(第一课时)课件(共26张PPT)-2022-2023学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-22 00:00:00 | ||
图片预览





文档简介
(共26张PPT)
第三节 醛 酮
第三章 烃的含氧衍生物
制作人:阳海斌
第一课时 醛
人的酒量大小,与酒精在人体内的代谢产物和过程有很大关系。乙醇进入人体内,首先在乙醇脱氢酶的作用下氧化为乙醛,然后又在乙醛脱氢酶的作用下将乙醛氧化为乙酸,并进一步转化为CO2和H2O。如果人体内这两种脱氢酶的含量都很多的话,酒精的代谢速度就很快。但如果人体内这两种脱氢酶的含量不够多,例如缺少乙醛脱氢酶,饮酒后就会引起体内乙醛积累,导致血管扩张而脸红。那么乙醛具有哪些性质呢
1、了解乙醛的物理性质和用途。
2、掌握乙醛的主要化学性质和醛基的检验方法。
3、了解醛的分类和命名。
4、理解饱和一元醛的一般通性和同分异构现象。
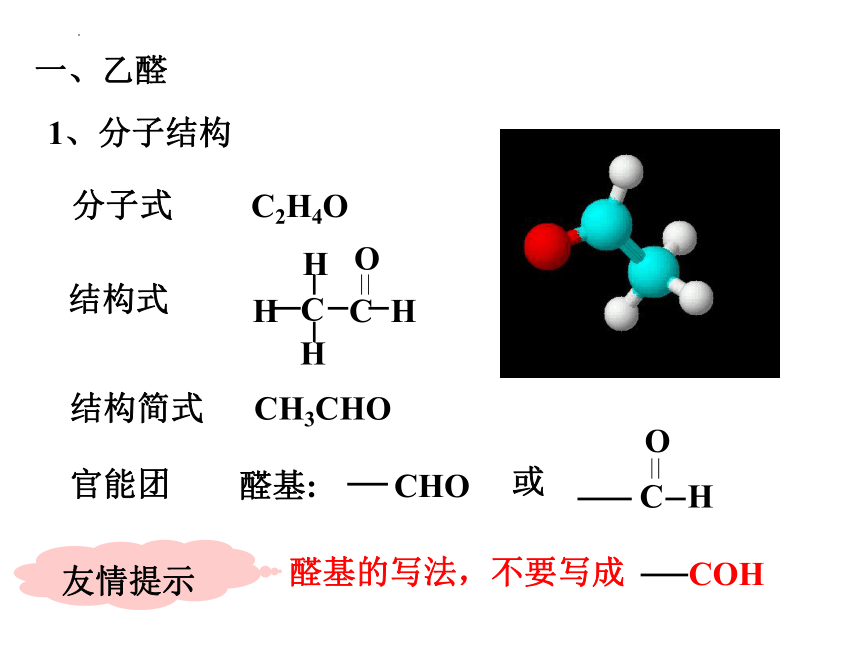
一、乙醛
分子式
结构简式 CH3CHO
结构式
H
H
H
H
C
C
O
官能团
醛基:
CHO
或
C
H
O
醛基的写法,不要写成
COH
C2H4O
友情提示
1、分子结构
2、物理性质
颜色:无色
味道:刺激性气味;
状态:液态
密度:比水的密度小;
溶解性:跟水、乙醇等互溶。
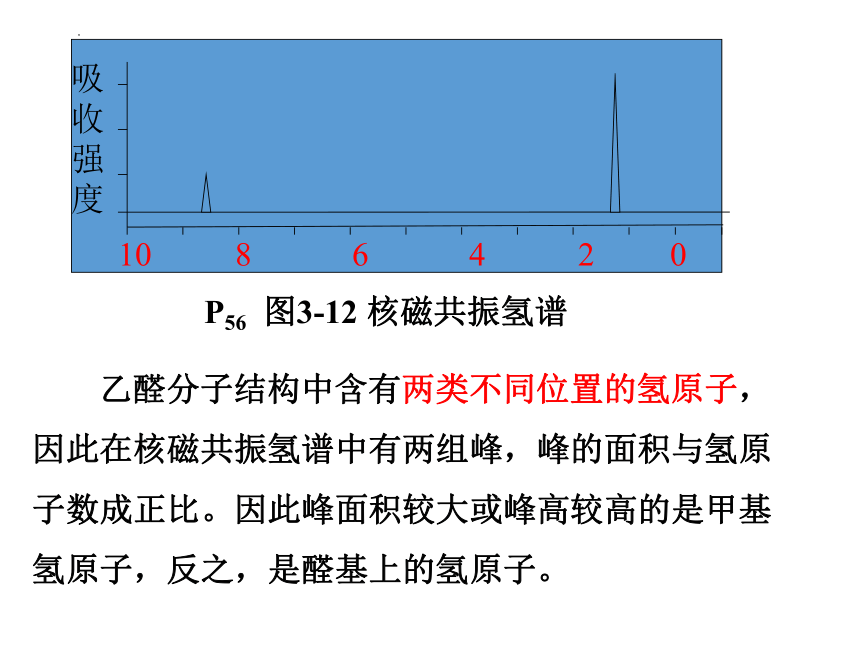
吸收强度
10 8 6 4 2 0
P56 图3-12 核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
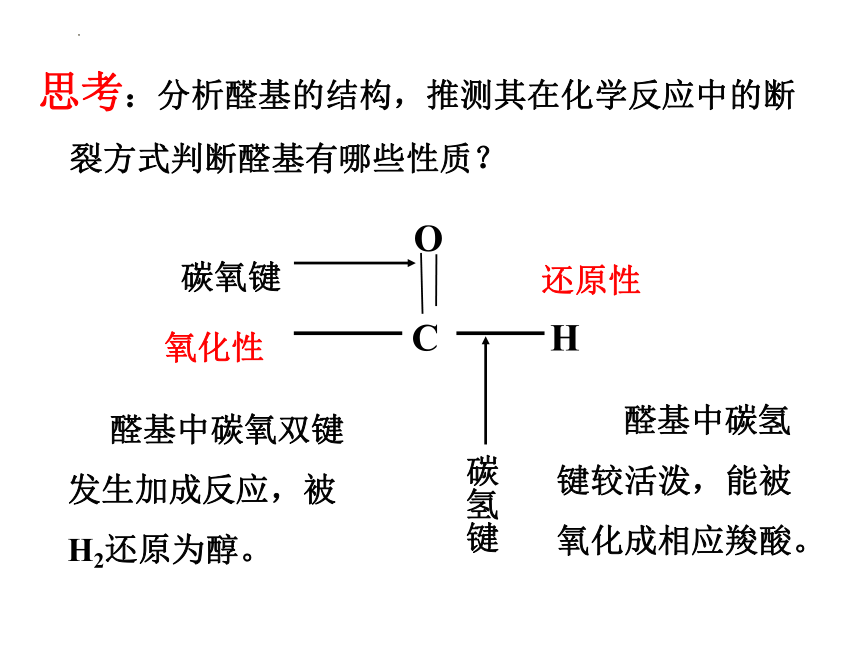
思考:分析醛基的结构,推测其在化学反应中的断裂方式判断醛基有哪些性质?
C
H
O
碳氧键
碳氢键
醛基中碳氧双键发生加成反应,被H2还原为醇。
氧化性
还原性
醛基中碳氢键较活泼,能被氧化成相应羧酸。
a、配制银氨溶液:取一洁净试管,加入1ml 2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
b、水浴加热生成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
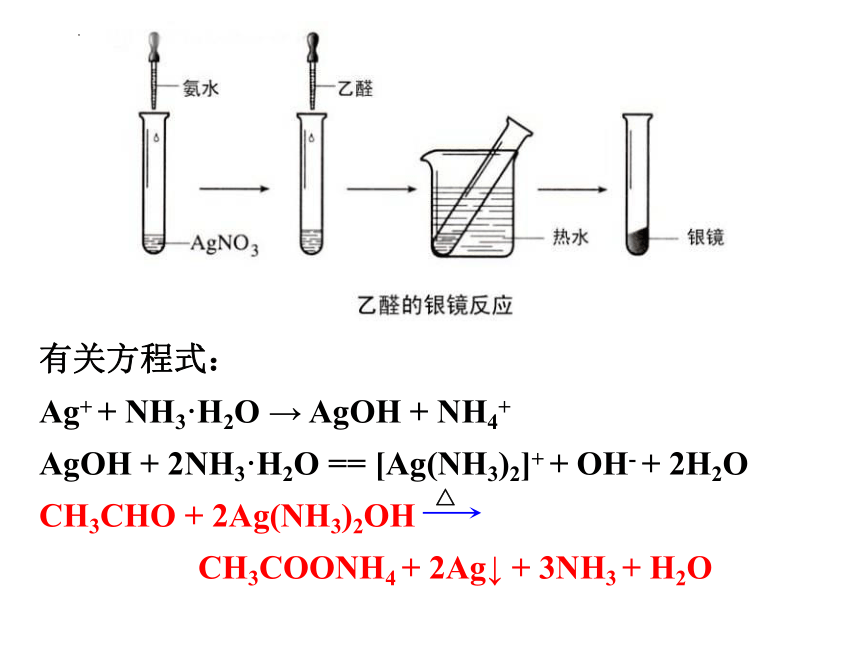
① 银镜反应
(1)氧化反应
3、化学性质
有关方程式:
Ag+ + NH3·H2O → AgOH + NH4+
AgOH + 2NH3·H2O == [Ag(NH3)2]+ + OH- + 2H2O
CH3CHO + 2Ag(NH3)2OH
CH3COONH4 + 2Ag↓ + 3NH3 + H2O
△
注意事项
(1)试管内壁要洁净,否则得不到光亮的银镜;
(2)必须水浴加热,不可振荡和摇动试管;
(3)须用新配制的银氨溶液,现用现配;
(4)乙醛用量不可太多实验后,银镜用HNO3浸泡,再用水洗;
(5)配制银氨溶液时向稀AgNO3中滴加稀氨水,直至最初生成的沉淀恰好溶解为止;(顺序不能反)
(6)该反应需在碱性环境中进行,酸性环境会破坏Ag(NH3)2;
(7)1mol –CHO被氧化,就应有2mol Ag生成;
(8)此反应可以用于检验和鉴定–CHO的存在。
a、配制新制的Cu(OH)2悬浊液:在试管里加入2mL 10%NaOH溶液,滴入2%CuSO4溶液4~6滴,振荡。
Cu2++2OH-= Cu(OH)2
b、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,加热至沸腾。
② 与新制的氢氧化铜反应
现象:
① 中有蓝色絮状沉淀,
② 中有红色(Cu2O)沉淀生成。
应用:检验醛基的存在——医学上检验病人是否患糖尿病。
CH3CHO + 2Cu(OH)2 + NaOH
CH3COONa + Cu2O↓+ 3H2O
△
注意事项:
(1)氢氧化铜溶液一定要新制,碱一定要过量;
(2)加热至沸腾,才能有明显的红色沉淀;
(3)加热煮沸时间不宜过长。
HCHO + 4 [Ag(NH3)2]OH
4Ag ↓+ CO2↑+ 8NH3 + 3H2O
加热
写出甲醛发生银镜反应,以及与新制的
氢氧化铜反应的化学方程式。
HCHO + 4Cu(OH)2 2Cu2O↓+CO2↑+5H2O
加热
学
与
问
③ 与氧气反应
O
+ O2
2CH3 —C — H
O
2CH3 —C — OH
△
催化剂
2CH3CHO + 5O2
4CO2 + 4H2O
点燃
燃烧:
在一定温度和催化剂条件下:
2、加成反应
Ni
CH3CHO + H2
CH3CH2OH
还原反应:
在有机化学反应里,通常还可以从加氢或去氢来分析氧化还原反应(得氢去氧)。
根据加成反应的概念写出CH3CHO和H2 加成反应的方程式。
二、醛类
1、定义:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。
2、分类:
饱和一元醛通式:CnH2n+1CHO或CnH2nO
一元醛
二元醛
多元醛
饱和醛
不饱和醛
醛
-OH
3、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体。如:C3H6O
CH3-CH2-C-H
O
O
CH3-C-CH3
CH2=CH-CH2-OH
(1)选主链: 选含醛基最长的碳链作为主链,根据主链的碳原子数称“某醛” 。
(2)编号位: 从醛基一端开始,醛基中的碳原子编号为1 。
(3)写名称: 把取代基名称写在母体名称前,用“二、三、四等”写出醛的个数。
4、醛的命名
CH3—CH—CHO
CH3
2-甲基丙醛
CH3—CH—CH2—CH3
CHO
2-甲基丁醛
5、常见的醛
甲醛:
HCHO是最简单的醛,为无色、有刺激性气味的气体,35%~40%的甲醛水溶液又称福尔马林,具有杀菌、防腐性能。
乙醛:
乙醛是一种没有颜色,有刺激性气味的液体,密度比水小,沸点20.8℃,易挥发易燃烧,易溶于水及乙醇、乙醚、氯仿等有机溶剂。
苯甲醛
肉桂醛
CH2=CH—CHO
CHO
一、醛的化学性质
1.和H2加成被还原成醇
2.氧化反应
(1)燃烧 (2)催化氧化成羧酸
(3)被弱氧化剂氧化
①银镜反应 ②与新制的氢氧化铜反应
(4)使酸性KMnO4溶液和溴水褪色
二、有机物的氧化还原反应
还原反应:加氢或失氧
氧化反应:加氧或失氢
1、某学生做乙醛的还原实验,取1mol·L-1的CuSO4溶液2mL和0.4mol·L-1的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是( )
A.乙醛溶液太少 B.氢氧化钠不够用
C.硫酸铜不够用 D.加热时间不够
B
2、为了鉴别己烯、甲苯和丙醛,使用的试剂组先后关系正确的是 ( )
A. 新制氢氧化铜悬浊液及溴水
B. 高锰酸钾酸性溶液及溴水
C. 银氨溶液及高锰酸钾酸性溶液
D. 新制氢氧化铜悬浊液及银氨溶液
A
3、在实验室里不宜长期放置,应在使用前配制的溶液是( )
①酚酞试剂 ②银氨溶液 ③Na2CO3溶液 ④Cu(OH)2悬浊液 ⑤酸化的FeCl3溶液
⑥硫化氢水溶液
A.只有②和④ B.除①之外
C.只有②④⑥ D.全部
C
4、 是某有机物加氢后的还原产
物,那么原有机物可能是 ( )
A. 乙醛的同分异构体
B. 丁醛的同分异构体
C. 丙醛的同分异构体
D. 戊醛
B
5、某天然拒食素具有防御非洲大群蚯蚓的作用,其结
构简式如图(未表示出原子或原子团的空间排列)。该
拒食素与下列某试剂充分反应,所得有机物分子的官
能团数目增加,则该试剂是 ( )
A.Br2的CCl4溶液 B.Ag(NH3)2OH溶液
C.HBr D.H2
A
第三节 醛 酮
第三章 烃的含氧衍生物
制作人:阳海斌
第一课时 醛
人的酒量大小,与酒精在人体内的代谢产物和过程有很大关系。乙醇进入人体内,首先在乙醇脱氢酶的作用下氧化为乙醛,然后又在乙醛脱氢酶的作用下将乙醛氧化为乙酸,并进一步转化为CO2和H2O。如果人体内这两种脱氢酶的含量都很多的话,酒精的代谢速度就很快。但如果人体内这两种脱氢酶的含量不够多,例如缺少乙醛脱氢酶,饮酒后就会引起体内乙醛积累,导致血管扩张而脸红。那么乙醛具有哪些性质呢
1、了解乙醛的物理性质和用途。
2、掌握乙醛的主要化学性质和醛基的检验方法。
3、了解醛的分类和命名。
4、理解饱和一元醛的一般通性和同分异构现象。
一、乙醛
分子式
结构简式 CH3CHO
结构式
H
H
H
H
C
C
O
官能团
醛基:
CHO
或
C
H
O
醛基的写法,不要写成
COH
C2H4O
友情提示
1、分子结构
2、物理性质
颜色:无色
味道:刺激性气味;
状态:液态
密度:比水的密度小;
溶解性:跟水、乙醇等互溶。
吸收强度
10 8 6 4 2 0
P56 图3-12 核磁共振氢谱
乙醛分子结构中含有两类不同位置的氢原子,因此在核磁共振氢谱中有两组峰,峰的面积与氢原子数成正比。因此峰面积较大或峰高较高的是甲基氢原子,反之,是醛基上的氢原子。
思考:分析醛基的结构,推测其在化学反应中的断裂方式判断醛基有哪些性质?
C
H
O
碳氧键
碳氢键
醛基中碳氧双键发生加成反应,被H2还原为醇。
氧化性
还原性
醛基中碳氢键较活泼,能被氧化成相应羧酸。
a、配制银氨溶液:取一洁净试管,加入1ml 2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
b、水浴加热生成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
① 银镜反应
(1)氧化反应
3、化学性质
有关方程式:
Ag+ + NH3·H2O → AgOH + NH4+
AgOH + 2NH3·H2O == [Ag(NH3)2]+ + OH- + 2H2O
CH3CHO + 2Ag(NH3)2OH
CH3COONH4 + 2Ag↓ + 3NH3 + H2O
△
注意事项
(1)试管内壁要洁净,否则得不到光亮的银镜;
(2)必须水浴加热,不可振荡和摇动试管;
(3)须用新配制的银氨溶液,现用现配;
(4)乙醛用量不可太多实验后,银镜用HNO3浸泡,再用水洗;
(5)配制银氨溶液时向稀AgNO3中滴加稀氨水,直至最初生成的沉淀恰好溶解为止;(顺序不能反)
(6)该反应需在碱性环境中进行,酸性环境会破坏Ag(NH3)2;
(7)1mol –CHO被氧化,就应有2mol Ag生成;
(8)此反应可以用于检验和鉴定–CHO的存在。
a、配制新制的Cu(OH)2悬浊液:在试管里加入2mL 10%NaOH溶液,滴入2%CuSO4溶液4~6滴,振荡。
Cu2++2OH-= Cu(OH)2
b、乙醛的氧化:在上述蓝色浊液中加入0.5ml乙醛溶液,加热至沸腾。
② 与新制的氢氧化铜反应
现象:
① 中有蓝色絮状沉淀,
② 中有红色(Cu2O)沉淀生成。
应用:检验醛基的存在——医学上检验病人是否患糖尿病。
CH3CHO + 2Cu(OH)2 + NaOH
CH3COONa + Cu2O↓+ 3H2O
△
注意事项:
(1)氢氧化铜溶液一定要新制,碱一定要过量;
(2)加热至沸腾,才能有明显的红色沉淀;
(3)加热煮沸时间不宜过长。
HCHO + 4 [Ag(NH3)2]OH
4Ag ↓+ CO2↑+ 8NH3 + 3H2O
加热
写出甲醛发生银镜反应,以及与新制的
氢氧化铜反应的化学方程式。
HCHO + 4Cu(OH)2 2Cu2O↓+CO2↑+5H2O
加热
学
与
问
③ 与氧气反应
O
+ O2
2CH3 —C — H
O
2CH3 —C — OH
△
催化剂
2CH3CHO + 5O2
4CO2 + 4H2O
点燃
燃烧:
在一定温度和催化剂条件下:
2、加成反应
Ni
CH3CHO + H2
CH3CH2OH
还原反应:
在有机化学反应里,通常还可以从加氢或去氢来分析氧化还原反应(得氢去氧)。
根据加成反应的概念写出CH3CHO和H2 加成反应的方程式。
二、醛类
1、定义:从结构上看,由烃基(或氢原子)跟醛基相连而成的化合物叫醛。
2、分类:
饱和一元醛通式:CnH2n+1CHO或CnH2nO
一元醛
二元醛
多元醛
饱和醛
不饱和醛
醛
-OH
3、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体。如:C3H6O
CH3-CH2-C-H
O
O
CH3-C-CH3
CH2=CH-CH2-OH
(1)选主链: 选含醛基最长的碳链作为主链,根据主链的碳原子数称“某醛” 。
(2)编号位: 从醛基一端开始,醛基中的碳原子编号为1 。
(3)写名称: 把取代基名称写在母体名称前,用“二、三、四等”写出醛的个数。
4、醛的命名
CH3—CH—CHO
CH3
2-甲基丙醛
CH3—CH—CH2—CH3
CHO
2-甲基丁醛
5、常见的醛
甲醛:
HCHO是最简单的醛,为无色、有刺激性气味的气体,35%~40%的甲醛水溶液又称福尔马林,具有杀菌、防腐性能。
乙醛:
乙醛是一种没有颜色,有刺激性气味的液体,密度比水小,沸点20.8℃,易挥发易燃烧,易溶于水及乙醇、乙醚、氯仿等有机溶剂。
苯甲醛
肉桂醛
CH2=CH—CHO
CHO
一、醛的化学性质
1.和H2加成被还原成醇
2.氧化反应
(1)燃烧 (2)催化氧化成羧酸
(3)被弱氧化剂氧化
①银镜反应 ②与新制的氢氧化铜反应
(4)使酸性KMnO4溶液和溴水褪色
二、有机物的氧化还原反应
还原反应:加氢或失氧
氧化反应:加氧或失氢
1、某学生做乙醛的还原实验,取1mol·L-1的CuSO4溶液2mL和0.4mol·L-1的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是( )
A.乙醛溶液太少 B.氢氧化钠不够用
C.硫酸铜不够用 D.加热时间不够
B
2、为了鉴别己烯、甲苯和丙醛,使用的试剂组先后关系正确的是 ( )
A. 新制氢氧化铜悬浊液及溴水
B. 高锰酸钾酸性溶液及溴水
C. 银氨溶液及高锰酸钾酸性溶液
D. 新制氢氧化铜悬浊液及银氨溶液
A
3、在实验室里不宜长期放置,应在使用前配制的溶液是( )
①酚酞试剂 ②银氨溶液 ③Na2CO3溶液 ④Cu(OH)2悬浊液 ⑤酸化的FeCl3溶液
⑥硫化氢水溶液
A.只有②和④ B.除①之外
C.只有②④⑥ D.全部
C
4、 是某有机物加氢后的还原产
物,那么原有机物可能是 ( )
A. 乙醛的同分异构体
B. 丁醛的同分异构体
C. 丙醛的同分异构体
D. 戊醛
B
5、某天然拒食素具有防御非洲大群蚯蚓的作用,其结
构简式如图(未表示出原子或原子团的空间排列)。该
拒食素与下列某试剂充分反应,所得有机物分子的官
能团数目增加,则该试剂是 ( )
A.Br2的CCl4溶液 B.Ag(NH3)2OH溶液
C.HBr D.H2
A
