化学鲁教版九年级下册参考课件:8.1 海洋化学资源(共27张PPT)
文档属性
| 名称 | 化学鲁教版九年级下册参考课件:8.1 海洋化学资源(共27张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-23 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
第八单元 海水中的化学
我们常把大海比作母亲,它就像一个摇篮,孕育我们成长,它是人类千百年来取之不尽、用之不竭的巨大资源宝库。同学们,你们知道海洋中有哪些资源吗?
★学习目标:
1.了解海水提镁的化学原理,能熟练写出利用海水提取镁的反应方程式。
2.通过对海水淡化的实验探究,学会蒸馏法分离物质、认识海水淡化的可行性。
3.通过海水提镁和海水淡化的学习,认识到从自然界中获取物质的两种主要思路(化学方法和物理方法)及获取物质的思想方法(富集法、筛选法)。
你知道海洋中的资源大致上有哪几类吗?
化学资源
海底矿物资源
海洋生物资源
海洋动力资源
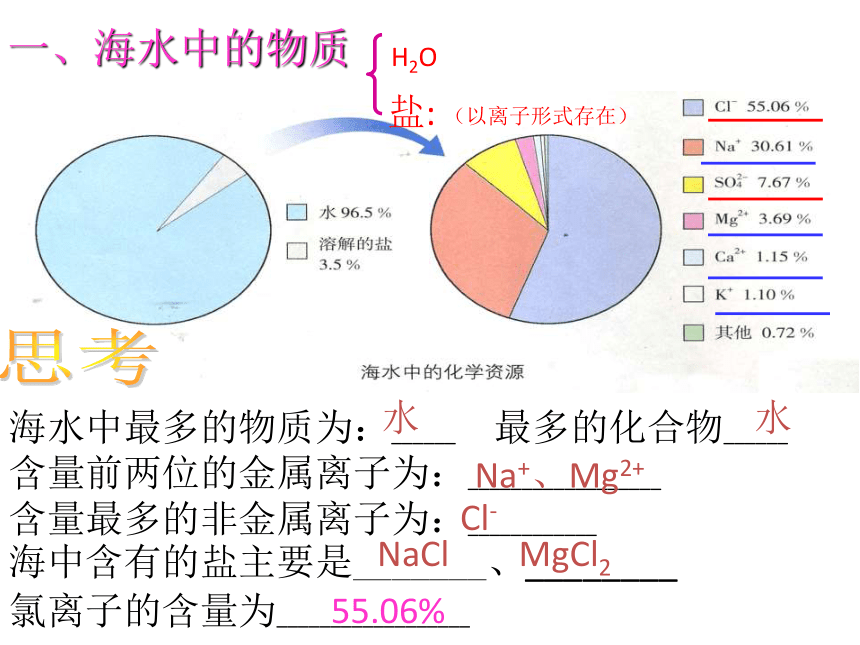
海水中最多的物质为:______ 最多的化合物______
含量前两位的金属离子为:__________________
含量最多的非金属离子为:____________
海中含有的盐主要是_______、________
氯离子的含量为__________________
水
Na+、Mg2+
Cl-
NaCl MgCl2
思考
一、海水中的物质
水
55.06%
H2O
盐:
(以离子形式存在)
人们提取海水中的化学元素,来制备有多种用途的物质。如广泛用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提取的镁盐制取的。
金属镁
含金属镁的飞机
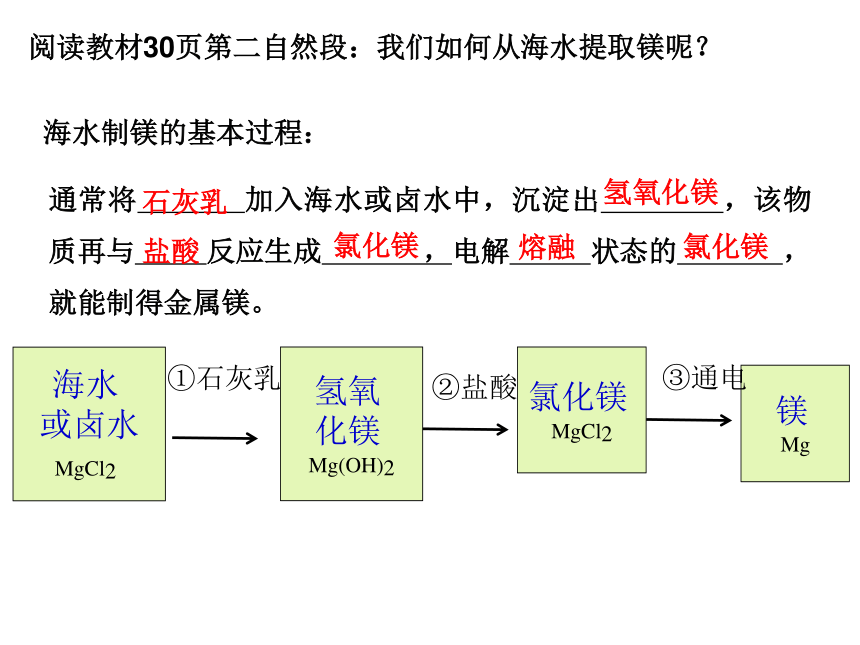
阅读教材30页第二自然段:我们如何从海水提取镁呢?
海水
或卤水
MgCl2
氢氧
化镁
Mg(OH)2
氯化镁
MgCl2
镁
Mg
①石灰乳
②盐酸
③通电
通常将 加入海水或卤水中,沉淀出 ,该物质再与 反应生成 ,电解 状态的 ,就能制得金属镁。
石灰乳
氢氧化镁
盐酸
氯化镁
海水制镁的基本过程:
氯化镁
熔融
写出上述流程图中的化学方程式并注明反应基本类型:
①______________(______)
②______________(______)
③______________(______)
MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl=MgCl2+2H2O
MgCl2 == Mg+Cl2↑
通电
复分解反应
复分解反应
分解反应
思考:
①除去其它杂质 ②将MgCl2富集起来
1.海水中本来就有氯化镁,为什么不直接通电?还要经过“MgCl2→Mg(OH)2→ MgCl2”的过程?
2.所加盐酸是否要过量?目的是什么?如果过量,如何除去?
要过量,目的是保证Mg(OH)2完全反应,过量的稀盐酸加热蒸发即可除去。
海水
或卤水
MgCl2
氯化镁
MgCl2
镁
Mg
?
通电
?
友情提示:NaOH的市场平均价格是2320元/吨,Ca(OH)2的市场平均价格是1500元/吨。
怎样得到Ca(OH)2? 你能用方程式表示吗?
氢氧
化镁
Mg(OH)2
石灰乳
Ca(OH)2
HCl
盐酸
海边的贝壳的主要成份是CaCO3。
海水制镁
流程
贝壳(含CaCO3) 石灰乳
水
CaO
高温煅烧
二、海底矿物
[自学指导] 海底矿物
阅读课本P31-32,解决以下问题:
1.海底蕴藏着哪些矿物资源?
2.“可燃冰”是如何形成的?
3.为什么“可燃冰”被誉为为“未来能源”、“21世纪能源”?
4.什么是锰结核?锰结核里主要含有哪些元素?
化石燃料:
为什么“可燃冰”被誉为21世纪能源?
可燃冰在海底储量大,产热多,且燃烧后几乎不产生任何残渣或废气。
煤、石油、天然气
天然气水合物——可燃冰
多金属结核——锰结核
(含锰、铁、镍、铜、钴、钛等20多种金属元素。 )
可燃冰燃烧化学方程式
CH4 + 2O2 ==== CO2 + 2 H2O
点燃
【动脑筋】
1.地球上的水资源很丰富,为什么淡水日益短缺?
2.采用什么方法解决淡水危机?
3.请你设计实验,从海水中得到淡水?
三、海水淡化
1.蒸馏法淡化海水
问题:为使水蒸气冷凝效果更好,你认为应对实验装置做哪些改进?
为了使水蒸气的冷凝效果更好,你认为应对实验做哪些改进?
海水蒸馏原理模拟实验
①加长导管长度
②将导管改为冷凝管
③将接受器放入冰水混合物中
④ 在导管上包上湿而冷的毛巾
混合物分离的方法——蒸馏法
蒸馏法:是利用混合物中各物质的 不同,将物质分开。
如:用蒸馏法分离酒精和水的混合物。
沸点
如何证明你得到的水是淡水,而不是海水?
食盐
食盐
思考
1.加氢氧化钠溶液或氢氧化钙溶液,看是否有白色沉淀生成(海水中有镁离子)
2.加硝酸银溶液看是否有白色沉淀生成(海水中有氯离子)
3.加热,看是否有白色固体剩余(海水中有可溶物)
4.做导电性实验,看能否导电等(海水中离子导电)
取少量样品,加入AgNO3溶液产生白色沉淀;再加入稀HNO3 ,白色沉淀不消失
应用:如何用化学方法区分自来水(含Cl-)与蒸馏水?
笔记:Cl-的检验方法:
分别取两种水少量,滴入AgNO3溶液,没有白色沉淀生成的水是蒸馏水,有白色沉淀生成的水是自来水
化学方程式:NaCl+AgNO3=AgCl↓+NaNO3
【多识一点】
膜法淡化海水
结晶法:
加入易挥发的物质丁烷,丁烷挥发带走热量,
使海水结冰,从而使水和盐分离。
【思考】图中右侧的海水淡化后与淡化前相比:溶质的质量,溶剂的质量,溶液的质量,溶质质量分数发生了怎样的改变?
你能根据你的生活经验说出造成海洋污染的主要原因吗?
海上石油的泄露
倾倒固体垃圾
各类污水的排放
国际上普遍采取的海洋保护措施:
①加强海洋环境立法
②建立海洋自然保护区
③加强海洋环境监测
④提高消除污染的技术水平
谈谈收获
通过学习你谈谈收获了什么?还有什么疑问和想法,说一说吧!
【课堂小结,深化提高】
1.请结合提取镁的流程图,写出相关化学方程式:
①MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
②Mg(OH)2+2HCl=MgCl2+2H2O
③MgCl2 Mg+Cl2↑
通电
====
2.海水淡化的方法
蒸馏法淡化海水
膜法淡化海水
结晶法
3.海底矿物资源:蕴藏着大量的煤、石油、天然气等常规化石燃料。
【挑战自我】
1.可能造成海洋污染的是( )
①海上油轮原油泄露②工厂污水向海洋排放③生活污水向海洋排放④塑料包装袋向海洋中抛弃⑤赤潮
A.仅①②③ B.近②③④
C.仅③④⑤ D.①②③④⑤
D
2.下列有关海洋资源的说法不正确的是( )
A.海水中溶有大量的盐;
B.人类从海水中提取用途广泛的金属镁;
C.海底蕴藏丰富的煤、石油,没有天然气和 “可燃冰”;
D.海底蕴藏着多金属结核,也称锰结核。
C
海水
或卤水
氢氧化镁
氯化镁
镁
①
②
③
①中加入的原料是( ),为了将海水中的MgCl2完全转化成Mg(OH)2 ,原料①的量应是( )。
②将Mg(OH)2沉淀从海水中分离出来的方法是( ),②中应加入的原料是( )。
③的反应条件是( ),该反应的反应类型是( )。
3.镁是一种用途广泛的金属,世界上60℅的金属镁是从海水中提取出来的,下面是海水制镁的流程图:
Ca(OH)2
足量
过滤
盐酸
通电
分解反应
4.如图,海水淡化可采用膜分离技术对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是 ( )
A.溶质质量增加
B.溶剂质量减少
C.溶液质量不变
D.溶质质量分数减少
B
祝同学们学习愉快!
第八单元 海水中的化学
我们常把大海比作母亲,它就像一个摇篮,孕育我们成长,它是人类千百年来取之不尽、用之不竭的巨大资源宝库。同学们,你们知道海洋中有哪些资源吗?
★学习目标:
1.了解海水提镁的化学原理,能熟练写出利用海水提取镁的反应方程式。
2.通过对海水淡化的实验探究,学会蒸馏法分离物质、认识海水淡化的可行性。
3.通过海水提镁和海水淡化的学习,认识到从自然界中获取物质的两种主要思路(化学方法和物理方法)及获取物质的思想方法(富集法、筛选法)。
你知道海洋中的资源大致上有哪几类吗?
化学资源
海底矿物资源
海洋生物资源
海洋动力资源
海水中最多的物质为:______ 最多的化合物______
含量前两位的金属离子为:__________________
含量最多的非金属离子为:____________
海中含有的盐主要是_______、________
氯离子的含量为__________________
水
Na+、Mg2+
Cl-
NaCl MgCl2
思考
一、海水中的物质
水
55.06%
H2O
盐:
(以离子形式存在)
人们提取海水中的化学元素,来制备有多种用途的物质。如广泛用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提取的镁盐制取的。
金属镁
含金属镁的飞机
阅读教材30页第二自然段:我们如何从海水提取镁呢?
海水
或卤水
MgCl2
氢氧
化镁
Mg(OH)2
氯化镁
MgCl2
镁
Mg
①石灰乳
②盐酸
③通电
通常将 加入海水或卤水中,沉淀出 ,该物质再与 反应生成 ,电解 状态的 ,就能制得金属镁。
石灰乳
氢氧化镁
盐酸
氯化镁
海水制镁的基本过程:
氯化镁
熔融
写出上述流程图中的化学方程式并注明反应基本类型:
①______________(______)
②______________(______)
③______________(______)
MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl=MgCl2+2H2O
MgCl2 == Mg+Cl2↑
通电
复分解反应
复分解反应
分解反应
思考:
①除去其它杂质 ②将MgCl2富集起来
1.海水中本来就有氯化镁,为什么不直接通电?还要经过“MgCl2→Mg(OH)2→ MgCl2”的过程?
2.所加盐酸是否要过量?目的是什么?如果过量,如何除去?
要过量,目的是保证Mg(OH)2完全反应,过量的稀盐酸加热蒸发即可除去。
海水
或卤水
MgCl2
氯化镁
MgCl2
镁
Mg
?
通电
?
友情提示:NaOH的市场平均价格是2320元/吨,Ca(OH)2的市场平均价格是1500元/吨。
怎样得到Ca(OH)2? 你能用方程式表示吗?
氢氧
化镁
Mg(OH)2
石灰乳
Ca(OH)2
HCl
盐酸
海边的贝壳的主要成份是CaCO3。
海水制镁
流程
贝壳(含CaCO3) 石灰乳
水
CaO
高温煅烧
二、海底矿物
[自学指导] 海底矿物
阅读课本P31-32,解决以下问题:
1.海底蕴藏着哪些矿物资源?
2.“可燃冰”是如何形成的?
3.为什么“可燃冰”被誉为为“未来能源”、“21世纪能源”?
4.什么是锰结核?锰结核里主要含有哪些元素?
化石燃料:
为什么“可燃冰”被誉为21世纪能源?
可燃冰在海底储量大,产热多,且燃烧后几乎不产生任何残渣或废气。
煤、石油、天然气
天然气水合物——可燃冰
多金属结核——锰结核
(含锰、铁、镍、铜、钴、钛等20多种金属元素。 )
可燃冰燃烧化学方程式
CH4 + 2O2 ==== CO2 + 2 H2O
点燃
【动脑筋】
1.地球上的水资源很丰富,为什么淡水日益短缺?
2.采用什么方法解决淡水危机?
3.请你设计实验,从海水中得到淡水?
三、海水淡化
1.蒸馏法淡化海水
问题:为使水蒸气冷凝效果更好,你认为应对实验装置做哪些改进?
为了使水蒸气的冷凝效果更好,你认为应对实验做哪些改进?
海水蒸馏原理模拟实验
①加长导管长度
②将导管改为冷凝管
③将接受器放入冰水混合物中
④ 在导管上包上湿而冷的毛巾
混合物分离的方法——蒸馏法
蒸馏法:是利用混合物中各物质的 不同,将物质分开。
如:用蒸馏法分离酒精和水的混合物。
沸点
如何证明你得到的水是淡水,而不是海水?
食盐
食盐
思考
1.加氢氧化钠溶液或氢氧化钙溶液,看是否有白色沉淀生成(海水中有镁离子)
2.加硝酸银溶液看是否有白色沉淀生成(海水中有氯离子)
3.加热,看是否有白色固体剩余(海水中有可溶物)
4.做导电性实验,看能否导电等(海水中离子导电)
取少量样品,加入AgNO3溶液产生白色沉淀;再加入稀HNO3 ,白色沉淀不消失
应用:如何用化学方法区分自来水(含Cl-)与蒸馏水?
笔记:Cl-的检验方法:
分别取两种水少量,滴入AgNO3溶液,没有白色沉淀生成的水是蒸馏水,有白色沉淀生成的水是自来水
化学方程式:NaCl+AgNO3=AgCl↓+NaNO3
【多识一点】
膜法淡化海水
结晶法:
加入易挥发的物质丁烷,丁烷挥发带走热量,
使海水结冰,从而使水和盐分离。
【思考】图中右侧的海水淡化后与淡化前相比:溶质的质量,溶剂的质量,溶液的质量,溶质质量分数发生了怎样的改变?
你能根据你的生活经验说出造成海洋污染的主要原因吗?
海上石油的泄露
倾倒固体垃圾
各类污水的排放
国际上普遍采取的海洋保护措施:
①加强海洋环境立法
②建立海洋自然保护区
③加强海洋环境监测
④提高消除污染的技术水平
谈谈收获
通过学习你谈谈收获了什么?还有什么疑问和想法,说一说吧!
【课堂小结,深化提高】
1.请结合提取镁的流程图,写出相关化学方程式:
①MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2
②Mg(OH)2+2HCl=MgCl2+2H2O
③MgCl2 Mg+Cl2↑
通电
====
2.海水淡化的方法
蒸馏法淡化海水
膜法淡化海水
结晶法
3.海底矿物资源:蕴藏着大量的煤、石油、天然气等常规化石燃料。
【挑战自我】
1.可能造成海洋污染的是( )
①海上油轮原油泄露②工厂污水向海洋排放③生活污水向海洋排放④塑料包装袋向海洋中抛弃⑤赤潮
A.仅①②③ B.近②③④
C.仅③④⑤ D.①②③④⑤
D
2.下列有关海洋资源的说法不正确的是( )
A.海水中溶有大量的盐;
B.人类从海水中提取用途广泛的金属镁;
C.海底蕴藏丰富的煤、石油,没有天然气和 “可燃冰”;
D.海底蕴藏着多金属结核,也称锰结核。
C
海水
或卤水
氢氧化镁
氯化镁
镁
①
②
③
①中加入的原料是( ),为了将海水中的MgCl2完全转化成Mg(OH)2 ,原料①的量应是( )。
②将Mg(OH)2沉淀从海水中分离出来的方法是( ),②中应加入的原料是( )。
③的反应条件是( ),该反应的反应类型是( )。
3.镁是一种用途广泛的金属,世界上60℅的金属镁是从海水中提取出来的,下面是海水制镁的流程图:
Ca(OH)2
足量
过滤
盐酸
通电
分解反应
4.如图,海水淡化可采用膜分离技术对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中的各离子不能通过淡化膜,从而得到淡水。对加压后右侧海水成分变化进行分析,正确的是 ( )
A.溶质质量增加
B.溶剂质量减少
C.溶液质量不变
D.溶质质量分数减少
B
祝同学们学习愉快!
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
