2.3.2 分子间的作用力 课件(共18张PPT) 化学人教版(2019)选择性必修2
文档属性
| 名称 | 2.3.2 分子间的作用力 课件(共18张PPT) 化学人教版(2019)选择性必修2 |

|
|
| 格式 | zip | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-24 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
100℃水沸腾
3000℃水分解
化学变化
分子内化学键破坏
水分子之间存在着相互作用力
物理变化
[情境创设]
第二章 分子结构与性质
第三节 分子结构与物质的性质
第2课时 分子间的作用力
一、范德华力
把分子聚集在一起的作用力,叫分子间作用力。范德华力就是其中一种。
①范德华力很弱,约比化学键键能小1-2个数量级。
②广泛存在于分子之间。
③只有分子充分接近时才有范德华力。
④范德华力没有方向性和饱和性。
微粒间 作用力 能量
kJ·mol -1
化学键 100 - 600
范德华力 2 - 20
某些分子间的范德华力
分子 Ar CO HI HBr HCl
分子量 40 28 128.5 81.5 36.5
范德华力 (kJ/mol) 8.50 8.75 26.00 23.11 21.14
[思考]为什么范德华力:CO>Ar
①分子极性越大,范德华力越大。
②相对分子质量越大,范德华力越大。
[思考]为什么:HI>HBr>HCl>CO
[影响因素]
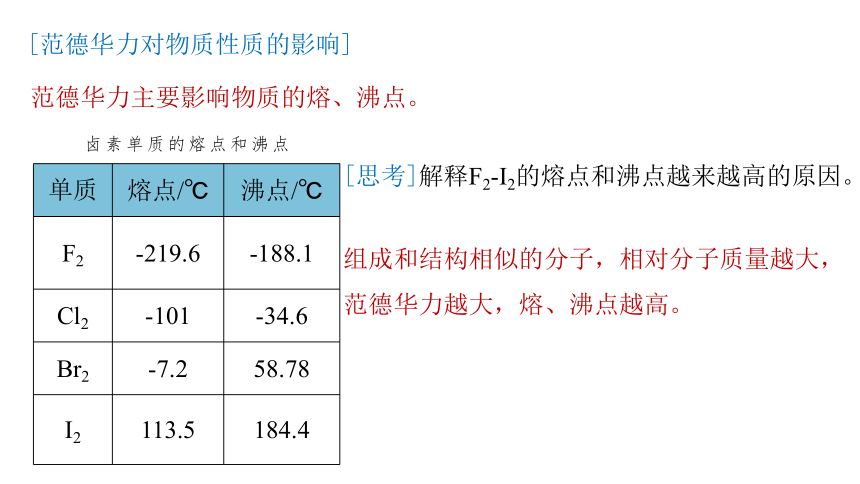
[范德华力对物质性质的影响]
单质 熔点/℃ 沸点/℃
F2 -219.6 -188.1
Cl2 -101 -34.6
Br2 -7.2 58.78
I2 113.5 184.4
卤素单质的熔点和沸点
范德华力主要影响物质的熔、沸点。
组成和结构相似的分子,相对分子质量越大,范德华力越大,熔、沸点越高。
[思考]解释F2-I2的熔点和沸点越来越高的原因。
夏天经常见到许多壁虎在墙壁或天花板上爬却掉不下来,为什么?
近年来,有人用计算机模拟,证明壁虎的足与墙体之间的作用力在本质上是它的细毛与墙体之间的范德华力。
科学 技术 社会
化学键 范德华力
概念
存在范围
作用力强弱
影响的性质
使原子(离子)结合的相互作用
把分子聚集在一起的作用力
分子内、原子间
分子间
强烈
微弱
影响物质的化学性质和物理性质
影响物质的物理性质(熔、沸点及溶解度等)
化学键与范德华力的比较
1、将干冰气化,破坏了CO2分子的—————
2、将CO2气体溶于水,破坏了CO2分子的————
范德华力
共价键
3、解释CCl4(液体),CH4及CF4是气体,CI4是固体的原因
它们空间构型均是正四面体,结构相似,相对分子质量越大,范德华力越大,聚集程度越大。范德华力比较小时呈气态,随范德华力增大时变为液体,大到一定程度时变为固体
【思考交流】
2
3
4
5
-150
-125
-100
-75
-50
-25
0
25
50
75
100
×
×
×
×
HI
CH4
SiH4
PH3
GeH4
SnH4
NH3
AsH3
SbH3
HF
HCl
HBr
H2O
H2S
H2Se
H2Te
沸点/℃
周期
IVA-VIIA氢化物的沸点
为什么H2O、HF、NH3的沸点反常?
二、氢键
- - - - - - - - - -
在水分子的O-H中,共用电子对强烈的偏向O,使得H几乎成为“裸露”的质子,其显正电性,它能与另一个水分子中相对显负电性的O的孤电子对产生静电作用,这种静电作用就是氢键。
二、氢键
由已经与电负性很大的原子(如N、O、F)形成共价键的氢原子与另一分子中电负性很大的原子(如N、O、F)之间的作用力。
[表示方法]
用X—H···Y — 表示,“—”表示共价键,“···”表示氢键(X、Y为N、O、F)
如:
H
F
H
F
H
F
H
F
[氢 键 特 征]
①氢键不属于化学键:化学键>氢键>范德华力。
②分子:有氢键一定有范德华力,有范德华力不一定有氢键。
③与氢原子形成氢键时,电负性越大,氢键越强。
④氢键会使物质熔、沸点大大增加。
⑤氢键具有一定的方向性和饱和性。
饱和性:每个氢原子只能形成一个氢键。
方向性:A—H…B—尽可能在同一直线上,
作用力最强。
H
F
H
F
H
F
H
F
[氢键分类]
① 分子间氢键:H2O NH3 HF
C2H5OH CH3COOH
② 分子内氢键
氢键
氢键
沸点:分子间氢键>分子内氢键
DNA分子有两条链,链内原子之间以很强的共价键结合,链之间则是两条链上的碱基以氢键配对,许许多多的氢键将两条链连成独特的双螺旋结构,这是遗传基因复制机理的化学基础。
生物大分子中的氢键
科学 技术 社会
大家知道,羊毛织品水洗后会变形,这是什么原因呢 羊毛纤维是蛋白质构成的,蛋白质上的氨基和羰基可能会形成氢键。羊毛在浸水和干燥的过程中,会在这些氢键处纳入水和去除水,而且其变化往往是不可逆的,从而改变了原先蛋白质的构造,即原先的氢键部位可能发生移动,由此引起羊毛织品变形。
化学与生活
羊毛织品水洗后为什么会变形
1、下列关于氢键的说法中正确的是( )
A. 每个水分子内含有两个氢键
B. 在所有的水蒸气、水、冰中都含有氢键
C. 分子间能形成氢键,使物质的熔沸点升高
D. HF稳定性很强,是因为其分子间能形成氢键
C
2、下列现象与氢键有关的是( )
①HF的熔、沸点比ⅦA族其他元素氢化物的高
②乙醇可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤ 邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A.②③④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
B
[达标检测]
1.液态水中分子间的作用力只有氢键吗?水分子的稳定性受氢键的影响吗?
2.H2O与H2S都是由分子构成的物质,结构相似,且H2S的相对分子质量比H2O的相对分子质量大,为什么H2O的沸点比H2S的沸点高。
液态水分子之间的作用力主要是氢键,但也存在范德华力。在水分子内部存在共价键(O-H),由于H-O键键长短,键能大,故分子稳定,水分子的稳定性与氢键无关。
液态水中,水分子间既存在范德华力,又存在氢键,而气态硫化氢中,H2S分子间只存在范德华力,故水分子间作用力大于硫化氢分子间的作用力,因此,H2O的沸点比H2S的沸点高。
100℃水沸腾
3000℃水分解
化学变化
分子内化学键破坏
水分子之间存在着相互作用力
物理变化
[情境创设]
第二章 分子结构与性质
第三节 分子结构与物质的性质
第2课时 分子间的作用力
一、范德华力
把分子聚集在一起的作用力,叫分子间作用力。范德华力就是其中一种。
①范德华力很弱,约比化学键键能小1-2个数量级。
②广泛存在于分子之间。
③只有分子充分接近时才有范德华力。
④范德华力没有方向性和饱和性。
微粒间 作用力 能量
kJ·mol -1
化学键 100 - 600
范德华力 2 - 20
某些分子间的范德华力
分子 Ar CO HI HBr HCl
分子量 40 28 128.5 81.5 36.5
范德华力 (kJ/mol) 8.50 8.75 26.00 23.11 21.14
[思考]为什么范德华力:CO>Ar
①分子极性越大,范德华力越大。
②相对分子质量越大,范德华力越大。
[思考]为什么:HI>HBr>HCl>CO
[影响因素]
[范德华力对物质性质的影响]
单质 熔点/℃ 沸点/℃
F2 -219.6 -188.1
Cl2 -101 -34.6
Br2 -7.2 58.78
I2 113.5 184.4
卤素单质的熔点和沸点
范德华力主要影响物质的熔、沸点。
组成和结构相似的分子,相对分子质量越大,范德华力越大,熔、沸点越高。
[思考]解释F2-I2的熔点和沸点越来越高的原因。
夏天经常见到许多壁虎在墙壁或天花板上爬却掉不下来,为什么?
近年来,有人用计算机模拟,证明壁虎的足与墙体之间的作用力在本质上是它的细毛与墙体之间的范德华力。
科学 技术 社会
化学键 范德华力
概念
存在范围
作用力强弱
影响的性质
使原子(离子)结合的相互作用
把分子聚集在一起的作用力
分子内、原子间
分子间
强烈
微弱
影响物质的化学性质和物理性质
影响物质的物理性质(熔、沸点及溶解度等)
化学键与范德华力的比较
1、将干冰气化,破坏了CO2分子的—————
2、将CO2气体溶于水,破坏了CO2分子的————
范德华力
共价键
3、解释CCl4(液体),CH4及CF4是气体,CI4是固体的原因
它们空间构型均是正四面体,结构相似,相对分子质量越大,范德华力越大,聚集程度越大。范德华力比较小时呈气态,随范德华力增大时变为液体,大到一定程度时变为固体
【思考交流】
2
3
4
5
-150
-125
-100
-75
-50
-25
0
25
50
75
100
×
×
×
×
HI
CH4
SiH4
PH3
GeH4
SnH4
NH3
AsH3
SbH3
HF
HCl
HBr
H2O
H2S
H2Se
H2Te
沸点/℃
周期
IVA-VIIA氢化物的沸点
为什么H2O、HF、NH3的沸点反常?
二、氢键
- - - - - - - - - -
在水分子的O-H中,共用电子对强烈的偏向O,使得H几乎成为“裸露”的质子,其显正电性,它能与另一个水分子中相对显负电性的O的孤电子对产生静电作用,这种静电作用就是氢键。
二、氢键
由已经与电负性很大的原子(如N、O、F)形成共价键的氢原子与另一分子中电负性很大的原子(如N、O、F)之间的作用力。
[表示方法]
用X—H···Y — 表示,“—”表示共价键,“···”表示氢键(X、Y为N、O、F)
如:
H
F
H
F
H
F
H
F
[氢 键 特 征]
①氢键不属于化学键:化学键>氢键>范德华力。
②分子:有氢键一定有范德华力,有范德华力不一定有氢键。
③与氢原子形成氢键时,电负性越大,氢键越强。
④氢键会使物质熔、沸点大大增加。
⑤氢键具有一定的方向性和饱和性。
饱和性:每个氢原子只能形成一个氢键。
方向性:A—H…B—尽可能在同一直线上,
作用力最强。
H
F
H
F
H
F
H
F
[氢键分类]
① 分子间氢键:H2O NH3 HF
C2H5OH CH3COOH
② 分子内氢键
氢键
氢键
沸点:分子间氢键>分子内氢键
DNA分子有两条链,链内原子之间以很强的共价键结合,链之间则是两条链上的碱基以氢键配对,许许多多的氢键将两条链连成独特的双螺旋结构,这是遗传基因复制机理的化学基础。
生物大分子中的氢键
科学 技术 社会
大家知道,羊毛织品水洗后会变形,这是什么原因呢 羊毛纤维是蛋白质构成的,蛋白质上的氨基和羰基可能会形成氢键。羊毛在浸水和干燥的过程中,会在这些氢键处纳入水和去除水,而且其变化往往是不可逆的,从而改变了原先蛋白质的构造,即原先的氢键部位可能发生移动,由此引起羊毛织品变形。
化学与生活
羊毛织品水洗后为什么会变形
1、下列关于氢键的说法中正确的是( )
A. 每个水分子内含有两个氢键
B. 在所有的水蒸气、水、冰中都含有氢键
C. 分子间能形成氢键,使物质的熔沸点升高
D. HF稳定性很强,是因为其分子间能形成氢键
C
2、下列现象与氢键有关的是( )
①HF的熔、沸点比ⅦA族其他元素氢化物的高
②乙醇可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定
⑤ 邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低
A.②③④⑤ B.①②③⑤ C.①②③④ D.①②③④⑤
B
[达标检测]
1.液态水中分子间的作用力只有氢键吗?水分子的稳定性受氢键的影响吗?
2.H2O与H2S都是由分子构成的物质,结构相似,且H2S的相对分子质量比H2O的相对分子质量大,为什么H2O的沸点比H2S的沸点高。
液态水分子之间的作用力主要是氢键,但也存在范德华力。在水分子内部存在共价键(O-H),由于H-O键键长短,键能大,故分子稳定,水分子的稳定性与氢键无关。
液态水中,水分子间既存在范德华力,又存在氢键,而气态硫化氢中,H2S分子间只存在范德华力,故水分子间作用力大于硫化氢分子间的作用力,因此,H2O的沸点比H2S的沸点高。
