2.3.3 溶解性手性 课件 (共17张PPT) 2022-2023学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 2.3.3 溶解性手性 课件 (共17张PPT) 2022-2023学年高二化学人教版(2019)选择性必修2 |  | |
| 格式 | pptx | ||
| 文件大小 | 9.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-27 15:58:43 | ||
图片预览






文档简介
(共17张PPT)
第二章 分子结构与性质
第三节 分子结构与物质的性质
第3课时 溶解性 手性
《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之”
屠呦呦团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终用乙醚在低温下成功提取了青蒿素,治疗疟疾,挽救了无数人的生命。
青蒿素
为什么需要用乙醚来提取青蒿素,用水不可以呢?
屠呦呦
【新课导入】
一、溶解性
1、“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
2、影响溶解度的因素
(2)内因
①如果溶剂和溶质之间形成氢键,则溶解度增大。
(1)外因:主要有温度、压强等
②分子结构的相似性。
乙醇化学式为CH3CH2OH,其中的羟基与水分子的羟基相近,因而乙醇能与水互溶;而戊醇CH3CH2CH2CH2CH2OH中的烃基较大,其中的—OH跟水分子的—OH的相似因素小得多了,因而它在水中的溶解度明显减小。
思考:乙醇、戊醇都是极性分子,为什么乙醇可以与水任意比例互溶,而戊醇的溶解度小?
③溶质与溶剂发生反应。
发生化学反应
形成氢键
分子的极性
分子结构的相似性
一、物质的溶解性
影响物质的溶解性的因素
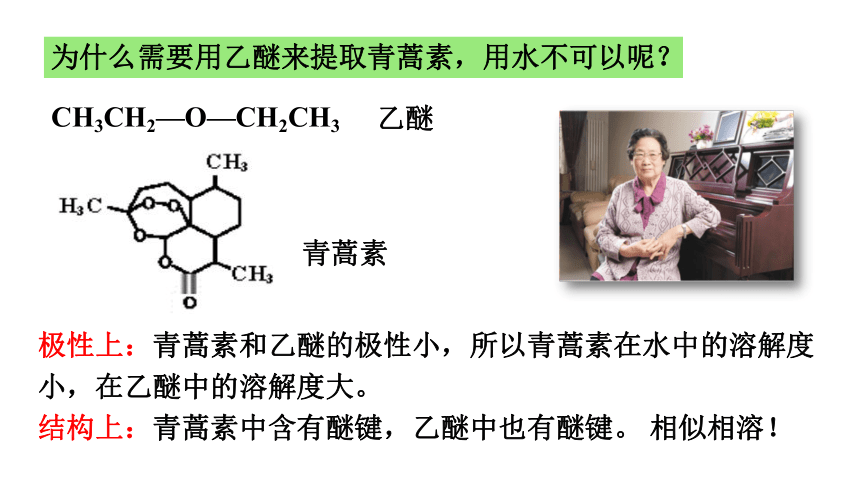
为什么需要用乙醚来提取青蒿素,用水不可以呢?
极性上:青蒿素和乙醚的极性小,所以青蒿素在水中的溶解度小,在乙醚中的溶解度大。
结构上:青蒿素中含有醚键,乙醚中也有醚键。 相似相溶!
CH3CH2—O—CH2CH3
乙醚
青蒿素
2、下列现象不能用“相似相溶”规律解释的是( )
A. 氯化氢易溶于水 B. 氯气易溶于NaOH溶液
C. 碘易溶于CCl4 D. 酒精易溶于水
1、已知 O3 的空间结构为 V 形,分子中正电中心和负电中心不重合,则下列关 于 O3 和 O2 在水中的溶解度叙述正确的是( )
A. O3 在水中的溶解度和 O2 一样 B. O3 在水中的溶解度比 O2 小
C. O3 在水中的溶解度比 O2 大 D. 无法比较
C
B
思考与讨论
1、比较NH3和CH4在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?
NH3分子在水中的溶解:
相似相溶:NH3分子和H2O分子都是极性分子。
氢 键:NH3分子与H2O分子之间形成氢键,促进了NH3的溶解。
反 应:部分NH3分子与H2O分子反应生成NH3·H2O,促进了NH3的溶解。
CH4分子在水中的溶解:
相似相溶:CH4是非极性分子,难溶于极性溶剂水中。
2、为什么在日常生活中用有机溶剂(如乙酸乙酯)溶解油漆而不用水?
油漆的主要成分
乙酸乙酯、苯、甲苯等有机溶剂
非极性或极性很小分子
思考与讨论
3、实验表明,碘在纯水还是在四氯化碳中溶解性较好?为什么?
思考与讨论
碘和四氯化碳是非极性分子,水是极性分子,根据“相似相溶”规律,所以碘在四氯化碳中溶解性较好。
在水溶液里可发生如下反应:I2+I-=I3-,故溶液紫色变浅。
具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间里不能叠合,互称手性异构体(或对映异构体)
二、分子的手性
1、手性异构体
2、手性分子:有手性异构体的分子
观察有机物分子中是否有手性碳原子(碳原子所连结的四个原子或原子团各不相同,记作﹡C )。
HOOC—CH—OH
CH3
﹡
3、手性分子的判断方法
CHFClBr
互为镜像关系的分子不能叠合,不是同种分子
绕轴旋转
不能叠合
观察实物分子与其镜像能否重合,如果不能重合,说明是手性分子。
1.下列化合物中含有手性碳原子的是( )
A.CCl2F2 B.Cl—CH—COOH
C.CH3CH2OH D.CH—OH
CH2—OH
CH2—OH
OH
B
2、 下列两分子的关系是 ( )
A.互为同分异构体 B.是同一物质
C.是手性分子 D.互为同系物
B
4、手性分子的应用
(1) 合成手性药物 (2) 合成手性催化剂
手性合成、手性催化方面做出贡献的科学家
第二章 分子结构与性质
第三节 分子结构与物质的性质
第3课时 溶解性 手性
《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之”
屠呦呦团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终用乙醚在低温下成功提取了青蒿素,治疗疟疾,挽救了无数人的生命。
青蒿素
为什么需要用乙醚来提取青蒿素,用水不可以呢?
屠呦呦
【新课导入】
一、溶解性
1、“相似相溶”规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
2、影响溶解度的因素
(2)内因
①如果溶剂和溶质之间形成氢键,则溶解度增大。
(1)外因:主要有温度、压强等
②分子结构的相似性。
乙醇化学式为CH3CH2OH,其中的羟基与水分子的羟基相近,因而乙醇能与水互溶;而戊醇CH3CH2CH2CH2CH2OH中的烃基较大,其中的—OH跟水分子的—OH的相似因素小得多了,因而它在水中的溶解度明显减小。
思考:乙醇、戊醇都是极性分子,为什么乙醇可以与水任意比例互溶,而戊醇的溶解度小?
③溶质与溶剂发生反应。
发生化学反应
形成氢键
分子的极性
分子结构的相似性
一、物质的溶解性
影响物质的溶解性的因素
为什么需要用乙醚来提取青蒿素,用水不可以呢?
极性上:青蒿素和乙醚的极性小,所以青蒿素在水中的溶解度小,在乙醚中的溶解度大。
结构上:青蒿素中含有醚键,乙醚中也有醚键。 相似相溶!
CH3CH2—O—CH2CH3
乙醚
青蒿素
2、下列现象不能用“相似相溶”规律解释的是( )
A. 氯化氢易溶于水 B. 氯气易溶于NaOH溶液
C. 碘易溶于CCl4 D. 酒精易溶于水
1、已知 O3 的空间结构为 V 形,分子中正电中心和负电中心不重合,则下列关 于 O3 和 O2 在水中的溶解度叙述正确的是( )
A. O3 在水中的溶解度和 O2 一样 B. O3 在水中的溶解度比 O2 小
C. O3 在水中的溶解度比 O2 大 D. 无法比较
C
B
思考与讨论
1、比较NH3和CH4在水中的溶解度。怎样用“相似相溶”规律理解它们的溶解度不同?
NH3分子在水中的溶解:
相似相溶:NH3分子和H2O分子都是极性分子。
氢 键:NH3分子与H2O分子之间形成氢键,促进了NH3的溶解。
反 应:部分NH3分子与H2O分子反应生成NH3·H2O,促进了NH3的溶解。
CH4分子在水中的溶解:
相似相溶:CH4是非极性分子,难溶于极性溶剂水中。
2、为什么在日常生活中用有机溶剂(如乙酸乙酯)溶解油漆而不用水?
油漆的主要成分
乙酸乙酯、苯、甲苯等有机溶剂
非极性或极性很小分子
思考与讨论
3、实验表明,碘在纯水还是在四氯化碳中溶解性较好?为什么?
思考与讨论
碘和四氯化碳是非极性分子,水是极性分子,根据“相似相溶”规律,所以碘在四氯化碳中溶解性较好。
在水溶液里可发生如下反应:I2+I-=I3-,故溶液紫色变浅。
具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间里不能叠合,互称手性异构体(或对映异构体)
二、分子的手性
1、手性异构体
2、手性分子:有手性异构体的分子
观察有机物分子中是否有手性碳原子(碳原子所连结的四个原子或原子团各不相同,记作﹡C )。
HOOC—CH—OH
CH3
﹡
3、手性分子的判断方法
CHFClBr
互为镜像关系的分子不能叠合,不是同种分子
绕轴旋转
不能叠合
观察实物分子与其镜像能否重合,如果不能重合,说明是手性分子。
1.下列化合物中含有手性碳原子的是( )
A.CCl2F2 B.Cl—CH—COOH
C.CH3CH2OH D.CH—OH
CH2—OH
CH2—OH
OH
B
2、 下列两分子的关系是 ( )
A.互为同分异构体 B.是同一物质
C.是手性分子 D.互为同系物
B
4、手性分子的应用
(1) 合成手性药物 (2) 合成手性催化剂
手性合成、手性催化方面做出贡献的科学家
