人教版(2019)高中化学必修第二册 《硅及其化合物》精品课件(共22张PPT)
文档属性
| 名称 | 人教版(2019)高中化学必修第二册 《硅及其化合物》精品课件(共22张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 30.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-29 15:40:30 | ||
图片预览







文档简介
(共22张PPT)
第1课时 硅及其化合物
第三节 无机非金属材料
我们生活中接触到的含硅及其化合物的物品
水泥
玻璃
陶瓷
通讯材料
——光导纤维(SiO2)
硅太阳能能电池(Si)
芯片的基础材料
——硅晶片(Si)
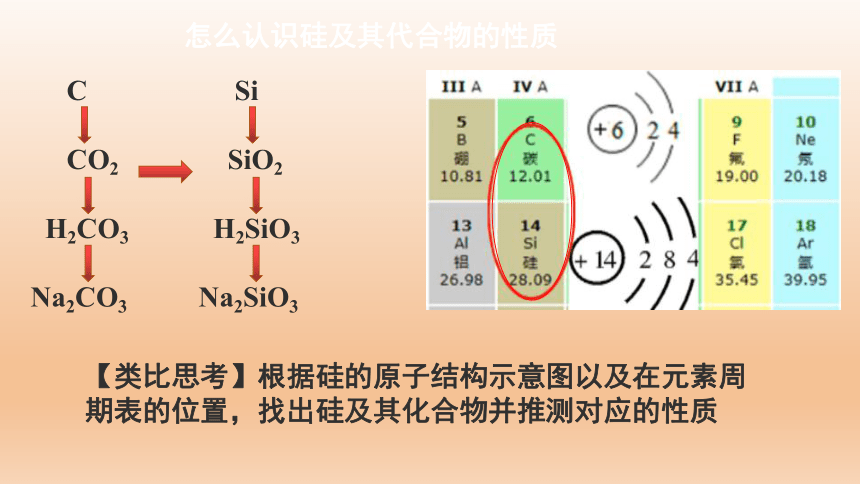
怎么认识硅及其代合物的性质
【类比思考】根据硅的原子结构示意图以及在元素周期表的位置,找出硅及其化合物并推测对应的性质
Si
SiO2
H2SiO3
Na2SiO3
C
CO2
H2CO3
Na2CO3
自然界中的碳元素既有游离态(石墨、金刚石、碳60等),又有化合态;碳的最外层都是4个电子,位于元素周期表的第IVA族,不容易失也不容易得电子,通常化学性质稳定,但在一定条件下也能与许多物质发生化学反应。
硅在自然界以什么形式存在?硅单质具有哪些性质?
硬度高、熔点高、难溶于水,化学性质稳定
C+O2(少量) 2CO
C+O2(足量) CO2
CO2 + C 2CO
C+H2O(g) CO+H2 2CuO+C 2Cu+CO2
素有“硬度之王”之称。
硅元素在地壳中含量仅次于氧,居于第二位。因有亲氧性,在自然界中它总是与氧相互化合,主要以氧化物(如水晶、玛瑙)和硅酸盐(如地壳中的大多数矿物)的形式存在。
硅在自然界中的存在
水晶
主要成分SiO2
玛瑙
主要成分SiO2
Na2SiO3泡花碱
水溶液俗称水玻璃
主要成分:
3MgO.2siO2.2H2O
蛇纹石石棉
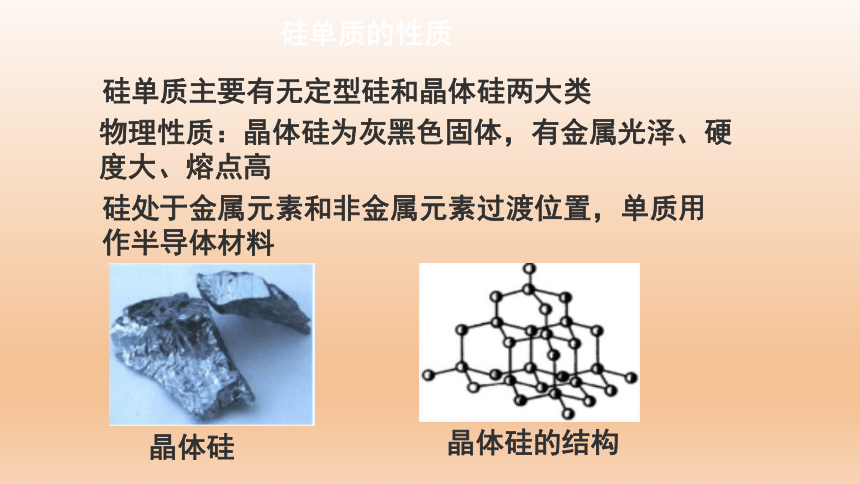
硅单质的性质
硅单质主要有无定型硅和晶体硅两大类
物理性质:晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高
硅处于金属元素和非金属元素过渡位置,单质用作半导体材料
晶体硅的结构
晶体硅
硅单质的性质
Si+2NaOH+H2O=Na2SiO3+2H2↑
化学性质:化学性质稳定,在常温下只能与氟气(F2)、HF、氢氧化钠反应,不能与H2、O2、Cl2、硫酸、硝酸等氧化剂反应,加热时能与氧气、氯气反应。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
石英砂
(主要矿物成分是SiO2)
SiO2+还原剂→Si
工业如何制备硅单质
1373K
石英砂
粗硅
SiHCl3(粗)
焦炭
高温
HCl
573K以上
粗馏
SiHCl3(纯)
高纯硅
H2
根据流程图写出涉及的主要化学反应
①SiO2+2C Si(粗)+2CO↑
②Si(粗)+3HCl=========SiHCl3+H2↑
573K以上
③SiHCl3+H2====== Si(纯)+3HCl
1373K
硅的用途
根据CO2与H2CO3的性质,推测SiO2与H2SiO3的性质,并写出相应的方程式。
SiO2具有哪些性质?
已知(1)CO2可以溶于水并生成H2CO3,作为酸性氧化物,可以与碱和碱性氧化物反应;(2)H2CO3是一种二元弱酸,能使紫色石蕊溶液变红,不稳定,受热易分解。
SiO2物理性质:常温下为固体,不溶于水,硬度大,熔、沸点高
1.不能与水反应生成硅酸
SiO2的化学性质
Si
SiO2
H2SiO3
Na2SiO3
2.具有酸性氧化物的性质
SiO2+2NaOH===Na2SiO3+H2O
SiO2+CaO CaSiO3
SiO2+Na2CO3 Na2SiO3+CO2
SiO2+CaCO3 CaSiO3+CO2
工业制玻璃
主要成分:
SiO2、CaSiO3、Na2SiO3
SiO2+4HF===SiF4↑+2H2O
特性
H2SiO3具有哪些性质?如何制备?
Si
SiO2
H2SiO3
Na2SiO3
Na2CO3+2HCl=NaCl+H2SiO3↓
硅酸是一种弱酸,比碳酸弱,不能使紫色石蕊溶液变红;不溶于水
Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
H2SiO3的制备
H2SiO3的性质
Na2CO3+2HCl=NaCl+H2SiO3↓
工业制硅胶
硅胶
(酸性干燥剂)
H2SiO3 SiO2+H2O
Na2SiO3:俗称泡花碱,水溶液显碱性,俗称水玻璃;常用作黏合剂(矿物胶),耐火阻燃材料
种类繁多的硅酸盐
Si
SiO2
H2SiO3
Na2SiO3
泡花碱
耐火胶水
SiO2+2NaOH==Na2SiO3+H2O
实验室盛放碱溶液的试剂瓶应使用橡胶塞,而不用玻璃塞
阻燃材料Na2SiO3
种类繁多的硅酸盐
主要成分:
3MgO.2SiO2.2H2O
蛇纹石石棉
黏土矿物
高岭土
主要成分
Al2O3.2SiO2.2H2O
沸石
1.下列叙述正确的是( )
A.碳、硅原子的最外层均有4个电子,易得电子表现出较强的氧化性
B.硅是构成岩石的基本元素,在地壳中的含量处于第二位
C.碳、硅在自然界中的存在都是既有游离态,又有化合态
D.碳、硅的氧化物在常温常压下均为气体
达标检测
B
2.下列关于二氧化硅的叙述正确的是( )
A.SiO2是酸性氧化物,能与水反应生成硅酸
B.SiO2能与氢氟酸反应,所以也能与盐酸反应
C.SiO2用于太阳能电池
D.SiO2与氢氧化钠反应生成的盐,储存在带橡胶塞的试剂瓶中
D
知识巩固
达标检测
A.硅酸可以通过SiO2和水化合反应直接制得
B.可用反应Na2SiO3+2HCl == 2NaCl+H2SiO3↓制取硅酸
C.因为硅酸难溶于水,所以它不能与NaOH溶液反应
D.干燥剂“硅胶”的主要成分是硅酸钠
B
达标检测
3. 下列关于硅酸的说法正确的是( )
4.氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
(1)根据以上描述,推测氮化硅可能有哪些用途:_____(填字母)。
a.制作坩埚
b.用作建筑陶瓷
c.制作耐高温轴承
d.制作切削刀具
(2)请写出氮和硅的原子结构示意图__________________,并根据元素周期律的知识,写出氮化硅的化学式______。
Si3N4
acd
达标检测
退出
第1课时 硅及其化合物
第三节 无机非金属材料
我们生活中接触到的含硅及其化合物的物品
水泥
玻璃
陶瓷
通讯材料
——光导纤维(SiO2)
硅太阳能能电池(Si)
芯片的基础材料
——硅晶片(Si)
怎么认识硅及其代合物的性质
【类比思考】根据硅的原子结构示意图以及在元素周期表的位置,找出硅及其化合物并推测对应的性质
Si
SiO2
H2SiO3
Na2SiO3
C
CO2
H2CO3
Na2CO3
自然界中的碳元素既有游离态(石墨、金刚石、碳60等),又有化合态;碳的最外层都是4个电子,位于元素周期表的第IVA族,不容易失也不容易得电子,通常化学性质稳定,但在一定条件下也能与许多物质发生化学反应。
硅在自然界以什么形式存在?硅单质具有哪些性质?
硬度高、熔点高、难溶于水,化学性质稳定
C+O2(少量) 2CO
C+O2(足量) CO2
CO2 + C 2CO
C+H2O(g) CO+H2 2CuO+C 2Cu+CO2
素有“硬度之王”之称。
硅元素在地壳中含量仅次于氧,居于第二位。因有亲氧性,在自然界中它总是与氧相互化合,主要以氧化物(如水晶、玛瑙)和硅酸盐(如地壳中的大多数矿物)的形式存在。
硅在自然界中的存在
水晶
主要成分SiO2
玛瑙
主要成分SiO2
Na2SiO3泡花碱
水溶液俗称水玻璃
主要成分:
3MgO.2siO2.2H2O
蛇纹石石棉
硅单质的性质
硅单质主要有无定型硅和晶体硅两大类
物理性质:晶体硅为灰黑色固体,有金属光泽、硬度大、熔点高
硅处于金属元素和非金属元素过渡位置,单质用作半导体材料
晶体硅的结构
晶体硅
硅单质的性质
Si+2NaOH+H2O=Na2SiO3+2H2↑
化学性质:化学性质稳定,在常温下只能与氟气(F2)、HF、氢氧化钠反应,不能与H2、O2、Cl2、硫酸、硝酸等氧化剂反应,加热时能与氧气、氯气反应。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
石英砂
(主要矿物成分是SiO2)
SiO2+还原剂→Si
工业如何制备硅单质
1373K
石英砂
粗硅
SiHCl3(粗)
焦炭
高温
HCl
573K以上
粗馏
SiHCl3(纯)
高纯硅
H2
根据流程图写出涉及的主要化学反应
①SiO2+2C Si(粗)+2CO↑
②Si(粗)+3HCl=========SiHCl3+H2↑
573K以上
③SiHCl3+H2====== Si(纯)+3HCl
1373K
硅的用途
根据CO2与H2CO3的性质,推测SiO2与H2SiO3的性质,并写出相应的方程式。
SiO2具有哪些性质?
已知(1)CO2可以溶于水并生成H2CO3,作为酸性氧化物,可以与碱和碱性氧化物反应;(2)H2CO3是一种二元弱酸,能使紫色石蕊溶液变红,不稳定,受热易分解。
SiO2物理性质:常温下为固体,不溶于水,硬度大,熔、沸点高
1.不能与水反应生成硅酸
SiO2的化学性质
Si
SiO2
H2SiO3
Na2SiO3
2.具有酸性氧化物的性质
SiO2+2NaOH===Na2SiO3+H2O
SiO2+CaO CaSiO3
SiO2+Na2CO3 Na2SiO3+CO2
SiO2+CaCO3 CaSiO3+CO2
工业制玻璃
主要成分:
SiO2、CaSiO3、Na2SiO3
SiO2+4HF===SiF4↑+2H2O
特性
H2SiO3具有哪些性质?如何制备?
Si
SiO2
H2SiO3
Na2SiO3
Na2CO3+2HCl=NaCl+H2SiO3↓
硅酸是一种弱酸,比碳酸弱,不能使紫色石蕊溶液变红;不溶于水
Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3
H2SiO3的制备
H2SiO3的性质
Na2CO3+2HCl=NaCl+H2SiO3↓
工业制硅胶
硅胶
(酸性干燥剂)
H2SiO3 SiO2+H2O
Na2SiO3:俗称泡花碱,水溶液显碱性,俗称水玻璃;常用作黏合剂(矿物胶),耐火阻燃材料
种类繁多的硅酸盐
Si
SiO2
H2SiO3
Na2SiO3
泡花碱
耐火胶水
SiO2+2NaOH==Na2SiO3+H2O
实验室盛放碱溶液的试剂瓶应使用橡胶塞,而不用玻璃塞
阻燃材料Na2SiO3
种类繁多的硅酸盐
主要成分:
3MgO.2SiO2.2H2O
蛇纹石石棉
黏土矿物
高岭土
主要成分
Al2O3.2SiO2.2H2O
沸石
1.下列叙述正确的是( )
A.碳、硅原子的最外层均有4个电子,易得电子表现出较强的氧化性
B.硅是构成岩石的基本元素,在地壳中的含量处于第二位
C.碳、硅在自然界中的存在都是既有游离态,又有化合态
D.碳、硅的氧化物在常温常压下均为气体
达标检测
B
2.下列关于二氧化硅的叙述正确的是( )
A.SiO2是酸性氧化物,能与水反应生成硅酸
B.SiO2能与氢氟酸反应,所以也能与盐酸反应
C.SiO2用于太阳能电池
D.SiO2与氢氧化钠反应生成的盐,储存在带橡胶塞的试剂瓶中
D
知识巩固
达标检测
A.硅酸可以通过SiO2和水化合反应直接制得
B.可用反应Na2SiO3+2HCl == 2NaCl+H2SiO3↓制取硅酸
C.因为硅酸难溶于水,所以它不能与NaOH溶液反应
D.干燥剂“硅胶”的主要成分是硅酸钠
B
达标检测
3. 下列关于硅酸的说法正确的是( )
4.氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。
(1)根据以上描述,推测氮化硅可能有哪些用途:_____(填字母)。
a.制作坩埚
b.用作建筑陶瓷
c.制作耐高温轴承
d.制作切削刀具
(2)请写出氮和硅的原子结构示意图__________________,并根据元素周期律的知识,写出氮化硅的化学式______。
Si3N4
acd
达标检测
退出
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
