【备考2023】浙教版科学中考核心考点训练(十六):空气【word,含解析】
文档属性
| 名称 | 【备考2023】浙教版科学中考核心考点训练(十六):空气【word,含解析】 |
|
|
| 格式 | docx | ||
| 文件大小 | 187.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-03-28 00:00:00 | ||
图片预览


文档简介
空气
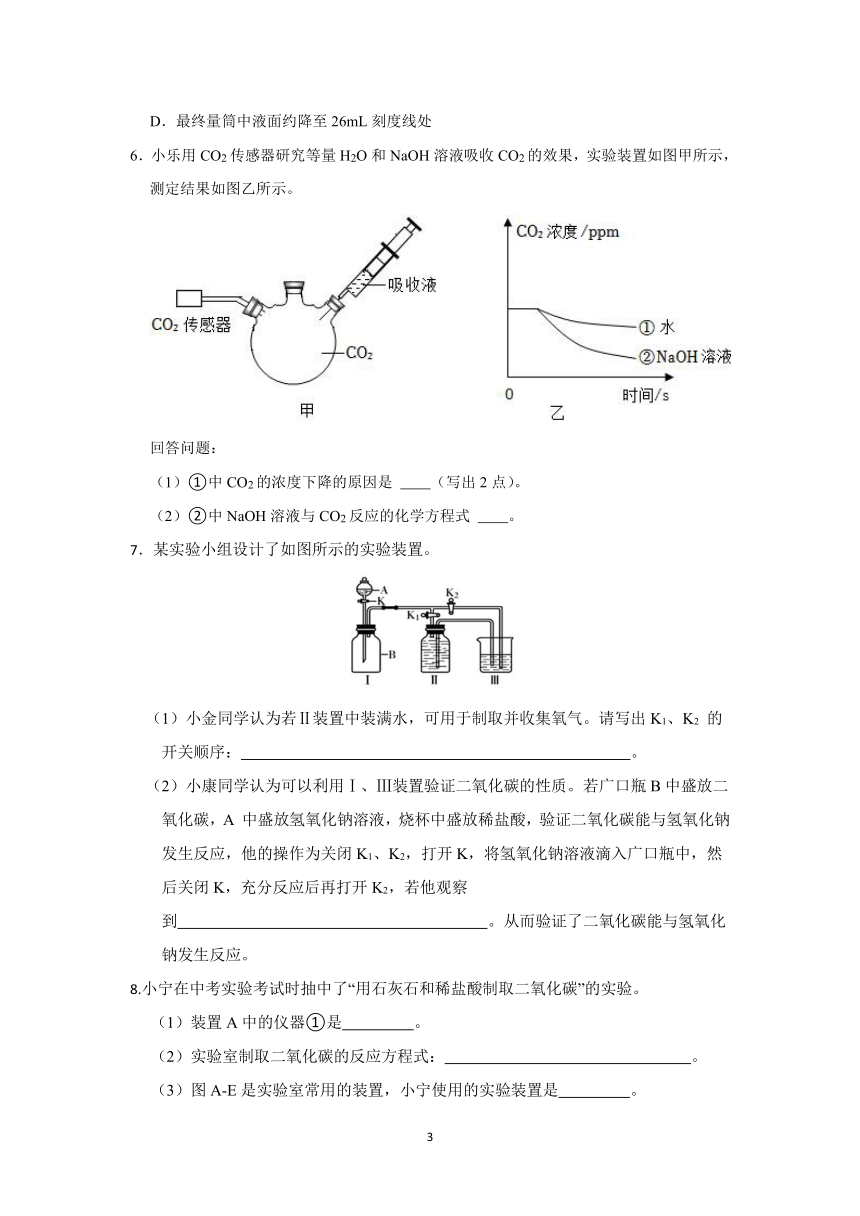
1.在做测定空气中氧气含量的实验时,需要一个如图所示的集气瓶。下列将集气瓶剩余的容积划为5等份的做法中,正确的是( )
A.用尺量出集气瓶中剩余容积的高度,平均分成等距的5等份
B.在集气瓶的剩余容积中,每倒入50ml水画一条线,标上1、2、3、4
C.先在集气瓶中装满水,然后把水全倒入量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4
D.先将集气瓶装满水,倒出部分水于量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4
2.如图,集气瓶中充满二氧化碳,大烧杯中燃着2支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
A.将观察到高的蜡烛先熄灭
B.不移开玻璃片,实验现象更明显
C.蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点
D.去掉烧杯中的1支蜡烛,也能得出同样的实验结论
3.小金用如图所示的装置测定石灰石样品中碳酸钙的质量分数,他加入足量的稀盐酸后,测得C装置中二氧化碳的体积,换算成质量后,再根据化学方程式计算碳酸钙的质量,从而测出石灰石中碳酸钙的质量分数。对该实验方案评价合理的是( )
A.稀盐酸换成稀硫酸也可以完成本实验
B.A装置中残留的二氧化碳对实验结果没影响
C.装置C在开始收集气体前必须装满液体
D.油层的作用是防止装置C中的水分蒸发
4.瑞典皇家科学院于2021年10月6日宣布,德国科学家Benjamin List和美国科学家DavidMacMillan因开发一种精确的分子构建新工具——不对 称有机催化剂而获得2021年诺贝尔化学奖。催化剂被称为化学家的“基本工具”。长期以来研究人员认为,原则上只有两种催化剂可用:金属和酶,但此次摘得桂冠的两位科学家独立开发出的第三种催化剂——不对称有机催化剂,利用它研究人员可以有效地构建很多物质,为人类带来了实实在在的福祉。以下有关催化剂的说法错误的是( )
A.催化剂的作用是改变化学反应速率
B.催化剂在化学反应前后的质量不变
C.催化剂在化学反应前后的物理性质保持不变
D.催化剂在化学反应前后的化学性质保持不变
5.利用如图装置验证空气中氧气的含量。下列叙述正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是燃烧放热
C.白磷熄火立即打开止水夹
D.最终量筒中液面约降至26mL刻度线处
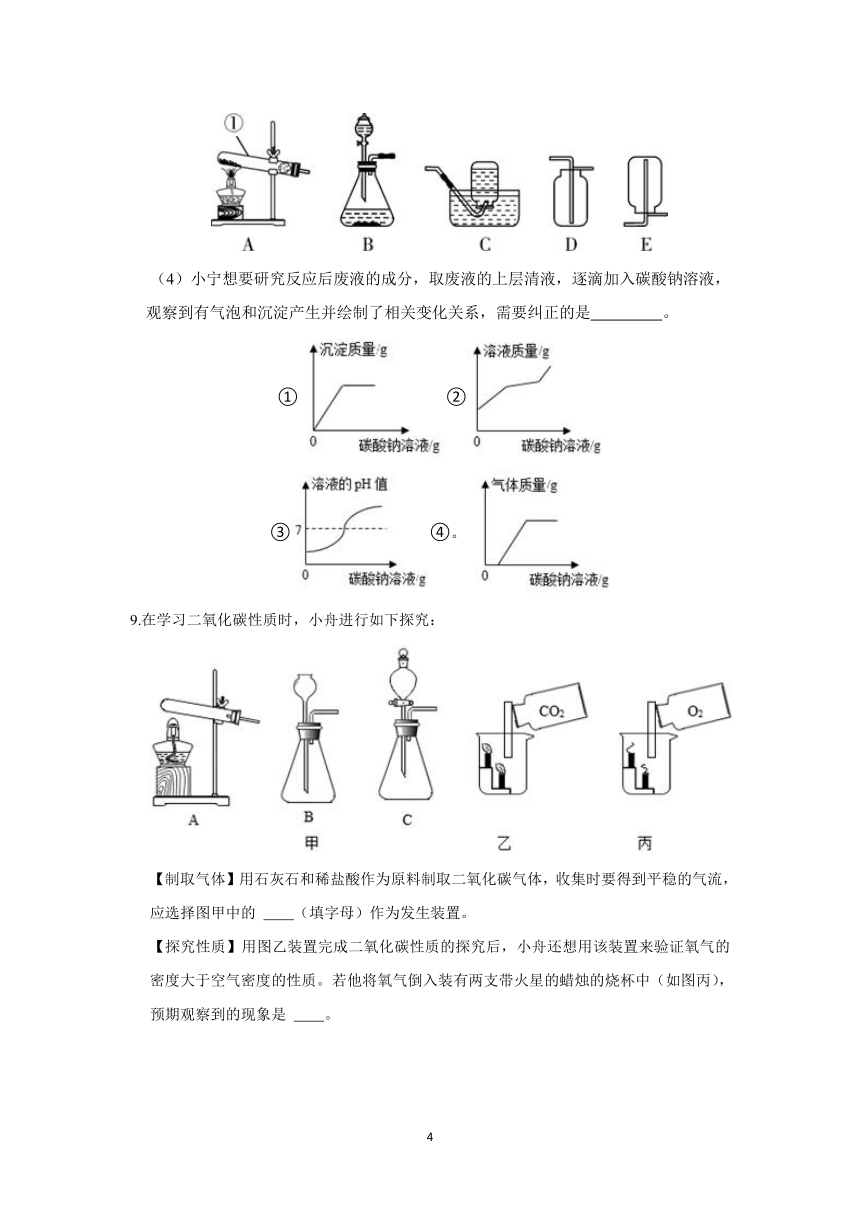
6.小乐用CO2传感器研究等量H2O和NaOH溶液吸收CO2的效果,实验装置如图甲所示,测定结果如图乙所示。
回答问题:
(1)①中CO2的浓度下降的原因是 (写出2点)。
(2)②中NaOH溶液与CO2反应的化学方程式 。
7.某实验小组设计了如图所示的实验装置。
(1)小金同学认为若Ⅱ装置中装满水,可用于制取并收集氧气。请写出K1、K2 的开关顺序: 。
(2)小康同学认为可以利用Ⅰ、Ⅲ装置验证二氧化碳的性质。若广口瓶B中盛放二氧化碳,A 中盛放氢氧化钠溶液,烧杯中盛放稀盐酸,验证二氧化碳能与氢氧化钠发生反应,他的操作为关闭K1、K2,打开K,将氢氧化钠溶液滴入广口瓶中,然后关闭K,充分反应后再打开K2,若他观察到 。从而验证了二氧化碳能与氢氧化钠发生反应。
8.小宁在中考实验考试时抽中了“用石灰石和稀盐酸制取二氧化碳”的实验。
(1)装置A中的仪器①是 。
(2)实验室制取二氧化碳的反应方程式: 。
(3)图A-E是实验室常用的装置,小宁使用的实验装置是 。
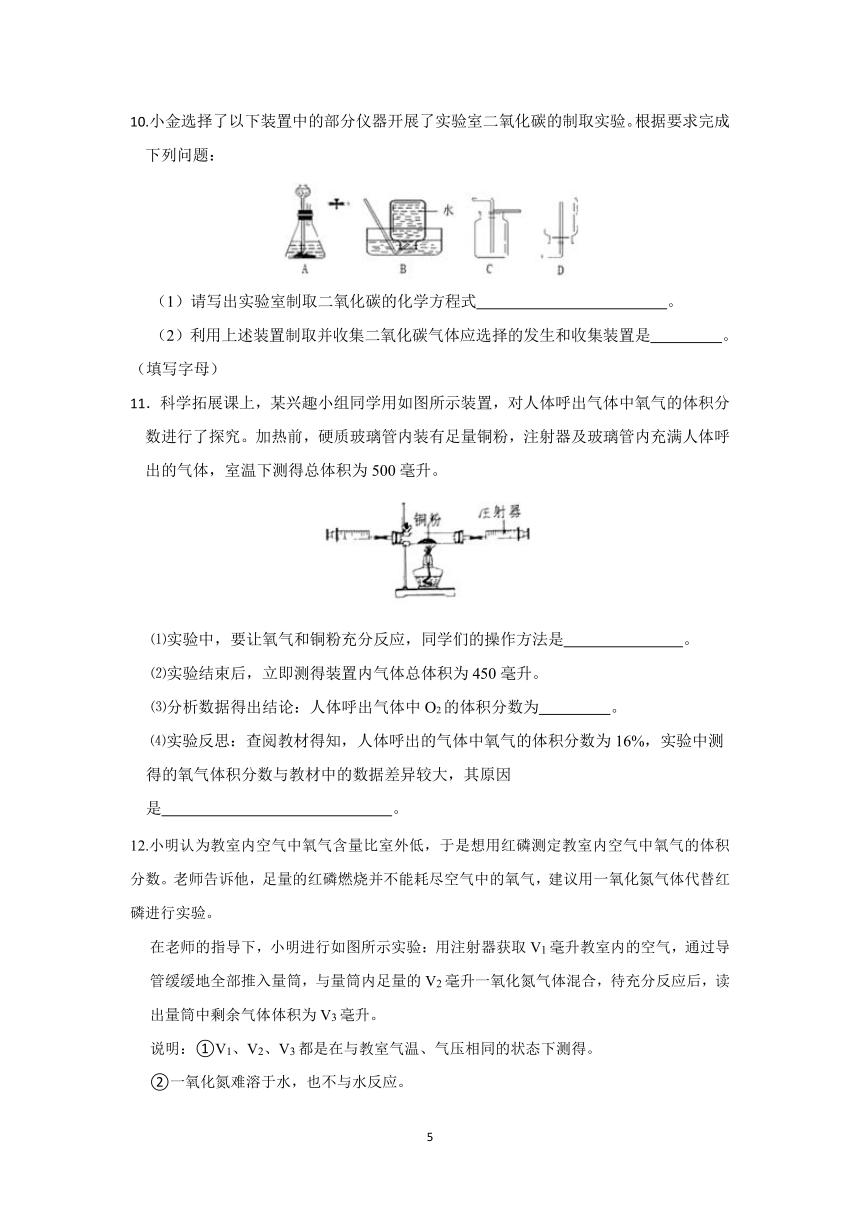
(4)小宁想要研究反应后废液的成分,取废液的上层清液,逐滴加入碳酸钠溶液,观察到有气泡和沉淀产生并绘制了相关变化关系,需要纠正的是 。
①②
③④。
9.在学习二氧化碳性质时,小舟进行如下探究:
【制取气体】用石灰石和稀盐酸作为原料制取二氧化碳气体,收集时要得到平稳的气流,应选择图甲中的 (填字母)作为发生装置。
【探究性质】用图乙装置完成二氧化碳性质的探究后,小舟还想用该装置来验证氧气的密度大于空气密度的性质。若他将氧气倒入装有两支带火星的蜡烛的烧杯中(如图丙),预期观察到的现象是 。
10.小金选择了以下装置中的部分仪器开展了实验室二氧化碳的制取实验。根据要求完成下列问题:
(1)请写出实验室制取二氧化碳的化学方程式 。
(2)利用上述装置制取并收集二氧化碳气体应选择的发生和收集装置是 。(填写字母)
11.科学拓展课上,某兴趣小组同学用如图所示装置,对人体呼出气体中氧气的体积分数进行了探究。加热前,硬质玻璃管内装有足量铜粉,注射器及玻璃管内充满人体呼出的气体,室温下测得总体积为500毫升。
⑴实验中,要让氧气和铜粉充分反应,同学们的操作方法是 。
⑵实验结束后,立即测得装置内气体总体积为450毫升。
⑶分析数据得出结论:人体呼出气体中O2的体积分数为 。
⑷实验反思:查阅教材得知,人体呼出的气体中氧气的体积分数为16%,实验中测得的氧气体积分数与教材中的数据差异较大,其原因是 。
12.小明认为教室内空气中氧气含量比室外低,于是想用红磷测定教室内空气中氧气的体积分数。老师告诉他,足量的红磷燃烧并不能耗尽空气中的氧气,建议用一氧化氮气体代替红磷进行实验。
在老师的指导下,小明进行如图所示实验:用注射器获取V1毫升教室内的空气,通过导管缓缓地全部推入量筒,与量筒内足量的V2毫升一氧化氮气体混合,待充分反应后,读出量筒中剩余气体体积为V3毫升。
说明:①V1、V2、V3都是在与教室气温、气压相同的状态下测得。
②一氧化氮难溶于水,也不与水反应。
③同温同压下,在氢氧化钠溶液参与下,4体积一氧化氮与3体积氧气恰好完全反应,且产物能完全被溶液吸收。
(1)小明用气密性良好的注射器,获取V1毫升教室内空气的具体操作是 。
(2)实验测得教室内空气中氧气的体积分数为 。(用V1、V2、V3表示)
(3)小明提出,注射器内空气中的二氧化碳也会被氢氧化钠溶液吸收,从而影响实验结果。但老师指出,相比空气中的氧气含量,二氧化碳对实验结果的影响属于“次要因素”,不是“主要因素”,可忽略不计。还有许多科学实验中存在“主要因素”和“次要因素”,请再举一例并指明次要因素。
答案及解析
1.D
【解析】A.集气瓶上口小下面大,不是规则的圆柱体,即它的容积与高度不成正比,故A错误;
B.如果剩余的容积恰好是200mL,那么每倒入50mL画一条线是可以的,但是没法保证剩余的容积是200ml,故B错误;
C.为了防止燃烧时滴落物烧坏集气瓶,里面要留部分水,不能全部倒入量筒,故C错误;
D.先将集气瓶装满水,倒出部分水于量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4,故D正确。 故选D。
2.解:A.由于二氧化碳的密度比空气大,且不燃烧也不支持燃烧,将观察到低的蜡烛先熄灭,故A错误;
B.如果不将玻璃片拿下,集气瓶中的二氧化碳形不成压强差,不会流下进入烧杯内,蜡烛不会熄灭,故B错误;
C.蜡烛会熄灭,是因为二氧化碳覆盖在蜡烛表面,隔绝了空气,故C错误;
D.由题干所给装置可知,二氧化碳从高处流到烧杯中,说明二氧化碳的密度比空气的大,蜡烛熄灭说明二氧化碳不能燃烧,也不支持燃烧,故D正确。
故选:D。
3.解:A、硫酸和碳酸钙反应生成微溶于水的硫酸钙覆盖在大理石表面,阻碍反应的继续进行来判断,所以稀盐酸不能换成稀硫酸,故A错误;
B、碳酸钙和盐酸反应生成多少二氧化碳,就会排出多少气体,所以A装置中残留的二氧化碳对实验结果不会产生影响,故B正确;
C、排出水的体积就是生成二氧化碳的体积,所以装置C在开始收集气体前可以不装满液体,故C错误;
D、二氧化碳和水反应生成会生成碳酸,二氧化碳溶于水,所以油层的作用是防止二氧化碳和水反应,二氧化碳溶于水,故D错误。
故选:B。
4.C
【解析】催化剂是改变其它物质的反应速率,而本身质量和化学性质不变的物质; 故选C。
5.解:A、该装置是利用白磷燃烧消耗装置内的氧气,反应后,装置内压强减小,由于存在压强差,量筒中的水进入试管,进入水的体积等于空气中氧气的体积,所以实验前需检查装置的气密性,防止装置漏气,外界空气进入,会使实验结果偏小,故A正确;
B、白磷的作用是将试管内的氧气耗尽,使装置内的压强减小,由于存在压强差,量筒中的水进入试管,进入水的体积就是空气中氧气的体积,故B错误;
C、白磷熄灭,试管冷却至室温后,再打开止水夹,否则,试管内的气体受热膨胀,占据了一定的空间,会使进入水的体积偏小,从而使实验结果偏小,故C错误;
D、空气中氧气的体积约占空气体积的五分之一,故进入水的体积大约是:130mL26mL,故最终量筒中液面约降至50mL﹣26mL=24mL刻度线处,故D错误。
故选:A。
6.解:(1)①中CO2的浓度下降的原因是二氧化碳溶于水,和水反应生成碳酸。
故答案为:二氧化碳溶于水,和水反应生成碳酸。
(2)②中NaOH与CO2反应生成碳酸钠和水,反应的化学方程式是2NaOH+CO2═Na2CO3+H2O。
故答案为:2NaOH+CO2═Na2CO3+H2O。
7.(1)先打开K2,关闭K1,一段时间后再打开K1,关闭K2(2)Ⅲ中稀盐酸倒流入Ⅰ中,且有气泡产生
【解析】(1) 若Ⅱ装置中装满水,用排水法收集氧气时,需先打开K2,关闭K1,让分液漏斗中液体流下,反应发生,且排出装置内空气,一段时间后再打开K1,关闭K2,收集气体;
(2)二氧化碳与氢氧化钠反应生成碳酸钠和水,并使得I中压强减小, Ⅲ中稀盐酸会被吸入I中,并与生成的碳酸钠反应产生二氧化碳气体,所以观察到的现象为Ⅲ中稀盐酸倒流入Ⅰ中,且有气泡产生。
8.(1)试管(2)CaCO3+2HCl=CaCl2+CO2↑+H2O(3)BC(4)①③④
【解析】(1)装置A中仪器①是试管。
(2)实验室制取二氧化碳原理是碳酸钙与盐酸反应,方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O .
(3)制取二氧化碳需选择固液常温型发生装置,选择向上排空气法收集,即BC组合。
(4) 取废液的上层清液,逐滴加入碳酸钠溶液,观察到有气泡和沉淀产生,说明废液中含有为氯化钙和盐酸,加入碳酸钠时,碳酸钠先与盐酸反应,然后再与氯化钙反应,所以沉淀需在加入碳酸钠一定量之后才产生,①错误;由方程式可知,碳酸钠与盐酸反应时产生二氧化碳质量小于所加碳酸钠的质量,碳酸钠与氯化钙反应时,产生碳酸钙质量虽小于所加碳酸钠质量,但溶液增加趋势要小于碳酸钠与盐酸的反应,当碳酸钠过量后,不再发生反应,溶液增加质量即为所加碳酸钠质量,所以溶液始终是增加趋势,且增加趋势先快后慢,再快, ②正确;最初溶液呈酸性,pH小于7,加入碳酸钠后,盐酸先反应,溶液pH增加,于等于7后,盐酸反应结束,氯化钙与碳酸钠反应,此时溶液pH保持7不变,当氯化钙完全反应后,继续加碳酸钠,溶液pH又增加, ③错误;碳酸钠先与盐酸反应,气体质量增加,且起点应从原点开始,④错误。
9.(1)用石灰石和稀盐酸作为原料制取二氧化碳气体,属于固液常温型制备气体,要得到平稳的气流,应控制液体的滴加速率,应选择图甲中的C,能通过分液漏斗控制滴加液体的速率,从而控制反应的速率;故答案为C;
(2)氧气具有助燃性,将氧气倒入装有两支带火星的蜡烛的烧杯中,氧气的密度比空气的大,且能支持燃烧,因此能观察到蜡烛自下而上复燃,故答案为蜡烛自下而上复燃。
10.(1)CaCO3+2HCl=CaCl2+CO2↑+H2O(2)AC
【解析】(1)实验室利用石灰石或大理石与稀盐酸反应制取二氧化碳,反应方程式为 CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)二氧化碳制取需用固液常温型发生装置,即A,二氧化碳能溶于水且能与水反应,密度比空气大,所以应选择向上排空气法收集,即C装置;
11.加热时反复推拉左右两侧的注射器,直至气体体积不再减少;10%;装置内的气体未冷却至室温
【解析】(1)加热时反复推拉左右两侧的注射器,直至气体体积不再减少,可使铜和氧气充分接触发生反应。
(3)原气体体积为500毫升,实验结束后,立即测得装置内气体总体积为450毫升,即减少了50毫升,减少体积即为消耗的氧气体积,则氧气体积分数为10%。
(4) 实验结束后,立即测得装置内气体总体积 ,装置内气体未冷却至室温,会使得实验结果偏小。
12.解:(1)用气密性良好的注射器,获取V1毫升教室内空气的具体操作是在教室外,将注射器活塞推到底,将注射器拿到教室,再拉动活塞至刻度为V1毫升处并密封。
(2)用注射器获取V1毫升教室内的空气,通过导管缓缓地全部推入量筒,与量筒内足量的V2毫升一氧化氮气体混合,待充分反应后,读出量筒中剩余气体体积为V3毫升。则一共消耗一氧化氮和氧气体积为V1+V2﹣V3;由题干信息:同温同压下,在氢氧化钠溶液参与下,4体积一氧化氮与3体积氧气恰好完全反应,且产物能完全被溶液吸收,故氧气体积为(V1+V2﹣V3);教室内空气中氧气的体积分数为100%100%;
(3)在探究影响重力势能大小的因素实验中,空气阻力是次要因素(其它合理答案也给分)。
故答案为:(1)在教室外,将注射器活塞推到底,将注射器拿到教室,再拉动活塞至刻度为V1毫升处并密封;
(2)100%;
(3)在探究影响重力势能大小的因素实验中,空气阻力是次要因素(合理即可)。
(
1
)
1.在做测定空气中氧气含量的实验时,需要一个如图所示的集气瓶。下列将集气瓶剩余的容积划为5等份的做法中,正确的是( )
A.用尺量出集气瓶中剩余容积的高度,平均分成等距的5等份
B.在集气瓶的剩余容积中,每倒入50ml水画一条线,标上1、2、3、4
C.先在集气瓶中装满水,然后把水全倒入量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4
D.先将集气瓶装满水,倒出部分水于量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4
2.如图,集气瓶中充满二氧化碳,大烧杯中燃着2支高低不等的蜡烛,实验时打开止水夹,移开玻璃片。下列说法正确的是( )
A.将观察到高的蜡烛先熄灭
B.不移开玻璃片,实验现象更明显
C.蜡烛会熄灭,是因为二氧化碳降低了蜡烛的着火点
D.去掉烧杯中的1支蜡烛,也能得出同样的实验结论
3.小金用如图所示的装置测定石灰石样品中碳酸钙的质量分数,他加入足量的稀盐酸后,测得C装置中二氧化碳的体积,换算成质量后,再根据化学方程式计算碳酸钙的质量,从而测出石灰石中碳酸钙的质量分数。对该实验方案评价合理的是( )
A.稀盐酸换成稀硫酸也可以完成本实验
B.A装置中残留的二氧化碳对实验结果没影响
C.装置C在开始收集气体前必须装满液体
D.油层的作用是防止装置C中的水分蒸发
4.瑞典皇家科学院于2021年10月6日宣布,德国科学家Benjamin List和美国科学家DavidMacMillan因开发一种精确的分子构建新工具——不对 称有机催化剂而获得2021年诺贝尔化学奖。催化剂被称为化学家的“基本工具”。长期以来研究人员认为,原则上只有两种催化剂可用:金属和酶,但此次摘得桂冠的两位科学家独立开发出的第三种催化剂——不对称有机催化剂,利用它研究人员可以有效地构建很多物质,为人类带来了实实在在的福祉。以下有关催化剂的说法错误的是( )
A.催化剂的作用是改变化学反应速率
B.催化剂在化学反应前后的质量不变
C.催化剂在化学反应前后的物理性质保持不变
D.催化剂在化学反应前后的化学性质保持不变
5.利用如图装置验证空气中氧气的含量。下列叙述正确的是( )
A.实验前需检查装置气密性
B.白磷的作用是燃烧放热
C.白磷熄火立即打开止水夹
D.最终量筒中液面约降至26mL刻度线处
6.小乐用CO2传感器研究等量H2O和NaOH溶液吸收CO2的效果,实验装置如图甲所示,测定结果如图乙所示。
回答问题:
(1)①中CO2的浓度下降的原因是 (写出2点)。
(2)②中NaOH溶液与CO2反应的化学方程式 。
7.某实验小组设计了如图所示的实验装置。
(1)小金同学认为若Ⅱ装置中装满水,可用于制取并收集氧气。请写出K1、K2 的开关顺序: 。
(2)小康同学认为可以利用Ⅰ、Ⅲ装置验证二氧化碳的性质。若广口瓶B中盛放二氧化碳,A 中盛放氢氧化钠溶液,烧杯中盛放稀盐酸,验证二氧化碳能与氢氧化钠发生反应,他的操作为关闭K1、K2,打开K,将氢氧化钠溶液滴入广口瓶中,然后关闭K,充分反应后再打开K2,若他观察到 。从而验证了二氧化碳能与氢氧化钠发生反应。
8.小宁在中考实验考试时抽中了“用石灰石和稀盐酸制取二氧化碳”的实验。
(1)装置A中的仪器①是 。
(2)实验室制取二氧化碳的反应方程式: 。
(3)图A-E是实验室常用的装置,小宁使用的实验装置是 。
(4)小宁想要研究反应后废液的成分,取废液的上层清液,逐滴加入碳酸钠溶液,观察到有气泡和沉淀产生并绘制了相关变化关系,需要纠正的是 。
①②
③④。
9.在学习二氧化碳性质时,小舟进行如下探究:
【制取气体】用石灰石和稀盐酸作为原料制取二氧化碳气体,收集时要得到平稳的气流,应选择图甲中的 (填字母)作为发生装置。
【探究性质】用图乙装置完成二氧化碳性质的探究后,小舟还想用该装置来验证氧气的密度大于空气密度的性质。若他将氧气倒入装有两支带火星的蜡烛的烧杯中(如图丙),预期观察到的现象是 。
10.小金选择了以下装置中的部分仪器开展了实验室二氧化碳的制取实验。根据要求完成下列问题:
(1)请写出实验室制取二氧化碳的化学方程式 。
(2)利用上述装置制取并收集二氧化碳气体应选择的发生和收集装置是 。(填写字母)
11.科学拓展课上,某兴趣小组同学用如图所示装置,对人体呼出气体中氧气的体积分数进行了探究。加热前,硬质玻璃管内装有足量铜粉,注射器及玻璃管内充满人体呼出的气体,室温下测得总体积为500毫升。
⑴实验中,要让氧气和铜粉充分反应,同学们的操作方法是 。
⑵实验结束后,立即测得装置内气体总体积为450毫升。
⑶分析数据得出结论:人体呼出气体中O2的体积分数为 。
⑷实验反思:查阅教材得知,人体呼出的气体中氧气的体积分数为16%,实验中测得的氧气体积分数与教材中的数据差异较大,其原因是 。
12.小明认为教室内空气中氧气含量比室外低,于是想用红磷测定教室内空气中氧气的体积分数。老师告诉他,足量的红磷燃烧并不能耗尽空气中的氧气,建议用一氧化氮气体代替红磷进行实验。
在老师的指导下,小明进行如图所示实验:用注射器获取V1毫升教室内的空气,通过导管缓缓地全部推入量筒,与量筒内足量的V2毫升一氧化氮气体混合,待充分反应后,读出量筒中剩余气体体积为V3毫升。
说明:①V1、V2、V3都是在与教室气温、气压相同的状态下测得。
②一氧化氮难溶于水,也不与水反应。
③同温同压下,在氢氧化钠溶液参与下,4体积一氧化氮与3体积氧气恰好完全反应,且产物能完全被溶液吸收。
(1)小明用气密性良好的注射器,获取V1毫升教室内空气的具体操作是 。
(2)实验测得教室内空气中氧气的体积分数为 。(用V1、V2、V3表示)
(3)小明提出,注射器内空气中的二氧化碳也会被氢氧化钠溶液吸收,从而影响实验结果。但老师指出,相比空气中的氧气含量,二氧化碳对实验结果的影响属于“次要因素”,不是“主要因素”,可忽略不计。还有许多科学实验中存在“主要因素”和“次要因素”,请再举一例并指明次要因素。
答案及解析
1.D
【解析】A.集气瓶上口小下面大,不是规则的圆柱体,即它的容积与高度不成正比,故A错误;
B.如果剩余的容积恰好是200mL,那么每倒入50mL画一条线是可以的,但是没法保证剩余的容积是200ml,故B错误;
C.为了防止燃烧时滴落物烧坏集气瓶,里面要留部分水,不能全部倒入量筒,故C错误;
D.先将集气瓶装满水,倒出部分水于量筒中,将其体积5等分,每倒入集气瓶中1份,在集气瓶上画一条线,标上1、2、3、4,故D正确。 故选D。
2.解:A.由于二氧化碳的密度比空气大,且不燃烧也不支持燃烧,将观察到低的蜡烛先熄灭,故A错误;
B.如果不将玻璃片拿下,集气瓶中的二氧化碳形不成压强差,不会流下进入烧杯内,蜡烛不会熄灭,故B错误;
C.蜡烛会熄灭,是因为二氧化碳覆盖在蜡烛表面,隔绝了空气,故C错误;
D.由题干所给装置可知,二氧化碳从高处流到烧杯中,说明二氧化碳的密度比空气的大,蜡烛熄灭说明二氧化碳不能燃烧,也不支持燃烧,故D正确。
故选:D。
3.解:A、硫酸和碳酸钙反应生成微溶于水的硫酸钙覆盖在大理石表面,阻碍反应的继续进行来判断,所以稀盐酸不能换成稀硫酸,故A错误;
B、碳酸钙和盐酸反应生成多少二氧化碳,就会排出多少气体,所以A装置中残留的二氧化碳对实验结果不会产生影响,故B正确;
C、排出水的体积就是生成二氧化碳的体积,所以装置C在开始收集气体前可以不装满液体,故C错误;
D、二氧化碳和水反应生成会生成碳酸,二氧化碳溶于水,所以油层的作用是防止二氧化碳和水反应,二氧化碳溶于水,故D错误。
故选:B。
4.C
【解析】催化剂是改变其它物质的反应速率,而本身质量和化学性质不变的物质; 故选C。
5.解:A、该装置是利用白磷燃烧消耗装置内的氧气,反应后,装置内压强减小,由于存在压强差,量筒中的水进入试管,进入水的体积等于空气中氧气的体积,所以实验前需检查装置的气密性,防止装置漏气,外界空气进入,会使实验结果偏小,故A正确;
B、白磷的作用是将试管内的氧气耗尽,使装置内的压强减小,由于存在压强差,量筒中的水进入试管,进入水的体积就是空气中氧气的体积,故B错误;
C、白磷熄灭,试管冷却至室温后,再打开止水夹,否则,试管内的气体受热膨胀,占据了一定的空间,会使进入水的体积偏小,从而使实验结果偏小,故C错误;
D、空气中氧气的体积约占空气体积的五分之一,故进入水的体积大约是:130mL26mL,故最终量筒中液面约降至50mL﹣26mL=24mL刻度线处,故D错误。
故选:A。
6.解:(1)①中CO2的浓度下降的原因是二氧化碳溶于水,和水反应生成碳酸。
故答案为:二氧化碳溶于水,和水反应生成碳酸。
(2)②中NaOH与CO2反应生成碳酸钠和水,反应的化学方程式是2NaOH+CO2═Na2CO3+H2O。
故答案为:2NaOH+CO2═Na2CO3+H2O。
7.(1)先打开K2,关闭K1,一段时间后再打开K1,关闭K2(2)Ⅲ中稀盐酸倒流入Ⅰ中,且有气泡产生
【解析】(1) 若Ⅱ装置中装满水,用排水法收集氧气时,需先打开K2,关闭K1,让分液漏斗中液体流下,反应发生,且排出装置内空气,一段时间后再打开K1,关闭K2,收集气体;
(2)二氧化碳与氢氧化钠反应生成碳酸钠和水,并使得I中压强减小, Ⅲ中稀盐酸会被吸入I中,并与生成的碳酸钠反应产生二氧化碳气体,所以观察到的现象为Ⅲ中稀盐酸倒流入Ⅰ中,且有气泡产生。
8.(1)试管(2)CaCO3+2HCl=CaCl2+CO2↑+H2O(3)BC(4)①③④
【解析】(1)装置A中仪器①是试管。
(2)实验室制取二氧化碳原理是碳酸钙与盐酸反应,方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O .
(3)制取二氧化碳需选择固液常温型发生装置,选择向上排空气法收集,即BC组合。
(4) 取废液的上层清液,逐滴加入碳酸钠溶液,观察到有气泡和沉淀产生,说明废液中含有为氯化钙和盐酸,加入碳酸钠时,碳酸钠先与盐酸反应,然后再与氯化钙反应,所以沉淀需在加入碳酸钠一定量之后才产生,①错误;由方程式可知,碳酸钠与盐酸反应时产生二氧化碳质量小于所加碳酸钠的质量,碳酸钠与氯化钙反应时,产生碳酸钙质量虽小于所加碳酸钠质量,但溶液增加趋势要小于碳酸钠与盐酸的反应,当碳酸钠过量后,不再发生反应,溶液增加质量即为所加碳酸钠质量,所以溶液始终是增加趋势,且增加趋势先快后慢,再快, ②正确;最初溶液呈酸性,pH小于7,加入碳酸钠后,盐酸先反应,溶液pH增加,于等于7后,盐酸反应结束,氯化钙与碳酸钠反应,此时溶液pH保持7不变,当氯化钙完全反应后,继续加碳酸钠,溶液pH又增加, ③错误;碳酸钠先与盐酸反应,气体质量增加,且起点应从原点开始,④错误。
9.(1)用石灰石和稀盐酸作为原料制取二氧化碳气体,属于固液常温型制备气体,要得到平稳的气流,应控制液体的滴加速率,应选择图甲中的C,能通过分液漏斗控制滴加液体的速率,从而控制反应的速率;故答案为C;
(2)氧气具有助燃性,将氧气倒入装有两支带火星的蜡烛的烧杯中,氧气的密度比空气的大,且能支持燃烧,因此能观察到蜡烛自下而上复燃,故答案为蜡烛自下而上复燃。
10.(1)CaCO3+2HCl=CaCl2+CO2↑+H2O(2)AC
【解析】(1)实验室利用石灰石或大理石与稀盐酸反应制取二氧化碳,反应方程式为 CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)二氧化碳制取需用固液常温型发生装置,即A,二氧化碳能溶于水且能与水反应,密度比空气大,所以应选择向上排空气法收集,即C装置;
11.加热时反复推拉左右两侧的注射器,直至气体体积不再减少;10%;装置内的气体未冷却至室温
【解析】(1)加热时反复推拉左右两侧的注射器,直至气体体积不再减少,可使铜和氧气充分接触发生反应。
(3)原气体体积为500毫升,实验结束后,立即测得装置内气体总体积为450毫升,即减少了50毫升,减少体积即为消耗的氧气体积,则氧气体积分数为10%。
(4) 实验结束后,立即测得装置内气体总体积 ,装置内气体未冷却至室温,会使得实验结果偏小。
12.解:(1)用气密性良好的注射器,获取V1毫升教室内空气的具体操作是在教室外,将注射器活塞推到底,将注射器拿到教室,再拉动活塞至刻度为V1毫升处并密封。
(2)用注射器获取V1毫升教室内的空气,通过导管缓缓地全部推入量筒,与量筒内足量的V2毫升一氧化氮气体混合,待充分反应后,读出量筒中剩余气体体积为V3毫升。则一共消耗一氧化氮和氧气体积为V1+V2﹣V3;由题干信息:同温同压下,在氢氧化钠溶液参与下,4体积一氧化氮与3体积氧气恰好完全反应,且产物能完全被溶液吸收,故氧气体积为(V1+V2﹣V3);教室内空气中氧气的体积分数为100%100%;
(3)在探究影响重力势能大小的因素实验中,空气阻力是次要因素(其它合理答案也给分)。
故答案为:(1)在教室外,将注射器活塞推到底,将注射器拿到教室,再拉动活塞至刻度为V1毫升处并密封;
(2)100%;
(3)在探究影响重力势能大小的因素实验中,空气阻力是次要因素(合理即可)。
(
1
)
同课章节目录
