第九单元溶液检测题(含答案) 九年级化学人教版下册
文档属性
| 名称 | 第九单元溶液检测题(含答案) 九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 230.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-28 00:00:00 | ||
图片预览

文档简介
第九单元《溶液》检测题
一、单选题
1.下列有关溶液说法正确的是
A.溶液都是均一、稳定的混合物 B.形成溶液的溶质都是固体
C.所有饱和溶液都比不饱和溶液要浓 D.溶液的体积等于溶质的体积与溶剂的体积之和
2.20℃时氯化钠的溶解度为36g,下列说法正确的是
A.100g水中溶解36g氯化钠一定饱和
B.20℃时100gNaCl的饱和溶液中含有36g氯化钠
C.20℃时136gNaCl的饱和溶液中含有36g氯化钠
D.20℃时NaCl的饱和溶液中NaCl质量分数为36%
3.对下列日常生活生产中的现象或事实解释不合理的是
生活中的现象 解释
A 春暖花开,香气宜人 分子在不断运动
B 洗洁精清洗餐具上油污 洗洁精能溶解油污
C 铁制品在潮湿地方易生锈 铁生锈过程是铁与氧气、水发生复杂的化学反应
D 活性炭用作冰箱去味剂 活性炭具有吸附性
A.A B.B C.C D.D
4.NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是
A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
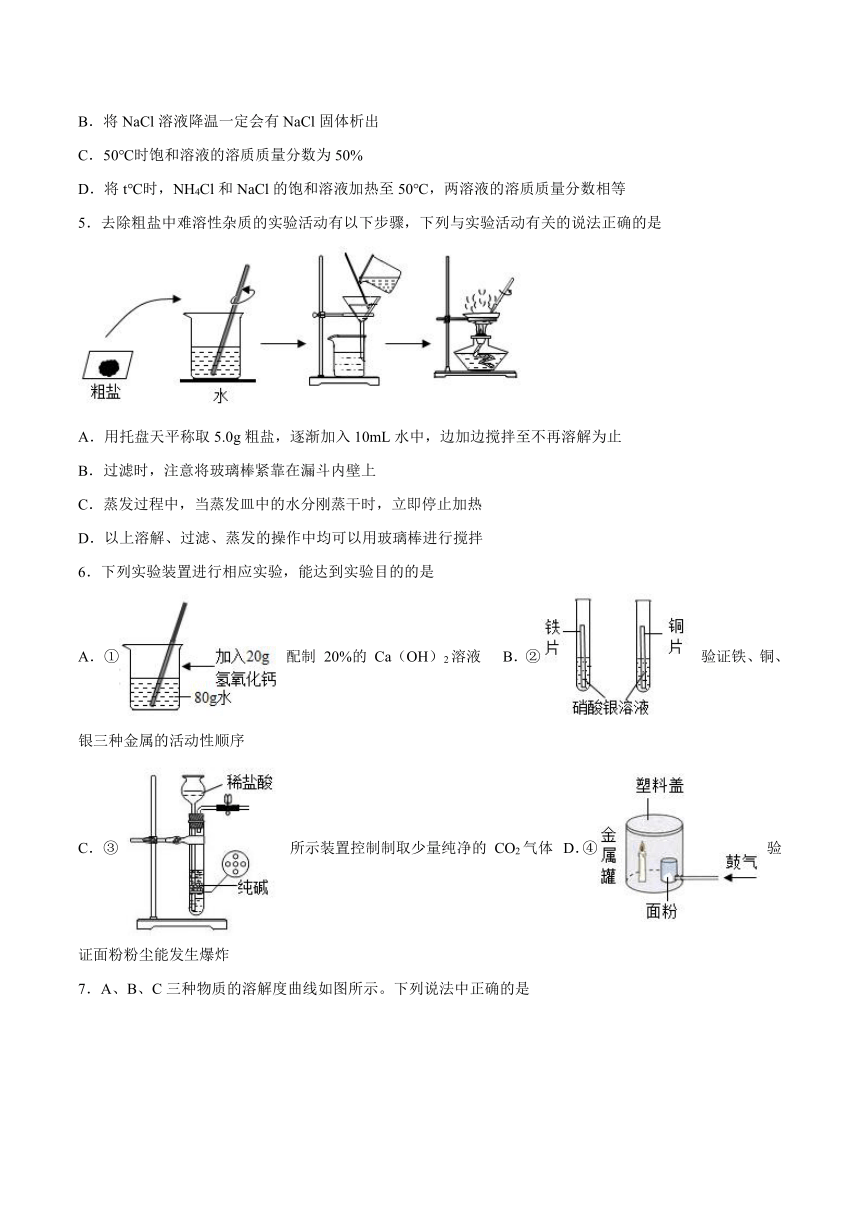
5.去除粗盐中难溶性杂质的实验活动有以下步骤,下列与实验活动有关的说法正确的是
A.用托盘天平称取5.0g粗盐,逐渐加入10mL水中,边加边搅拌至不再溶解为止
B.过滤时,注意将玻璃棒紧靠在漏斗内壁上
C.蒸发过程中,当蒸发皿中的水分刚蒸干时,立即停止加热
D.以上溶解、过滤、蒸发的操作中均可以用玻璃棒进行搅拌
6.下列实验装置进行相应实验,能达到实验目的的是
A.① 配制 20%的 Ca(OH)2溶液 B.② 验证铁、铜、银三种金属的活动性顺序
C.③ 所示装置控制制取少量纯净的 CO2气体 D.④ 验证面粉粉尘能发生爆炸
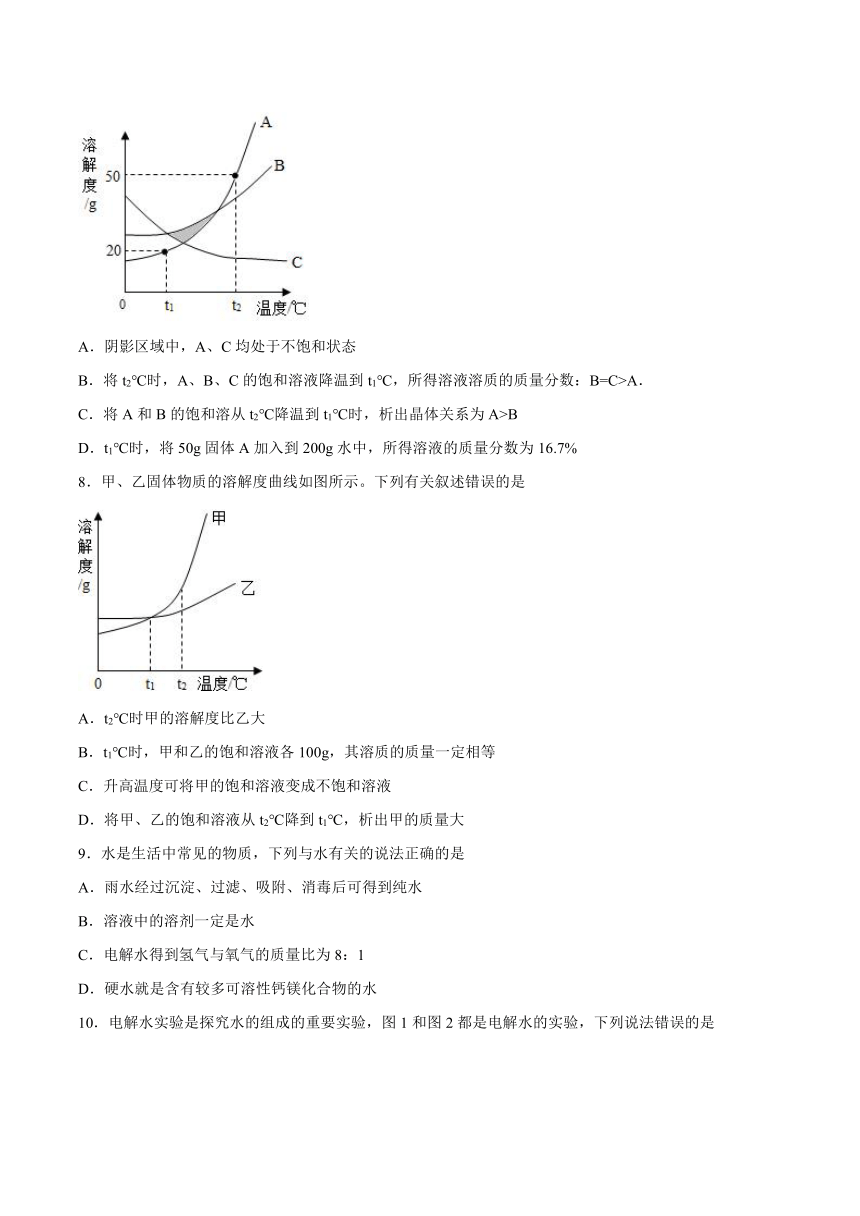
7.A、B、C三种物质的溶解度曲线如图所示。下列说法中正确的是
A.阴影区域中,A、C均处于不饱和状态
B.将t2℃时,A、B、C的饱和溶液降温到t1℃,所得溶液溶质的质量分数:B=C>A.
C.将A和B的饱和溶从t2℃降温到t1℃时,析出晶体关系为A>B
D.t1℃时,将50g固体A加入到200g水中,所得溶液的质量分数为16.7%
8.甲、乙固体物质的溶解度曲线如图所示。下列有关叙述错误的是
A.t2℃时甲的溶解度比乙大
B.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
C.升高温度可将甲的饱和溶液变成不饱和溶液
D.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
9.水是生活中常见的物质,下列与水有关的说法正确的是
A.雨水经过沉淀、过滤、吸附、消毒后可得到纯水
B.溶液中的溶剂一定是水
C.电解水得到氢气与氧气的质量比为8:1
D.硬水就是含有较多可溶性钙镁化合物的水
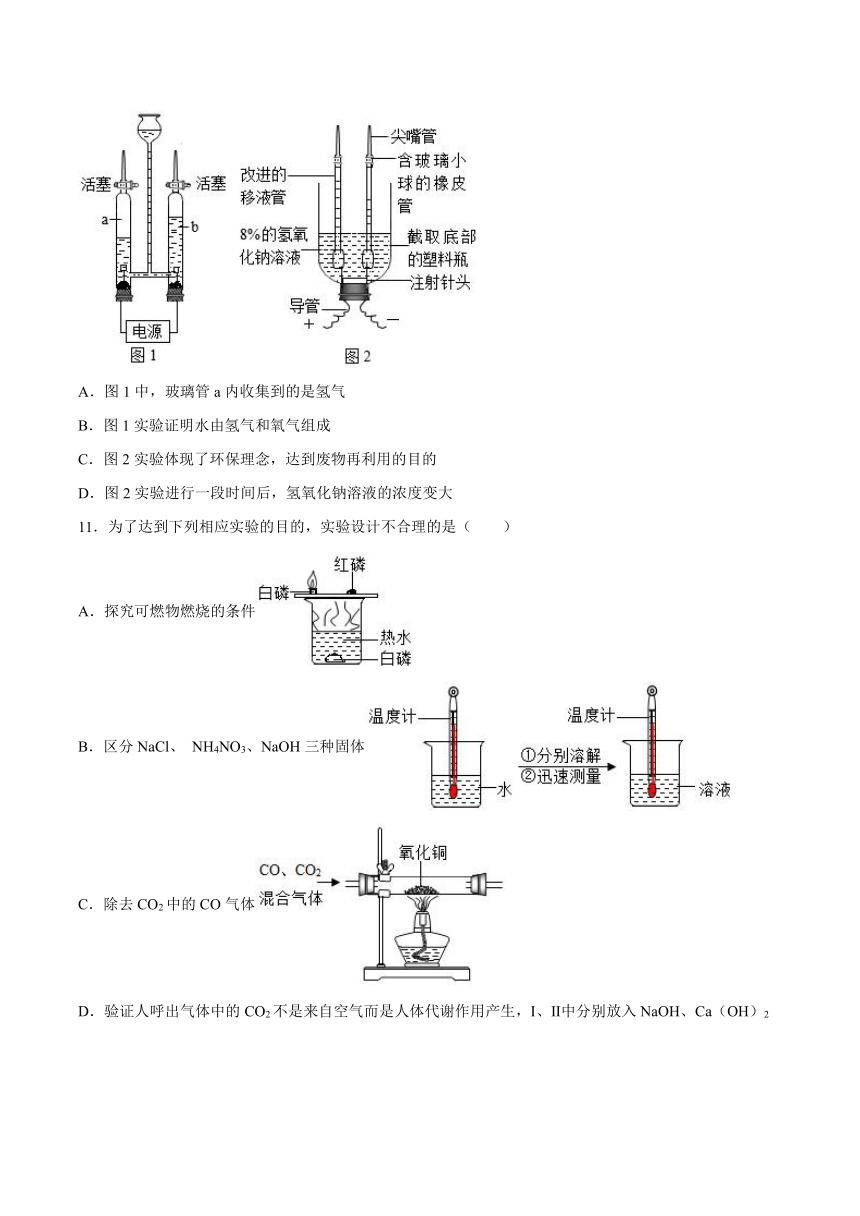
10.电解水实验是探究水的组成的重要实验,图1和图2都是电解水的实验,下列说法错误的是
A.图1中,玻璃管a内收集到的是氢气
B.图1实验证明水由氢气和氧气组成
C.图2实验体现了环保理念,达到废物再利用的目的
D.图2实验进行一段时间后,氢氧化钠溶液的浓度变大
11.为了达到下列相应实验的目的,实验设计不合理的是( )
A.探究可燃物燃烧的条件
B.区分NaCl、 NH4NO3、NaOH三种固体
C.除去CO2中的CO气体
D.验证人呼出气体中的CO2不是来自空气而是人体代谢作用产生,Ⅰ、Ⅱ中分别放入NaOH、Ca(OH)2溶液
12..KCl和 KNO3的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃ 10 20 30 40 50 60
溶 解 度 /g KCl 31.0 34.0 37.0 40.0 42.6 45.5
KNO3 20.9 31.6 45.8 53.9 85.5 110
A.t2应介于 40℃~50℃
B.甲表示 KNO3溶解度曲线
C.55℃时,溶液的溶质质量分数:KNO3>KCl
D.甲、乙饱和溶液从 t1升温到 t2时,溶质的质量分数相等
二、填空题
13.实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液。配制步骤为:
(1)计算:需氢氧化钠固体___________g,水 ___________mL(水的密度是1g/cm3)。
(2)称量:用质量为23.1g的烧杯作称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在___________盘(填:“左”或“右”),在下表所列的砝码中,选出所需砝码(打“√”表示选用)___________;并在下列标尺中选出能正确表示游码位置的选项___________(填字母)
砝码/g 100 50 20 20 10 5
打“√”表示选用
(3)溶解:将氢氧化钠固体溶于水,用___________搅拌,使氢氧化钠全部溶解,冷却至室温。如果配制的溶液溶质质量分数小于4%,则造成误差的原因可能有___________、___________。
①称量时砝码和氢氧化钠放反了,并且使用了游码;
②取水时仰视读数;
③溶解时有少量水溅出;
④装瓶时有溶液洒落。
14.向装有等量水的A、B、C烧杯中分别加入15 g、30 g、30 g氯化钾固体,充分溶解后,现象如图一所示。
(1)烧杯中的溶液一定属于饱和溶液的是_____(填序号);
(2)图二中能表示氯化钾溶解度曲线的是_____(填“甲”或“乙”);
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是_____;
(4)由图二分析,若分别将100 g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是_____(填序号)。
A 甲、乙都是饱和溶液 B 所含溶剂质量:甲<乙
C 溶液质量:甲>乙 D 溶质质量分数:甲>乙
15.请用所学的化学知识,回答下列问题。
(1)用汽油能除去衣服上的油污,其原理是________。
(2)铝制品耐腐蚀的原因_______(用化学方程式表示)。
三、简答题
16.不同物质在水中的溶解度不同,时,将甲、乙各分别放到盛有 水的两个烧杯中,充分溶解后,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是 ______ (填“”或“”)。
(2)向烧杯①的溶液中继续加入甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是 __________ 。
(3)将曲线对应物质的饱和溶液变为 时的饱和溶液,需蒸发掉水 ______(保留一位小数)。
(4)将等质量的甲、乙饱和溶液分别降温到时,所得溶液的有关说法正确的是 ______ (填字母)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
四、实验题
17.根据如图回答问题:
(1)写出标号仪器名称a______;b______。
(2)用C所示的方法称取NaC1配制溶液,若其他操作正确,易使配制溶液的溶质质量分数______。
(3)由D现象可知装置气密性______;B操作引起的后果是______。
五、计算题
18.某化学兴趣小组同学欲测定某铁粉与碳粉混合物中铁的质量分数,他们进行了如图所示的实验,若反应后烧杯中稀硫酸无剩余,请计算
(1)生成氢气的质量;_____
(2)所用稀硫酸的溶质质量分数。______
19.下图是一瓶未开启的化学试剂标签,请根据标签回答问题:(浓盐酸是氯化氢气体的水溶液)
(1)溶质的化学名称是__________。
(2)这瓶试液含溶质的质量是__________,溶剂的质量是__________。(精确到0.1%)。
参考答案:
1.A 2.C 3.B 4.D 5.A 6.D 7.D 8.D 9.D 10.B 11.D 12.B
13.(1) 40 960
(2) 左
砝码/g 100 50 20 20 10 5
打“√”表示选用 √ √
B
(3) 玻璃棒 ① ②
14. B 甲 升高温度 BD
15.(1)汽油能溶解油污
(2)
16. 甲物质溶于水放热,溶液温度升高,溶解度增大 27.8 ab
17. 胶头滴管 烧杯 偏小 良好 配置溶液质量分数偏大
18.(1)解:生成氢气的质量为:10g+50g-55.g-4.4g=0.2g。
答:生成氢气的质量是0.2g。
(2)设参与反应的稀硫酸的质量为x
所用稀硫酸的溶质质量分数为
答:所用稀硫酸的溶质质量分数为19.6%。
19.(1)氯化氢
(2) 217.2g 377.8g
一、单选题
1.下列有关溶液说法正确的是
A.溶液都是均一、稳定的混合物 B.形成溶液的溶质都是固体
C.所有饱和溶液都比不饱和溶液要浓 D.溶液的体积等于溶质的体积与溶剂的体积之和
2.20℃时氯化钠的溶解度为36g,下列说法正确的是
A.100g水中溶解36g氯化钠一定饱和
B.20℃时100gNaCl的饱和溶液中含有36g氯化钠
C.20℃时136gNaCl的饱和溶液中含有36g氯化钠
D.20℃时NaCl的饱和溶液中NaCl质量分数为36%
3.对下列日常生活生产中的现象或事实解释不合理的是
生活中的现象 解释
A 春暖花开,香气宜人 分子在不断运动
B 洗洁精清洗餐具上油污 洗洁精能溶解油污
C 铁制品在潮湿地方易生锈 铁生锈过程是铁与氧气、水发生复杂的化学反应
D 活性炭用作冰箱去味剂 活性炭具有吸附性
A.A B.B C.C D.D
4.NH4Cl和NaCl的溶解度随温度变化如图所示,下列说法正确的是
A.NH4Cl的溶解度一定大于NaCl
B.将NaCl溶液降温一定会有NaCl固体析出
C.50℃时饱和溶液的溶质质量分数为50%
D.将t℃时,NH4Cl和NaCl的饱和溶液加热至50℃,两溶液的溶质质量分数相等
5.去除粗盐中难溶性杂质的实验活动有以下步骤,下列与实验活动有关的说法正确的是
A.用托盘天平称取5.0g粗盐,逐渐加入10mL水中,边加边搅拌至不再溶解为止
B.过滤时,注意将玻璃棒紧靠在漏斗内壁上
C.蒸发过程中,当蒸发皿中的水分刚蒸干时,立即停止加热
D.以上溶解、过滤、蒸发的操作中均可以用玻璃棒进行搅拌
6.下列实验装置进行相应实验,能达到实验目的的是
A.① 配制 20%的 Ca(OH)2溶液 B.② 验证铁、铜、银三种金属的活动性顺序
C.③ 所示装置控制制取少量纯净的 CO2气体 D.④ 验证面粉粉尘能发生爆炸
7.A、B、C三种物质的溶解度曲线如图所示。下列说法中正确的是
A.阴影区域中,A、C均处于不饱和状态
B.将t2℃时,A、B、C的饱和溶液降温到t1℃,所得溶液溶质的质量分数:B=C>A.
C.将A和B的饱和溶从t2℃降温到t1℃时,析出晶体关系为A>B
D.t1℃时,将50g固体A加入到200g水中,所得溶液的质量分数为16.7%
8.甲、乙固体物质的溶解度曲线如图所示。下列有关叙述错误的是
A.t2℃时甲的溶解度比乙大
B.t1℃时,甲和乙的饱和溶液各100g,其溶质的质量一定相等
C.升高温度可将甲的饱和溶液变成不饱和溶液
D.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大
9.水是生活中常见的物质,下列与水有关的说法正确的是
A.雨水经过沉淀、过滤、吸附、消毒后可得到纯水
B.溶液中的溶剂一定是水
C.电解水得到氢气与氧气的质量比为8:1
D.硬水就是含有较多可溶性钙镁化合物的水
10.电解水实验是探究水的组成的重要实验,图1和图2都是电解水的实验,下列说法错误的是
A.图1中,玻璃管a内收集到的是氢气
B.图1实验证明水由氢气和氧气组成
C.图2实验体现了环保理念,达到废物再利用的目的
D.图2实验进行一段时间后,氢氧化钠溶液的浓度变大
11.为了达到下列相应实验的目的,实验设计不合理的是( )
A.探究可燃物燃烧的条件
B.区分NaCl、 NH4NO3、NaOH三种固体
C.除去CO2中的CO气体
D.验证人呼出气体中的CO2不是来自空气而是人体代谢作用产生,Ⅰ、Ⅱ中分别放入NaOH、Ca(OH)2溶液
12..KCl和 KNO3的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃ 10 20 30 40 50 60
溶 解 度 /g KCl 31.0 34.0 37.0 40.0 42.6 45.5
KNO3 20.9 31.6 45.8 53.9 85.5 110
A.t2应介于 40℃~50℃
B.甲表示 KNO3溶解度曲线
C.55℃时,溶液的溶质质量分数:KNO3>KCl
D.甲、乙饱和溶液从 t1升温到 t2时,溶质的质量分数相等
二、填空题
13.实验室欲配制1000g溶质质量分数为4%的氢氧化钠溶液。配制步骤为:
(1)计算:需氢氧化钠固体___________g,水 ___________mL(水的密度是1g/cm3)。
(2)称量:用质量为23.1g的烧杯作称量容器,在托盘天平上称取氢氧化钠固体时,盛有氢氧化钠固体的烧杯应放在___________盘(填:“左”或“右”),在下表所列的砝码中,选出所需砝码(打“√”表示选用)___________;并在下列标尺中选出能正确表示游码位置的选项___________(填字母)
砝码/g 100 50 20 20 10 5
打“√”表示选用
(3)溶解:将氢氧化钠固体溶于水,用___________搅拌,使氢氧化钠全部溶解,冷却至室温。如果配制的溶液溶质质量分数小于4%,则造成误差的原因可能有___________、___________。
①称量时砝码和氢氧化钠放反了,并且使用了游码;
②取水时仰视读数;
③溶解时有少量水溅出;
④装瓶时有溶液洒落。
14.向装有等量水的A、B、C烧杯中分别加入15 g、30 g、30 g氯化钾固体,充分溶解后,现象如图一所示。
(1)烧杯中的溶液一定属于饱和溶液的是_____(填序号);
(2)图二中能表示氯化钾溶解度曲线的是_____(填“甲”或“乙”);
(3)要使B烧杯中剩余固体继续溶解,可采用的方法是_____;
(4)由图二分析,若分别将100 g甲、乙的饱和溶液从t2℃降温到t1℃,对所得溶液的叙述正确的是_____(填序号)。
A 甲、乙都是饱和溶液 B 所含溶剂质量:甲<乙
C 溶液质量:甲>乙 D 溶质质量分数:甲>乙
15.请用所学的化学知识,回答下列问题。
(1)用汽油能除去衣服上的油污,其原理是________。
(2)铝制品耐腐蚀的原因_______(用化学方程式表示)。
三、简答题
16.不同物质在水中的溶解度不同,时,将甲、乙各分别放到盛有 水的两个烧杯中,充分溶解后,现象如图一。甲和乙的溶解度曲线如图二。请结合图示回答下列问题:
(1)固体甲对应的溶解度曲线是 ______ (填“”或“”)。
(2)向烧杯①的溶液中继续加入甲物质,充分搅拌,发现固体先全部溶解,一段时间后又有部分固体甲析出。你认为“全部溶解”的原因是 __________ 。
(3)将曲线对应物质的饱和溶液变为 时的饱和溶液,需蒸发掉水 ______(保留一位小数)。
(4)将等质量的甲、乙饱和溶液分别降温到时,所得溶液的有关说法正确的是 ______ (填字母)。
a.甲溶液仍为饱和溶液 b.两溶液质量甲<乙
c.两溶液中溶剂质量甲=乙 d.两溶液溶质质量甲>乙
四、实验题
17.根据如图回答问题:
(1)写出标号仪器名称a______;b______。
(2)用C所示的方法称取NaC1配制溶液,若其他操作正确,易使配制溶液的溶质质量分数______。
(3)由D现象可知装置气密性______;B操作引起的后果是______。
五、计算题
18.某化学兴趣小组同学欲测定某铁粉与碳粉混合物中铁的质量分数,他们进行了如图所示的实验,若反应后烧杯中稀硫酸无剩余,请计算
(1)生成氢气的质量;_____
(2)所用稀硫酸的溶质质量分数。______
19.下图是一瓶未开启的化学试剂标签,请根据标签回答问题:(浓盐酸是氯化氢气体的水溶液)
(1)溶质的化学名称是__________。
(2)这瓶试液含溶质的质量是__________,溶剂的质量是__________。(精确到0.1%)。
参考答案:
1.A 2.C 3.B 4.D 5.A 6.D 7.D 8.D 9.D 10.B 11.D 12.B
13.(1) 40 960
(2) 左
砝码/g 100 50 20 20 10 5
打“√”表示选用 √ √
B
(3) 玻璃棒 ① ②
14. B 甲 升高温度 BD
15.(1)汽油能溶解油污
(2)
16. 甲物质溶于水放热,溶液温度升高,溶解度增大 27.8 ab
17. 胶头滴管 烧杯 偏小 良好 配置溶液质量分数偏大
18.(1)解:生成氢气的质量为:10g+50g-55.g-4.4g=0.2g。
答:生成氢气的质量是0.2g。
(2)设参与反应的稀硫酸的质量为x
所用稀硫酸的溶质质量分数为
答:所用稀硫酸的溶质质量分数为19.6%。
19.(1)氯化氢
(2) 217.2g 377.8g
同课章节目录
