2023年中考化学一轮复习课件 第03单元 溶液(鲁教版)(共40张PPT)
文档属性
| 名称 | 2023年中考化学一轮复习课件 第03单元 溶液(鲁教版)(共40张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 773.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-03-29 00:00:00 | ||
图片预览








文档简介
(共40张PPT)
第三单元 溶液
第三单元 溶液
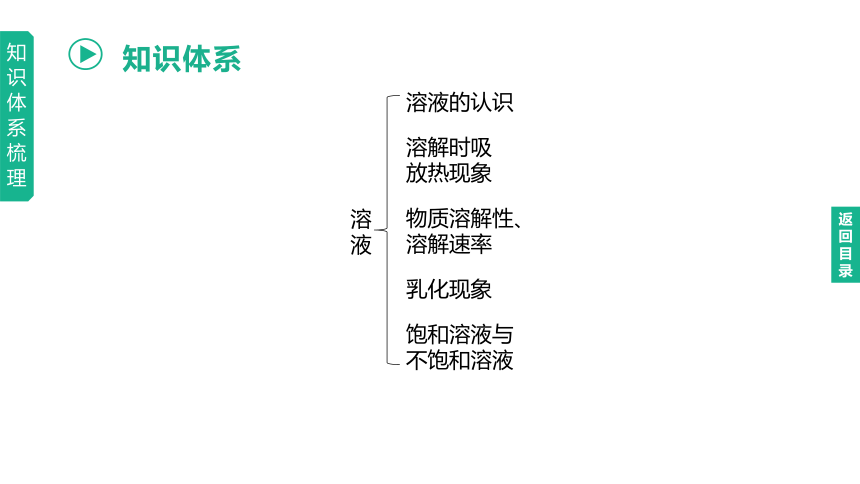
知识体系
溶液
溶液的认识
溶解时吸
放热现象
物质溶解性、溶解速率
乳化现象
饱和溶液与不饱和溶液
均一
稳定
水
硝酸铵
氢氧化钠
氯化钠
温度
溶解
一定温度
一定量溶剂
不能继续
还能继续
增加溶剂
蒸发溶剂、增加溶质
溶质质量分数
溶质
溶液
溶质
1.均一、稳定、透明的液体一定是溶液 ( )
2.饱和溶液与不饱和溶液在一定条件下可以互相转化( )
3.溶液的体积等于溶质体积与溶剂体积之和 ( )
4.不饱和溶液变为饱和溶液,溶质质量分数一定增大( )
5.任何饱和溶液,在温度升高时,一定会变成不饱和溶液( )
易错判断
×
√
×
×
×
6.相同温度时,同种溶质的饱和溶液一定比它的不饱和溶液浓( )
7.洗涤剂除去衣服上的油污是利用了乳化作用,汽油除去衣服上的油污也是利用了乳化作用( )
√
×
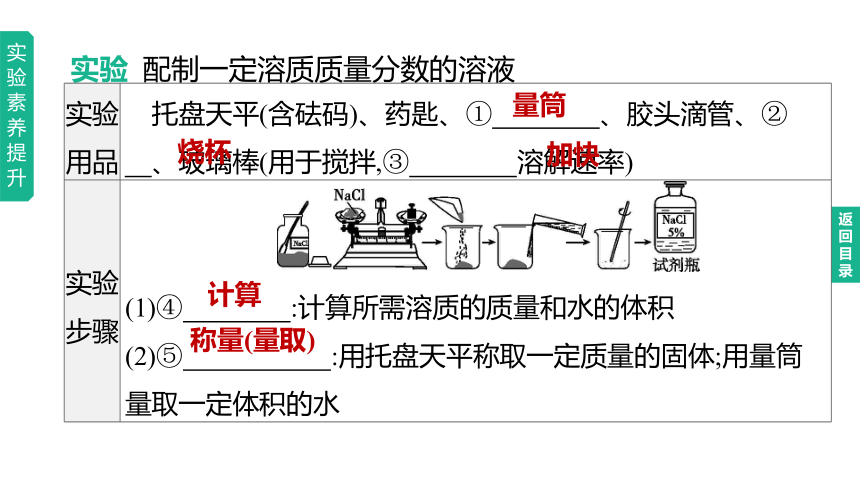
实验 配制一定溶质质量分数的溶液
实验用品 托盘天平(含砝码)、药匙、① 、胶头滴管、② 、玻璃棒(用于搅拌,③ 溶解速率)
实验步骤
(1)④ :计算所需溶质的质量和水的体积
(2)⑤ :用托盘天平称取一定质量的固体;用量筒量取一定体积的水
量筒
烧杯
加快
计算
称量(量取)
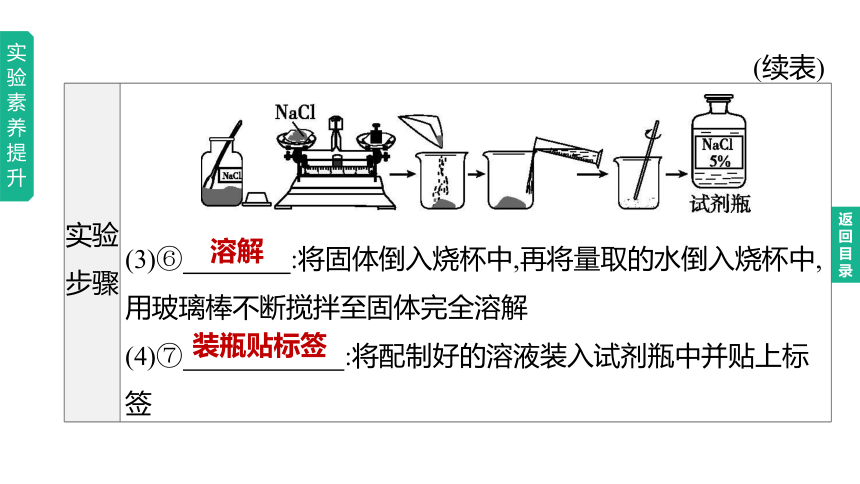
(续表)
实验步骤
(3)⑥ :将固体倒入烧杯中,再将量取的水倒入烧杯中,用玻璃棒不断搅拌至固体完全溶解
(4)⑦ :将配制好的溶液装入试剂瓶中并贴上标签
溶解
装瓶贴标签
(续表)
注意事项 (1)用托盘天平称量时要遵循“⑧ ”的原则,且左右两盘上要垫上相同的称量纸(目的是防止污染托盘且称量准确),有腐蚀性或易潮解的药品(如⑨ )应放在玻璃器皿中称量
(2)用量筒量取液体,读数时视线应与量筒内液体⑩_________
相平
(3)选取量筒的量程要等于或比所要量取液体体积稍大且越接近越好,方便一次量取,且量取准确
左物右码
氢氧化钠
凹液面的
最低处
(续表)
误差分析 溶质质量分数偏大 溶质质量分数偏小 无影响
溶质 质量 偏大 (1)砝码生锈或沾有污渍 (2)天平空载时指针向 (填“左”或“右”)偏 溶质 质量 偏小 (1)药品中含有杂质 (2)药品和砝码位置颠倒,且使用了游码 (3)天平空载时指针向 (填“左”或“右”)偏 (4)药品没有完全转移 转移过程中有少量溶液洒出
右
左
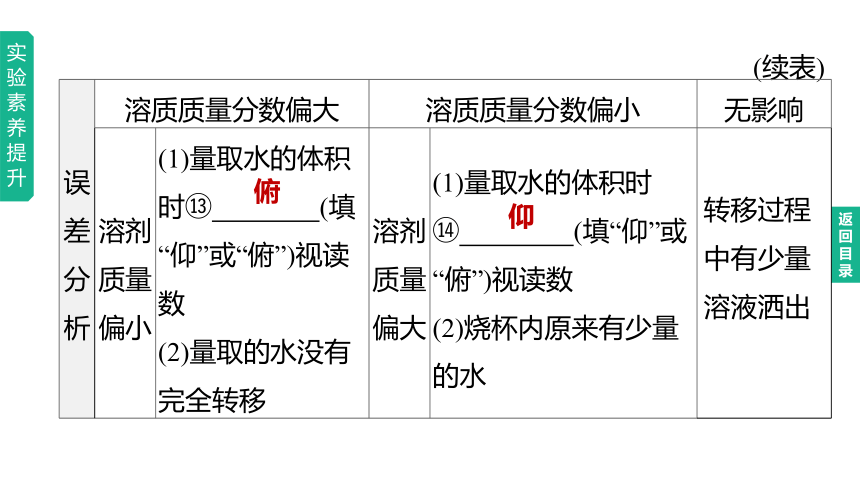
(续表)
误差分析 溶质质量分数偏大 溶质质量分数偏小 无影响
溶剂 质量 偏小 (1)量取水的体积时 (填“仰”或“俯”)视读数 (2)量取的水没有完全转移 溶剂 质量 偏大 (1)量取水的体积时 (填“仰”或“俯”)视读数 (2)烧杯内原来有少量的水
转移过程中有少量溶液洒出
俯
仰
(续表)
用浓溶 液配制 稀溶液 (1)依据:利用稀释前后溶质质量不变,计算出需量取的浓溶液质量,再根据稀释后溶液质量-浓溶液质量= _________
的质量
(2)步骤:计算;量取;混匀;装瓶、贴标签
加入溶剂
1.[2022·天津节选]2021年“世界水日”的主题为“珍惜水、爱护水”。
某同学配制50 g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为 g。
|基础训练|
5
②配制过程有以下步骤:
a.称量及量取 b.计算
c.溶解 d.装瓶贴标签
正确的顺序是 (填序号)。
A.bcad B.bacd
③将50 g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水的质量为 g。
B
50
2.小明用氯化钠固体配制100 g溶质质量分数为18%的氯化钠溶液。
|变形拓展|
图3-1
(1)小明称取氯化钠、量取水的操作如图3-1所示,他实际称得的氯化钠的质量为 g,实际量取的水的体积为 mL。在老师指导下小明重新称量,在第二次称取氯化钠过程中,天平指针向右偏,他接下来的操作是 (填序号)。
A.调整平衡螺母,使天平平衡
B.向左盘加入氯化钠至天平平衡
C.向左移游码或减少砝码,使天平平衡
图3-1
12.2
80
B
(2)在配制过程中,下列操作对所配溶液浓度的影响与其他三个不同的操作是 (填序号)。
A.往烧杯中加水时有水洒出
B.用量筒量取水时仰视读数
C.烧杯用水洗涤后未干燥就使用
D.称量的氯化钠固体中含有不溶性杂质
A
(3)盛放配制好的氯化钠溶液应选择图3-2甲中的仪器
(填序号),请将图乙中的标签填写完整。
图3-2
氯化钠溶液
18%
A
3.菊花的无土栽培营养液主要成分如配方表所示。
成分 质量/(mg·L-1)
硫酸钾 626
硫酸铵 205
磷酸二氢钾 449
硫酸镁 738
硝酸钙 1 675
(1)现在要按以上配方配制约5 L的菊花栽培营养液,实验步骤如下:
①计算:分别算出各种成分所需质量,如需硫酸钾的质量为
mg。
②称量:用 (填“托盘天平”或“电子天平”)称出各成分质量。
3 130
电子天平
③溶解:将称得的物质倒入烧杯中,加入少量水,用 搅拌,完全溶解后再将其倒入5 L的容量瓶中(一种专用于配溶液的容器),再用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液全部倒入容量瓶中,再向容量瓶中加入蒸馏水,液面离容量瓶颈刻度线下1~2 cm时,改用 滴加蒸馏水至液面与刻度线相切。
④装瓶:将容量瓶中配好的溶液全部倒入特定塑料桶中待用。
玻璃棒
胶头滴管
反思与评价
(2)步骤③中,如果缺少“再用少量蒸馏水洗涤烧杯内壁2~3次”操作,则配出的营养液浓度将 (填“偏高”“偏低”或“不受影响”)。如果步骤④中有部分溶液不小心洒出,则配出的营养液浓度 (填“偏高”“偏低”或“不受影响”)。
偏低
不受影响
(3)医学治疗中,有时要用到25%的硫酸镁注射液,下表是硫酸镁的部分溶解度数据。
医学人士认为,该注射液在10 ℃以下不宜使用,请结合上表说明理由:______________________________________________
。
温度/℃ 10 20 30 40 60 80
溶解度/g 28.2 33.7 38.9 44.5 54.6 55.8
10 ℃以下时,硫酸镁饱和溶液中溶质质量分数小于
25%
1.[2022·营口]下列物质能溶于水形成溶液的是 ( )
A.蔗糖 B.面粉 C.植物油 D.泥沙
2.[2022·重庆B]将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是 ( )
A.CaCO3 B.NaOH
C.NaCl D.NH4NO3
考向一
溶解的过程 (8年5考,1~2分)
A
B
3.[2022·株洲]下列说法正确的是 ( )
A.溶液一定是均一、稳定、无色透明的混合物
B.降低温度,不饱和溶液一定能变成饱和溶液
C.用洗洁精洗去餐具上的油污利用的是洗洁精的乳化作
D.常温下蔗糖的水溶液密封放置一段时间后会析出固体
C
4.[盐城节选]学习化学概念“饱和溶液”——实验“KNO3溶于水”。
实验用品 KNO3(研磨处理)、水、玻璃棒、三脚架、石棉网、酒精灯、烧杯等。
实验探究 在室温20 ℃下,向小烧杯中加入20 mL水,按下表中设计的操作步骤进行实验。
考向二
饱和溶液与不饱和溶液 (8年1考,2分)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅰ 加入2 g KNO3,搅拌 全部溶解 不一定形成饱和溶液 在一定温度下,一定量水中不能无限制地溶解溶质
Ⅱ 再加入5 g KNO3,搅拌 部分溶解 一定形成饱和溶液
(续表)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅲ 加热,搅拌 不一定形成饱和溶液 KNO3的溶解度随温度的升高而
Ⅳ 再加入5 g KNO3,搅拌 全部溶解 不一定形成饱和溶液 全部溶解
增大
(续表)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅴ 放在冷水的大烧杯中冷却 析出晶体 一定形成饱和溶液 KNO3可用
的方法结晶
增加溶剂的质量,可将饱和溶液转化为不饱和溶液
Ⅵ _________ ,搅拌 全部溶解 一定形成不饱和溶液 加入过量
的水
降温
实验反思
(1)KNO3预先研磨处理的目的是 。
(2)实验步骤 (填实验序号,下同)中KNO3的溶质质量分数最大。
(3)比较实验步骤 中观察到的实验现象,经分析推理,可得出将KNO3饱和溶液转化为不饱和溶液的另一种方法,即升高饱和溶液的温度。
增大接触面积,加速溶解
Ⅳ
Ⅱ和Ⅲ
5.[2022·北京]用MgCl2溶液喷洒路面可融雪、防尘。20 ℃时,按下表数据配制溶液。
(已知:20 ℃时,MgCl2的溶解度为54.6 g)
①中溶质的质量分数约为 ( )
A.23% B.30% C.35% D.43%
考向三
溶质质量分数的综合计算 (必考,2~3分)
序号 ① ② ③ ④
MgCl2的质量/g 30 40 50 60
水的质量/g 100 100 100 100
A
6.[2022·台州]下表是氢氧化钠溶液的密度与其质量分数对照表(20 ℃)。回答下列问题。
(1)20 ℃时,随着溶质质量分数增大,氢氧化钠溶液的密度逐渐 。
(2)配制100 g 10%的氢氧化钠溶液,需要氢氧化钠固体
。
质量分数/% 10 20 30 40 50
密度/(g·cm-3) 1.11 1.22 1.33 1.43 1.53
增大
10 g
6.[2022·台州]下表是氢氧化钠溶液的密度与其质量分数对照表(20 ℃)。回答下列问题。
(3)20 ℃,10%的氢氧化钠溶液,体积为100 mL时的质量为
。
质量分数/% 10 20 30 40 50
密度/(g·cm-3) 1.11 1.22 1.33 1.43 1.53
111 g
(详见实验素养提升)
考向四
配制一定溶质质量分数的溶液 (8年1考,1~2分)
1.[2022·宿迁]下列物质溶于水,会导致溶液温度明显降低的是( )
A.硝酸铵 B.蔗糖
C.浓硫酸 D.氢氧化钠
A
2.[2017·宿迁]下列说法正确的是 ( )
A.均一、稳定的液体一定是溶液
B.饱和溶液一定是浓溶液
C.汽油洗涤油污属于乳化现象
D.将氢氧化钠溶于水,所得溶液温度升高
D
3.[2015·宿迁]下列有关溶液的说法中,正确的是 ( )
A.溶液不一定都是混合物
B.将100 g KCl饱和溶液蒸干得到25 g固体,则KCl在该温度下的溶解度为25 g
C.常温下将饱和Ca(OH)2溶液加热到50 ℃,会使溶液由饱和变为不饱和
D.从25%的H2SO4溶液中取出10 mL,则取出溶液的质量分数仍为25%
D
4.真题组合 判断下列说法是否正确。
(1)[2014·宿迁]凡是均一、稳定的液体都是溶液,溶液中只能有一种溶质 ( )
(2)[宿迁]溶液一定是混合物 ( )
(3)[宿迁]用洗洁精洗油污是乳化作用,用汽油洗油污也是乳化作用 ( )
(4)[2014·宿迁]20 ℃时,配制2%的氢氧化钙溶液 ( )
×
√
×
×
(5)[2014·宿迁]将100 g 10%的稀盐酸加热蒸发掉50 g水,可使稀盐酸溶质质量分数变成20% ( )
(6)[2018·宿迁]将硝酸铵固体溶于水,溶液温度会升高( )
(7)[2014·宿迁]物质溶于水放热或吸热取决于扩散与水合过程的相对强弱 ( )
×
×
√
第三单元 溶液
第三单元 溶液
知识体系
溶液
溶液的认识
溶解时吸
放热现象
物质溶解性、溶解速率
乳化现象
饱和溶液与不饱和溶液
均一
稳定
水
硝酸铵
氢氧化钠
氯化钠
温度
溶解
一定温度
一定量溶剂
不能继续
还能继续
增加溶剂
蒸发溶剂、增加溶质
溶质质量分数
溶质
溶液
溶质
1.均一、稳定、透明的液体一定是溶液 ( )
2.饱和溶液与不饱和溶液在一定条件下可以互相转化( )
3.溶液的体积等于溶质体积与溶剂体积之和 ( )
4.不饱和溶液变为饱和溶液,溶质质量分数一定增大( )
5.任何饱和溶液,在温度升高时,一定会变成不饱和溶液( )
易错判断
×
√
×
×
×
6.相同温度时,同种溶质的饱和溶液一定比它的不饱和溶液浓( )
7.洗涤剂除去衣服上的油污是利用了乳化作用,汽油除去衣服上的油污也是利用了乳化作用( )
√
×
实验 配制一定溶质质量分数的溶液
实验用品 托盘天平(含砝码)、药匙、① 、胶头滴管、② 、玻璃棒(用于搅拌,③ 溶解速率)
实验步骤
(1)④ :计算所需溶质的质量和水的体积
(2)⑤ :用托盘天平称取一定质量的固体;用量筒量取一定体积的水
量筒
烧杯
加快
计算
称量(量取)
(续表)
实验步骤
(3)⑥ :将固体倒入烧杯中,再将量取的水倒入烧杯中,用玻璃棒不断搅拌至固体完全溶解
(4)⑦ :将配制好的溶液装入试剂瓶中并贴上标签
溶解
装瓶贴标签
(续表)
注意事项 (1)用托盘天平称量时要遵循“⑧ ”的原则,且左右两盘上要垫上相同的称量纸(目的是防止污染托盘且称量准确),有腐蚀性或易潮解的药品(如⑨ )应放在玻璃器皿中称量
(2)用量筒量取液体,读数时视线应与量筒内液体⑩_________
相平
(3)选取量筒的量程要等于或比所要量取液体体积稍大且越接近越好,方便一次量取,且量取准确
左物右码
氢氧化钠
凹液面的
最低处
(续表)
误差分析 溶质质量分数偏大 溶质质量分数偏小 无影响
溶质 质量 偏大 (1)砝码生锈或沾有污渍 (2)天平空载时指针向 (填“左”或“右”)偏 溶质 质量 偏小 (1)药品中含有杂质 (2)药品和砝码位置颠倒,且使用了游码 (3)天平空载时指针向 (填“左”或“右”)偏 (4)药品没有完全转移 转移过程中有少量溶液洒出
右
左
(续表)
误差分析 溶质质量分数偏大 溶质质量分数偏小 无影响
溶剂 质量 偏小 (1)量取水的体积时 (填“仰”或“俯”)视读数 (2)量取的水没有完全转移 溶剂 质量 偏大 (1)量取水的体积时 (填“仰”或“俯”)视读数 (2)烧杯内原来有少量的水
转移过程中有少量溶液洒出
俯
仰
(续表)
用浓溶 液配制 稀溶液 (1)依据:利用稀释前后溶质质量不变,计算出需量取的浓溶液质量,再根据稀释后溶液质量-浓溶液质量= _________
的质量
(2)步骤:计算;量取;混匀;装瓶、贴标签
加入溶剂
1.[2022·天津节选]2021年“世界水日”的主题为“珍惜水、爱护水”。
某同学配制50 g溶质质量分数为10%的氯化钠溶液。
①需要固体氯化钠的质量为 g。
|基础训练|
5
②配制过程有以下步骤:
a.称量及量取 b.计算
c.溶解 d.装瓶贴标签
正确的顺序是 (填序号)。
A.bcad B.bacd
③将50 g溶质质量分数为10%的氯化钠溶液,稀释成5%的氯化钠溶液,需要加水的质量为 g。
B
50
2.小明用氯化钠固体配制100 g溶质质量分数为18%的氯化钠溶液。
|变形拓展|
图3-1
(1)小明称取氯化钠、量取水的操作如图3-1所示,他实际称得的氯化钠的质量为 g,实际量取的水的体积为 mL。在老师指导下小明重新称量,在第二次称取氯化钠过程中,天平指针向右偏,他接下来的操作是 (填序号)。
A.调整平衡螺母,使天平平衡
B.向左盘加入氯化钠至天平平衡
C.向左移游码或减少砝码,使天平平衡
图3-1
12.2
80
B
(2)在配制过程中,下列操作对所配溶液浓度的影响与其他三个不同的操作是 (填序号)。
A.往烧杯中加水时有水洒出
B.用量筒量取水时仰视读数
C.烧杯用水洗涤后未干燥就使用
D.称量的氯化钠固体中含有不溶性杂质
A
(3)盛放配制好的氯化钠溶液应选择图3-2甲中的仪器
(填序号),请将图乙中的标签填写完整。
图3-2
氯化钠溶液
18%
A
3.菊花的无土栽培营养液主要成分如配方表所示。
成分 质量/(mg·L-1)
硫酸钾 626
硫酸铵 205
磷酸二氢钾 449
硫酸镁 738
硝酸钙 1 675
(1)现在要按以上配方配制约5 L的菊花栽培营养液,实验步骤如下:
①计算:分别算出各种成分所需质量,如需硫酸钾的质量为
mg。
②称量:用 (填“托盘天平”或“电子天平”)称出各成分质量。
3 130
电子天平
③溶解:将称得的物质倒入烧杯中,加入少量水,用 搅拌,完全溶解后再将其倒入5 L的容量瓶中(一种专用于配溶液的容器),再用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液全部倒入容量瓶中,再向容量瓶中加入蒸馏水,液面离容量瓶颈刻度线下1~2 cm时,改用 滴加蒸馏水至液面与刻度线相切。
④装瓶:将容量瓶中配好的溶液全部倒入特定塑料桶中待用。
玻璃棒
胶头滴管
反思与评价
(2)步骤③中,如果缺少“再用少量蒸馏水洗涤烧杯内壁2~3次”操作,则配出的营养液浓度将 (填“偏高”“偏低”或“不受影响”)。如果步骤④中有部分溶液不小心洒出,则配出的营养液浓度 (填“偏高”“偏低”或“不受影响”)。
偏低
不受影响
(3)医学治疗中,有时要用到25%的硫酸镁注射液,下表是硫酸镁的部分溶解度数据。
医学人士认为,该注射液在10 ℃以下不宜使用,请结合上表说明理由:______________________________________________
。
温度/℃ 10 20 30 40 60 80
溶解度/g 28.2 33.7 38.9 44.5 54.6 55.8
10 ℃以下时,硫酸镁饱和溶液中溶质质量分数小于
25%
1.[2022·营口]下列物质能溶于水形成溶液的是 ( )
A.蔗糖 B.面粉 C.植物油 D.泥沙
2.[2022·重庆B]将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是 ( )
A.CaCO3 B.NaOH
C.NaCl D.NH4NO3
考向一
溶解的过程 (8年5考,1~2分)
A
B
3.[2022·株洲]下列说法正确的是 ( )
A.溶液一定是均一、稳定、无色透明的混合物
B.降低温度,不饱和溶液一定能变成饱和溶液
C.用洗洁精洗去餐具上的油污利用的是洗洁精的乳化作
D.常温下蔗糖的水溶液密封放置一段时间后会析出固体
C
4.[盐城节选]学习化学概念“饱和溶液”——实验“KNO3溶于水”。
实验用品 KNO3(研磨处理)、水、玻璃棒、三脚架、石棉网、酒精灯、烧杯等。
实验探究 在室温20 ℃下,向小烧杯中加入20 mL水,按下表中设计的操作步骤进行实验。
考向二
饱和溶液与不饱和溶液 (8年1考,2分)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅰ 加入2 g KNO3,搅拌 全部溶解 不一定形成饱和溶液 在一定温度下,一定量水中不能无限制地溶解溶质
Ⅱ 再加入5 g KNO3,搅拌 部分溶解 一定形成饱和溶液
(续表)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅲ 加热,搅拌 不一定形成饱和溶液 KNO3的溶解度随温度的升高而
Ⅳ 再加入5 g KNO3,搅拌 全部溶解 不一定形成饱和溶液 全部溶解
增大
(续表)
实验序号 实验步骤 实验现象 实验推理 实验结论
Ⅴ 放在冷水的大烧杯中冷却 析出晶体 一定形成饱和溶液 KNO3可用
的方法结晶
增加溶剂的质量,可将饱和溶液转化为不饱和溶液
Ⅵ _________ ,搅拌 全部溶解 一定形成不饱和溶液 加入过量
的水
降温
实验反思
(1)KNO3预先研磨处理的目的是 。
(2)实验步骤 (填实验序号,下同)中KNO3的溶质质量分数最大。
(3)比较实验步骤 中观察到的实验现象,经分析推理,可得出将KNO3饱和溶液转化为不饱和溶液的另一种方法,即升高饱和溶液的温度。
增大接触面积,加速溶解
Ⅳ
Ⅱ和Ⅲ
5.[2022·北京]用MgCl2溶液喷洒路面可融雪、防尘。20 ℃时,按下表数据配制溶液。
(已知:20 ℃时,MgCl2的溶解度为54.6 g)
①中溶质的质量分数约为 ( )
A.23% B.30% C.35% D.43%
考向三
溶质质量分数的综合计算 (必考,2~3分)
序号 ① ② ③ ④
MgCl2的质量/g 30 40 50 60
水的质量/g 100 100 100 100
A
6.[2022·台州]下表是氢氧化钠溶液的密度与其质量分数对照表(20 ℃)。回答下列问题。
(1)20 ℃时,随着溶质质量分数增大,氢氧化钠溶液的密度逐渐 。
(2)配制100 g 10%的氢氧化钠溶液,需要氢氧化钠固体
。
质量分数/% 10 20 30 40 50
密度/(g·cm-3) 1.11 1.22 1.33 1.43 1.53
增大
10 g
6.[2022·台州]下表是氢氧化钠溶液的密度与其质量分数对照表(20 ℃)。回答下列问题。
(3)20 ℃,10%的氢氧化钠溶液,体积为100 mL时的质量为
。
质量分数/% 10 20 30 40 50
密度/(g·cm-3) 1.11 1.22 1.33 1.43 1.53
111 g
(详见实验素养提升)
考向四
配制一定溶质质量分数的溶液 (8年1考,1~2分)
1.[2022·宿迁]下列物质溶于水,会导致溶液温度明显降低的是( )
A.硝酸铵 B.蔗糖
C.浓硫酸 D.氢氧化钠
A
2.[2017·宿迁]下列说法正确的是 ( )
A.均一、稳定的液体一定是溶液
B.饱和溶液一定是浓溶液
C.汽油洗涤油污属于乳化现象
D.将氢氧化钠溶于水,所得溶液温度升高
D
3.[2015·宿迁]下列有关溶液的说法中,正确的是 ( )
A.溶液不一定都是混合物
B.将100 g KCl饱和溶液蒸干得到25 g固体,则KCl在该温度下的溶解度为25 g
C.常温下将饱和Ca(OH)2溶液加热到50 ℃,会使溶液由饱和变为不饱和
D.从25%的H2SO4溶液中取出10 mL,则取出溶液的质量分数仍为25%
D
4.真题组合 判断下列说法是否正确。
(1)[2014·宿迁]凡是均一、稳定的液体都是溶液,溶液中只能有一种溶质 ( )
(2)[宿迁]溶液一定是混合物 ( )
(3)[宿迁]用洗洁精洗油污是乳化作用,用汽油洗油污也是乳化作用 ( )
(4)[2014·宿迁]20 ℃时,配制2%的氢氧化钙溶液 ( )
×
√
×
×
(5)[2014·宿迁]将100 g 10%的稀盐酸加热蒸发掉50 g水,可使稀盐酸溶质质量分数变成20% ( )
(6)[2018·宿迁]将硝酸铵固体溶于水,溶液温度会升高( )
(7)[2014·宿迁]物质溶于水放热或吸热取决于扩散与水合过程的相对强弱 ( )
×
×
√
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
